|
|
(21), (22) Заявка: 2006135411/04, 06.10.2006
(24) Дата начала отсчета срока действия патента:
06.10.2006
(46) Опубликовано: 27.01.2008
(56) Список документов, цитированных в отчете о
поиске:
ТОЛПЫГИН И.Е. и др. Новые флуоресцентные хемосенсоры на основе 9-аминометилантрацена. ЖОХ, 2003, №9, с.1435-1437. S.A. de SILVA et al. Tetrahedron Letters, 1997, №13, p.2237-2240. SU 1419507 A3, 23.08.1988. RU 2056628 C1, 20.03.1996.
Адрес для переписки:
344090, г.Ростов-на-Дону, пр. Стачки, 194/2, НИИФОХ, патентная служба, М.И. Румянцевой
|
(72) Автор(ы):
Толпыгин Иван Евгеньевич (RU),
Рыбалкин Владимир Петрович (RU),
Ревинский Юрий Владимирович (RU),
Дубоносов Александр Дмитриевич (RU),
Брень Владимир Александрович (RU),
Минкин Владимир Исаакович (RU)
(73) Патентообладатель(и):
Федеральное государственное образовательное учреждение высшего профессионального образования “Южный Федеральный Университет” (RU)
|
(54) N, N’ БИС(9-АНТРИЛМЕТИЛ)ЦИКЛОГЕКСАН-1, 2-ДИАМИН-ФЛУОРЕСЦЕНТНЫЙ ХЕМОСЕНСОР НА КАТИОНЫ Zn2+
(57) Реферат:
Изобретение относится к новым производным ряда N,N’-бис(9-антрилметил)замещенных алкандиаминов, а именно N,N’-бис(9-антрилметил)циклогексан-1,2-диамину формулы I:
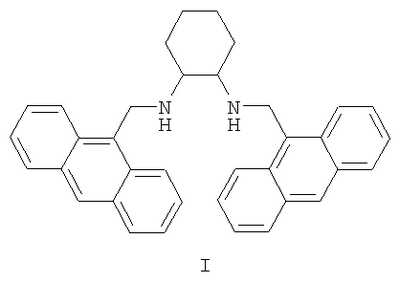
обладающему в нейтральной среде свойствами высокоселективного флуоресцентного хемосенсора на катионы Zn2+. По сравнению с аналогом по строению и применению N,N’-бис(9-антрилметил)этан-1,2-диамином предложенный N,N’-бис(9-антрилметил)циклогексан-1,2-диамин проявляет более эффективные и селективные хемосенсорные свойства по отношению к ионам Zn2+. 1 ил.
Изобретение относится к новым производным ряда N,N’-бис(9-ан-трилметил)замещенных алкандиаминов, а именно к N,N’-бис(9-антрилметил)циклогексан-1,2-диамину формулы I:
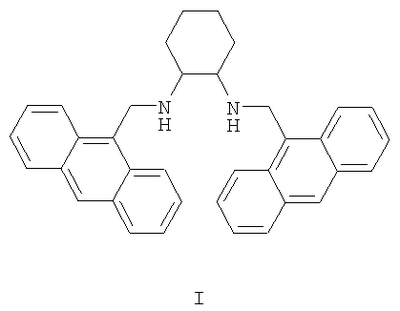
обладающему в нейтральной среде свойствами высокоселективного флуоресцентного хемосенсора на катионы Zn2+.
В настоящее время достаточно большое количество соединений, содержащих тот или иной рецептор (комплексообразующий фрагмент, ответственный за избирательное связывание субстрата) и флуорофор (так называемый «сигнальный» фрагмент молекулы хемосенсора, оптические свойства которого меняются при взаимодействии рецептора с субстратом), представлены авторами как эффективные хемосенсоры на катионы цинка (J.F.Callan, A.P. de Silva, D.C.Magri. Luminescent sensors and switches in the early 21st century, Tetrahedron, 2005, №36, p.8551-8558; E.Kimura, T.Koike. Recent development of zinc-fluorophores, Chemical Society Reviews, 1998, №3, p.179-184; B.A.Брень. Флуоресцентные и фотохромные хемосенсоры, Успехи химии, 2001, №12, с.1152-1174; В.Valeur, I.Leray. Design principles of fluorescent molecular sensors for cation recognition. Coordination Chemistry Reviews, 2000, v.205, №1, p.3-40). Функцию рецепторов в таких соединениях выполняют различные азотсодержащие структуры – азакраунэфиры, азаподанды, каликсарены, азагетероциклы. В большинстве случаев в этих системах проявляется так называемый РЕТ-эффект (Photoinduced Electron Transfer) – фотоиндуцируемый перенос электрона (G.J.Kavarnos, Fundamentals of Photoinduced Electron Transfer, NY, Wiley-VCH, 1993, 359 p.). Рецептор у сенсора, основанном на РЕТ-эффекте, является донором электронов, а флуорофор – акцептором. При возбуждении молекулы происходит перенос электрона с высшей занятой молекулярной орбитали (ВЗМО) флуорофора на низшую свободную молекулярную орбиталь (НСМО). Это позволяет осуществиться электронному переходу с ВЗМО донора-рецептора на ВЗМО акцептора-флуорофора, тем самым вызывая тушение флуоресценции последнего. При комплексообразовании происходит резкое снижение уровня энергии ВЗМО рецептора, приводящее к тому, что перенос электрона на ВЗМО флуорофора становится энергетически невыгодным. Происходит свободный переход возбужденного электрона с НСМО на ВЗМО флуорофора, и сенсор начинает флуоресцировать. Эффективность таких хемосенсоров оценивается двумя факторами – степенью изменения исходной интенсивности флуоресценции при добавлении субстрата и селективностью обнаружения определенного катиона.
Недавно {[3-(бискарбоксиметиламино)-2-метокси-5-метилфенил]карбоксиметиламино}уксусная кислота была заявлена авторами (J.N.Ngwendson, C.L.Amiot, D.K.Srivastava, A.Banerjee, Design of a zinc (II) specific fluorescence sensor. Tetrahedron Letters, 2006, №14, p.2327-2330) как селективный флуоресцентный сенсор на катионы Zn2+. При взаимодействии данного соединения с катионами цинка происходит лишь десятикратное увеличение интенсивности флуоресценции, а заявленная селективность сенсора была установлена только по отношению к ионам: Mg2+, Са2+, Со2+, Ni2+, Cu2+, Отношение хемосенсора к таким ионам как Cd2+, Hg2+ (которые зачастую сопровождают катионы цинка) не было исследовано, так же как не были изучены люминесцентные свойства синтезированной кислоты в присутствии смеси различных катионов, что свидетельствует о незавершенности работы.
Был также синтезирован и исследован хемосенсор на катионы Zn2+, содержащий в основе каликс[4]арен модифицированный введением N-(2-гидроксинафтил-1-метилимино)групп (J.Dessingou, R.Joseph, C.P.Rao, A direct fluorescence-on chemosensor for selective recognition of Zn(II) by rim 1,3-di-derivative of calix[4]arene possessing bis-{N-(2-hydroxynaphthyl-1-methylimine)}pendants, Tetrahedron Letters, 2005, №47, p.7967-7971). В данном случае зафиксировано более чем 20-кратное разгорание флуоресценции при комплексообразовании с ионами Zn2+, при этом выделенный цинковый комплекс показывает интенсивность флуоресценции в 58 раз большую, чем исходный каликс[4]арен. Отмечена селективность сенсора в присутствии значительного числа катионов – Ti4+, VO2+, Cr3+, Mn2+, Fe2+, Со2+, Ni2+, Cu2+, Mg2+, Hg2+. Однако, как и в вышеописанном случае, не исследовались спектральные свойства соединения в присутствии смеси катионов.
Примером высокоселективного флуоресцентного сенсора может служить 6-[2-(бис-пиридин-2-илметиламино)-этиламино]-2-метилбензо[de]изо-хинолин-1,3-дион (J.Fan, X.Peng, Y.Wu, E.Lu, J.Hou, H.Zhang, R.Zhang, X.Fu, A new PET fluorescent sensor for Zn2+, Journal of Luminescence, 2005, vol.114, №2, p.125-130). В результате проведенных исследований с использованием широкой группы катионов: Zn2+, Na+, K+, Са2+, Mg2+, Mn2+, Co2+, Cu2+, Fe2+, Ni2+, Cr3+ было показано, что синтезированное соединение проявляет хемосенсорную активность по отношению к ионам Zn2+ c разгоранием флуоресценции в 5 раз. Остальные исследованные катионы или практически не влияют на интенсивность флуоресценции или, как в случае с Со2+ и Cu2+ или снижают ее. Добавление к раствору сенсора, содержащему катионы цинка пятикратного мольного избытка других катионов, таких как Na+, K+, Са2+, Mg2+ не вызывает каких-либо изменений в интенсивности флуоресценции, что свидетельствует о достаточно высокой степени селективности.
Одним из наиболее эффективных флуоресцентных сенсоров на катионы Zn2+ является 9-антрилметил-бис(2-пиколил)амин (S.A. de Silva, A.Zavaleta, D.E.Baron, A Fluorescent photoinduced electron transfer sensor for cations with off-on-off proton switch, Tetrahedron Letters, 1997, №13, p.2237-2240) – при комплексообразовании с хлоридом цинка происходит разгорание исходной флуоресценции в 77 раз. На примере этого сенсора была реализована принципиальная возможность включения-выключения флуоресценции при изменении рН. Однако в этом случае авторами не исследована селективность полученного соединения по отношению к катионам цинка.
В ряду N,N’-бис(9-антрилметил)замещенных алкандиаминов известен N,N’-бис(9-антрилметил)этан-1,2-диамин, проявляющий высокую хемосенсорную активность по отношению к катионам Zn2+ – разгорание исходной флуоресценции в 42 раза (И.Е.Толпыгин, В.А.Брень, А.Д.Дубоносов, В.И.Минкин, В.П.Рыбалкин. Новые флуоресцентные хемосенсоры на основе 9-аминометилантрацена, Журнал органической химии, 2003, №9, с.1435-1437).
Техническим результатом изобретения является новое соединение в ряду N,N’-бис(9-антрилметил)замещенных алкандиаминов, проявляющее более эффективные и селективные хемосенсорные свойства по отношению к ионам Zn2+.
Технический результат достигается соединением формулы I, синтез которого заключается во взаимодействии 1,2-диаминоциклогексана с 9-антральдегидом и восстановлением полученного N,N’-бис(9-антрилметилен)циклогексан-1,2-диимина боргидридом натрия до N,N’-бис(9-антрил-метил)циклогексан-1,2-диамина (I).
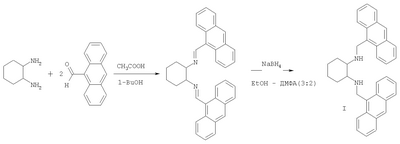
Строение всех синтезированных соединений доказано элементным анализом, данными ИК- и ЯМР Н1 спектров. В ИК-спектре соединения I, снятого в вазелиновом масле, имеется полоса валентных колебаний вторичной аминогруппы при 3400 см-1. В спектре ЯМР 1Н амина I присутствуют сигналы от двух протонов аминогрупп, а также дублетдублетов двух СН2-групп ( 4,56, J1 151,5 Гц, J2 11,9 Гц), непосредственно связанных с антраценовыми фрагментами. 4,56, J1 151,5 Гц, J2 11,9 Гц), непосредственно связанных с антраценовыми фрагментами.
Ниже приведена методика синтеза предлагаемого соединения.
Пример 1. Стадия 1. N,N’-бис(9-антрилметилен)циклогексан-1,2-диимин. Растворяли 4,12 г (20 ммоль) 9-антральдегида в 40 мл 1-бутанола, добавляли 1,14 г (10 ммоль) 1,2-диаминоциклогексана и 0,5 мл ледяной уксусной кислоты. Смесь нагревали до кипения и охлаждали. Выпавший осадок отфильтровывали, промывали горячим этанолом, сушили на воздухе. Выход 98,6%, т.пл. 223-224°С (1-BuOH-ДМФА – 2:1). ИК-спектр,  , см-1: 1630, 1445, 1360, 1080, 1040. Спектр ЯМР 1Н, , см-1: 1630, 1445, 1360, 1080, 1040. Спектр ЯМР 1Н,  , м.д.: 1,60-2,40 (8Н, м., (CH2)4); 3,87-4,05 (2Н, м, 2СН); 7,00 (8Н, д.т., 2,3,6,7 – аром. Н, J1 126,5 Гц, J2 7,6 Гц); 8,00 (8Н, д.д, 1,4,5,8-аром. Н, J1 81,8 Гц, J2 8.7 Гц); 8,39 (2Н, с, 3-аром. Н); 9,37 (2Н, с, 2СН=). Найдено, %: С 88,04; Н 6,26; N 5,70. С36Н30N2. Вычислено, %: С 88,13; Н 6,16; N 5,71. , м.д.: 1,60-2,40 (8Н, м., (CH2)4); 3,87-4,05 (2Н, м, 2СН); 7,00 (8Н, д.т., 2,3,6,7 – аром. Н, J1 126,5 Гц, J2 7,6 Гц); 8,00 (8Н, д.д, 1,4,5,8-аром. Н, J1 81,8 Гц, J2 8.7 Гц); 8,39 (2Н, с, 3-аром. Н); 9,37 (2Н, с, 2СН=). Найдено, %: С 88,04; Н 6,26; N 5,70. С36Н30N2. Вычислено, %: С 88,13; Н 6,16; N 5,71.
Стадия 2. N,N’-бис(9-антрилметил)циклогексан-1,2-диамин (I). К суспензии 5 ммоль N,N’-бис(9-антрилметилен)циклогексан-1,2-диимина в 100 мл смеси этанол – ДМФА (3:2) при нагревании и перемешивании постепенно в течение 2 часов добавляли 1,9 г мелкоизмельченного NaBH4 (50 ммоль). Перемешивание при нагревании продолжали еще 2 часа, затем раствор разбавляли втрое водой и избыток боргидрида разлагали разбавленной СН3СООН. Осадок отфильтровывали, сушили и кристаллизовали из 1-бутанола. Выход 77,8%, т.пл. 204-205°С (1-BuOH). ИК-спектр,  , см-1: 3400, 1465, 1365. Спектр ЯМР 1Н, 5, м.д.: 1,20-2,67 (12Н, м., (СН2)4+2СН+2NН); 4,56 (4Н, д.д., 2СН2, J1 151,5 Гц, J2 11,9 Гц); 7,13 (8Н, д.т., 2,3,6,7-аром. Н, J1 93,8 Гц, J2 7,7 Гц); 7,99 (8Н, д.д., 1,4,5,8-аром. Н, J1 38,9 Гц, J2 8.4 Гц); 8,34 (2Н, с, 3-аром. Н). Спектр флуоресценции в ацетонитриле, , см-1: 3400, 1465, 1365. Спектр ЯМР 1Н, 5, м.д.: 1,20-2,67 (12Н, м., (СН2)4+2СН+2NН); 4,56 (4Н, д.д., 2СН2, J1 151,5 Гц, J2 11,9 Гц); 7,13 (8Н, д.т., 2,3,6,7-аром. Н, J1 93,8 Гц, J2 7,7 Гц); 7,99 (8Н, д.д., 1,4,5,8-аром. Н, J1 38,9 Гц, J2 8.4 Гц); 8,34 (2Н, с, 3-аром. Н). Спектр флуоресценции в ацетонитриле,  макс., нм (с=5×10-5 моль/л): 418. Найдено, %: С 87,34; Н 6,96; N 5,70. C36H34N2. Вычислено, %: С 87,41; Н 6,93; N 5,66. макс., нм (с=5×10-5 моль/л): 418. Найдено, %: С 87,34; Н 6,96; N 5,70. C36H34N2. Вычислено, %: С 87,41; Н 6,93; N 5,66.
Исследование хемосенсорных свойств.
Методы исследования. Оценку сенсорной способности соединения I проводили по данным спектров флуоресценции в области локальной флуоресценции антрацена. Для этого к раствору соединения I (c=5×10-7 моль/л) добавляли расчетный пятикратный мольный избыток ацетата металла (Zn2+, Cd2+, Cu2+, Со2+, Ni2+, Pb2+, Hg2+) или их смеси и перемешивали раствор до полного растворения соли. Затем проводили съемку спектров флуоресценции на длине волны  флуор=418 нм ( флуор=418 нм ( возб=355 нм): исходного раствора и растворов, содержащих помимо соединения I другие катионы. Съемка спектров люминесценции проводилась на спектрофлуориметре Hitachi 650-60. возб=355 нм): исходного раствора и растворов, содержащих помимо соединения I другие катионы. Съемка спектров люминесценции проводилась на спектрофлуориметре Hitachi 650-60.
Расчет относительного изменения интенсивности флуоресценции проводили по формуле: ОИИФ=I/I0, где:
I0 – исходная интенсивность флуоресценции раствора соединения I.
I – интенсивность флуоресценции раствора соединения I после добавления пятикратного мольного избытка катиона.
Результаты испытаний.
Исследование спектральных свойств амина I показало, что данное соединение проявляет высокую сенсорную активность по отношению к катионам Zn2+.
Хемосенсор I вследствие проявления РЕТ-эффекта обладает весьма слабой флуоресценцией антраценового типа в нейтральных растворах ацетонитрила при возбуждении светом  возб. 355 нм (три индивидуальных максимума в области 390-440 нм и плечо 460-470 нм). В спектре испускания этого соединения также наблюдается полоса при 470-600 нм, соответствующая образованию эксимера. возб. 355 нм (три индивидуальных максимума в области 390-440 нм и плечо 460-470 нм). В спектре испускания этого соединения также наблюдается полоса при 470-600 нм, соответствующая образованию эксимера.
Комплексообразование с различными катионами за счет связывания неподеленной электронной пары азота существенно видоизменяет термодинамику РЕТ-эффекта, что приводит к изменению интенсивности флуоресценции.
Добавление ацетатов меди или свинца к раствору сенсора I вызывает затухание флуоресценции, тогда как ионы Zn2+ резко увеличивают интенсивность флуоресценции (I/I0=79). Все исследования проводились в нейтральной среде.
Чертеж Относительное изменение интенсивности флуоресценции (I/I0) диамина (I) (С=5·10-7 моль/л) в ацетонитриле при добавлении различных катионов (С=2,5·10-6 моль/л).
Селективность данного сенсора была показана при добавлении к исходному раствору амина I смеси катионов (каждый из катионов был взят в пятикратном мольном избытке относительно соединения I). В этом случае происходит увеличение относительной интенсивности флуоресценции (разгорание) в 77 раз. Таким образом, отклонение интенсивности флуоресценции раствора соединения I с добавлением смеси катионов от раствора соединения I с добавлением только ацетата цинка составляет менее 3%, что свидетельствует о высокой избирательности данного флуоресцентного хемосенсора по отношению к ионам Zn2+ в нейтральной среде.
Проведенные нами сравнительные исследования показали, что N,N’-бис(9-антрилметил)этан-1,2-диамин менее селективен, чем его циклический аналог I, и менее эффективен, что объясняется более жесткой геометрией координационного узла в соединении I и более полным соответствием стерических параметров рецептора и катиона Zn2+.
Таким образом, по уровню хемосенсорной активности и селективности по отношению к ионам Zn2+ N,N’-бис(9-антрилметил)циклогексан-1,2-диамин (I) превосходит описанные ранее флуоресцентные сенсоры на катионы Zn2+.
Формула изобретения
N,N’-бис(9-антрилметил)циклогенсан-1,2-диамин формулы I
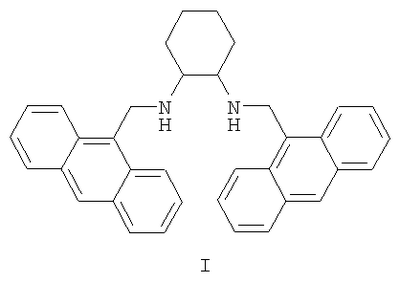
РИСУНКИ
|
|