Патент на изобретение №2315055
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 1,2,5-ТРИАЛКИЛ-3,4-ФУЛЛЕРО[60]ФОСФОЛАНОВ
(57) Реферат:
Изобретение относится к области органической химии, а именно к способу получения 1,2,5-триалкил-3,4-фуллеро[60]фосфоланов формулы (1), которые могут найти применение в качестве комплексообразователей, сорбентов, биологически активных соединений, а также при создании новых материалов с заданными электронными, магнитными и оптическими свойствами. Сущность способа заключается во взаимодействии фуллерена С60 с триалкилфосфином в присутствии катализатора Cp2TiCl2 в среде толуола при комнатной температуре (20°С) в течение 66-78 часов. Выход целевого продукта составляет 47-70%. Технический результат – селективное получение соединения формулы (1) с высоким выходом. 1 табл.
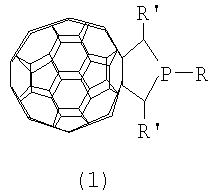
где R=Pr, R’=Et R=Bu, R’=Pr R=Hex, R’=Am
(56) (продолжение): CLASS=”b560m”синтез карбонил и фосфорилсодержащих метано[60]фуллеренов”, Известия АН серия химическая, 2004, 12, 2088-2085. ГУБСКАЯ В.П. И ДР. “Синтез и строение новых производных фуллерена С60, содержащих карбонильные группы”, Известия АН серия химическая, 2005, 6, 1424-1439. ГУБСКАЯ В.П. И ДР. “Синтез, строение и электрохимическое поведение фосфорилированных метано[60]фуллеренов, содержащих нитроксильные радикалы”, Известия АН серия химическая, 2005, 7, 1594-1617. CHUANG SH. AND ALL, “Novel acid-catalyzed rearrangement of methanofullerenes bearing an
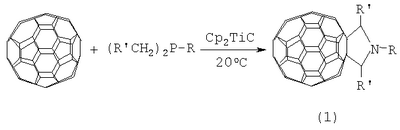
Предлагаемое изобретение относится к органической химии, конкретно к способу получения 1,2,5-триалкил-3,4-фуллеро[60]фосфоланов общей формулы (1):
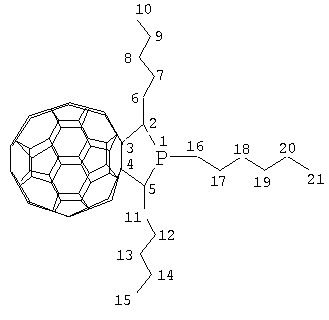
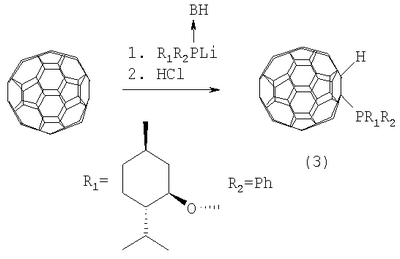
R=Bu, R’=Pr R=Hex, R’=Am Функционально замещенные фуллерены могут найти применение в качестве комплексообразователей, сорбентов, биологически активных соединений, а также при создании новых материалов с заданными электронными, магнитными и оптическими свойствами. Известен способ ([1], И.А.Нуретдинов, В.П.Губская, Л.Ш.Бережная, А.В.Ильясов, Н.М.Азанчеев. Изв. АН. Сер. хим. 2000, 12, 2083-2085) электрохимичекого получения фосфорилированных метанофуллеренов формулы (2) реакцией С60 с алкоксифосфорилбромацетатами в растворе о-дихлорбензола. Известный способ не позволяет получать 1,2,5-триалкил-3,4-фуллеро[60]фосфоланы (1). Известен способ ([2], S.Yamamoto, M.Yanagawa, H.Mukai, E.Nakamura. Tetrahedron, 1996, 52, 5091) получения 1-(Р-диалкилфосфино)-1,2-дигидро[60]фуллерена формулы (3) реакцией присоединения боранового комплекса вторичного фосфина к С60 в толуоле при температуре 80°С по схеме: Известный способ не позволяет получать 1,2,5-триалкил-3,4-фуллеро[60]фосфоланы (1). Таким образом, в литературе отсутствуют сведения по селективному синтезу 1,2,5-триалкил-3,4-фуллеро[60]фосфоланов (1). Предлагается новый способ получения 1,2,5-триалкил-3,4-фуллеро[60]фосфоланов (1). Сущность способа заключается во взаимодействии фуллерена С60 с триалкилфосфином общей формулы (R’CH2)2P-R, где R=Pr, Bu, Hex, R’=Et, Pr, Am, взятыми в мольном соотношении 0.01:(0.01-0.011), предпочтительно 0.01:0.0105, в присутствии катализатора титаноцендихлорида (Ср2TiCl2), взятого в количестве 15-25 мол.% по отношению к фуллерену С60 при комнатной температуре (20°С) в течение 66-78 ч, предпочтительно 72 ч в растворе толуола. Выход 1,2,5-триалкил-3,4-фуллеро[60]фосфоланов (1) составляет (по данным ВЭЖХ) 47-70%. Реакция протекает по схеме: 1) R=Pr, R’=Et 2) R=Bu, R’=Pr 3) R=Hex, R’=Am Триалкилфосфин берут с избытком по отношению к фуллерену С60 с целью повышения выхода целевого продукта (1). Снижение количества триалкилфосфина по отношению к С60 нецелесообразно, так как приводит к уменьшению выхода целевого продукта. 1,2,5-Триалкил-3,4-фуллеро[60]фосфоланы (1) образуются только с участием фуллерена[60] и триалкилфосфина. Проведение указанной реакции в присутствии катализатора Ср2TiCl2 больше 25 мол.% по отношению к С60 не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора Ср2TiCl2 менее 15 мол.% по отношению к С60 снижает выход продукта (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Изменение соотношения исходных реагентов в сторону значительного увеличения содержания триалкилфосфина по отношению к фуллерену[60] приводит к присоединению дополнительных молекул исходного третичного фосфина к молекуле С60. Существенные отличия предлагаемого способа. 1. Предлагаемый способ базируется на использовании в качестве исходного реагента триалкилфосфина и катализатора Cp2TiCl2. В известном способе используется борановый комплекс вторичного фосфина. Предлагаемый способ, в отличие от известного, позволяет селективно получать 1,2,5-триалкил-3,4-фуллеро[60]фосфоланы (1), синтез которых в литературе не описан. Способ поясняется следующими примерами. ПРИМЕР 1. В стеклянную колбу объемом 50 мл в атмосфере аргона помещают 0.01 ммоля фуллерена С60, 10 мл “сухого” толуола, 0.0105 ммоля тригексилфосфина и 0.002 ммоль катализатора Cp2TiCl2, перемешивают 72 ч при температуре 20°С, получают 1-гексил-2,3-дипентил-3,4-фуллеро[60]фосфолан общей формулы (1) с выходом 64% (по данным ВЭЖХ). Спектр ЯМР13С 1-гексил-2,3-дипентил-3,4-фуллеро[60]фосфолана (1) (
55.33 (С2,5), 74.83 (С3,4), 30.99 (С6,11), 30.29 (С7,12), 31.51 (С8,13), 20.84 (С9,14), 13.97 (С10,15), 22.44 (С16), 25.45 (С17), 29.59 (С18), 31.83 (С19), 21.59 (С20), 14.07 (С21). Сигналы углеродных атомов фуллеренового фрагмента располагаются в области 128-152. Другие примеры, подтверждающие способ, приведены в табл.1.
В качестве растворителя использовали толуол, т.к. в нем наибольшая растворимость фуллерена С60.
Формула изобретения
Способ получения 1,2,5-триалкил-3,4-фуллеро[60]фосфоланов общей формулы (1)
где R=Pr, R’=Et R=Bu, R’=Pr R=Hex, R’=Am путем взаимодействия фуллерена С60 с триалкилфосфином общей формулы (R’CH2)2P-R, где R=Pr, Bu, Hex, R’=Et, Pr, Am, при мольном соотношении С60:триалкилфосфин 0,01:(0,01-0,011), в присутствии катализатора титаноцендихлорида (Cp2TiCl2), взятого в количестве 15-25 мол.% по отношению к фуллерену С60, в среде толуола в качестве растворителя, при комнатной температуре (20°С) в течение 66-78 ч.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 22.06.2008
Извещение опубликовано: 20.06.2010 БИ: 17/2010
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

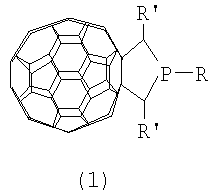
 -ylidic ester to cyclopentanofullerenes: a vinyl cyclopropane-type ring expansion”, Journal of organic chemistry, 2003, 68, 10, 3811-3816.
-ylidic ester to cyclopentanofullerenes: a vinyl cyclopropane-type ring expansion”, Journal of organic chemistry, 2003, 68, 10, 3811-3816.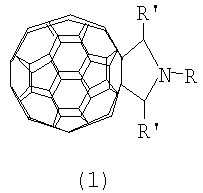 где R=Pr, R’=Et
где R=Pr, R’=Et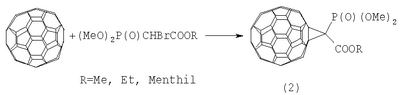
 , м.д.):
, м.д.):