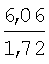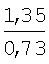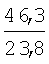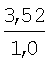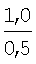Патент на изобретение №2314311
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ДИГИДРОХЛОРИД 1-(3-ПИПЕРИДИНОПРОПИЛ)-2-(4-ФТОРОФЕНИЛ)ИМИДАЗО[1,2-A]-БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ
(57) Реферат:
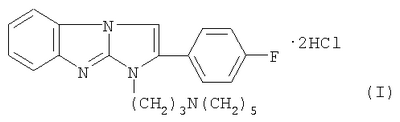
Изобретение относится к новому 1,2-дизамещенному имидазо[1,2-а] бензимидазола, обладающему местноанестезирующим действием при инфильтрационной и проводниковой анестезиях. Описывается дигидрохлорид 1-(3-пиперидинопропил)-2-(4-фторофенил)имидазо[1,2-а]-бензимидазола формулы I: Технический результат – получено новое соединение, обладающее полезными биологическими свойствами. 3 табл.
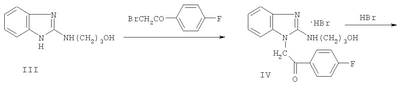
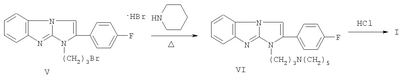
Изобретение относится к новому 1,2-дизамещенному имидазо[1,2-а]-бензимидазола, а именно к водорастворимому дигидрохлориду 1-(3-пиперидинопропил)-2-(4-фторофенил)имидазо[1,2-а]бензимидазола формулы I: обладающему местноанестезирующим действием при инфильтрационной и проводниковой анестезиях. Следует отметить, что маркаин, подобно дикаину, не только высокоактивный, но и весьма токсичный анестетик (Рациборинская Н.Б.. Местноанестезирующие свойства некоторых новых производных пиперидина и индола. Автореф. дис…. канд. мед. наук. Ростов-на-Дону, 1991; Kambarn J., Mets В., Hickman R. et al. Comparative systemic toxicity of intravenously infused bupivacaine (B), cocaine (C) and lidocaine (L) inpigs: [Abstr.] Int. Anesth. Res. Soc. 66th Congr., San Francisco, Calif., March 13-17, 1992; anesth. and Analg., 1992, Vol.74, №25, p.87), что требует повышенного внимания при его использовании в практической медицине. Кроме того, маркаин может вызывать генерализованную сыпь, отек Квинке, стридор гортани, бронхоспазм (Gall H., Reichert V., Kaufmann R. Localanastheticaintoleranz auf Leitungsanasthesia mit Prilocain und Bupivacain. Allergologie, 1992, Bd. 15, №3, S.89-91). В ряду 1,2-дизамещенных имидазо[1,2-а]бензимидазола известны соединения, обладающие местноанестезирующим действием. Наиболее близким по структуре веществом среди 1,2-дизамещенных имидазо[1,2-а]-бензимидазола является дигидрохлорид 1-(3-пирролидинопропил)-2-фенилимидазо[1,2-а]бензимидазола, обладающий местноанестезирующим действием [Анисимова В.А., Галенко-Ярошевский А.П., Попков В.А., Каде Е.А., Осипова М.М., Спасов А.А. Дигидрохлорид 1-(3-пирролидинопропил)-2-фенилимидазо[1,2-а]бензимидазола, обладающий местноанестезирующим действием. Патент РФ №2160265 (2000), С07D 487/04, А61К 31/4188, А61Р 23/02]. Техническим результатом изобретения является новое соединение в ряду 1,2-дизамещенных имидазо[1,2-а]бензимидазола, проявляющее местно-анестезирующее действие, более эффективное, чем известный в этом ряду дигидрохлорид 1-(3-пирролидинопропил)-2-фенилимидазо[1,2-а]бензимидазола [Патент РФ №2160265 (2000)], а также более эффективное, чем известный, широко применяемый обезболивающий препарат маркаин. Технический результат изобретения достигается соединением I, синтез которого заключается во взаимодействии 2-(3-гидроксипропиламино)бензимидазола (III) с 4-фторофенацилбромидом, дальнейшей циклизации образующегося гидробромида 1-(4-фторофенацил)-2-(3-гидроксипропиламино)бензимидазола (IV) с одновременным замещением гидроксигруппы на атом брома при кипячении в конц. HBr. Последующее замещение атома брома в гидробромиде 1-(3-бромопропил)-2-(4-фторофенил)имидазо[1,2-а]-бензимидазола (V) на пиперидин и перевод полученного 1-(3-пиперидино-пропил)замещенного (VI) в дигидрохлорид обычными методами приводит к соединению I: Ниже приведены методики синтеза предлагаемого соединения. Пример. Дигидрохлорид 1-(3-пиперидинопропил)-2-(4-фторофенил)-имидазо[1,2-а]бензимидазола (I). Стадия 1. Гидробромид 2-(3-гидроксипропиламино)-1-(4-фторофенацил)бензимидазола (IV). В нагретый почти до кипения раствор 1,9 г (10 ммоль) 2-(3-гидроксипропиламино)бензимидазола (III) в 15 мл 2-пропанола вносят 2,75 г (10,5 ммоль) 4-фторофенацилбромида, синтезированного бромированием 4-фтороацетофенона эквимолярным количеством брома в этаноле, и смесь кипятят до полного протекания реакции (контроль – ТСХ, 4-5 ч). По окончании реакции массу охлаждают, выпавший осадок отфильтровывают и тщательно промывают ацетоном. Выход 3,8 г (93,13%). Белоснежные блестящие чешуйки с т.пл. 264-265°С (разложение, из этанола). Найдено, %: С 52,8; Н 4,9; Br 19,4; F 4,5; N 10,5. C18H18FN3O2·HBr. Вычислено, %: С 52,9; H 4,7; Br 19,6; F 4,7; N 10,3. ИК-спектр (вазелин, масло), см-1: 1705 (С=O), 1675 (C=N+<), 3070-3310 (ОН, NH). Спектр 1Н ЯМР (DMSO-d6), Стадия 2. Гидробромид 1-(3-бромопропил)-2-(4-фторофенил)имидазо-[1,2-а]бензимидазола (V). Кипятят 3,05 г (7,5 ммоль) соединения IV в 30 мл конц. HBr до полного протекания реакции (6-8 ч, контроль – ТСХ: Al2O3, CHCl3; Rf исходного 0,1, Rf конечного 0,85). Выпавший осадок после охлаждения реакционной массы отфильтровывают на стеклянном фильтре, хорошо отжимают и тщательно промывают от кислоты ацетоном. Получают 3,34 г (97,9%) практически чистого гидробромида V, которое можно вводить в дальнейшие реакции без дополнительной очистки. Т.пл. 237-238°С (из этанола). Найдено, %: С 48,0; Н 3,5; Br 34,8; N 9,5. C18H15BrFN3·HBr. Вычислено, %: С 47,9; Н 3,6; Br 35,0; N9,3. ИК-спектр (вазелин, масло), см-1: 1500, 1595, 1605 (C=С), 1665 (C=N+<). Спектр 1H ЯМР (DMSO-d6 – CCl4), Стадия 3. Дигидрохлорид 1-(3-пиперидинопропил)-2-(4-фторофенил)-имидазо[1,2-а]бензимидазола (I). Смесь 0,91 г (2 ммоль) гидробромида V и 2,5 мл свежеперегнанного пиперидина кипятят 2 часа, следя за ходом реакции с помощью ТСХ на Al2О3 (элюент – хлороформ, Rf исходного IV 0,85, Rf конечного VI 0,4). После окончания реакции массу охлаждают и выливают в 15 мл холодной воды. Выпавший осадок основания VI отделяют, промывают водой для удаления избытка пиперидина и сушат на воздухе, получая 0,75 г (выход количественный) хроматографически чистого вещества. Т.пл. 96-97°С. Дигидрохлорид I получают подкислением раствора основания VI в сухом ацетоне насыщенным раствором HCl в изопропиловом спирте до рН 1-2, при этом вначале выделяется масло, которое при растирании закристаллизовывается в белоснежные кристаллы. Через 1 ч их отфильтровывают, промывают ацетоном и перекристаллизовывают из ацетонитрила (0,75 г/10 мл). Т.пл. 248-250°С (разл.). Найдено, %: С 61,6; Н 5,9; Cl 16,0; F 4,1; N 12,7. C23H25FN4·2HCl. Вычислено, %: С 61,5; H 6,1; Cl 15,8; F 4,2; N 12,5. ИК-спектр (вазелин, масло), см-1: 1665 (С=N+<), 2430-2700, 3140-3280 (N+Н). Спектр 1Н ЯМР (DMSO-d6 – CCl4), Эксперименты проведены в соответствии со статьей 11-й Хельсинкской декларации Всемирной медицинской ассоциации (1964), “Международными рекомендациями по проведению медико-биологических исследований с использованием животных” (1985) и Правилами лабораторной практики в Российской Федерации (приказ МЗ РФ №267 от 19.06.2003 г.). Проводниковую анестезию изучали в экспериментах на седалищном нерве кроликов (Прянишникова Н.Т., Шаров Н.А., Тримекаин. Фармакология и клиническое применение. – Л.: Медицина, 1967. – 239 с.). Острую токсичность исследовали [определяли среднюю летальную (смертельную) дозу – ЛД50 Статистическую обработку данных, учитываемых в градированной форме, проводили по М.Л.Беленькому (Беленький М.Л. Элементы количественной оценки фармакологического эффекта. – Л., 1963. – 152 с.) и с помощью таблиц Н.Н.Самойлова (Самойлов Н.Н. Таблицы значений средней ошибки и доверительного интервала средней арифметической величины вариационного ряда. – Томск. 1970. – 63 с.). Учет результатов исследований, выраженных в альтернативной форме, определение ЛД50, ЭК50, границ доверительного интервала и терапевтического индекса, или широты терапевтического действия (ЛД50/ЭК50) осуществляли по методам, описанным В.Б.Прозоровским (1962) и М.Л.Беленьким (1963). Установлено, что в условиях инфильтрационной анестезии в экспериментах на морских свинках минимальной обезболивающей концентрацией для соединения I является 0,0039%, для маркаина – 0,0156% и соединения II – 0,0078%. Полный обезболивающий эффект (100%-ная анестезия в течение 30 мин) вызывает соль I в 0,0312% растворе, маркаин – в 0,125%, II – в 0,0625% растворах (табл.1). Сопоставление ЭК50, выраженных в мМ, показало (табл.2), что I в 6,06 и 1,72 раза более активно, чем маркаин и II, соответственно. При этом по широте терапевтического действия I в 46,3 и 23,8 раза превосходит маркаин и II соответственно. В условиях проводниковой анестезии в экспериментах на седалищном нерве кроликов выявлено (табл.3), что при применении 0,5% раствора соединения I обезболивающее действие наступает соответственно в 2,39 и 1,35 раза быстрее, чем под влиянием аналогичных растворов маркаина и II. По продолжительности полной анестезии и общей длительности обезболивания дигидрохлорид I статистически значимо в 1,91 и 1,98, 1,54 и 1,56 раза соответственно превосходит маркаин и соль II. По глубине анестезирующего действия I маркаин и II равнозначны. Соединение I в 0,25, 0,5 и 1,0% растворах не оказывает раздражающего и повреждающего действия на кожу крыс. Таким образом, соединение I по эффективности и широте терапевтического действия значительно превосходит маркаин и соединение II. На основе его возможно создание местнообезболивающего лекарственного средства, предназначенного подобно маркаину для инфильтрационной и проводниковой анестезии.
Формула изобретения
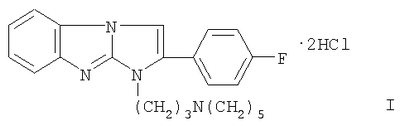
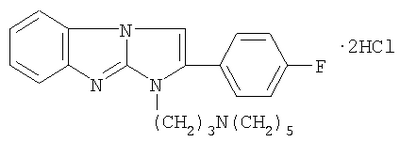
Дигидрохлорид 1-(3-пиперидинопропил)-2-(4-фторофенил)имидазо[1,2-а]бензимидазола формулы I
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 , м.д.: 1,87 (2Н, кв, СН2), 3,6 (4Н, к, NCH2, СН2О), 6,15 (2Н, с, CH2СО), 7,1-8,2 (8Н, м, аромат. Н), 9,12 (1Н, т, NH).
, м.д.: 1,87 (2Н, кв, СН2), 3,6 (4Н, к, NCH2, СН2О), 6,15 (2Н, с, CH2СО), 7,1-8,2 (8Н, м, аромат. Н), 9,12 (1Н, т, NH).