Патент на изобретение №2314310
|
||||||||||||||||||||||||||
(54) ГИДРОХЛОРИД 3-МЕТОКСИКАРБОНИЛ-4-(2-ПИПЕРИДИНОЭТИЛ)-2-ЭТИЛПИРАЗОЛО[1,5-А] БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ
(57) Реферат:
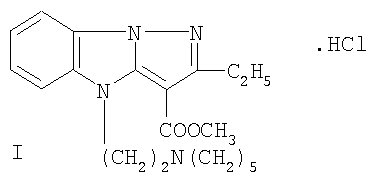
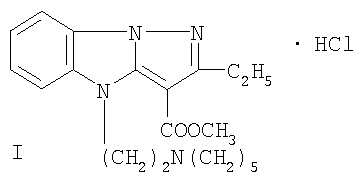
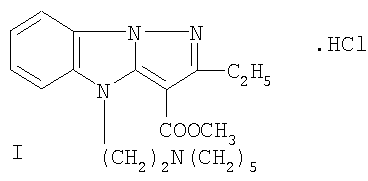
Изобретение относится к новому производному в ряду пиразоло[1,5-а]бензимидазола, обладающему местно-анестезирующим действием при поверхностной (терминальной), инфильтрационной и проводниковой анестезии. Описывается гидрохлорид 3-метоксикарбонил-4-(2-пиперидиноэтил)-2-этилпиразоло[1,5-а]бензимидазола формулы I:
Технический результат – получено новое соединение, обладающее полезными биологическими свойствами. 6 табл.
Изобретение относится к новому производному в ряду пиразоло-[1,5-а]бензимидазола, а именно к гидрохлориду 3-метоксикарбонил-4-(2-пиперидиноэтил)-2-этилпиразоло[1,5-а]бензимидазола формулы I:
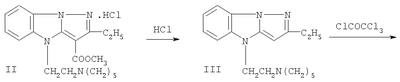
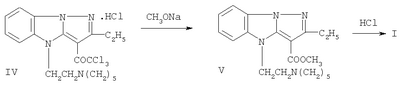
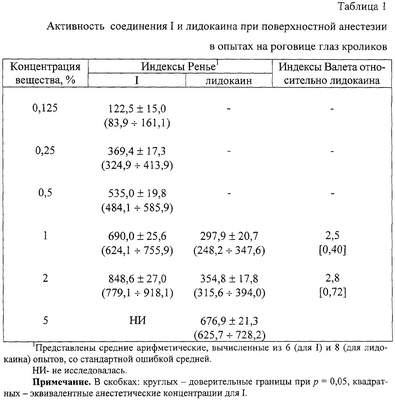
обладающему местно-анестезирующим действием при поверхностной (терминальной), инфильтрационной и проводниковой анестезии. Эффективным лекарственным средством, широко применяемым в качестве местного анестетика при инфильтрационном, проводниковом и терминальном методах обезболивания, является лидокаин (А.И. Левшанков, А.Л. Костюченко, Е.Т. Ростомашвили и др. Каудальная эпидуральная анестезия при операциях на нижних конечностях в травматологии и ортопедии. Анестезиол. и реаниматол., 1992, №5-6, с.15-17; М.Д. Машковский, Лекарственные средства, 15-е изд., перераб. и дополн., М.: Медицина, 1998, ч.1, с.371-382). Лидокаин обычно хорошо переносится, однако иногда может вызывать коллапс, анафилактическую реакцию, изменения в содержании цитоплазматических белков, поверхности и форме эритроцитов (Г.И. Карицкий, А.Н. Куйбида и др. Выведение из анафилактического шока с клинической смертью после введения лидокаина. Вестн. хир. им. И.И. Грекова, 1987, №4, с.131; Н.Х. Вахидов, И.А.Абдуллаева, Т.Р. Мурадов. Успешная реанимация больных после побочной токсической реакции на введение лидокаина. Журнал ушных, носовых и горловых болезней, 1989, №6, с.60-61; E.Nidhiguchi et al. Factors of the share change of human erythrocytes induced with lidocaine. Cell. struct. and Funct., 1989, Vol.14, №, p.569-577; М.Д. Машковский, 1998). В ряду пиразоло[1,5-а]бензимидазола не известны соединения, обладающие местно-анестезирующим действием. Наиболее близкими по структуре среди производных пиразоло[1,5-а]-бензимидазола являются 3-алкоксикарбонил-2,4-диметилпиразоло[1,5-а]-бензимидазолы (Кузьменко Т.А., Кузьменко В.В., Симонов A.M. 3- Техническим результатом изобретения является новое соединение в ряду пиразоло[1,5-а]бензимидазола, проявляющее неизвестное для данного класса веществ местно-анестезирующее действие, более эффективное, чем действие известного местно-анестезирующего средства. Технический результат достигается соединением I, синтез которого заключается в омылении ацильной группы в 3-пропионил-2-этил-4-(2-пиперидиноэтил)пиразоло[1,5-а]бензимидазоле под действием конц. HCl, дальнейшем ацилировании полученного 2-этил-4-пиперидиноэтилпиразоло[1,5-а]бензимидазола хлорангидридом трихлоруксусной кислоты при нагревании в ксилоле до 3-трихлороацетилзамещенного и последующем галоформном расщеплении последнего под действием метилата натрия. Синтезированный 3-метоксикарбонил-2-этил-4-(2-пиперидиноэтил)пиразоло[1,5-а]-бензимидазол переводят в искомый водорастворимый гидрохлорид I обычными методами. Ниже приведены методики синтеза предлагаемого соединения. Пример. Гидрохлорид 3-метоксикарбонил-2-этил-4-(2-пиперидиноэтил)пиразоло[1,5-а]бензимидазола (I). Стадия 1. 2-Этил-4-(2-пиперидиноэтил)пиразоло[1,5-а]бензимидазол (III). Раствор 7,8 г (0,02 моль) гидрохлорида 3-пропионил-2-этил-4-(2-пиперидиноэтил)пиразоло[1,5-а]бензимидазола (II) в 100 мл конц. HCl кипятят 6 ч. Охлаждают, подщелачивают 22%-ным раствором аммиака, выделившееся масло экстрагируют CHCl3 (3×30 мл). Экстракт упаривают досуха и после высушивания в вакуум-эксикаторе над Р2O5 основание III в виде густого масло используют на следующей стадии без дополнительной очистки. Выход 5,2 г (88%). Стадия 2. Гидрохлорид 2-этил-3-трихлорацетил-4-(2-пиперидиноэтил)-пиразоло[1,5-а]бензимидазола (IV). В нагретый до 70-80°С раствор 2,96 г (0,01 моль) соединения III в 50 мл сухого ксилола вносят при перемешивании 1,1 мл (0,01 моль) свежеперегнанного хлорангидрида трихлоруксусной кислоты в течение 10 мин. Затем реакционную смесь нагревают до кипения и кипятят 2 ч. После охлаждения осадок соединения IV отфильтровывают, промывают ацетоном. Выход 4,2 г (87%). Бледно-желтые иглы с т.пл. 253-255°С (разл., из бутанола), нерастворимые в воде. Найдено, %: С 50,0; Н 5,3; Cl 30,0; N 12,0. С20Н23Cl3N4O·HCl. Вычислено, %: С 50,2; Н 5,0; Cl 29,7; N 11,7. ИК-спектр (вазел. масло), см-1: 1640 (С=O), 2380-2600 (N+Н). Стадия 3. Гидрохлорид 3-метоксикарбонил-2-этил-4-(2-пиперидиноэтил)пиразоло[1,5-а]бензимидазола (I). В раствор метилата натрия, полученный из 0,6 г натрия и 20 мл метилового спирта, вносят небольшими порциями 4,78 г (0,01 моль) гидрохлорида IV. После прекращения бурной реакции смесь кипятят 3-5 мин. Спирт испаряют досуха, остаток хроматографируют на колонке с Al2O3, элюируя хлороформом. Элюат упаривают досуха, оставшееся густое масло после высушивания в вакуум-эксикаторе над P2O5 растворяют в сухом ацетоне и подкисляют раствором HCl в эфире. Осадок гидрохлорида отделяют, промывают сухим эфиром. Выход 3,7 г (94%). Бесцветные кристаллы с т.пл. 222-223°С (из спирта). Найдено, %: С 61,3; Н 6,7; Cl 8,8; N 14,0. C20H26N4O2·HCl. Вычислено, %: С 61,5; Н 6,9; Cl 9,1; N 14,3. ИК-спектр (вазел. масло), см-1: 1675 (С=O), 2380-2700 (N+H). Эксперименты проведены в соответствии со статьей 11-й Хельсинкской декларации Всемирной медицинской ассоциации (1964), “Международными рекомендациями по проведению медико-биологических исследований с использованием животных” (1985) и Правилами лабораторной практики в Российской Федерации (приказ МЗ РФ №267 от 19.06.2003 г.). Проводниковую анестезию изучали в экспериментах на седалищном нерве кроликов (Н.Т. Прянишникова, Н.А. Шаров, 1967). Острую токсичность исследовали [определяли среднюю летальную (смертельную) дозу – ЛД50 Статистическую обработку данных, учитываемых в градированной форме, проводили по М.Л. Беленькому (Беленький М.Л. Элементы количественной оценки фармакологического эффекта. – Л., 1963. – 152 с.) и с помощью таблиц Н.Н. Самойлова (Самойлов Н.Н. Таблицы значений средней ошибки и доверительного интервала средней арифметической величины вариационного ряда. – Томск. 1970. – 63 с.). Учет результатов исследований, выраженных в альтернативной форме, определение ЛД50, ЭК50, границ доверительного интервала и терапевтического индекса, или широты терапевтического действия (ЛД50/ЭК50) осуществляли по методам, описанным В.Б. Прозоровским (1962) и М.Л. Беленьким (1963). Установлено, что в условиях поверхностной анестезии в опытах на роговице глаз кроликов минимальной и максимальной анестезирующими концентрациями для соединения I являются 0,125 и 2,0%, а для лидокаина – 1,0 и 5,0% соответственно. Индексы Ренье, выражающие силу анестезирующего действия в испытуемых концентрациях, для I в 0,125, 0,25, 0,5, 1 и 2% растворах составляют 122,5, 369,4, 535,0, 690,0 и 848,6, для лидокаина в 1, 2 и 5% растворах – 297,9, 354,8 и 676,9 соответственно. Индексы Валета для соли I относительно лидокаина, взятого для сопоставления в 1 и 2% растворах, равны 2,5 и 2,8; эквивалентные анестетические концентрации составили 0,4 и 0,72% соответственно (табл.1). Вещество I, как и лидокаин, в исследованных растворах не оказывает раздражающего действия на конъюнктиву глаза. По местно-анестезирующей активности – при сопоставлении ЭК50, выраженных в мМ, и терапевтических индексов – соединение I соответственно в 8,38 раза более значимо, и в 6,08 раза имеет большую широту терапевтического действия, чем лидокаин (табл.2). При инфильтрационной анестезии в экспериментах на морских свинках минимальной обезболивающей концентрацией для соли I является 0,0156%, для лидокаина – 0,0625%. Полный обезболивающий эффект (100%-ная анестезия в течение 30 мин) соединение I вызывает в 0,125% растворе, тогда как лидокаин – в 0,5% растворе (табл.3). Сопоставление ЭК50, выраженных в мМ, показало (табл.4), что I в 3,94 раза более активно, чем лидокаин. При этом по широте терапевтического действия оно в 2,84 раза превосходит лидокаин. В опытах на кроликах установлено (табл.5), что под влиянием 0,5% раствора I обезболивающий эффект наступает в 1,52 раза быстрее, чем при использовании лидокаина. По продолжительности полной анестезии и общей длительности обезболивания соль I в 3,38 и 3,04 раза соответственно превосходит лидокаин. По глубине анестезирующего действия I и лидокаин сопоставимы. В условиях проводниковой анестезии в экспериментах на седалищном нерве кроликов выявлено (табл.6), что при применении 0,5% раствора гидрохлорида I обезболивающее действие наступает в 1,33 раза быстрее, чем при использовании лидокаина в аналогичной концентрации. По общей длительности анестезии I в 2,45 раза превосходит лидокаин. Важно отметить, что I индуцирует полный обезболивающий эффект в течение 262,0 мин, тогда как лидокаин не проявляет полной анестезии: глубина обезболивания в первом случае составляет 100,0%, а во втором – 64,0%. Таким образом, соединение I по активности и широте терапевтического действия значительно превосходит лидокаин. На его основе возможно создание местно-обезболивающего лекарственного средства, предназначенного, подобно лидокаину, для поверхностной, инфильтрационной и проводниковой анестезии.
Формула изобретения
Гидрохлорид 3 -метоксикарбонил-4-(2-пиперидиноэтил)-2-этилпиразоло [1,5-а]бензимидазола формулы I
|
||||||||||||||||||||||||||

 -Галогенкарбонильные производные пиразоло[1,5-а]бензимидазола и их превращения. ХГС, 1988, №1, с.43-48. WO 92/22552 A1, 23.12.1992.
-Галогенкарбонильные производные пиразоло[1,5-а]бензимидазола и их превращения. ХГС, 1988, №1, с.43-48. WO 92/22552 A1, 23.12.1992.