Патент на изобретение №2314304
|
||||||||||||||||||||||||||||||||||||||||||||||||
(54) 3-(5-АЛКОКСИ-1,2-ДИМЕТИЛ-1Н-ИНДОЛ-3-ИЛ)-4-[(1E)-АЛК-1-ЕНИЛ]ФУРАН-2,5-ДИОНЫ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ФЛУОРЕСЦИРУЮЩИХ ФОТОХРОМОВ
(57) Реферат:
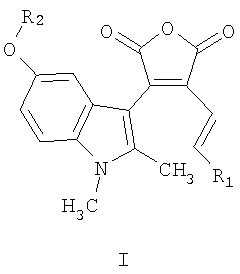
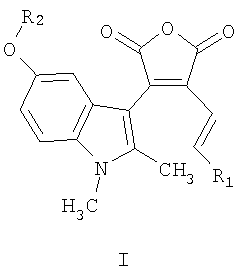
Изобретение относится к новым 3-(5-алкокси-1,2-диметил-1 Н-индол-3-ил)-4-[(1Е)-алк-1-енил]фуран-2,5-дионам общей формулы I
где R1=C1-С6алкил, R2=С1-С6алкил. Соединения I проявляют фотохромные и флуоресцентные свойства. Изобретение относится также к применению 3-(5-алкокси-1,2-диметил-1 Н-индол-3-ил)-4-[(1Е)-алк-1-енил]фуран-2,5-дионов общей формулы I, в качестве флуоресцирующих фотохромов, которые могут быть использованы, например, в системах хранения и обработки информации, в частности, в качестве светочувствительной компоненты материалов для трехмерной записи и хранения информации, а также могут быть использованы при создании элементной базы для молекулярных компьютеров, в частности в качестве молекулярных переключателей. 2 н. и 3 з.п. ф-лы, 1 табл.
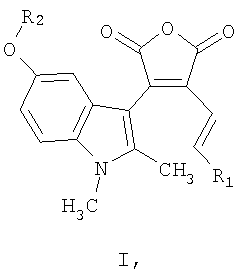
Изобретение относится к новым соединениям, а именно к 3-(5-алкокси-1,2-диметил-1Н-индол-3-ил)-4-[(1Е)-алк-1-енил]фуран-2,5-дионам общей формулы
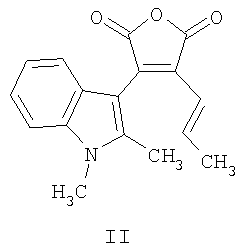
где R1=С1-С6алкил, R2=С1-С6алкил. Соединения I проявляют фотохромные и флуоресцентные свойства. Изобретение относится также к применению 3-(5-алкокси-1,2-диметил-1Н-индол-3-ил)-4-[(1E)-алк-1-енил]фуран-2,5-дионов выше приведенной общей формулы I в качестве флуоресцирующих фотохромов, которые могут быть использованы, например, в системах хранения и обработки информации, в частности, в качестве светочувствительной компоненты материала для трехмерной записи и хранения информации, а также могут быть использованы при создании элементной базы для молекулярных компьютеров, в частности в качестве молекулярных переключателей. Наиболее близким по выполнению и достигаемому результату является (1,2-диметил-1Н-индол-3-ил)-4-[(1Е)-проп-1-енил]фуран-2,5-дион (II)
проявляющий фотохромные свойства (полоса поглощения исходной формы Задачей изобретения является новые соединения в ряду 3-(1,2-диметил-1Н-индол-3-ил)-4-[(1Е)-алк-1-енил]фуран-2,5-дионов, проявляющие одновременно фотохромные и флуоресцентные свойства. Техническим результатом изобретения являются новые соединения в ряду 3-(1,2-диметил-1Н-индол-3-ил)-4-[(1E)-алк-1-енил]фуран-2,5-дионов, проявляющие фотохромные свойства и характеризующиеся полосой поглощения фотоиндуцированных изомеров в более длинноволновой области спектра, /что в результате приводит к увеличению интенсивности окрашивания/, а также проявляющие в исходной нециклической изомерной форме одновременно флуоресцентные свойства с достаточно высокими квантовыми выходами. Технический результат достигается соединениями общей формулы I и их применением в качестве флуоресцирующих фотохромов. Изобретение удовлетворяет критерию изобретательского уровня, так как не известны соединения ряда 3-(1,2-диметил-1Н-индол-3-ил)-4-[(1E)-алк-1-енил]фуран-2,5-дионов, проявляющие одновременно фотохромные и флуоресцентные свойства. Способ получения соединений I заключается во взаимодействии (3E)-алк-3-еновых кислот в присутствии триэтиламина с полученным in situ (5-алкокси-1,2-диметилиндол-3-ил)(оксо)ацетилхлоридом. Ниже приведены примеры получения соединений. Пример 1. 3-(5-Метокси-1,2-диметил-1Н-индол-3-ил)-4-[(1Е)-проп-1-енил]фуран-2,5-дион. (R1=R2=CH3). К раствору 0,53 г (3 ммоль) 5-метокси 1,2-диметилиндола в 5 мл сухого 1,2-дихлорэтана прикапывают 0,26 мл (3 ммоль) оксалил хлорида при 5°С, смесь перемешивают 10 минут при 5°С. В эту колбу при 5°С по каплям добавляют раствор 0,3 мл (3 ммоль) (3E)-пент-3-еновой кислоты и 1 мл (3.2 ммоль) триэтиламина в 7 мл 1,2-дихлорэтана. Реакционную смесь перемешивают 1 ч и раствор упаривали в вакууме. Остаток очищают колоночной хроматографией на силикагеле (элюент: хлороформ). Выход целевого продукта 0,26 г (28%). Красные кристаллы, т.пл. 185-187°С. Найдено, %: С 69,32, Н 5,41, N 4,46. Для С18H17NO4, вычислено, %: С 69,44, Н 5,50, N 4,50. ИК-спектр, см-1: 1750, 1820 (C=O). Спектр 1Н ЯМР, CDCl3, Соединения I в примерах 2-3 получены аналогично примеру 1 с использованием (3E)-гекс-3-еновой и (3E)-дец-3-еновой кислот соответственно. Пример 2. 3-[(1Е)-бут-1-енил]-4-(5-метокси-1,2-диметил-1Н-индол-3-ил)фуран-2,5-дион (R1=С2Н5, R2=CH3). Выход целевого продукта 0,32 г (32,7%). Красные кристаллы, т.пл. 175-177°С. Найдено, %: С 70,02, Н 5,63, N 4,21. Для C19H19NO4, вычислено, %: С 70,14, Н 5,69, N 4,30. ИК-спектр, см-1: 1750, 1820 (C=O). Спектр 1Н ЯМР, CDCl3, Пример 3. 3-(5-Метокси-1,2-диметил-1Н-индол-3-ил)-4-[(1Е)-окт-1-енил]фуран-2,5-дион (R1=С6Н13, R2=CH3). Выход 0,3 г (26.4%). Красные кристаллы, т.пл. 112-114°С. Найдено, %: С 72,86, Н 7,01, N 3,54. Для C23H27NO4 вычислено, %: С 73,00, Н 7,15, N 3,68. ИК-спектр, см-1: 1750, 1820 (C=O). Спектр 1Н ЯМР, CDCl3, У полученных соединений исследованы по стандартным методикам спектрально-абсорбционные и спектрально-флуресцентные характеристики в гептане при 293°К. Электронные спектры поглощения регистрировали на спектрофотометре «Cary 1000» (Varian). Флуоресцентные измерения проводили на спектрофлуориметре «Cary Eclips» (Varian). Значения квантовых выходов флуоресценции определяли методом Паркера – Риса с использованием 3-метоксибензантрона в толуоле (
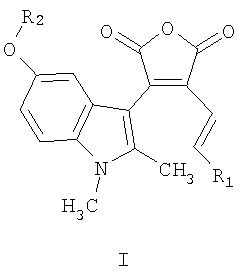
Исследуемые соединения получены в нециклической форме А. При облучении растворов этих соединений /форма А/ в полосах их длинноволнового поглощения ( Как следует из таблицы, для соединений 2-4 по сравнению с соединением 1 наблюдается более длинноволновое – на 36-38 нм, поглощение окрашенных изомеров 2В-4В. Такое изменение поглощения циклических изомеров В, в условиях когда поглощение нециклических форм А практически не изменилось, приводит к уменьшению перекрывания полос длинноволнового поглощения изомерных форм А и В для соединений 2-4. А это при наличии прямой и обратной фотореакций означает, что в случае соединений 2-4 достигается большая степень конверсии А Исследуемые соединения в своей нециклической форме А проявляют также флуоресцентные свойства. Как видно из таблицы, соединения 2-4 по сравнению с соединением 1 проявляют существенно более высокие значения квантовых выходов флуоресценции изомерных форм А. Квантовые выходы флуоресценции изомеров А для соединений 2-4 в 2,6-3 раза больше чем для описанного соединения 1.
Формула изобретения
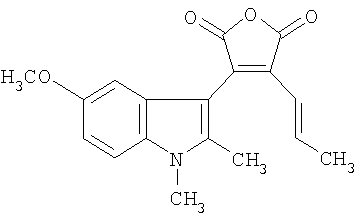
1. 3-(5-алкокси-1,2-диметил-1Н-индол-3-ил)-4-[(1Е)-алк-1-енил]фуран-2,5-дионы общей формулы
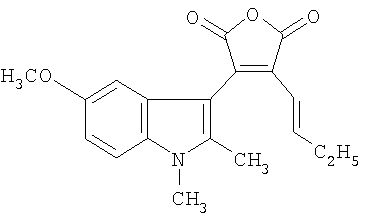
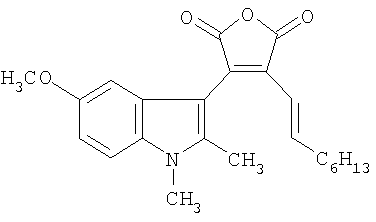
где R1=C1-C6 алкил, R2=С1-С6 алкил. 2. 3-(5-Алкокси-1,2-диметил-1Н-индол-3-ил)-4-[(1Е)-алк-1-енил]фуран-2,5-дионы по п.1, где R1=R2=СН3 – 3-(5-метокси-1,2-диметил-1Н-индол-3-ил)-4-[1(Е)-проп-1-енил]фуран-2,5-дион. 3. 3-(5-Алкокси-1,2-диметил-1Н-индол-3-ил)-4-[(1Е)-алк-1-енил]фуран-2,5-дионы по п.1, где R1=C2H5, R2=СН3 – 3-[(1Е)-бут-1-енил]-4-(5-метокси-1,2-диметил-1Н-индол-3-ил)фуран-2,5-дион. 4. 3-(5-Алкокси-1,2-диметил-1Н-индол-3-ил)-4-[(1Е)-алк-1-енил]фуран-2,5-дионы по п.1, где R1=C6H13, R1=CH3 – 3-(5-метокси-1,2-диметил-1Н-индол-3-ил)-4-[(1Е)-окт-1-енил]фуран-2,5-дион. 5. Применение в качестве флуоресцирующих фотохромов 3-(5-алкокси-1,2-диметил-1Н-индол-3-ил)-4-[(1Е)-алк-1-енил]фуран-2,5-дионов общей формулы
где R1=C1-С6 алкил, R2=С1-С6 алкил.
|
||||||||||||||||||||||||||||||||||||||||||||||||

 ,
, ,
,
 макс=436 нм, полоса поглощения циклической формы
макс=436 нм, полоса поглощения циклической формы 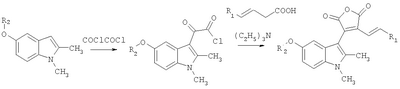
 , м.д.: 1,94 (д.д, 3H, J1=7.0 Гц, J2=l,7 Гц, CH3), 2.43 (с, 3H, CH3), 3,74 (с, 3H, CH3), 3,80 (с, 3H, CH3), 6,26 д.к, 1Н, J1=16,0 Гц, J2=1,7 Гц, СН), 6,79 (д, 1Н, J=2,4 Гц, СНаром), 6,90 (д.д, 1Н, J1=8,9 Гц, J2=2,4 Гц, СНаром), 7,10-7,30 (м, 2Наром).
, м.д.: 1,94 (д.д, 3H, J1=7.0 Гц, J2=l,7 Гц, CH3), 2.43 (с, 3H, CH3), 3,74 (с, 3H, CH3), 3,80 (с, 3H, CH3), 6,26 д.к, 1Н, J1=16,0 Гц, J2=1,7 Гц, СН), 6,79 (д, 1Н, J=2,4 Гц, СНаром), 6,90 (д.д, 1Н, J1=8,9 Гц, J2=2,4 Гц, СНаром), 7,10-7,30 (м, 2Наром). =0.1,
=0.1,  ·103, л·моль-1·см-1)
·103, л·моль-1·см-1)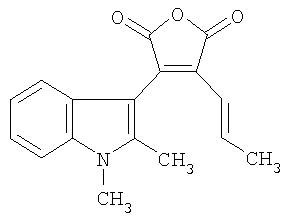
 А, приводящая систему в исходное состояние. Изомерные формы А и В термически устойчивы /после прекращения облучения содержание форм А и В со временем не меняется при повышении температуры/. То есть соединения проявляют фотохромные свойства и обладают свойством бистабильности – способностью существовать в двух устойчивых, структурно обусловленных состояниях.
А, приводящая систему в исходное состояние. Изомерные формы А и В термически устойчивы /после прекращения облучения содержание форм А и В со временем не меняется при повышении температуры/. То есть соединения проявляют фотохромные свойства и обладают свойством бистабильности – способностью существовать в двух устойчивых, структурно обусловленных состояниях.