Патент на изобретение №2313517
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ДИХЛОРГЛИОКСИМА
(57) Реферат:
Изобретение относится к усовершенствованному способу получения дихлорглиоксима. Способ заключается в том, что в суспензию глиоксима в концентрированном водном растворе хлористого кальция дозируют одновременно и пропорционально при перемешивании концентрированную соляную кислоту и пергидроль при мольном соотношении глиоксима, хлористого водорода и перекиси водорода соответственно 1,0:2,0…2,4:2,2…2,4, при весовом соотношении общего количества воды и хлористого кальция 1,2…2,8:1,0 при температуре 15…25°С. Способ обеспечивает получение целевого продукта с выходом 81-93%. 1 табл.
Предлагаемое изобретение относится к способу получения хлорглиоксимов – исходных веществ для получения функциональных производных глиоксимов, а также гетероциклических соединений: триазолов, тетразолов, 1,2,5-оксадиазолов и их N-оксидов [Ж. Всес. хим. о-ва им. Д.И.Менделеева, 2, 65, (1974)]. Известен способ получения дихлорглиоксима (ДХГ), хлорированием водного раствора Малый выход (около 50%) ДХГ, по мнению авторов, можно объяснить гидролизом исходного глиоксима, который ускоряется при повышении температуры. Известен способ получения ДХГ взаимодействием ди – N – окиси динитрила щавелевой кислоты с хлористым водородом [Angew. Chim. 75, 10, 450 (1963)]. Недостатком метода является получение ди-N-окиси динитрила и сложность работы из-за малой ее живучести при обычной температуре. Несмотря на хороший выход ДХГ этот способ не может быть использован для применения ДХГ в укрупненных количествах. Известно получение ДХГ хлорированием хлором фуроксанкарбоновой кислоты [Ponzio. de Paolini, Gazz, Chim. Ital; 56, 247-256 (1926)]. Недостатком метода является побочное образование хлорнитроловой кислоты, Известно получение ДХГ из глиоксима при действии хлора в 10%-ной соляной кислоте при охлаждении [Ponzio, F.Baldrocco, Gazz. Chim. Ital, 60, 429 (1930)]. По данным Унгнэйд и Киссенжера выход ДХГ не превышает 52% [Н.Е.Ungnade, W.Kissinger, Tetrahedron 19, Supple 1, 143 (1963)]. Этот метод выбран нами в качестве прототипа. Недостатками прототипа являются неудовлетворительный выход ДХГ, связанный с гидролизом глиоксима, и сложность аппаратурного оформления процесса, поскольку применение хлора требует применение баллонов, находящихся под давлением, и утилизации отходящих газов. Наличие побочного продукта реакции – хлористого водорода также является недостатком метода. Общим признаком заявляемого изобретения с прототипом является хлорирование глиоксима с применением соляной кислоты. Техническая задача заключается в получении высокого выхода ДХГ, в упрощении аппаратного оформления процесса и в исключении побочного продукта реакции – хлористого водорода. Технический результат предлагаемого изобретения достигается тем, что в суспензию глиоксима в концентрированном водном растворе хлористого кальция дозируют одновременно и пропорционально при перемешивании концентрированную соляную кислоту и пергидроль при мольном соотношении глиоксима, хлористого водорода и перекиси водорода соответственно 1,0:2,0…2,4:2,2…2,4, при весовом соотношении воды и хлористого кальция 1,2…2,8:1,0 при температуре 15…25°С. Для получения высокого выхода необходимым условием является соблюдение весового соотношения общего количества воды, вводимой в реакционную массу вместе со всеми компонентами, и хлористого кальция 1,2…2,8:1,0. Увеличение этого соотношения свыше 2,8:1,0 приводит к существенному снижению выхода независимо от количества используемых соляной кислоты и пергидроля, а уменьшение этого соотношения ниже 1,2:1,0 – к получению трудно перемешиваемой реакционной массы вследствие выпадения агломератов кристаллов хлористого кальция, шестиводного, т.е. делает процесс нетехнологичным. По приведенным данным наиболее приемлемым является использование общедоступной 36%-ной соляной кислоты и 30%-ного раствора перекиси водорода (пергидроля). Нижний предел значений для хлористого водорода соответствует стехиометрическому количеству, а верхний – стехиометрическому количеству с 20% избытком. Дальнейшее повышение избытка нежелательно, поскольку приводит к пенообразованию в конце процесса. Следует отметить, что при дозировке соляной кислоты в суспензию глиоксима в концентрированном растворе хлористого кальция и перекиси водорода наблюдается пенообразование, обусловленное частичным разложением перекиси водорода, катализируемое примесями металлов, внесенных в раствор хлористым кальцием. Выход дихлорглиоксима при этом снижается. При смешении реагентов оптимальной является температура в пределах от 15 до 25°С. При температуре ниже 15°С реакционная масса становится нетехнологичной, а свыше 25°С снижается выход ДХГ. Количество применяемого раствора хлористого кальция для суспендирования в нем глиоксима можно увеличить в 1,5 раза без существенного изменения выхода ДХГ (опыт 8). Дальнейшее увеличение количества этого раствора экономически нецелесообразно. Уменьшение делает реакционную массу вязкой и поэтому нетехнологичной. В отличии от прототипа разработанный метод описывается следующим уравнением: Согласно схеме весь хлористый водород полностью вступает в реакцию, что является достоинством предлагаемого метода. ПРИМЕР В суспензию 88 вес.ч. глиоксима в растворе 188 вес.ч. хлористого кальция в 226 вес.ч. воды при перемешивании одновременно и пропорционально, поддерживая температуру в пределах 15…25°С добавляют раствор 119 вес.ч. хлористого кальция в 223 вес.ч. 36%-ной соляной кислоты и раствор 145 вес.ч. хлористого кальция в 250 вес.ч. 30%-ной перекиси водорода. Реакционную массу выдерживают при температуре 18…20°С в течение 30 минут, отфильтровывают, полученные кристаллы промывают водой до исчезновения катиона кальция Са++ (2×500 вес.ч.) и сушат. Выход составил 153,9 г (98% от теоретического). Выделенные кристаллы имеют температуру плавления 206°С (с сублимацией). ИК-спектр вещества идентичен спектру дихлорглиоксима. Остальные примеры для наглядности представлены в таблице, в которой приведены конкретные весовые параметры техпроцесса получения дихлорглиоксима, осуществляемого в рамках заявляемого изобретения. Положительный эффект изобретения состоит в получении высокого выхода ДХГ, в отсутствии побочного продукта реакции – хлористого водорода и в упрощении аппаратурного оформления процесса, поскольку устраняется необходимость работы с газовыми баллонами. К достоинству метода следует отнести тот факт, что полученный дихлорглиоксим не требует очистки.
Формула изобретения
Способ получения дихлорглиоксима из глиоксима и соляной кислоты, отличающийся тем, что в суспензию глиоксима в концентрированном водном растворе хлористого кальция дозируют одновременно и пропорционально при перемешивании концентрированную соляную кислоту и пергидроль при мольном соотношении глиоксима, хлористого водорода и перекиси водорода соответственно 1,0:2,0 – 2,4:2,2…2,4, при весовом соотношении общего количества воды и хлористого кальция 1,2 – 2,8:1,0 при температуре 15 – 25°С.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 -глиоксимкарбоновой кислоты [Ponzio. de Paolini, Gazz, Chim. Ital; 56,252 (1926)].
-глиоксимкарбоновой кислоты [Ponzio. de Paolini, Gazz, Chim. Ital; 56,252 (1926)].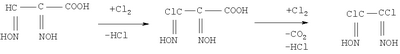
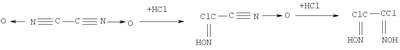
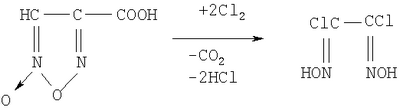
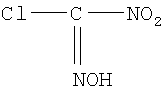 . К тому же фуроксанкарбоновая кислота не является доступным продуктом.
. К тому же фуроксанкарбоновая кислота не является доступным продуктом.