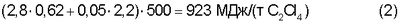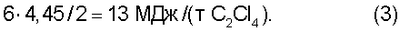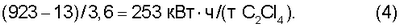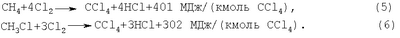Патент на изобретение №2313514
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ТЕТРАХЛОРЭТИЛЕНА ИЗ ХЛОРОРГАНИЧЕСКИХ ОТХОДОВ C1-C2
(57) Реферат:
Изобретение относится к способу получения тетрахлорэтилена из хлорорганических отходов С1-С2 и возвратного тетрахлорметана газофазной конверсией при температуре 450-600°С в присутствии акцептора хлора и избытке хлора в реакционных газах 10-15% масс. Причем процесс газофазной конверсии совмещают с экзотермической реакцией исчерпывающего хлорирования метана и/или хлорметана. Технический результат – обеспечение автотермичности процесса утилизации жидких и газообразных хлорорганических отходов производства хлорметанов путем совмещения с экзотермической реакцией исчерпывающего хлорирования метана и/или хлорметана, приводящее к получению целевого продукта тетрахлорэтилена и уменьшению образования высококипящих побочных хлорорганических веществ. 1 табл.
Изобретение относится к химической промышленности и может использоваться в хлорорганических производствах, в частности для утилизации хлорорганических отходов производства хлорметанов. Тетрахлорэтилен (перхлорэтилен) является хлорорганическим взрыво- и пожаробезопасным растворителем, который применяется для обезжиривания металлических поверхностей перед нанесением покрытий, очистки одежды в химчистках, а также как полупродукт в производстве фторуглеводородов. Промышленный способ получения тетрахлорэтилена из хлорорганических отходов C1-С3 включает исчерпывающее их хлорирование при температуре 500-600°С в полом аппарате или в аппарате с псевдоожиженным слоем песка и последующее разделение полученной смеси [Промышленные хлорорганические продукты. Справочник / Под ред. Л.А.Ошина. – М.: Химия, 1978. – С.187-196]. В таком процессе попутно образуется в значительных количествах тетрахлорметан, который Монреальским протоколом отнесен к озоно-разрушающим веществам и их производство запрещено. В связи с этим практический интерес представляют только способы получения тетрахлорэтилена, включающие одновременно и переработку тетрахлорметана. Известные способы получения тетрахлорэтилена из хлоруглеводородов, в том числе из тетрахлорметана, в зависимости от рабочей температуры процесса подразделяются на три группы: высокотемпературные, каталитические, среднетемпературные. К высокотемпературным относятся: – способ получения тетрахлорэтилена путем пиролиза тетрахлорметана в расплаве хлоридов щелочных или щелочно-земельных металлов при температуре 600-800°С [SU №201386, МПК С07С, опубл. 08.09.1967]; – способ получения тетрахлорэтилена пиролизом тетрахлорметана при температуре 800-900°С на углеродсодержащих частицах в присутствии хлорсодержащих алифатических соединений, хлора и/или хлористого водорода [SU №559639, МПК2 С07С 21/12, опубл. 25.05.1977]. Недостатками высокотемпературных способов являются образование углеродистых частиц и значительный расход электроэнергии, который составляет 400-450 кВт·ч на 1 тонну получаемого тетрахлорэтилена. К каталитическим относятся: – способ получения тетрахлорэтилена окислительным хлорированием низших алифатических хлоруглеводородов при температуре 400-475°С в присутствии катализатора реакции Дикона, который дополнительно содержит 0,5-1,5 вес.% гидроокиси рубидия [SU №521247, МПК2 С07С 21/04, С 17/15, опубл. 15.07.1976]; – способ получения тетрахлорэтилена на аналогичном катализаторе пиролизом тетрахлорметана при температуре 300-390°С [SU №713860, МПК2 С07С 21/12, С 17/24, опубл. 05.02.1980]; – способ получения тетрахлорэтилена хлорированием тетрахлорэтана при температуре 180-300°С в присутствии активного угля в адиабатическом режиме с рециркуляцией побочных продуктов реакции [SU №910574, МПК3 С07С 21/12, С 17/10, опубл. 07.03.1982]; – способ получения тетрахлорэтилена путем конверсии тетрахлорметана при температуре 250-400°С на медьсодержащем катализаторе в присутствии метана при мольном соотношении тетрахлорметан:метан 1:(1-2,5) соответственно [RU №2253648, МПК7 С07С 21/12, 17/26, 17/275, опубл. 2005.06.10]. Недостатком каталитических способов является постепенное снижение эффективности процесса из-за образования смолистых отложений на поверхности гетерогенного катализатора. К среднетемпературным относятся: – газофазное хлорирование хлоруглеводородов в полом реакторе при температуре до 600°С с последующей закалкой [Трегер Ю.А. Карташов Л.М., Кришталь Н.Ф. Основные хлорорганические растворители. – М.: Химия, 1984. – Стр.141-149]; Такие процессы по сравнению с каталитическими процессами более надежны, так как их осуществляют в полом реакторе без гетерогенного катализатора. Недостатком среднетемпературных процессов является существенный расход электроэнергии на нагрев реакционной массы до рабочей температуры из-за очень малого теплового эффекта реакции конверсии. В последней работе, которая взята в качестве прототипа, в трубчатом реакторе диаметром 30 мм и длиной 8,4 м исследован, в частности, процесс: При температуре t=560-580°C, давлении Р=3,0-3,5 ат, длительности реакции Из этих данных следует, что для получения 1 тонны тетрахлорэтилена ( Расчетный расход тепла составляет Тепловой эффект реакции (1) при получении 6 кмоль тетрахлорэтилена составляет Необходимый удельный расход электроэнергии на поддержание теплового режима реактора составляет Целью изобретения является обеспечение автотермичности процесса газофазной конверсии хлоруглеводородов C1-C2 и возвратного тетрахлорметана в тетрахлорэтилен. Поставленная цель достигается тем, что процесс газофазной конверсии исходных хлоруглеводородов C1-C2 и возвратного тетрахлорметана совмещают с экзотермическим процессом исчерпывающего хлорирования дополнительного количества метана и/или хлорметана. Реакции исчерпывающего хлорирования метана и хлорметана записываются: В качестве источника метана и хлорметана можно использовать, например, газовые сдувки производства хлорметанов, с которыми из системы циркуляции газов выводятся инертные компоненты. В качестве источника хлора можно использовать испаренный хлор, используемый в производстве хлорметанов или хлор-газ с инертными компонентами, который остается после получения сжиженного хлора. В таблице приведен материальный баланс получения 1 тонны тетрахлорэтилена из жидких и газообразных хлорорганических отходов производства хлорметанов с использованием испаренного хлора.
Для нагрева реагентов на 500 градусов требуется тепловая энергия в количестве 1511 МДж/т. Тепловой эффект химических реакций составляет 1661 МДж/т, что обеспечивает автотермичность совмещенного процесса. Хлор, метан и хлорметан, которые дополнительно вводят в реактор, относятся к инициаторам радикальных реакций. В исходной реакционной массе мольное соотношение инициаторы:хлоруглеводороды в условиях прототипа составляет максимум 0,6/3=0,2, а в совмещенном процессе оно равно (22,79+9,95-2,51)/(5,21+7,38)=2,4, т.е. на порядок выше. Это дает возможность проводить совмещенный процесс по сравнению с прототипом при пониженной температуре с меньшим образованием высококипящих побочных хлорорганических веществ. Способ позволяет утилизировать как жидкие, так и газообразные хлорорганические отходы C1-C2 производства хлорметанов.
Формула изобретения
Способ получения тетрахлорэтилена из хлорорганических отходов C1-C2 и возвратного тетрахлорметана газофазной конверсией при температуре 450-600°С в присутствии акцептора хлора и избытке хлора в реакционных газах 10-15 мас.%, отличающийся тем, что процесс газофазной конверсии совмещают с экзотермической реакцией исчерпывающего хлорирования метана и/или хлорметана.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

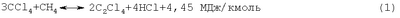
 =11-13 с и количестве метана от стехиометрии
=11-13 с и количестве метана от стехиометрии  =0,17-0,49 конверсия тетрахлорметана за проход составляла 50-60%, а селективность образования тетрахлорэтилена по углероду на израсходованные тетрахлорметан и метан находилась на уровне 50%. При повышении количества метана от стехиометрии
=0,17-0,49 конверсия тетрахлорметана за проход составляла 50-60%, а селективность образования тетрахлорэтилена по углероду на израсходованные тетрахлорметан и метан находилась на уровне 50%. При повышении количества метана от стехиометрии 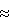 6 кмоль) необходимо нагреть примерно 2,8 тонны (
6 кмоль) необходимо нагреть примерно 2,8 тонны (