Патент на изобретение №2312135
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ШТАММ БАКТЕРИЙ PAENIBACILLUS CAMPINASENSIS – ПРОДУЦЕНТ ЦИКЛОДЕКСТРИНГЛЮКАНОТРАНСФЕРАЗЫ
(57) Реферат:
Изобретение относится к биотехнологии и касается нового штамма бактерий, продуцирующего циклодекстринглюканотрансферазу (ЦГТазу К.Ф.2.4.1.19), с повышенной специфичностью в отношении образования бета-циклодектрина. Штамм бактерий Paenibacillus campinasensis ИБ-10155 депонирован и хранится в Коллекции микроорганизмов Института биологии УНЦ РАН. Активность бета-ЦГТазы в культуральной жидкости 5,8 ед/мл. За единицу принято количество ЦГТазы, катализирующее образование 1 мкМ АСВ бета-циклодекстрина в течение 1 минуты из 2% раствора крахмала при рН 6.0. Доля бета-циклодекстрина в сумме других циклических продуктов превышает 70%. Изобретение обеспечивает высокую термостабильность ЦГТазы, катализирующую реакцию трансформации крахмала в бета-ЦД при относительном постоянстве доли этого продукта в сумме других циклических декстринов на разных стадиях реакции. 2 табл.
Изобретение относится к биотехнологии, а именно к технологии получения препаратов циклодекстринглюканотрансферазы (ЦГТаз К.Ф.2.4.1.19), фермента для получения циклодекстринов из крахмала. В частности, изобретение относится к технологии бета-циклодекстринглюканотрансферазы (бета-ЦГТазы), трансформирующей крахмал преимущественно в бета-циклодекстрин. Этот циклический олигосахарид наиболее востребован в пищевой, фармакологической, текстильной промышленности, косметике и др. [1-3] ЦГТазы катализируют образование одновременно трех макроциклических олигосахаридов (или циклодекстринов, отличающихся своими молекулярными размерами и свойствами. Бета-циклодекстрин состоит из семи остатков альфа-D-глюкозы, в то время как альфа- и гамма- макроциклические гомологи имеют в кольцах своих молекул шесть и восемь глюкопиранозных звеньев. Из-за универсальной способности образовывать комплексы включения с целым спектром органических и неорганических соединений бета-циклодекстрин востребован на рынке и промышленно выпускается в больших объемах [4]. Сырьем для получения циклодекстринов является крахмал, а в результате реакции образуется смесь альфа-, бета- и гамма-циклодекстринов, а также смесь линейных и разветвленных декстринов различного молекулярного размера. Выход и соотношение количества синтезированных индивидуальных циклических олигосахаридов зависит от каталитических свойств использованной ЦГТазы. Имеющаяся информация о продуцентах и каталитических свойствах ЦГТаз и, в частности бета-ЦГТаз, не позволяет провести их объективное сравнение потому, что эти анализы были выполнены в неидентичных условиях и разных лабораториях. Между тем, характер и глубина реакции ферментативной трансформации крахмала в циклодекстрины существенно зависят от многих составляющих: природы и источника крахмала, соотношения в нем амилопектина и амилозы, режима предобработки крахмала перед ферментативной реакцией, от рН среды, температуры, дозировок фермента и др. Объективная сравнительная информация о каталитических свойств различных препаратов ЦГТаз также не может быть получена из-за ограниченной доступности как образцов ферментов, так и их продуцентов, отсутствия методических стандартов при измерении циклизующей активности. Тем не менее, среди главных критериев, определяющих эффективность продуцентов бета-ЦГТаз, находятся: селективность ЦГТазы в отношении синтеза бета-ЦД, общий выход бета-ЦД, их термостабильность. Известны штаммы бактерий вида Paenibacillus macerans (устаревшее название Bacillus macerans) и Bacillus sterothermophilus, образующие ЦГТазы, катализирующие образование, преимущественно, альфа-циклодекстрина [3]. В процессах получения бета-циклодекстринов эти ферменты могут использоваться лишь в технологии с использованием органических сольвентов, зачастую весьма токсичных, таких, например, как толуол [3, 5]. Бета-циклодекстрин, полученный в контакте с толуолом, не отвечает современным требованиям экологической безопасности конечного продукта. Известны штаммы Bacillus sp., Bacillus circulans и Bacillus alkalophilus, [3, 5, 6], для которых характерно образование бета-специфичных ЦГТаз, катализирующих главным образом синтез бета-циклодекстрина в сумме трех макроциклических олигосахаридов. Бета-ЦГТазы также отличаются более глубокой степенью (по сравнению с ЦГТазами Paenibacillus macerans) транс-трансформации крахмала в циклические продукты. Названные культуры как продуценты ЦГТ-аз приемлемы для процессов получения бета-циклодекстрина по бессольвентной технологии. Наиболее близким аналогом по совокупности существенных признаков и достигаемому результату является штамм Bacillus sp.(депонированный во Всероссийской коллекции промышленных микроорганизмов под номером ВКМ Б-1793Д), образующий внеклеточную бета-ЦГТазу, основным продуктом которой при воздействии на крахмал является бета-циклодекстрин [7]. Недостатком ЦГТазы, продуцируемой культурой, является ее сравнительно низкая термостабильность. Другим недостатком бета-ЦГТазы штамма Bacillus sp ВКМ Б-1793Д является то, что доля бета-циклодектрина в сумме других циклических олигосахаридов непрерывно меняется процессе ферментативной реакции. Выраженное непостоянство в соотношении между циклодекстринами в конверсионной смеси приводит к технологической нестабильности на стадии выделения и очистки конечного продукта – кристаллического бета-циклодекстрина. Задачей, на решение которой было направлено заявляемое изобретение, являлся поиск природного штамма, обеспечивающего синтез внеклеточной бета-ЦГТАзы, обладающей достаточной термостабильностью, катализирующий реакцию трансформации крахмала в бета-ЦД при относительном постоянстве доли этого продукта в сумме других циклических декстринов на разных стадиях реакции. Технический результат, который может быть получен при осуществлении изобретения, заключается в обнаружении культуры микроорганизмов, обладающих способностью к образованию ЦГТазы, пригодной для синтеза бета-циклодекстрина при температуре не менее 55°С и катализирующей реакцию трансформации крахмала до получения конверсионной смеси при относительном постоянстве доли бета-ЦД. Сущность объекта изобретения – штамм Paenibacillus campinasensis ИБ-10155. Новый штамм ИБ-10155 выделен из образца почвы, отобранного в Кармаскалинском районе (д.Старо-Мусино) Республики Башкортостан, путем микроаэрофильной накопительной культуры на элективной питательной среде, содержавшей минеральные буферные компоненты и циклодекстрин в качестве единственного источника углерода и энергии. Морфологические признаки штамма. Клетки палочковидные, размером 0,3-0,6·2-3,5 мкм через 24 ч инкубации при 37°С подвижные, грамвариабельные. Образуют эндоспоры. Спорообразование терминальное и субтерминальное, споры эллиптические, спорангий раздувающий. Штамм при росте на мясопептонном агаре (МПА) через сутки при 37°С образует плоские полупрозрачные колонии размером в диаметре 3-5 мм с ровным краем и гладкой поверхностью, с консистенцией сливочного масла. На влажном картофельно-глюкозном агаре при упомянутых выше условиях штамм формирует плоские, неправильной формы и размером 5-10 мм, прозрачные, беловатого цвета мигрирующие колонии, большинство из которых обладает нечетко оформленным центром с радиально мигрирующими микроколониями. Описанный характер роста колоний нарушается при использовании подсушенного агара или при температуре выше 45°С. В жидком мясопептонном бульоне культура образует слизь. Как в жидкой, так и на плотной среде культура не образует пигментов. Биохимические признаки штамма Аэроб, но способен к аноксическому росту в присутствии нитратов. Реакция Фогес-Проскауэра (образование ацетилметилкарбинола) отрицательная, рН в бульоне Фогес-Проскауэра после роста <6 (5,95). Реакция на каталазу суточной культуры положительная. Штамм образует кислоту (но не газ) из глюкозы, ксилозы, арабинозы и маннита. Способен к сбраживанию этих сахаров при посеве уколом в столбике агара. Гидролизует (вызывает деполимеризацию) крахмал, казеин и слабо желатин. Не утилизирует цитрат, тирозин и фенилаланин. Мочевину не разлагает, индол не образует. Восстанавливает нитраты до нитритов. Штамм способен к росту в питательном бульоне с 7% NaCl. Хорошо растет в интервале рН 7,4-10,0 с оптимумом 9-9,5. Температурный интервал для роста 20-46°С с оптимумом 38-40°С. Штамм может храниться без потери полезных свойств при температуре 5-10°С на картофельно-глюкозном (или картофельном) агаре не менее 6 месяцев с обязательным пересевом не реже 1 раза в 3 месяца. Филогенетические характеристики штамма. Сравнение последовательности 1484 нуклеотидов участка гена, кодирующего 16S рРНК, штамма ИБ-10155 выявило 99,7% сходство с участком аналогичной последовательности (номер последовательности в Генбанке AF021924), обнаруженной ранее у типового штамма Paenibacillus campinasensis, депонированного в Корейской коллекции типовых культур КСТС под номером 0364BPT. На основании изучения совокупности морфологических, биохимических и филогенетических характеристик описываемой культуры новый штамм, продуцирующий бета-ЦГТазу, был идентифицирован как Paenibacillus campinasensis ИБ-10155. Для роста культуры и биосинтеза бета-циклодекстринглюканотрансферазы источником углерода могут служить крахмал, гидролизованный крахмал, кукурузная и другая зерновая мука, отходы производства кукурузы, картофель, или же их экстракты. Источниками азота могут служить пептон, дрожжевой экстракт, кукурузный экстракт, дрожжевые клетки, аммонийный азот. В качестве минеральных добавок может использоваться двузамещенный фосфат калия, сода, карбонат кальция. Культивирование штамма осуществляют в аэробных условиях в ферментере или колбах при температуре 40°С в течение 64-72 часов, рН среды 8-9,5. В процессе культивирования осуществляется контроль за активностью бета-ЦГТазы в культуральной жидкости. Возможность использования изобретения иллюстрируется примерами, которые не ограничивают объем и сущность притязаний, связанных с ними. Пример 1. Иллюстрируется возможность получения жидкого ферментного препарата бета-ЦГТазы путем культивирования патентуемого штамма в колбах на качалках с последующим сгущением ферментационной жидкости на модуле ультрафильтрации. Посевной материал получают выращиванием штамма на твердой питательной среде состава: крахмал растворимый 1%; пептон 0,4%, дрожжевой экстракт 0,5%, фосфат калия двузамещенный 0,2, карбонат натрия 0,3% агар 1,6%, рН среды 8,6-9,0. Колбы с жидкой средой того же состава, но не содержащей агара, инокулируют биомассой отдельных колоний. Культивирование проводят в 250 мл колбах, содержащих 60 мл стерильной среды, на качалке с 240 об/мин при 40°С в течение 64-72 часов. Активность бета-ЦГТазы в культуральной жидкости и количество единиц фермента при дозировании определяют по способности исследуемого препарата катализировать образование бета-циклодекстрина из 2% раствора крахмала. За единицу активности принимают такое количество фермента, которое в течение 1 минуты при 50°С катализирует образование 1 мкМ бета-ЦД из 2% картофельного крахмала. Ферментативную реакцию осуществляют смешиванием двух объемов 3%-го свежеприготовленного растворимого картофельного крахмала в 0,1 М ацетатном буфере при рН 5,7 с одним объемом раствора фермента (КЖ), разбавленным ацетатным буфером в 50-400 раз. Пробирку с реакционной смесью термостатируют в течение 60 минут при 50°С в твердотельном термостате. Порцию реакционной смеси в объеме 500 мкл добавляют к 3000 мкл измерительного раствора, приготовленного на основе 0,1 М углекислого калия и 0,4% спиртового фенолфталеина. Полученный раствор перемешивают и определяют поглощение полученной смеси D1 при 553 нм в стеклянной кювете с длиной оптического пути 1 см. Концентрацию фенолфталеина в измерительном растворе подбирают таким образом, чтобы в момент определения активности оптическая плотность этой жидкости составляла величину E553=1,00±0,1. Контролем служит проба смеси фермента с крахмалом, идентичная той, что была использована в опыте, но не прошедшая 1 часовую термическую обработку при 50°С. Порцию жидкости контрольного образца смешивают с измерительным раствором, аналогично тому, как это было сделано с реакционной смесью, после чего проводят измерение оптической плотности полученной контрольной смеси D2 при 553 нм. Активность фермента определяют по формуле (I): где N – степень разбавления фермента. Средние величины бета-ЦГТазной активности патентуемого штамма и других циклодекстриногенных микроорганизмов, использованных с целью сравнения, измеренные в культуральной жидкости через 70 часов роста, даны в таблице 1. Средняя активность бета-ЦГТазы Paenibacillus campinasensis ИБ-10155 в бесклеточной культуральной жидкости составляет величину 5,8±1,0 ед/мл. Пример 2. В сопоставимых условиях измерений, демонстрируются каталитические особенности бета-ЦГТазы Paenibacillus campinasensis ИБ-10155 в сравнении с действием бета-циклизующих ферментов из других продуцентов (таблица 1). Опыт выполняют следующим образом. В пластиковые пробирки объемом 5 мл помещают по 2 мл 4% картофельного крахмала в 50 мМ ацетатном буфере рН 6,0, подвергнутого 30 минутному автоклавированию при 120°С. В эти же пробирки дозируют порции растворов бета-ЦГТаз, полученных из различных источников, чтобы достичь соотношения 1, 2, 4, 8, 15, 30 ед. бета-ЦГТазы на 1 г АСВ крахмала в пробирке. Туда же также вводят порции консерванта, предотвращающего микробный рост. Для выравнивания концентрации субстрата (крахмала) до 2,75% по АСВ во все пробирки добавляют расчетные порции 50 мМ ацетатного буфера рН 6,0. Через 24 часа экспозиции при 50°С из полученных растворов отбирают по 900 мкл жидкости, которую смешивают со 90 мкл 10 мас.% ксилозы (внутреннего стандарта), с 990 мкл ацетонитрила. Образовавшийся осадок отделяют центрифугированием и далее супернатант анализируют методом ВЭЖХ на колонке с аминированным силикагелем. В качестве элюэнта используют смесь ацетонитрил-вода в соотношении 60:40. Концентрацию циклодекстринов в пробах рассчитывают методом внутреннего стандарта по площадям пиков программно-аппаратными средствами. Выход ЦД в опытах, характеризовавшихся максимальным выходом суммы циклических продуктов, а также другие расчетные параметры, определенные в этом примере, также представлены в таблице 1. Пример 3. Демонстрируется устойчивость ЦГТазы Paenibacillus campinasensis ИБ-10155 к термическому воздействию в сравнении с ферментами других продуцентов. Опыт выполняют с использованием образцов препаратов ЦГТаз, разбавленных 50 мМ ацетатным буфером при рН 6,0 до удельной активности 1,0 ед/мл, без добавления стабилизаторов (солей кальция). Пробирки с одинаковыми объемами разведении исследуемого фермента 1000 мкл помещают в твердотельный термостат и инкубируют при 55°С. Через определенные интервалы времени термообработанные образцы извлекают и измеряют в них остаточную бета-ЦГТазную активность согласно процедуре, описанной в примере 1. Время инактивации 50% активности ферментных препаратов различных продуцентов в условиях настоящего опыта, измеренное методом графической экстраполяции и интерполяции, представлено в таблице 1. Пример 4. Демонстрируется относительное постоянство доли бета-циклодекстрина на разных стадиях ферментативного воздействия при обработке крахмала ферментом в сравнении с ЦГТазой Bacillus sp. BKM Б-1793Д в условиях избыточных дозировок ферментов. В два стеклянных реактора объемом 200 мл, снабженных устройствами перемешивания и термостатирования, вносят раствор картофельного крахмала, подвергнутого 30 минутной обработке при 120°С, и ацетат натрия. В реакторы добавляют образцы лиофильно высушенных ферментных препаратов бета-ЦГАаз Paenibacillus campinasensis ИБ-10155 и Bacillus sp. BKM Б-1793Д. Дозировку ферментов подбирают по количеству субстрата, внесенного в реактор, при этом она составляет 30 ед. бета-ЦГТазы на 1 грамм АСВ крахмала. В реактор также добавляют 50 мМ ацетатный буфер для достижения требуемых концентраций ингредиентов, которые составляют: по крахмалу 2,75 мас.% (по АСВ), по ацетату натрия – 50 мМ. Стартовое значение рН смеси должно составлять величину 6,00±0,05. Через определенные промежутки времени из реактора извлекают объемы жидкости, останавливают в них ферментативную реакцию добавлением 50 об.% ацетонитрила и измеряют концентрацию циклодекстринов методом ВЭЖХ, как это описано в примере 2. Результаты определения, показанные в таблице 2, свидетельствуют о том, что при использовании ЦГТазы патентуемого штамма Paenibacillus campinasensis ИБ-10155 (в сравнении с циклизующим ферментом штамма-прототипа Bacillus sp. BKM Б-1793Д) наблюдается более высокий выход суммы циклических продуктов по отношению к крахмалу при относительном постоянстве доли бета циклодекстрина в продуктах конверсии.
Источники информации 1. Szente L., Szejtli J. Cyclodextrins as food ingredients. Trends in Food Science & Technology (2004), v15, p.137-142. 2. Szeitli J. Cyclodextrins in the Textile Industry. Starch/Starke (2003) v.55 p.191-196. 4. Абелян В.А. Циклодекстрины: Получение и применение. Изд. Дом “Ван-Арьян”, Ереван, 2001, 519 с. 5. Szeitli J. Cyclodextrin technology. Kluwer academic publishers, 1989. 450 p. 6. Патент России N2244742, кл. С12N 1/20, 2000. 7. Авторское свидетельство SU 1738852 A1, кл. С12N 9/10, 1990.
Формула изобретения
Штамм бактерий Paenibacillus campinasensis, Коллекция микроорганизмов Института биологии УНЦ РАН ИБ-10155 – продуцент бета-циклодекстринглюканотрансферазы.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

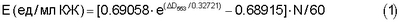
 D553=(D2-D1) – разность оптической плотности между измеряемым и контрольным растворами;
D553=(D2-D1) – разность оптической плотности между измеряемым и контрольным растворами;