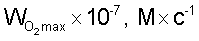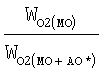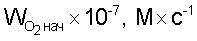|
|
(21), (22) Заявка: 2006108715/13, 20.03.2006
(24) Дата начала отсчета срока действия патента:
20.03.2006
(46) Опубликовано: 10.12.2007
(56) Список документов, цитированных в отчете о
поиске:
RU 2077558 C1, 20.04.1997. RU 2157829 C1, 20.10.2000. RU 2181757 C2, 27.04.2002. ЭМАНУЭЛЬ Н.М., ЛЯСКОВСКАЯ Ю.Н. “Торможение процессов окисления жиров”, М., Пищепромиздат, 1961, с.236-282.
Адрес для переписки:
625000, г.Тюмень, ул. Володарского, 38, ТюмГНГУ, патентно-информационный отдел
|
(72) Автор(ы):
Перевозкина Маргарита Геннадьевна (RU),
Сторожок Надежда Михайловна (RU)
(73) Патентообладатель(и):
Государственное образовательное учреждение высшего профессионального образования “Тюменский государственный нефтегазовый университет” (RU)
|
(54) СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ
(57) Реферат:
Изобретение относится к масложировой промышленности, а именно к способам защиты липидов, масел и жиров от окисления. Состав включает в себя  -токоферол и синергист антиоксиданта. При этом в качестве синергиста антиоксиданта используют N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферол и синергист антиоксиданта. При этом в качестве синергиста антиоксиданта используют N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил)пропановой кислоты бромид. Заявленный состав добавляют в количестве 0,04-0,28% от массы липидов. При этом все компоненты взяты при определенном соотношении. Изобретение позволяет снизить скорость процесса окисления липидов в 2-5 раз, а также снизить уровень гидропероксидов, образующихся в процессе окисления липидов, на 51,0%. 3 табл. ‘-(3,5-дитретбутил-4-гидроксифенил)пропановой кислоты бромид. Заявленный состав добавляют в количестве 0,04-0,28% от массы липидов. При этом все компоненты взяты при определенном соотношении. Изобретение позволяет снизить скорость процесса окисления липидов в 2-5 раз, а также снизить уровень гидропероксидов, образующихся в процессе окисления липидов, на 51,0%. 3 табл.
Изобретение относится к области пищевой технологии, а именно к способам защиты липидов, масел, жиров от окисления и окислительной деструкции, и может быть использовано в пищевой, косметической и химико-фармацевтической промышленности для получения стабильных липидосодержащих пищевых добавок (нутрицевтиков), лечебно-косметических средств и лекарственных препаратов.
Во всем мире ведется целенаправленный скрининг (отбор) полифункциональных стабилизаторов, лекарств антиоксидантного действия, синергических смесей. Использование синергических смесей позволяет получать высокоэффективные композиции и при этом снижать количество антиоксиданта.
Известен состав для стабилизации липидов, включающий следующие компоненты, масса в %:
 -токоферол (или -токоферол (или  -токоферола ацетат) -токоферола ацетат) |
2,4-80,0 |
| бензафлавин |
2,3-76,9 |
| лецитин |
8,3-93,8, |
добавляемые в количестве 0,4-5,2% от массы липидов /Патент 2077558 RU, МПК6 С11В 5/00, опубликованный 20. 07. 1996 г./.
Указанный состав тормозит процесс окисления липидов за счет антиоксидантного действия ингибиторов природного происхождения  -токоферола (6-гидрокси-2,5,7,8-тетраметил-2-фитил-хромана, витамина Е), бензафлавина (аналога витамина В2) и лецитина (яичного фосфатидилхолина). В составе указанной композиции бензафлавин и лецитин проявляют по отношению к -токоферола (6-гидрокси-2,5,7,8-тетраметил-2-фитил-хромана, витамина Е), бензафлавина (аналога витамина В2) и лецитина (яичного фосфатидилхолина). В составе указанной композиции бензафлавин и лецитин проявляют по отношению к  -токоферолу или -токоферолу или  -токоферола ацетату синергическое действие. Однако практическое применение указанной синергической смеси затруднено в силу многокомпонентности ее состава, отсутствия промышленного производства бензафлавина, дороговизны препаратов, получаемых в экспериментальном производстве. -токоферола ацетату синергическое действие. Однако практическое применение указанной синергической смеси затруднено в силу многокомпонентности ее состава, отсутствия промышленного производства бензафлавина, дороговизны препаратов, получаемых в экспериментальном производстве.
В связи с этим целесообразен поиск высокоэффективных синергических смесей, способных значительно тормозить окисление жиров, масел, липидов, применяемых в качестве основ фармпрепаратов, пищевых добавок, разнообразной косметической продукции, но более простых по составу и доступных для практического применения.
Задачей заявляемого изобретения является расширение ассортимента эффективных смесей природных и синтетических антиоксидантов, экономия использования дорогостоящих соединений, достижение ингибирующего эффекта меньшим количеством антиоксиданта.
Техническим результатом изобретения является упрощение состава и повышение его ингибирующего эффекта при наименьших концентрациях антиоксидантов.
Указанный технический результат достигается тем, что в составе для стабилизации липидов, включающем  -токоферол и синергист антиоксиданта, особенностью является то, что в качестве синергиста антиоксиданта использован N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферол и синергист антиоксиданта, особенностью является то, что в качестве синергиста антиоксиданта использован N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид при следующих соотношениях компонентов в смеси, масса в %: ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид при следующих соотношениях компонентов в смеси, масса в %:
 -токоферол -токоферол |
29,4-93,8 |
| N,N-диметил-N-гексадецил-аминоэтиловый |
|
эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) ‘-(3,5-дитретбутил-4-гидроксифенил) |
|
| пропановой кислоты бромид |
6,2-70,6, |
добавляемых в количестве 0,04-0,28% от массы липидов.
Отличие заявляемого состава от известного состоит в том, что вместо бензафлавина и лецитина используют N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид. Предлагаемое соединение N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид. Предлагаемое соединение N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид было синтезировано в Институте биохимической физики (ИБХФ) им. Н.М.Эмануэля РАН на основе фенозана (метилокса) ( ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид было синтезировано в Институте биохимической физики (ИБХФ) им. Н.М.Эмануэля РАН на основе фенозана (метилокса) (
Предложенное производное фенозана, в отличие от  -токоферола, обладает бифункциональными свойствами – антиокислительным действием и наличием в молекуле положительно заряженного атома азота, позволяющего удерживать ее на поверхности клеточных мембран с фиксацией на определенном месте за счет липовильного фрагмента (поплавковый эффект). Подобная структура обеспечивает адресную посылку антиоксидантов и создает возможность использования их для подавления патологических процессов в клетке организма, при которых нарушаются проницаемость клеточных мембран и интенсифицируются процессы перекисного окисления липидов. -токоферола, обладает бифункциональными свойствами – антиокислительным действием и наличием в молекуле положительно заряженного атома азота, позволяющего удерживать ее на поверхности клеточных мембран с фиксацией на определенном месте за счет липовильного фрагмента (поплавковый эффект). Подобная структура обеспечивает адресную посылку антиоксидантов и создает возможность использования их для подавления патологических процессов в клетке организма, при которых нарушаются проницаемость клеточных мембран и интенсифицируются процессы перекисного окисления липидов.
На основе такого подхода новое производное фенозана может применяться для лечения заболеваний, вызываемых вирусом иммунодефицита, цитомегаловирусом, а также при воспалительных заболеваниях, вызванных грамположительными бактериями (стафилококки, менингококки) и др.
Предлагаемое соединение N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид проявляет активность в реакции с пероксильными радикалами и обладает дополнительно способностью непосредственно взаимодействовать с гидропероксидами, разрушая их без образования свободных радикалов, что не наблюдается в присутствии ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид проявляет активность в реакции с пероксильными радикалами и обладает дополнительно способностью непосредственно взаимодействовать с гидропероксидами, разрушая их без образования свободных радикалов, что не наблюдается в присутствии  -токоферола. Разрушение гидропероксидов под влиянием изучаемого соединения, в свою очередь, является причиной выигрыша в периодах индукции и обеспечения высокой эффективности соединения по сравнению с прототипом. -токоферола. Разрушение гидропероксидов под влиянием изучаемого соединения, в свою очередь, является причиной выигрыша в периодах индукции и обеспечения высокой эффективности соединения по сравнению с прототипом.
Для предлагаемого синтетического антиоксиданта имеет место положительная корреляционная связь между концентрацией и величиной ингибирующего эффекта, что не наблюдается для  -токоферола, указанная зависимость имеет экстремальный характер и при высоких концентрациях антиоксидантное действие -токоферола, указанная зависимость имеет экстремальный характер и при высоких концентрациях антиоксидантное действие  -токоферола сменяется на проантиоксидантное. -токоферола сменяется на проантиоксидантное.
Минимальная токсичность и высокие антиоксидантные свойства позволяют широко использовать N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид в составе смеси с ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид в составе смеси с  -токоферолом в косметической и химико-фармацевтической промышленности для получения стабильных липидосодержащих лечебно-косметических средств и лекарственных препаратов. -токоферолом в косметической и химико-фармацевтической промышленности для получения стабильных липидосодержащих лечебно-косметических средств и лекарственных препаратов.
– изучалась кинетика поглощения кислорода при инициированном окислении липидных субстратов различного происхождения в присутствии предлагаемого состава и прототипа;
– тестировалась кинетика накопления первичных продуктов окисления – гидропероксидов методом йодометрического титрования (ПЧ) при аутоокислении липидов при повышенных температурах (60±0,2°С).
Изучение кинетики поглощения кислорода проводилось манометрическим методом в установках типа Варбурга при инициированном окислении липидов в присутствии инициатора азобисизобутиронитрила (АИБН) в концентрации 3 мМ при температуре 60±0,2°С. Контролем служили образцы липидов без добавок антиоксидантов.
Эффективность индивидуальных компонентов и их комбинаций исследовалась в широком диапазоне концентраций и соотношений компонентов:
 -токоферол -токоферол |
0,10-8,0 мМ |
| N,N-диметил-N-гексадецил-аминоэтиловый |
|
эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) ‘-(3,5-дитретбутил-4-гидроксифенил) |
|
| пропановой кислоты бромид |
0,05-1,50 мМ, |
добавляемых в количестве 0,02-1,29% от массы липидов.
В присутствии определенной добавки ингибиторов окисления  -токоферола, N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола, N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, смеси ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, смеси  -токоферола и N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола и N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, а также прототипа записывалась кинетика окисления с использованием вышеописанных методов. На основании полученных данных строились кинетические кривые поглощения кислорода (О2, мм3) либо накопления пероксидов (г I2/100 г липида). ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, а также прототипа записывалась кинетика окисления с использованием вышеописанных методов. На основании полученных данных строились кинетические кривые поглощения кислорода (О2, мм3) либо накопления пероксидов (г I2/100 г липида).
Из кинетических кривых определялись периоды индукции ( ), за которые принимали: ), за которые принимали:
– время (в мин), за которое процесс инициированного окисления липидов достигал максимальной скорости ( инд); инд);
– время (в часах) накопления пероксидов, количественно соответствующих значению ПЧ 0,1% I2.
Эффективность совместного ингибирующего действия смеси количественно характеризовали абсолютным значением разности (  ) периодов индукции окисления метилолеата (МО) в присутствии композиции антиоксидантов (АО) ( ) периодов индукции окисления метилолеата (МО) в присутствии композиции антиоксидантов (АО) (  ) и простой суммы индивидуальных компонентов ( ) и простой суммы индивидуальных компонентов (  i) (аддитивное действие) ( i) (аддитивное действие) (  = =  – –  i) либо выражали в относительных единицах – ( i) либо выражали в относительных единицах – (  / /  i)100%. Выполнение неравенства i)100%. Выполнение неравенства   > >  i свидетельствовало о проявлении синергизма в совместном действии компонентов, а i свидетельствовало о проявлении синергизма в совместном действии компонентов, а   < <  i – об эффекте антагонизма. i – об эффекте антагонизма.
Критерием антиоксидантного действия служили начальная 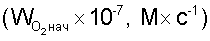 и максимальная и максимальная 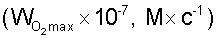 скорости процесса окисления в присутствии и в отсутствии антиоксиданта. Эффективность стабилизации окисления определяли также по величине скорости процесса окисления в присутствии и в отсутствии антиоксиданта. Эффективность стабилизации окисления определяли также по величине 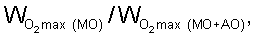 количественно характеризующей степень уменьшения скорости поглощения кислорода в присутствии метилолеата (МО) и метилолеата с добавками антиоксидантов (МО+АО). количественно характеризующей степень уменьшения скорости поглощения кислорода в присутствии метилолеата (МО) и метилолеата с добавками антиоксидантов (МО+АО).
Было установлено, что зависимость изменения периодов индукции для индивидуального  -токоферола носит экстремальный характер. Диапазон эффективных концентраций расположен в области (0,25-8,00) мМ, что соответствует (0,03-1,08)% от массы липидов, максимум указанной зависимости определялся при концентрации 2,5 мМ (0,34% от массы липидов). Зависимости изменения величины периодов индукции от концентрации N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола носит экстремальный характер. Диапазон эффективных концентраций расположен в области (0,25-8,00) мМ, что соответствует (0,03-1,08)% от массы липидов, максимум указанной зависимости определялся при концентрации 2,5 мМ (0,34% от массы липидов). Зависимости изменения величины периодов индукции от концентрации N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида в системе окисления носили линейный характер, указанное соединение в смеси с ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида в системе окисления носили линейный характер, указанное соединение в смеси с  -токоферолом проявляло синергическое действие, превосходящее по своему ингибирующему действию прототип. -токоферолом проявляло синергическое действие, превосходящее по своему ингибирующему действию прототип.
Изучение ингибирующего действия смесей  -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом с постоянными концентрациями ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом с постоянными концентрациями  -токоферола показало, что зависимость периодов индукции от концентрации N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола показало, что зависимость периодов индукции от концентрации N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида также носит экстремальный характер с максимумом в области 4×10-4 моль/л (0,05% от массы липидов). Диапазон эффективных концентраций соответствовал (1,0-6,0)×10-4 моль/л, что составляет (0,01-0,08)% от массы липидов. Диапазон эффективных концентраций смесей ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида также носит экстремальный характер с максимумом в области 4×10-4 моль/л (0,05% от массы липидов). Диапазон эффективных концентраций соответствовал (1,0-6,0)×10-4 моль/л, что составляет (0,01-0,08)% от массы липидов. Диапазон эффективных концентраций смесей  -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом с постоянными концентрациями N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом с постоянными концентрациями N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида соответствовал (2,5-15,0)×10-4 моль/л, что составляет (0,03-0,20)% от массы липидов. ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида соответствовал (2,5-15,0)×10-4 моль/л, что составляет (0,03-0,20)% от массы липидов.
В связи с этим с целью отбора наиболее эффективных синергических смесей более подробно изучались двухкомпонентные составы, включающие  -токоферол с N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферол с N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом, при этом концентрации каждого из компонентов смеси выбирались из указанной области наибольшей эффективности смесей. ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом, при этом концентрации каждого из компонентов смеси выбирались из указанной области наибольшей эффективности смесей.
Диапазоны изменения концентрации каждого из компонентов, составляющих в целом наиболее высокоэффективные смеси, представлены следующими значениями, масса в %:
 -токоферол -токоферол |
29,4-93,8 |
| N,N-диметил-N-гексадецил-аминоэтиловый |
|
эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) ‘-(3,5-дитретбутил-4-гидроксифенил) |
|
| пропановой кислоты бромид |
6,2-70,6, |
добавляемых в количестве 0,04-0,28% от массы липидов.
Сущность изобретения иллюстрируется следующими примерами, для технологии приготовления антиоксидантных композиций расчеты также приведены в граммах.
ПРИМЕР 1
Берут 10 г (точная навеска) (7,4×10-1 моль/л) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0044 г (0,04%) смеси  -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом. Стабилизирующая комбинация содержит 0,0034 г (2,5×10-4 моль/л) ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом. Стабилизирующая комбинация содержит 0,0034 г (2,5×10-4 моль/л)  -токоферола, 0,0010 г (1,0×10-4 моль/л) N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола, 0,0010 г (1,0×10-4 моль/л) N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, что составляет соответственно 0,03% и 0,01% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %: ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, что составляет соответственно 0,03% и 0,01% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %:
 -токоферол -токоферол |
71,4 |
| N,N-диметил-N-гексадецил-аминоэтиловый |
|
эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) ‘-(3,5-дитретбутил-4-гидроксифенил) |
|
| пропановой кислоты бромид |
28,6. |
ПРИМЕР 2
Берут 10 г (точная навеска) (7,4×10-1 моль/л) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0064 г (0,06%) смеси  -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом. Стабилизирующая комбинация содержит 0,0034 г (2,5×10-4 моль/л) ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом. Стабилизирующая комбинация содержит 0,0034 г (2,5×10-4 моль/л)  -токоферола, 0,0030 г (2,0×10-4 моль/л) N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола, 0,0030 г (2,0×10-4 моль/л) N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, что составляет соответственно 0,03% и 0,03% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %: ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, что составляет соответственно 0,03% и 0,03% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %:
 -токоферол -токоферол |
55,6 |
| N,N-диметил-N-гексадецил-аминоэтиловый |
|
эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) ‘-(3,5-дитретбутил-4-гидроксифенил) |
|
| пропановой кислоты бромид |
44,4. |
ПРИМЕР 3
Берут 10 г (точная навеска) (7,4×10-1 моль/л) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0078 г (0,08%) смеси  -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом. Стабилизирующая комбинация содержит 0,0068 г (5,0×10-4 моль/л) ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом. Стабилизирующая комбинация содержит 0,0068 г (5,0×10-4 моль/л)  -токоферола, 0,0010 г (1,0×10-4 моль/л) N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола, 0,0010 г (1,0×10-4 моль/л) N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, что составляет соответственно 0,07% и 0,01% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %: ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, что составляет соответственно 0,07% и 0,01% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %:
 -токоферол -токоферол |
83,3 |
| N,N-диметил-N-гексадецил-аминоэтиловый |
|
эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) ‘-(3,5-дитретбутил-4-гидроксифенил) |
|
| пропановой кислоты бромид |
16,7. |
ПРИМЕР 4
Берут 10 г (точная навеска) (7,4×10-1 моль/л) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0110 г (0,11%) смеси  -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом. Стабилизирующая комбинация содержит 0,0100 г (7,5×10-4 моль/л) ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом. Стабилизирующая комбинация содержит 0,0100 г (7,5×10-4 моль/л)  -токоферола, 0,0010 г (1,0×10-4 моль/л) N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола, 0,0010 г (1,0×10-4 моль/л) N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, что составляет соответственно 0,10% и 0,01% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %: ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, что составляет соответственно 0,10% и 0,01% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %:
 -токоферол -токоферол |
88,2 |
| N,N-диметил-N-гексадецил-аминоэтиловый |
|
эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) ‘-(3,5-дитретбутил-4-гидроксифенил) |
|
| пропановой кислоты бромид |
11,8. |
ПРИМЕР 5
Берут 10 г (точная навеска) (7,4×10-1 моль/л) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0170 г (0,17%) смеси  -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом. Стабилизирующая комбинация содержит 0,0140 г (10,0×10-4 моль/л) ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом. Стабилизирующая комбинация содержит 0,0140 г (10,0×10-4 моль/л)  -токоферола, 0,0030 г (2,0×10-4 моль/л) N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола, 0,0030 г (2,0×10-4 моль/л) N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, что составляет соответственно 0,14% и 0,03% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %: ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, что составляет соответственно 0,14% и 0,03% от массы липидов. При этом соотношение компонентов стабилизирующей смеси следующее, масса в %:
 -токоферол -токоферол |
83,3 |
| N,N-диметил-N-гексадецил-аминоэтиловый |
|
эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) ‘-(3,5-дитретбутил-4-гидроксифенил) |
|
| пропановой кислоты бромид |
16,7. |
Эффективность ингибирующего действия смесей указанных выше веществ оценивали на основании данных кинетики поглощения кислорода, получаемых с использованием манометрического метода, подробно изложенного в описании изобретения.
Полученные результаты приведены в табл.1. Из данных табл.1 видно, что все рекомендуемые сочетания ингибиторов окисления превосходят по величине эффективности прототип. Наибольшую эффективность по сравнению с прототипом проявляет смесь (пример 5), включающая 83,3%  -токоферола и 16,7% N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола и 16,7% N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, добавляемых в концентрации 0,14% и 0,03% соответственно от массы липидов, максимально достигаемый ингибирующий эффект составляет 1160 мин, соотношение компонентов смеси 5:1, при этом эффект синергизма составляет 58,9%. ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, добавляемых в концентрации 0,14% и 0,03% соответственно от массы липидов, максимально достигаемый ингибирующий эффект составляет 1160 мин, соотношение компонентов смеси 5:1, при этом эффект синергизма составляет 58,9%.
Было установлено, что эффективность синергизма при совместном использовании  -токоферола и N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола и N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида в разных субстратах составляет от (20-63)%, тогда как для прототипа эффективность смесей изменялась в пределах (16-20)% (табл.1). ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида в разных субстратах составляет от (20-63)%, тогда как для прототипа эффективность смесей изменялась в пределах (16-20)% (табл.1).
Из сравнения ингибирующего действия исследуемых смесей видно, что абсолютная величина периодов индукции смеси, включающей 83,3%  -токоферола и 16,7% N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола и 16,7% N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, добавляемых в количестве 0,14% и 0,03% от массы липидов соответственно, выше при окислении метилолеата (1160 мин), чем при окислении рыбных липидов (270 мин). Эти данные объясняются более высокой степенью ненасыщенности входящих в состав рыбных липидов высших жирных кислот, а следовательно, и более высокой их окисляемостью. Однако сравнение для указанной смеси величин ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида, добавляемых в количестве 0,14% и 0,03% от массы липидов соответственно, выше при окислении метилолеата (1160 мин), чем при окислении рыбных липидов (270 мин). Эти данные объясняются более высокой степенью ненасыщенности входящих в состав рыбных липидов высших жирных кислот, а следовательно, и более высокой их окисляемостью. Однако сравнение для указанной смеси величин   / /  i i
Установлен наиболее эффективный диапазон концентраций антиоксидантов, масса в %:
 -токоферол -токоферол |
29,4-93,8 |
| N,N-диметил-N-гексадецил-аминоэтиловый |
|
эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) ‘-(3,5-дитретбутил-4-гидроксифенил) |
|
| пропановой кислоты бромид |
6,2-70,6, |
добавляемых в количестве 0,04-0,28% от массы липидов.
При изучении кинетики накопления гидропероксидов было показано, что в опытах с концентрацией 83,3%  -токоферола и 16,7% N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола и 16,7% N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида в концентрации 0,14% и 0,03% от массы липидов соответственно процент разрушения гидропероксидов составляет 51,0%, что не наблюдается в присутствии прототипа (табл.3). ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида в концентрации 0,14% и 0,03% от массы липидов соответственно процент разрушения гидропероксидов составляет 51,0%, что не наблюдается в присутствии прототипа (табл.3).
Причинно-следственная связь между существенными признаками изобретения и достижением технического результата следующая. Полученные впервые эффекты ингибирования синергической смесью  -токоферола и N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола и N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида могут быть объяснены, исходя из представлений о механизме антиоксидантного действия. Установлено, что оба компонента смеси воздействуют на сложный многостадийный процесс окисления по различным механизмам. ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида могут быть объяснены, исходя из представлений о механизме антиоксидантного действия. Установлено, что оба компонента смеси воздействуют на сложный многостадийный процесс окисления по различным механизмам.
Так, в соответствии с литературными данными,  -токоферол проявляет чрезвычайно высокую активность только в реакции с пероксильными радикалами (RO2 -токоферол проявляет чрезвычайно высокую активность только в реакции с пероксильными радикалами (RO2  ), ведущими окисление. Константа скорости реакции ), ведущими окисление. Константа скорости реакции  -токоферола с RO2 -токоферола с RO2  (реакции 7 согласно классической схемы) составляет 3,60×106 М-1×с-1 (реакции 7 согласно классической схемы) составляет 3,60×106 М-1×с-1
Таким образом, соединение N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид проявляет активность в реакции с пероксильными радикалами с константой скорости реакции К7=0,94×104 М-1×с-1, снижает скорость процесса окисления липидов в смеси с ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид проявляет активность в реакции с пероксильными радикалами с константой скорости реакции К7=0,94×104 М-1×с-1, снижает скорость процесса окисления липидов в смеси с  -токоферолом в 2-5 раз, а также дополнительно снижает уровень гидропероксидов, образующихся в процессе окисления липидов, на 51,0% (табл.3). Разрушение гидропероксидов под влиянием смеси заявляемого соединения с -токоферолом в 2-5 раз, а также дополнительно снижает уровень гидропероксидов, образующихся в процессе окисления липидов, на 51,0% (табл.3). Разрушение гидропероксидов под влиянием смеси заявляемого соединения с  -токоферолом, в свою очередь, является причиной выигрыша в периодах индукции и обеспечения высокой эффективности. -токоферолом, в свою очередь, является причиной выигрыша в периодах индукции и обеспечения высокой эффективности.
Предлагаемый состав, включающий  -токоферол и N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферол и N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид, достигает эффекта ингибирования окисления липидов при низких концентрациях компонентов смеси по сравнению с прототипом. Сочетание в одной композиции ингибиторов, действующих на разные элементарные реакции сложного окислительного процесса, а также присутствие эффекта синергизма антиоксидантов позволяют увеличить ингибирующую способность смеси и эффективно тормозить окисление полиненасыщенных субстратов. ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид, достигает эффекта ингибирования окисления липидов при низких концентрациях компонентов смеси по сравнению с прототипом. Сочетание в одной композиции ингибиторов, действующих на разные элементарные реакции сложного окислительного процесса, а также присутствие эффекта синергизма антиоксидантов позволяют увеличить ингибирующую способность смеси и эффективно тормозить окисление полиненасыщенных субстратов.
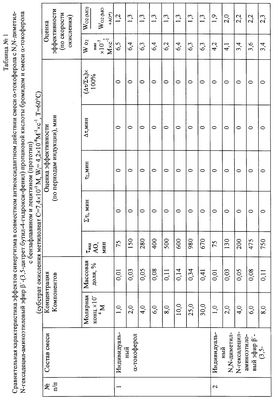 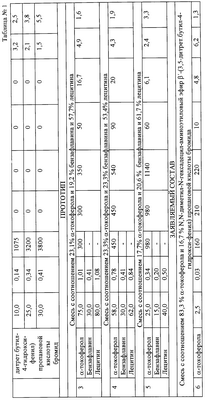  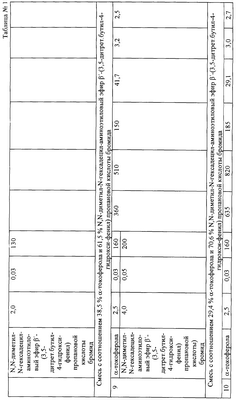 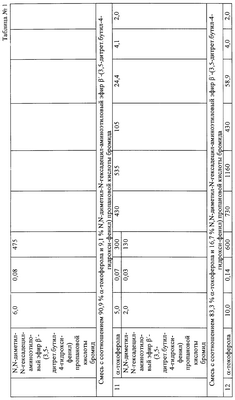 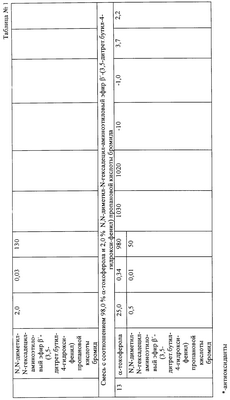
Таблица 2
Кинетические эффекты антиоксидантного действия смеси  -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола с N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом при окислении липидов различной природы Ссубстрата=7,4×10-1 М, С(АИБН)=3 мМ, Т=60°С, P ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромидом при окислении липидов различной природы Ссубстрата=7,4×10-1 М, С(АИБН)=3 мМ, Т=60°С, P 0,05 0,05 |
| № п/п |
Состав смеси |
Концентрация компонентов |
Оценка эффективности (по периодам индукции), мин |
Оценка эффективности (по скорости окисления) |
| Молярная конц.×10-4 М |
Массовая доля, % |
 инд AO, мин инд AO, мин |
  i, мин i, мин |
  , мин , мин |
  , мин , мин |
(  / /  i)×100% i)×100% |
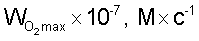 |
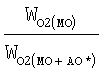 |
| Субстрат окисления – метилолеат |
| 1 |
Индивидуальный  -токоферол -токоферол |
2,0 |
0,03 |
150 |
0 |
0 |
0 |
0 |
6,4 |
1,3 |
| 25,0 |
0,34 |
980 |
0 |
0 |
0 |
0 |
6,3 |
1,3 |
| 2 |
Индивидуальный N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид |
2,0 |
0,03 |
130 |
0 |
0 |
0 |
0 |
4,1 |
2,0 |
| 25,0 |
0,34 |
3200 |
0 |
0 |
0 |
0 |
2,1 |
3,8 |
Смесь с соотношением 83,3%  -токоферола и 16,7% N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола и 16,7% N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида |
| 3 |
 -токоферола -токоферола |
10,0 |
0,14 |
600 |
730 |
1160 |
430 |
58,9 |
4,0 |
2,0 |
| |
N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид |
2,0 |
0,03 |
130 |
|
|
|
|
|
|
| Субстрат окисления – жир сиговых рыб |
| 4 |
Индивидуальный  -токоферол -токоферол |
2,0 |
0,03 |
46 |
0 |
0 |
0 |
0 |
29,0 |
1,2 |
| 25,0 |
0,34 |
240 |
0 |
0 |
0 |
0 |
24,0 |
1,5 |
| 5 |
Индивидуальный N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид |
2,0 |
0,03 |
55 |
0 |
0 |
0 |
0 |
18,4 |
1,9 |
| 25,0 |
0,34 |
1250 |
0 |
0 |
0 |
0 |
8,3 |
4,2 |
Смесь с соотношением 83,3%  -токоферола и 16,7% N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола и 16,7% N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида |
| 6 |
 -токоферола -токоферола |
10,0 |
0,14 |
110 |
165 |
270 |
105 |
63,4 |
14,5 |
2,4 |
| |
N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромид |
2,0 |
0,03 |
55 |
|
|
|
|
|
|
| * – антиоксиданты |
Таблица 3
Величины начальной, максимальной скоростей поглощения кислорода при инициированном окислении метилолеата (МО), разрушения гидропероксидов при аутоокислении МО (Ссубстрата=7,4×10-1 М) в присутствии смеси антиоксидантов (АО) и прототипа Т=60°С, p 0,05 0,05 |
| № п/п |
Состав |
Инициированное окисление, Wi=4,2×10-8М-1×c-1 |
Аутоокисление МО |
Процент разрушения ROOH за 7 часов |
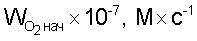 |
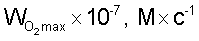 |
Wнакопления ROOH×10-4; г I2/100 г лип.*×с-1 |
Wразрушения ROOH×10-4, г I2/100 г лип.*×с-1 |
| 1 |
МО (контроль) |
1,9 |
8,0 |
8,9 |
– |
– |
| 2 |
МО + Смесь с соотношением 83,3%  -токоферола (1,0 мМ) и 16,7% N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферола (1,0 мМ) и 16,7% N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида (0,2 мМ) ‘-(3,5-дитретбутил-4-гидроксифенил) пропановой кислоты бромида (0,2 мМ) |
0,9 |
4,0 |
– |
5,1 |
51,0 |
| 3 |
МО + Смесь с соотношением 17,7%  -токоферола (2,5 мМ), 20,6% бензафлавина (1,5 мМ) и 61,7% лецитина (4,0 мМ) (ПРОТОТИП) -токоферола (2,5 мМ), 20,6% бензафлавина (1,5 мМ) и 61,7% лецитина (4,0 мМ) (ПРОТОТИП) |
0,7 |
2,4 |
– |
– |
– |
| * – липиды |
Формула изобретения
Состав для стабилизации липидов, включающий  -токоферол и синергист антиоксиданта, отличающийся тем, что в качестве синергиста антиоксиданта использован N,N-диметил-N-гексадецил-аминоэтиловый эфир -токоферол и синергист антиоксиданта, отличающийся тем, что в качестве синергиста антиоксиданта использован N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил)пропановой кислоты бромид при следующих соотношениях компонентов в смеси, мас.%: ‘-(3,5-дитретбутил-4-гидроксифенил)пропановой кислоты бромид при следующих соотношениях компонентов в смеси, мас.%:
 -токоферол -токоферол |
29,4-93,8 |
| N,N-диметил-N-гексадецил- |
|
аминоэтиловый эфир  ‘-(3,5-дитретбутил- ‘-(3,5-дитретбутил- |
|
| 4-гидроксифенил)пропановой кислоты бромид |
6,2-70,6 |
добавляемых в количестве 0,04-0,28% от массы липидов.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 21.03.2008
Извещение опубликовано: 27.03.2010 БИ: 09/2010
|
|

 -токоферол и синергист антиоксиданта. При этом в качестве синергиста антиоксиданта используют N,N-диметил-N-гексадецил-аминоэтиловый эфир
-токоферол и синергист антиоксиданта. При этом в качестве синергиста антиоксиданта используют N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитретбутил-4-гидроксифенил)пропановой кислоты бромид. Заявленный состав добавляют в количестве 0,04-0,28% от массы липидов. При этом все компоненты взяты при определенном соотношении. Изобретение позволяет снизить скорость процесса окисления липидов в 2-5 раз, а также снизить уровень гидропероксидов, образующихся в процессе окисления липидов, на 51,0%. 3 табл.
‘-(3,5-дитретбутил-4-гидроксифенил)пропановой кислоты бромид. Заявленный состав добавляют в количестве 0,04-0,28% от массы липидов. При этом все компоненты взяты при определенном соотношении. Изобретение позволяет снизить скорость процесса окисления липидов в 2-5 раз, а также снизить уровень гидропероксидов, образующихся в процессе окисления липидов, на 51,0%. 3 табл. ), за которые принимали:
), за которые принимали:
 ) и простой суммы индивидуальных компонентов (
) и простой суммы индивидуальных компонентов (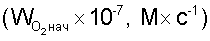 и максимальная
и максимальная 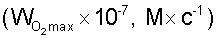 скорости процесса окисления в присутствии и в отсутствии антиоксиданта. Эффективность стабилизации окисления определяли также по величине
скорости процесса окисления в присутствии и в отсутствии антиоксиданта. Эффективность стабилизации окисления определяли также по величине 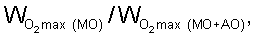 количественно характеризующей степень уменьшения скорости поглощения кислорода в присутствии метилолеата (МО) и метилолеата с добавками антиоксидантов (МО+АО).
количественно характеризующей степень уменьшения скорости поглощения кислорода в присутствии метилолеата (МО) и метилолеата с добавками антиоксидантов (МО+АО). ), ведущими окисление. Константа скорости реакции
), ведущими окисление. Константа скорости реакции 





 0,05
0,05