Патент на изобретение №2312107
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
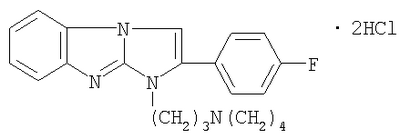
(54) ДИГИДРОХЛОРИД 1-(3-ПИРРОЛИДИНОПРОПИЛ)-2-(4-ФТОРОФЕНИЛ)ИМИДАЗО[1,2-a]-БЕНЗИМИДАЗОЛА, ОБЛАДАЮЩИЙ МЕСТНОАНЕСТЕЗИРУЮЩИМ ДЕЙСТВИЕМ
(57) Реферат:
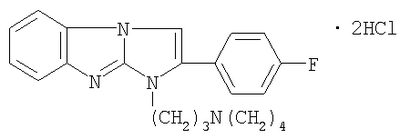
Изобретение относится к новому 1,2-дизамещенному имидазо[1,2-а]бензимидазола. Описывается дигидрохлорид 1-(3-пирро-лидинопропил)-2-(4-фторофенил)имидазо[1,2-а]бензимидазола формулы I: Соединение обладает местноанестезирующим действием при поверхностной (терминальной) анестезии. Технический результат – получено новое соединение, обладающее полезными биологическими свойствами. 3 табл.
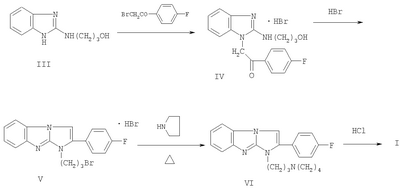
Изобретение относится к новому 1,2-дизамещенному имидазо[1,2-а]-бензимидазола, а именно к водорастворимому дигидрохлориду 1-(3-пирролидинопропил)-2-(4-фторофенил)имидазо[1,2-а]бензимидазола формулы I: обладающему местноанестезирующим действием при поверхностной (терминальной) анестезии. Широкое применение в клинике для терминальной (поверхностной) анестезии получил анестетик дикаин (тетракаин), который по обезболивающей активности в 2-3 раза превосходит кокаин и в 10-12 раз – новокаин, однако подобно кокаину обладает высокой токсичностью (М.Д.Машковский. Лекарственные средства, 15-е изд., перераб. и дополн. – М.: Медицина, 1998, ч.1, с.371-382). Кроме того, побочные явления, (тахикардии, судороги, потеря сознания, паралич дыхательного центра), вызываемые им (Б.М.Бобров. Наш опыт применения раствора тримекаина для поверхностной анестезии в ЛОР-хирургии. Мед. сестра, 1990, №9, с.14-17), затрудняют его широкое применение (О.Ф.Конобевцев, Н.П.Полевая. Действие водных растворов дикаина и пиромекаина на эпителий слизистой оболочки полости рта. Стоматология, 1990, т.69, №3, с.39-41). В ряду 1,2-дизамещенных имидазо[1,2-а]бензимидазола известны соединения, обладающие местноанестезирующим действием. Наиболее близким по структуре веществом среди 1,2-дизамещенных имидазо[1,2-а]бензимидазола является дигидрохлорид 1-(3-пирролидинопропил)-2-фенилимидазо[1,2-а]бензимидазола (II), обладающий местноанестезирующим действием [Анисимова В.А., Галенко-Ярошевский А.П., Попков В.А., Каде Е.А., Осипова М.М., Спасов А.А. Дигидрохлорид 1-(3-пирролидинопропил)-2-фенилимидазо[1,2-а]бензимидазола, обладающий местноанестезирующим действием. Патент РФ №2160265(2000), С07D 487/04, А61К 31/4188, А61Р 23/02]. Техническим результатом изобретения является новое соединение в ряду 2-замещенных 1-(3-пирролидинопропил)имидазо[1,2-а]бензимидазола, проявляющее местноанестезирующее действие, более эффективное, чем известный в этом ряду дигидрохлорид 1-(3-пирролидинопропил)-2-фенилимидазо[1,2-а]бензимидазола [Патент РФ №2160265 (2000)], а также более эффективное, чем известный, широко применяемый обезболивающий препарат дикаин. Технический результат изобретения достигается соединением I, синтез которого заключается во взаимодействии 2-(3-гидроксипропиламино)бенз-имидазола (III) с 4-фторофенацилбромидом, дальнейшей циклизации образующегося гидробромида 1-(4-фторофенацил)-2-(3-гидроксипропиламино)бензимидазола (IV) с одновременным замещением гидроксигруппы на атом брома при кипячении в конц. НВг. Последующее замещение атома брома в гидробромиде 1-(3-бромопропил)-2-(4-фторофенил)имидазо[1,2-а]-бензимидазола (V) на пирролидин и перевод полученного 1-(3-пирролидинопропил)замещенного (VI) в дигидрохлорид обычными методами приводит к соединению I: Ниже приведены методики синтеза предлагаемого соединения. Пример. Дигидрохлорид 1-(3-пирролидинопропил)-2-(4-фторофенил)-имидазо[1,2-а]бензимидазола (I). Стадия 1. Гидробромид 2-(3-гидроксипропиламино)-1-(4-фторофенацил)бензимидазола (IV). В нагретый почти до кипения раствор 1,9 г (10 ммоль) 2-(3-гидроксипропиламино)бензимидазола (III) в 15 мл 2-пропанола вносят 2,75 г (10,5 ммоль) 4-фторофенацилбромида, синтезированного бромированием 4-фтороацетофенона эквимолярным количеством брома в этаноле, и смесь кипятят до полного протекания реакции (контроль – ТСХ, 4-5 ч). По окончании реакции массу охлаждают, выпавший осадок отфильтровывают и тщательно промывают ацетоном. Выход 3,8 г (93,13%). Белоснежные блестящие чешуйки с т.пл. 264-265°С (разложение, из этанола). Найдено, %: С 52,8; Н 4,9; Br 19,4; F 4,5; N 10,5. C18H18FN3O2·HBr. Вычислено, %: С 52,9; H 4,7; Br 19,6; F 4,7; N 10,3. ИК-спектр (вазелин, масло), см-1: 1705 (С=O), 1675 (C=N<), 3070-3310 (ОН, NH). Спектр 1Н ЯМР (DMSO-d6), Стадия 2. Гидробромид 1-(3-бромопропил)-2-(4-фторофенил)имидазо-[1,2-а]бензимидазола (V). Кипятят 3,05 г (7,5 ммоль) соединения IV в 30 мл конц. HBr до полного протекания реакции (6-8 ч, контроль – ТСХ: Al2О3, CHCl3; Rf исходного 0,1, Rf конечного 0,85). Выпавший осадок после охлаждения реакционной массы отфильтровывают на стеклянном фильтре, хорошо отжимают и тщательно промывают от кислоты ацетоном. Получают 3,34 г (97,9%) практически чистого гидробромида V, которые можно вводить в дальнейшие реакции без дополнительной очистки. Т. пл. 237-238°С (из этанола). Найдено, %: С 48,0; Н 3,5; Br 34,8; N 9,5. C18H15BrFN3·HBr. Вычислено, %: С 47,9; Н3,6; Br 35,0; N 9,3. ИК-спектр (вазелин, масло), см-1: 1500, 1595,1605 (С=С), 1665 (C=N+<). Спектр 1H ЯМР (DMSO-d6 – CCl4), Стадия 3. Дигидрохлорид 1-(3-пирролидинопропил)-2-(4-фторофе-нил)имидазо[1,2-а]бензимидазола (I). Смесь 0,91 г (2 ммоль) гидробромида V и 2,5 мл свежеперегнанного пирролидина кипятят 2-3 часов, следя за ходом реакции с помощью ТСХ. После окончания реакции массу охлаждают, выливают в 25 мл холодной воды и экстрагируют хлороформом. Хлороформный экстракт промывают водой, сушат безводным Na2SO4 и после упаривания до небольшого объема пропускают через слой оксида алюминия, элюируя 1-(3-пирролидинопропил)-2-(4-фторофенил)имидазо[1,2-а]-бензимидазол хлороформом. Масло (0,67 г, 92,3%), оставшееся после упаривания элюата, растворяют в сухом эфире или ацетоне и раствор подкисляют эфирным раствором HCl или насыщенным раствором HCl в изопропиловом спирте. Осадок дигидрохлорида I отделяют, промывают ацетоном и высушивают при 105-110°С. Белоснежные кристаллы с т.пл. 227-229°С (разл., из ацетонитрила). Найдено, %: С 60,5; Н 5,7; Cl 16,5; F 4,2; N 13,0. C22H23FN4·2HCl. Вычислено, %: С 60,7; Н 5,8; С1 16,3; F 4,4; N 12,9. ИК-спектр (вазелин, масло), см-1: 1660 (С=N+<), 2450-2720, 3150-3275 N+Н). Спектр 1Н ЯМР (DMSO-d6 – CCl4), Эксперименты проведены в соответствии со статьей 11-й Хельсинкской декларации Всемирной медицинской ассоциации (1964), “Международными рекомендациями по проведению медико-биологических исследований с использованием животных” (1985) и Правилами лабораторной практики в Российской Федерации (приказ МЗ РФ №267 от 19.06.2003 г.). Острую токсичность исследовали [определяли среднюю летальную (смертельную) дозу – ЛД50 Статистическую обработку данных, учитываемых в градированной форме, проводили по М.Л.Беленькому (Беленький М.Л. Элементы количественной оценки фармакологического эффекта. – Л., 1963. – 152 с.) и с помощью таблиц Н.Н.Самойлова (Самойлов Н.Н. Таблицы значений средней ошибки и доверительного интервала средней арифметической величины вариационного ряда. – Томск. 1970. – 63 с.). Учет результатов исследований, выраженных в альтернативной форме, определение ЛД50, ЭК50, границ доверительного интервала и терапевтического индекса, или широты терапевтического действия (ЛД50/ЭК50) осуществляли по методам, описанным В.Б.Прозоровским (1962) и М.Л.Беленьким (1963). Установлено, что в условиях поверхностной анестезии в опытах на роговице глаз кроликов минимальной и максимальной анестезирующими концентрациями для соединения I являются 0,0039 и 0,25%, а для дикаина и соединения II – 0,0312 и 1%, 0,0156 и 0,5% соответственно. Индексы Ренье, выражающие силу анестезирующего действия вещества в испытуемой концентрации, для соли I в 0,0039, 0,0078, 0,0156, 0,0312, 0,0625, 0,125, 0,25, 0,5 и 1% растворах составляют 114,0, 218,0, 324,0, 788,5, 956,0, 1175,0 и 1300,0, для дикаина в 0,0312, 0,0625, 0,125, 0,25, 0,5 и 1% растворах – 116,8, 174,4, 346,4, 821,0, 1038,0 и 1300,0, для соли II в 0,0156, 0,0312, 0,0625, 0,125, 0,25 и 0,5% – 125,0, 561,8, 742,5, 852,3, 1250,0 и 1300,0, соответственно. Индексы Валета для соединения I составили: относительно дикаина (взятого для сопоставления в 0,0312, 0,0625, 0,125, 0,25 и 0,5% растворах) равны 7,8, 7,7, 6,8, 1,7 и 1,3 соответственно, при этом эквивалентные анестетические концентрации составили 0,0040, 0,0081, 0,0184, 0,1506 и 0,3904% соответственно; относительно соединения II (взятого для сопоставления в 0,0156, 0,0312, 0,0625, 0,125, 0,25 и 0,5% растворах) равны 3,5, 1,4, 1,3, 1,4, 1,04 и 1,0, при этом эквивалентные анестетические концентрации составили 0,0045, 0,0220, 0,0476, 0,0882, 0,2396 и 0,5% (табл.1). Важно отметить, что соединения I и II ни в одной из исследованных концентраций не оказывают раздражающего действия на ткани переднего отдела глаза, тогда как дикаин в 1% растворе индуцировал гиперемию конъюнктивы век в течение 30-300 мин. Время наступления анестезии при инстилляции в конъюнктивальный мешок глаза равнозначных (одинаковых концентрациях) растворов соединений I и II было практически сопоставимо и колебалось в пределах 2-4 мин, а дикаина – 1-3 мин. Время наступления полной анестезии в случаях использования соединений I и II в одинаковых концентрациях также существенно не отличалось и было в пределах 3-4 мин, а дикаина – 2-3 мин. Время окончания полной анестезии под влиянием соединения I (в соответствующих растворах) в 3,85, 2,99 и 2,47 раза и в 2,06, 1,56, 1,45, 1,46 и 1,49 раза больше, чем при использовании дикаина (0,125, 0,25 и 0,5% растворы) и соединения II (0,0312, 0,0625, 0,125, 0,25 и 0,5% растворы), соответственно. Общая продолжительность анестезии при применении соли I (в соответствующих растворах) в 3,30, 2,83 и 2,52 раза и в 1,47, 1,45, 1,38, 2,63, 1,47 и 1,30 раза больше, чем под влиянием дикаина (0,125, 0,25 и 0,5% растворы) и соли II (0,0312, 0,0625, 0,125, 0,25 и 0,5% растворы), соответственно (табл.2). По местноанестезирующей активности – при сопоставлении ЭК50, выраженных в мМ, и терапевтических индексов – соединение I соответственно в 10,1 и 1,9 раза более значимо и в 10,5 и 2,7 раза имеет большую широту терапевтического действия, чем дикаин и соединение II (табл.3). Таким образом, при поверхностном методе анестезии соединение I по активности и широте терапевтического действия значительно превосходит дикаин и соединение II. На его основе возможно создание местнообезболивающего лекарственного средства, предназначенного для поверхностной анестезии.
Формула изобретения
Дигидрохлорид 1 -(3-пирролидинопропил)-2-(4-фторофенил)имидазо [1,2-а]бензимидазола формулы I
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

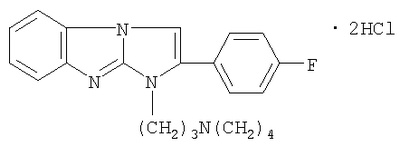
 , м.д.: 1,87 (2Н, кв, CHr), 3,6 (4Н, к, NCH2, СН2О), 6,15 (2Н, с, CH2СО), 7,1-8,2 (8Н, м, аромат. Н), 9,12 (1Н, т, NH).
, м.д.: 1,87 (2Н, кв, CHr), 3,6 (4Н, к, NCH2, СН2О), 6,15 (2Н, с, CH2СО), 7,1-8,2 (8Н, м, аромат. Н), 9,12 (1Н, т, NH).