|
|
(21), (22) Заявка: 2005134510/14, 28.10.2005
(24) Дата начала отсчета срока действия патента:
28.10.2005
(43) Дата публикации заявки: 27.05.2007
(46) Опубликовано: 10.12.2007
(56) Список документов, цитированных в отчете о
поиске:
RU 4060 U1, 16.05.1997. RU 2207052 С2, 27.06.2003. US 2002/0103437 A1, 01.08.2002. US 2004/0138568 A1, 15.07.2004. EP 1683486 A1, 26.07.2006. CN 1257695 A, 28.06.2000. Клиническое руководство по ультразвуковой диагностике. Под ред. Митькова В.В., М., ВИДАР, 1997, т.5, с.31-33.
Адрес для переписки:
197136, Санкт-Петербург, а/я 55, пат.пов. Ю.В.Рыбакову
|
(72) Автор(ы):
Монаков Александр Георгиевич (RU),
Степанов Андрей Борисович (RU),
Степанов Евгений Андреевич (RU)
(73) Патентообладатель(и):
Общество с ограниченной ответственностью “Афалина” (RU)
|
(54) СПОСОБ РЕГИСТРАЦИИ КРОВОТОКА
(57) Реферат:
Изобретение относится к медицине, в частности к ангионеврологии, конкретно к способам и устройствам для регистрации кровотока, и может быть использовано как в экспериментальных исследованиях, так и в клинической практике, например для функциональной диагностики. В основу изобретения поставлена задача повышения диагностических возможностей при регистрации высокоскоростных кровотоков, преимущественно в краниальных сосудах, с использованием импульсной генерации при одновременном повышении помехоустойчивости и чувствительности, а техническим результатом является повышение точности определения более полного набора диагностических индексов при одновременном упрощении структуры, повышении надежности устройства. Поставленная задача регистрации кровотока решается тем, что исследуемый объем ткани облучают генерируемой ультразвуковой волной, принимают ответный сигнал, переносят частоту несущего колебания в ноль, разделяют на два канала «прямого» и «обратного» кровотока, усиливают, фильтруют и подают на вход оснащенного соответствующим программным обеспечением компьютера стандартной мультимедийной конфигурации для визуализации, обработки, хранения и архивации полученной информации. Способ характеризуется тем, что параметры усиления и фильтрации выбирают для каналов раздельно, обеспечивая максимально соответствие полос пропускания каналов диагностически значимым составляющим спектра принимаемого сигнала. 2 ил.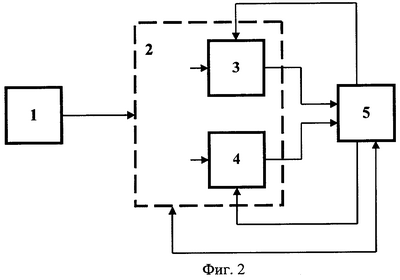
Изобретение относится к медицине, в частности к ангионеврологии, конкретно к способам регистрации кровотока, и может быть использовано как в экспериментальных исследованиях, так и в клинической практике, например для функциональной диагностики.
Известна система, определяющая скорость кровотока с использованием дисплея (1).
Известна компьютерная система анализа доплеровских сигналов кровотока, включающая набор датчиков, аналоговый блок предварительной обработки информации и персональный компьютер, связанные через последовательный интерфейс RS 232 (2).
Известен способ регистрации кровотока с использованием импульсной локации и квадратурным разделением каналов (3).
Наиболее близким к предлагаемому способу по технической сущности и достигаемому результату является способ спектрального анализа кровотока, в котором исследуемый объем ткани облучают генерируемой ультразвуковой волной, принимают ответный сигнал, переносят в область низких частот, усиливают, фильтруют и подают на вход оснащенного соответствующим программным обеспечением компьютера стандартной мультимедийной конфигурации для визуализации, диагностической обработки, хранения и архивации полученной информации (4).
Реализующее способ устройство состоит из по меньшей мере одного датчика, электрически связанного с аналоговым блоком предварительной обработки информации и персонального компьютера мультимедийной конфигурации, линейный вход которого непосредственно подключен к выходу аналогового блока (4).
Устройство работает следующим образом. Аналоговый блок предварительной обработки информации генерирует электрический сигнал, поступающий на датчик, излучающий ультразвуковую волну в направлении исследуемого объема ткани (например, сосуда). Часть рассеянного форменными элементами крови ультразвукового сигнала вновь поступает на датчик и преобразуется им в частотно-зависимый электрический сигнал, спектральный состав которого представляет адекватную информацию о скоростях движения крови в исследуемых сосудах, в том числе с учетом направления и характера кровотока. Электрический сигнал с выхода датчика поступает на вход аналогового блока предварительной обработки информации, на выходе которого формируется электрический сигнал акустического диапазона частот, содержащий информацию о распределении скоростей кровотока. Этот сигнал подается на вход компьютера стандартной мультимедийной конфигурации с соответствующим программным обеспечением, который осуществляет аналого-цифровое преобразование сигнала, расчет спектральных и скоростных характеристик кровотока, на основе полученных данных обеспечивает точный расчет полного набора диагностических индексов, визуализирует полученную информацию, обеспечивает ее хранение и архивацию.
Существенными недостатками известного способа и реализующего его устройства являются ограниченные диагностические возможности при регистрации высокоскоростных кровотоков, например, в краниальных сосудах с использованием импульсной генерации (локации), низкая помехоустойчивость и чувствительность.
В основу изобретения поставлена задача повышения диагностических возможностей при регистрации высокоскоростных кровотоков, преимущественно в краниальных сосудах, с использованием импульсной генерации (локации) при одновременном повышении помехоустойчивости и чувствительности, а техническим результатом – повышение точности определения более полного набора диагностических индексов при одновременном упрощении структуры, повышении надежности устройства.
Поставленная задача регистрации кровотока решается тем, что исследуемый объем ткани облучают генерируемой ультразвуковой волной, принимают ответный сигнал, переносят частоту несущего колебания в ноль, разделяют на два канала «прямого» и «обратного» кровотока, усиливают, фильтруют и подают на вход оснащенного соответствующим программным обеспечением компьютера стандартной мультимедийной конфигурации для визуализации, обработки, хранения и архивации полученной информации. Изобретение отличается тем, что параметры усиления и фильтрации выбирают для каналов раздельно, обеспечивая максимально соответствие полос пропускания каналов диагностически значимым составляющим спектра принимаемого сигнала.
Фиг.1 иллюстрирует сущность заявляемого способа, а на фиг.2 приведена функциональная схема устройства для осуществления предлагаемого способа.
На фиг.1 показано:
А. Спектр в случае дискретизации (частоты повторения импульсов зондирования) с частотой Fe=2Fm;
В. Спектр в случае дискретизации (частоты повторения импульсов зондирования) с частотой Fe<2Fm 1;
С. Спектр сигнала с сегмента M1 средней мозговой артерии в случае дискретизации (частоты повторения импульсов зондирования) с частотой Fe<2Fm3.
Сущность предлагаемого способа заключается в следующем. При диагностике состояния объема ткани, например сосудов, с использованием импульсной ультразвуковой доплеровской локации входным сигналом аналогового блока предварительной обработки информации является снимаемый с датчика частотно-зависимый сигнал, изменяющийся в соответствии с проявлением эффекта Допплера. Этот сигнал имеет достаточно сложный спектр. В общем случае он приведен на фиг.1А и фиг 1B. На этих двух графиках приведены результаты, стандартно поясняющие теорему отсчетов (Котельникова, Шеннона), в соответствии с которой для того, чтобы периодическое повторение спектра, вызванное дискретизацией сигнала, не изменяло повторяемый спектр, необходимо и достаточно выполнение неравенства Fe>2Fm, где Fe – частота дискретизации (частота повторения зондирующих импульсов), a Fm – максимальная частота, присутствующая в спектре сигнала кровотока. При стандартном решении аналогового блока устройства осуществляют фильтрацию данного сигнала, ограничивая полосу пропускания каналов прямого и обратного кровотока по верхней пропускаемой частоте Ff1, равной или меньшей половины частоты повторения зондирующих импульсов. Данное решение приводит к ограничению максимально возможной наблюдаемой частоты при заданной частоте повторения импульсов, определяющих максимально возможную глубину локации. В случае, если скорость кровотока окажется настолько высокой, что максимальная доплеровская частота в спектре Fm1 превысит значение Fe/2, будет проявляться явление «алиасинга», при котором сигналы прямого и обратного кровотока могут быть спутаны или неразличимы из-за наложения спектров этих сигналов в стандартной заданной полосе пропускания от -Ff1 до Ff1 (фиг.1В). Диагностика окажется невозможной. Сказанное справедливо в общем случае. Для построения лучших систем регистрации может быть использована априорная информация о сигналах кровотока. На фиг.1C приведены спектры, характерные, например, для сигналов сегмента M1 среднемозговой артерии. Обратный кровоток в этом сосуде создает спектр с максимальной доплеровской частотой Fm2, а прямой – с частотой Fm3. Принципиально, что Fm2Fe/2. При стандартной симметричной фильтрации, приводящей к полосе пропускания от -Ff1 до Ff1 (Ff1=Fe/2) будут наблюдаться явления «алиасинга» («маскировки»), а сигналы кровотока искажаться: в канале «прямого» кровотока за счет «обрезания» части спектра, а в канале «обратного» кровотока за счет «заварачивания», т.е. появления высоких (превышающих Fe/2) частотных составляющих сигнала прямого кровотока. Избежать этих искажений удается, применив раздельную (по каналам) регулировку полосы пропускания. Из рисунка, приведенного на фиг.1C видно, что при использовании полосы от -Ff2 до 0 в канале обратного кровотока и от 0 до Ff3 в канале прямого кровотока искажений спектров сигналов не происходит. Регулировка полос пропускания по каналам может осуществляться врачом-диагностом по аудиальным или визуальным критериям появления искажений, а также автоматически – по алгоритмам, заложенным в программное обеспечение персонального компьютера мультимедийной конфигурации.
Предлагаемый способ позволяет практически вдвое повысить диапазон регистрируемых скоростей при сохранении возможной глубины зондирования для большинства краниальных сосудов при одновременном повышении чувствительности и помехоустойчивости за счет оптимального согласования полосы пропускания устройства в целом с полосой реально исследуемого сигнала. Оптимальный прием обеспечивается также для всех других диагностических случаев тканевой (сосудистой) диагностики.
Таким образом, параметры усиления и фильтрации выбирают для каналов раздельно, обеспечивая максимально соответствие полос пропускания каналов диагностически значимым составляющим спектра принимаемого сигнала.
Способ может быть реализован с помощью устройства, функциональная схема которого приведена на фиг 2.
Устройство содержит по меньшей мере один датчик 1, аналоговый блок предварительной обработки информации 2, управляемый полосовой усилитель канала «прямого» кровотока 3, управляемый полосовой усилитель канала «обратного» кровотока 4, компьютер мультимедийной конфигурации с соответствующим программным обеспечением 5.
Устройство работает следующим образом. Компьютер мультимедийной конфигурации с соответствующим программным обеспечением 5 задает начальные, выбранные оператором параметры работы устройства. Аналоговый блок предварительной обработки информации 2 генерирует электрический сигнал, поступающий на датчик 1, излучающий ультразвуковую волну в направлении исследуемого объема ткани. Часть рассеянного форменными элементами крови ультразвукового сигнала вновь поступает на датчик 1 и преобразуется им в частотно-зависимый электрический сигнал, спектральный состав которого представляет адекватную информацию о скоростях движения крови в исследуемых сосудах, в том числе с учетом направления и характера кровотока. Электрический сигнал с выхода датчика 1 поступает на вход аналогового блока предварительной обработки информации 2, стандартным способом, например квадратурной обработкой (демодуляцией), разделяется на два канала. Разделенные сигналы «прямого» и «обратного» кровотоков поступают на входы управляемых полосовых усилителей каналов 3 и 4, усиливаются и фильтруются ими. Выходы усилителей могут являться также выходами аналогового блока предварительной обработки информации 2, через которые анализируемый и разделенный на два канала сигнал поступает на входы компьютера мультимедийной конфигурации с соответствующим программным обеспечением 5. Последний осуществляет преобразование сигнала, расчет спектральных и скоростных характеристик кровотока, на основе полученных данных обеспечивает точный расчет полного набора диагностических индексов, визуализирует полученную информацию, обеспечивает ее хранение и архивацию. Если полоса пропускания каналов («прямого» и/или «обратного» кровотока) аналогового блока предварительной обработки информации 2 оказывается не согласованной со спектром (полосой) реально принимаемого сигнала кровотока, сигналы «обрезаются», наблюдается «заворот» высокоскоростных сигналов одного направления кровотока в канал противоположного направления, параметры усиления и фильтрации управляемых полосовых усилителей каналов 3 и 4 изменяют раздельно, таким образом обеспечивая максимально соответствие полос пропускания каналов диагностически значимым составляющим спектра принимаемого сигнала.
Аналогично поступают при наличии шумов, наводок или других мешающих сигналов. Благодаря отличию действий, состава и структуры устройства, связи его частей, их схемных решений, а также параметров элементов предлагаемое техническое решение характеризуется повышенной чувствительностью, помехоустойчивостью, точностью и стабильностью регистрации сигналов кровотока.
Раздельное регулирование в ряде принципиально важных диагностических ситуаций позволяет проводить визуальную и аудиальную диагностику объема ткани, в которых скорости кровотока создают доплеровские сдвиги частот, значительно превышающие половину частоты повторения зондирующих их импульсов.
По сравнению с известными аналогами решение позволяет значительно повысить диагностические возможности за счет одновременного повышения чувствительности и помехоустойчивости посредством оптимального согласования полосы пропускания устройства с реальной полосой исследуемого сигнала.
Наиболее успешно заявляемое изобретение может быть использовано для диагностики патологий, связанных со значительным увеличением максимальных скоростей кровотока в краниальных сосудах.
Источники информации
1. Заявка Японии №3-176036, «ИСМ», #3, 1993.
2. Проспект фирмы Huntleigh Healthcare, Германия, “Multi Dopplex П, Dopplex Reporter”, 2005.
3. Doppler Ultrasound. Ed. by D.Evans, W.N.McDicken, New York, 1985.
4. Свидетельство на ПМ РФ №4060, А61В 5/02, G01N 27/00, 1996.
Формула изобретения
Способ регистрации кровотока, заключающийся в том, что исследуемый объем ткани облучают генерируемой ультразвуковой волной, принимают ответный сигнал, который преобразуется датчиком в частотно-зависимый электрический сигнал, спектральный состав которого представляет адекватную информацию о скоростях движения крови в исследуемых сосудах с учетом направления кровотока и после обработки полученного сигнала осуществляют его преобразование, расчет спектральных и скоростных характеристик кровотока, визуализацию, хранение и архивацию с использованием мультимедийного компьютера, отличающийся тем, что при обработке сигнала его разделяют на два канала с соответствующими полосами пропускания, усиливают и фильтруют, при этом параметры усиления и фильтрации выбирают для каналов раздельно с обеспечением максимального соответствия полос пропускания каналов диагностически значимым составляющим спектра сигнала при его визуализации.
РИСУНКИ
|
|