Патент на изобретение №2311455
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ХОЛЕСТЕРОЛЭСТЕРАЗЫ, ТРИПСИНА, ДЕЗОКСИРИБОНУКЛЕАЗЫ И РИБОНУКЛЕАЗЫ ИЗ ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ КРУПНОГО РОГАТОГО СКОТА
(57) Реферат:
Изобретение относится к биотехнологии и может найти применение в производстве медицинских препаратов – рибонуклеазы панкреатической, дезоксирибонуклеазы панкреатической, трипсина, а также холестеролэстеразы. Способ предусматривает измельчение поджелудочной железы крупного рогатого скота, ее гомогенизацию. Полученный гомогенат экстрагируют охлажденным этиловым спиртом при постоянном перемешивании. Центрифугируют. Проводят повторную экстракцию серной кислотой, содержащей сульфат магния, при постоянном перемешивании. Экстракт, содержащий целевые ферменты, отделяют от осадка центрифугированием. Балластные белки осаждают сульфатом аммония при 30-35%-ном насыщении и удаляют центрифугированием из супернатанта. Холестеролэстеразу осаждают сульфатом аммония при 45-50% насыщении экстракта, трипсин осаждают при 60-65% насыщении, дезоксирибонуклеазу (ДНК-аза) осаждают при 80-85% насыщении. Полученный при осаждении ДНК-азы супернатант, содержащий рибонуклеазу, подвергают ультрафильтрации и осаждению сернокислым аммонием при 95-98% насыщении с последующим диализом и хроматографической очисткой на колонке с ДЭАЭ-целлюлозой. Изобретение позволяет получать четыре фермента из поджелудочной железы в рамках единой технологической схемы, увеличить выход рибонуклеазы панкреатической, увеличить ее удельную активность. 4 з.п. ф-лы, 8 табл., 6 ил.14 кДа, соответствующая ферменту рибонуклеаза панкреатическая (Фиг.2). В элеатах 2 М с раствором NaCl содержится смесь белков с молекулярной массой в пределах 20-60 кДа, удельная активность которых не превышает 160000 е.а./мг (Фиг.2). Разделение рибонуклеазы на моно- и поликомпонентную фракции является операцией целесообразной, поскольку открывается возможность создания на их основе ферментных препаратов селективного действия. Так, можно полагать, что белок с молекулярной массой Отдиализованный раствор рибонуклеазы центрифугируют и пропускают через колонку с гранулированным активированным углем для удаления пирогенных примесей, затем раствор очищенной рибонуклеазы фильтруют через фильтр с размерами пор 0,22 микрон. Полученный раствор рибонуклеазы подвергают стерилизации, розливу и сушке методами, предусмотренными для лекарственных препаратов. Существенными отличительными признаками предлагаемого способа получения биологически активных веществ являются: – использование повышающейся концентрации сульфата аммония как приема, обеспечивающего селективное разделение всех четырех ферментов, содержащихся в сернокислотном экстракте ПЖ КРС после экстракции этанолом при (-18°С); – применение для тонкой очистки рибонуклеазы панкреатической ультрафильтрации на полых волокнах и ионообменной хроматографии на колонках с ДЭАЭ-целлюлозой. Таким образом, нами предлагается новый подход, позволяющий осуществлять комплексную переработку поджелудочной железы крупного рогатого скота с получением четырех ферментов (холестеролэстеразы, трипсина, ДНК-азы и РНК-азы) высокой чистоты и удельной активности. Отличие заявляемого способа от ближайших аналогов и прототипа состоит в следующем. В заявляемом способе измельченную поджелудочную железу экстрагируют охлажденным до ((-18)-(+20)°С) этанолом, так как денатурирующее действие органических растворителей становится заметным уже при температуре (+10°С) и связано с изменением молекулярных гидрофобных взаимодействий, стабилизирующих структуру белка. При высоких температурах небольшие молекулы органического растворителя проникают через поверхностные «трещины», образующиеся спонтанно за счет естественной подвижности структуры, во внутренние участки белковой молекулы и дестабилизируют ее. Отсутствие денатурации при низких температурах обусловлено малой вероятностью того, что молекулы органического растворителя проникают во внутренние структуры белка и дестабилизируют их. Кроме того, экстракция поджелудочной железы этиловым спиртом позволяет осаждать целевые ферменты и переводить в экстракт низкомолекулярные вещества, тем самым проводится начальная стадия очистки целевых ферментов. В прототипе стадии осаждения белков из поджелудочной железы этиловым спиртом отсутствуют. В прототипе раствор рибонуклеазы подвергался воздействию высоких температур в течение длительного времени (до +95°С). Использование высоких температур и агрессивных сред при получении рибонуклеазы в соответствующих аналогах приводит к низкому выходу целевого продукта и низкой его активности. В соответствующем аналоге [Пат. РФ 2152995] при хроматографической очистке рибонуклеазы была использована агрессивная среда смеси щелочи со спиртом, которые могут привести к частичной и даже полной инактивации и денатурации фермента. В заявляемом способе дробным сульфатаммонийным фракционированием было достигнуто разделение четырех продуктов (РНК-азы, ДНК-азы, трипсина и холестеролэстеразы) из одной и той же порции поджелудочной железы. В прототипе было достигнуто разделение только трех ферментов (трипсина, химотрипсина и рибонуклеазы). Причем в заявляемом способе трипсин осаждался при 60-65% насыщении сульфатом аммония, а в прототипе высол был получен при 70% насыщении сульфатом аммония (Фиг.4). В заявляемом способе на стадии очистки рибонуклеазы используют ультрафильтрацию на установке с полыми полимерными волокнами УПВ-6, укомплектованной колонками с размерами пор 50 кДа и 5 кДа. Ультрафильтрация позволяет легко очищать большие объемы экстракта, содержащего рибонуклеазу панкреатическую, от высокомолекулярных примесей и концентрировать ферментсодержащий раствор. В прототипе высол рибонуклеазы панкреатической растворяется в воде и подвергается обработке кизельгуром и фильтрации на воронке Бюхнера, а ультрафильтрация не используется. На последней стадии очистки рибонуклеазы панкреатической в заявляемом способе диализат подвергают сорбции на ДЭАЭ-целлюлозе с последующей элюцией градиентом солевого раствора хлорида натрия, при этом полученный раствор рибонуклеазы панкреатической подвергают диализу против 30±0,1 мМ Na-фосфатного буфера (рН 6,4±0,01) и инкубации против Na-фосфатного буфера при 40-44°С в течение 12 ч. Тем самым достигается полное отделение электрофоретически и хроматографически гомогенного мономерного целевого фермента от полимеров фермента и других белковых примесей. В соответствующем аналоге [Пат. РФ 2152995, С12N 9/22, 20.07.2000] фильтрат подвергают сорбции на изопористом макросетчатом сульфокатионите, являющемся сополимером полистирола и монохлордиэтилового эфира, при этом в качестве элюента используют этанол или изопропанол в 0,1-0,5 н. HCl. В прототипе очистку на ионообменной колонке не используют. Пример 1. 1 кг измельченной поджелудочной железы крупного рогатого скота экстрагируют 1,2 л охлажденным до ((-18)-(+20)°С) этанолом в течение 50 мин при постоянном перемешивании, при этом белки переходят в осадок. Осадок с целевыми ферментами отделяют от спиртового раствора, содержащего спирторастворимые компоненты (основной компонент инсулин), центрифугированием при 13000 g в течение 20 мин при +5°С. Осадок, полученный после обработки поджелудочной железы этанолом, экстрагируют при перемешивании в течение 60 мин при +5°С 2,5±0,1 мМ серной кислотой (рН 3±0,1), содержащей 5±0,01 мМ Mg+2, в соотношении 1:8, соответственно. Экстракт центрифугируют при 13000 g в течение 20 мин при +5°С и в полученном экстракте определяют активность РНК-азы спектрофотометрическим методом при длине волны 260 нм. Осаждения балластных белков. Для отделения балластных белков полученный сернокислый экстракт насыщают сульфатом аммония до концентрации 30-35%. К экстракту (V=915 мл) при +5°С добавляют 151,89 г сульфата аммония при постоянном перемешивании на магнитной мешалке до полного растворения соли. Раствор белков оставляют на 1 ч в холодильнике и центрифугируют при 13000 g в течение 20 мин при температуре +5°С. Осадок отбрасывают и получают супернатант № 1. Получение фермента холестеролэстеразы. К полученному супернатанту № 1 (Фиг.3) (V=905 мл) добавляют сульфат аммония до 45-50% насыщения (79 г соли) (Фиг.4). Соль растворяют при +5°С, затем раствор помещают на 1 ч в холодильник для формирования осадка. Полученный осадок отделяют центрифугированием при 13000 g в течение 20 мин при температуре +5°С. В результате этой процедуры осаждается холестеролэстераза. Супернатант-2, полученный при центрифугировании, используют на следующих стадиях выделения ферментов. Для получения индивидуального фермента холестеролэстеразы осадок сырого фермента, полученный при 45-50% сульфатаммонийном осаждении, растворяют в минимальном объеме 100±0,1 мМ калий-фосфатном буфере (рН 7±0,1). Раствор дотитровывают гидроокисью натрия (NaOH) до рН 7,3±0,01, добавляют холат натрия до концентрации 0,33 мг/мл и центрифугируют в течение 1 ч при 15000 g. Осадок отбрасывают, а супернатант, содержащий очищенную холестеролэстеразу, замораживают в морозильной камере при ((-18)-(+20)°С). Таким образом, из 1 кг поджелудочной железы получают 3 г очищенного фермента холестеролэстеразы.
Получение фермента трипсина. Супернатант № 2 (Фиг.3) далее насыщают сульфатом аммония до концентрации 60-65% (Фиг.4). Соль растворяют на магнитной мешалке до полного растворения. Полученный раствор помещают в холодильник на 2 ч для формирования осадка. Осадок отделяют центрифугированием при 13000 g 20 мин при температуре +5°С (супернатант № 3, полученный в ходе центрифугирования, используют для получения ферментов ДНК-азы и РНК-азы), разводят дистиллированной водой до полного растворения, а затем диализуют его против 10-кратного объема 2,5±0,1 мМ серной кислоты (рН 3-4). Диализ ведут в течение 12 ч при непрерывном перемешивании, меняя каждые 4 ч раствор серной кислоты в сборнике. Раствор после диализа центрифугируют при 10000 g в течение 20 мин при +5°С и в полученном супернатанте определяют содержание трипсина. Проанализированный супернатант, содержащий трипсин, замораживают до температуры ниже -50°С жидким азотом и направляют на лиофильную сушку. Таким образом, из 1 кг поджелудочной железы получают 1,8 г трипсина.
Получение фермента дезоксирибонуклеазы (ДНК-аза). На Фиг.5 представлен анализ дезоксирибонуклеазы в 10% ПААГ, полученной по предлагаемой технологии (3 и 5 дорожки), и препарата ОАО «Самсон-мед» (2 и 4 дорожки). 1 и 6 дорожки – маркеры: Human albumin (65 кДа), Ovalbumin (45 кДа) и Carbonic anhydrase (30 кДа). В таблице 3 приведены основные характеристики процесса выделения и очистки фермента дезоксирибонуклеазы (ДНК-азы).
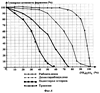
Получение фермента рибонуклеазы (РНК-аза). Супернатант № 4 (Фиг.3), содержащий фермент рибонуклеазу (РНК-азу), полученный после 80-85% высаливания сульфатом аммония, подвергают очистке методом ультрафильтрации на установках с полыми волокнами. Для проведения ультрафильтрации выбирают установку с полыми полимерными волокнами УПВ-6 укомплектованную колонками с размерами пор 50 кДа и 5 кДа. Принципиальная схема установки представлена на Фиг.6, где центробежный насос 1, предфильтр 2, колонка с размерами пор 50 кДа 3, колонка с размерами пор 5 кДа 4, фильтр РНК-азы 5, концентрированный раствор РНК-азы 6, фильтр, содержащий низкомолекулярные белки и сульфат аммония, 7. Для очистки от высокомолекулярных примесей с молекулярной массой более 50 кДа супернатант № 4 пропускают через колонку с размером пор 50 кДа, а затем для концентрирования и очистки от избытка соли через колонку с размером пор 5 кДа. В результате использования стадии ультрафильтрации на колонках с полыми волокнами был получен фермент рибонуклеаза панкреатическая с высокой удельной активностью и степенью очистки фермента. При этом удельная активность и степень очистки фермента увеличилась в 13 раз по сравнению с результатами, полученными на предыдущей стадии (см. таблицу 5). Результаты отражены в таблице 4.
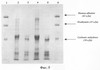
Осаждение и диализ РНК-азы. Раствор РНК-азы, полученный после ультрафильтрации, насыщают сульфатом аммония до конечной концентрации 95-98% (на 4 л концентрата 565 г сульфата аммония). Соль растворяют в течение 12 ч на механической мешалке при +5°С, а затем оставляют на 1,5 ч при +5°С для формирование осадка. Солевой раствор рибонуклеазы центрифугируют в течение 20 мин при 10000 g. Осадок № 4 (Фиг.3) растворяют в минимальном объеме 2,5±0,1 мМ серной кислоты (рН 3-4) в течение 2 ч на магнитной мешалке при интенсивном перемешивании. Для удаления избытка сульфат-ионов полученный раствор рибонуклеазы диализуют против 2,5±0,1 мМ серной кислоты (рН 3-4). Диализ ведут в течение 12 ч при непрерывном перемешивании, меняя каждые 4 ч раствор серной кислоты в сборнике. Отдиализованный раствор центрифугируют при 10000 g в течение 20 мин при +5°С. Полученный супернатант-5 хроматографируют на колонке с ДЭАЭ-целлюлозой. Получение высокоочищенной рибонуклеазы панкреатической. Колонку (V=50 мл) с ДЭАЭ-целлюлозой промывают 2 М раствором NaCl, затем уравновешивают 10±0,1 мМ раствором NaCl. Раствор белка в концентрации 6,5 мг/мл наносят на колонку и элюируют водным раствором NaCl в градиенте концентраций от 0,01-2 М NaCl (V=S-50 мл, R-50 мл). Оптимальная скорость элюции фермента V=50 мл составляет 25 мл/ч. В ходе всего процесса элюции отбирают пробы для анализа активности и чистоты рибонуклеазы в пиках, соответствующих белкам с разной молекулярной массой. Собирают пик, соответствующий белку с молекулярной массой Молекулярный вес и чистоту белка определяют методом электрофореза в полиакриламидном геле (ПААГ). На Фиг.2 представлен анализ рибонуклеазы в 12,5% ПААГ, полученной по предлагаемой технологии (4 и 5 дорожки), и препарата ОАО «Самсон-мед» (2 и 3 дорожки). Дорожка 1 – маркеры. Дорожки 6 и 7 – рибонуклеаза, полученная с использованием диализа против NaP-буфера (рН 6,4). Очищенный раствор фермента упаривают на ротационном испарителе при 45-55°С до концентрации белка 6-7 мг/мл, диализуют против 30±0,1 мМ Na-фосфатного буфера (рН 6,4±0,01). Диализ ведут при непрерывном перемешивании в течение 6 ч, заменяя каждые 2 ч Na-фосфатный буфер в сборнике. Раствор, отдиализованный против Na-фосфатного буфера, инкубируют при 40-44°С в течение 12 ч. Затем полученный после диализа и инкубации раствор центрифугируют при 10000 g в течение 20 мин при +5°С и пропускают через колонку (V=50 мл) с гранулированным активированным углем. Скорость прохождения раствора фермента через колонку 25 мл/ч. Раствор фермента замораживают до температуры ниже -50°С и лиофильно высушивают. В таблице 5 приведены основные характеристики процесса выделения рибонуклеазы панкреатической (РНК-азы).
В таблице 8 приводятся данные по стадиям получения рибонуклеазы панкреатической в аналоге и прототипе в сравнение с заявляемым способом.
Главными особенностями нашего подхода являются: – использование повышающейся концентрации сульфата аммония как приема, обеспечивающего селективное разделение всех четырех ферментов, содержащихся в сернокислотном экстракте ПЖ КРС после экстракции этанолом при (-18°С); – применение для тонкой очистки РНК-азы ультрафильтрации на полых волокнах и ионообменной хроматографии на колонках с ДЭАЭ-целлюлозой. Предлагаемый способ позволяет: получать четыре фермента (рибонуклеазу панкреатическую, дезоксирибонуклеазу, трипсин и холестеролэстеразу) из поджелудочной железы в рамках единой технологической схемы; более чем в 2 раза увеличить выход препарата рибонуклеазы панкреатической и более чем в 3 раза повысить ее удельную активность по сравнению с прототипом; снизить количество стадий технологического процесса; уменьшить список используемых реактивов.
Формула изобретения
1. Способ получения холестеролэстеразы, трипсина, дезоксирибонуклеазы и рибонуклезы панкреатической из поджелудочной железы крупного рогатого скота, предусматривающий измельчение поджелудочной железы крупного рогатого скота, ее гомогенизацию, экстракцию охлажденным этиловым спиртом, центрифугирование, повторную экстракцию серной кислотой, содержащей сульфат магния, центрифугирование, осаждение балластных белков сульфатом аммония при 30-35%-ном насыщении, центрифугирование, осаждение холестеролэстеразы сульфатом аммония при 45-50% насыщении экстракта, осаждение трипсина – при 60-65% насыщении, осаждение дезоксирибонуклеазы – при 80-85% насыщении, причем полученный при осаждении ДНК-азы супернатант, содержащий рибонуклеазу, подвергают ультрафильтрации и осаждению сернокислым аммонием при 95-98% насыщении с последующим диализом и хроматографической очисткой на колонке с ДЭАЭ-целлюлозой. 2. Способ по п.1, отличающийся тем, что гомогенат экстрагируют холодным этиловым спиртом ((-18)-(+20)°С) в соотношении 1:1,5. 3. Способ по п.1, отличающийся тем, что экстракцию поджелудочной железы проводят 2,5±0,1 мМ раствором серной кислоты, содержащим 5±0,01 мМ сульфата магния в соотношении 1:4-1:8. 4. Способ по п.1, отличающийся тем, что рибонуклеазу панкреатическую подвергают диализу против 30±0,1 мМ Na-фосфатного буфера (рН 6,4±0,01) и инкубации против Na-фосфатного буфера при 40-44°С. 5. Способ по п.1, отличающийся тем, что после диализа рибонуклеазу панкреатическую стерильно фильтруют и осуществляют лиофильную сушку.
РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 28.10.2007
Извещение опубликовано: 10.03.2009 БИ: 07/2009
NF4A – Восстановление действия патента СССР или патента Российской Федерации на изобретение
Дата, с которой действие патента восстановлено: 10.07.2009
Извещение опубликовано: 10.07.2009 БИ: 19/2009
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||


 A (ЕА/кг)
A (ЕА/кг)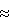 14 кДа (Фиг.1).
14 кДа (Фиг.1).