Патент на изобретение №2311418
|
||||||||||||||||||||||||||
(54) СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРИМЕНЕНИЕ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ
(57) Реферат:
Изобретение описывает соединения общей формулы I /значения радикалов см. в формуле изобретения/, являющиеся новыми антагонистами рецептора гистамина. Предпочтительным соединением является 3-[2-[4-(11,12-дигидро-6Н-бензимидазо[2,1-b][3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2-
Данное изобретение относится к новому антагонисту рецептора гистамина и применению антагониста рецептора гистамина для снижения внутричерепного давления (ICP), в частности для предотвращения и лечения повышенного внутричерепного давления и/или вторичной ишемии, вызываемых, например, черепно-мозговой травмой, более конкретно травматическим (TBI) и нетравматическим повреждением головного мозга. TBI представляет серьезную проблему в развитых странах. В США каждый год около 500000 человек получают черепно-мозговые травмы, которые являются достаточно тяжелыми и требуют госпитализации. Указанные травмы сопровождаются высокой смертностью, при этом примерно у 80000 человек с травматическим повреждением головного мозга жизненно важные функции не восстанавливаются в течение всей последующей жизни, у 5000 человек возникает эпилепсия и 2000 человек постоянно находятся в вегетативном состоянии. В настоящее время TBI является главной причиной смерти и инвалидности у молодежи, и затраты на лечение таких травм составили в 1989 г. более 25 миллиардов долларов. Первичное необратимое повреждение после черепно-мозговой травмы включает кровоизлияние, контузию, некроз нервных клеток и диффузное повреждение аксонов. Подобное повреждение в сочетании с возможным угнетением сердечно-сосудистой деятельности и дыхания может вызвать острые вторичные поражения, включающие отек (поражающий кровеносные сосуды и/или клетки), вторичное кровотечение, изменение объема церебральной крови (CBV), нарушение ауторегуляции церебрального кровотока (CBF) и ишемию. Отек, кровотечение и повышение CBV увеличивают общий объем головного мозга и вследствие этого внутричерепное давление (ICP). Это в свою очередь может привести к дальнейшему развитию ишемии, инфаркта и в тяжелых случаях к образованию грыжи ствола мозга с возможным острым угнетением дыхания и летальным исходом. Поэтому лечение в случае TBI должно быть направлено на прерывание последовательности патологических явлений, уменьшение объема головного мозга и снижение внутричерепного давления. Целью лекарственного лечения является также предотвращение опасного для жизни вторичного повышения внутричерепного давления, что часто происходит, например, после острой фазы травмы или восстановления сердечной деятельности. В настоящее время клинические средства снижения внутричерепного давления весьма ограничены. Стандартные схемы лечения включают хирургическое дренирование желудочков головного мозга, поддержание нормального кровяного давления, вливание маннита, гипервентиляцию легких и введение высоких доз барбитурата. Побочные эффекты нехирургических методов лечения включают ишемию головного мозга, вредное воздействие на внутричерепное давление и повышенный риск бактериальных инфекций и сепсиса. Кроме того, различные соединения, обладающие отличительными механизмами воздействия (например, антагонистическое воздействие на брадикинин и кальций, ингибирование окислительного стресса, блокада рецепторов глутамата и противоэпилептическое воздействие), прошли II и III стадии клинических испытаний или все еще находятся на стадии исследования (причем основное внимание уделяется общему результату, а не ICP). До настоящего времени не было получено разрешение на применение соединения для экстренного лечения внутричерепного давления (K.K. Jain, Chapter 4: Neuroprotection in Acute Trauma, ‘Neuroprotection in CNS Disorders: Commercial Opportunities’. A Jain PharmaBiotech Report: 65-73, 2000). Совершенно очевидно, что существует потребность в фармацевтических препаратах и/или методах лечения повышенного внутричерепного давления (ICP) и/или вторичной ишемии, вызываемых, в частности, черепно-мозговой травмой, более конкретно травматическим повреждением головного мозга (TBI). Авторы настоящего изобретения обнаружили, что производные замещенного тетрациклического имидазола общей формулы (I) обладают антагонистической активностью в отношении Н1- и/или Н2-рецепторов гистамина. Кроме того, установлено, что указанные соединения особенно пригодны для снижения внутричерепного давления (ICP), в частности, для профилактики и лечения повышенного внутричерепного давления и/или вторичной ишемии, вызываемых, в частности, черепно-мозговой травмой, более конкретно травматическим (TBI) и нетравматическим повреждением головного мозга. Кроме того, авторы настоящего изобретения обнаружили, что соединения, являющиеся антагонистами Н1- и/или Н2-рецепторов гистамина (обычно называемые антигистаминными средствами), пригодны также для снижения внутричерепного давления (ICP), в частности, для предотвращения и лечения повышенного внутричерепного давления и/или вторичной ишемии, вызываемых, в частности, травмой головного мозга, более конкретно травматическим (TBI) и нетравматическим повреждением головного мозга. Отличительной особенностью всех соединений является то, что они способны быстро снижать внутричерепное давление при введение в кровоток млекопитающего, в частности, при внутривенном введении. Весьма полезным и очень важным фактором является то, что, снижая ICP, указанные соединения оказывают незначительное воздействие или вообще не воздействуют на кровяное давление, в частности, такие соединения не снижают кровяное давление, что является наиболее желательным свойством потенциального лекарственного средства. До настоящего времени не были получены антагонисты Н1- и/или Н2-рецепторов гистамина, предназначенные для снижения ICP, в частности, для снижения ICP после травмы. Mohanty et al., in Journal of the Neurological Sciences, 1989, 90:87-97 установили, что гистамин играет определенную роль в образовании вызванного травмой отека головного мозга. Повышение содержания воды в головном мозге и уровней гистамина в плазме и головном мозге предотвращали путем предварительного введения циметидина, являющегося антагонистом Н2-рецептора гистамина. Однако мейпирамин (антагонист Н1-рецептора гистамина) не вызывал снижения повышенного содержания воды в головном мозге, при этом уровни гистамина в плазме и головном мозге оставались высокими. До сих пор не было исследовано воздействие антагонистов гистамина на ICP, в частности, на экстренное снижение повышенного внутричерепного давления после травмы, а также на кровяное давление. Не ограничивая себя вышеизложенными теоретическими фактами, авторы настоящего изобретения считают, что с учетом того, что антагонисты рецепторов гистамина способны снижать нормальное внутричерепное давление при отсутствии отека мозга, а также того, что антагонисты рецепторов гистамина не влияют или лишь незначительно влияют на кровяное давление, то есть не вызывают эффект, приписываемый периферической вазодилатации, следует признать, что механизм действия указанных антагонистов не сводится к простому уменьшению отека головного мозга и вазодилатации, в частности, к оказанию таких воздействий, которые, как было известно раньше, присущи антигистаминным средствам. Таким образом, целью настоящего изобретения является создание производных замещенного тетрациклического имидазола общей формулы (I), предназначенных для использования в качестве антагониста гистамина, в частности, в качестве антагониста Н1-рецептора гистамина, более конкретно антагониста Н1- и Н2-рецепторов гистамина, Фармацевтически приемлемые кислотно-аддитивные соли включают терапевтически активные нетоксичные кислотно-аддитивные соли, которые могут образовывать соединения формулы (I). Указанные кислотно-аддитивные соли можно получить, обрабатывая основную форму соединений формулы (I) соответствующими кислотами, например, неорганическими кислотами, такими как галогенводородная кислота, в частности, хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота и фосфорная кислота; органическими кислотами, такими как уксусная кислота, гидроксиуксусная кислота, пропановая кислота, молочная кислота, пировиноградная кислота, щавелевая кислота, малоновая кислота, янтарная кислота, малеиновая кислота, фумаровая кислота, яблочная кислота, винная кислота, лимонная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, цикламиновая кислота, салициловая кислота, п-аминосалициловая кислота и памовая кислота. Соединения формулы (I), содержащие кислотные протоны, могут быть также превращены в терапевтически активные нетоксичные основно-аддитивные соли в результате обработки соответствующими органическими и неорганическими основаниями. Соответствующие основные соли включают, например, соли аммония, соли щелочных и щелочноземельных металлов, в частности, соли лития, натрия, калия, магния и кальция, соли с органическими основаниями, такие как соли бензатина, N-метил-D-глюкамина, гибрамина, и соли с аминокислотами, такими как аргинин и лизин. И наоборот, указанные кислотно- или основно-аддитивные соли могут быть превращены в свободные формы в результате обработки соответствующим основанием или кислотой. Термин “аддитивная соль” в значении, используемом в данной заявке, означает также сольваты, которые могут образовывать соединения формулы (I), и их соли. Такими сольватами являются, например, гидраты и алкоголяты. Среди кислотно-аддитивных солей наиболее предпочтительным соединением является гидрат (1:1) (Е)-2-бутендиоата 3-[2-[4-(11,12-дигидро-6Н-бензимидазо[2,1-b][3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2- Особенно предпочтительными соединениями являются (А)[(2 N-оксиды соединений формулы (I) являются соединениями формулы (I), в которых один или несколько атомов азота окислены в так называемые N-оксиды, в частности, такие N-оксиды, в которых один или несколько атомов азота пиперидинильного радикала в формуле (I) представляют собой N-окислен. Термин “стереохимические изомерные формы” в используемом значении означает все возможные изомерные формы, которые могут иметь соединения формулы (I). За исключением особо оговоренных случаев, данное химическое обозначение соединений включает смесь всех возможных стереохимически изомерных форм, причем указанные смеси содержат все диастереомеры и энантиомеры основной молекулярной структуры. В частности, стереогенные центры могут иметь R- или S-конфигурацию; заместители двухвалентных циклических (частично) насыщенных радикалов могут иметь цис- или транс-конфигурацию. Соединения, включающие двойные связи, могут иметь Е- или Z-стереохимическую структуру в положении указанной двойной связи. Совершенно очевидно, что стереохимически изомерные формы соединений формулы (I) входят в объем данного изобретения. В соответствии с условными обозначениями номенклатуры CAS при наличии в молекуле двух стереогенных центров известной абсолютной конфигурации идентификатор R или S присваивается (на основе правила последовательности Кана-Инголда-Прелога) хиральному центру с наименьшим номером, который является центром отсчета. Для обозначения конфигурации второго стереогенного центра используют относительные идентификаторы [R*,R*] или [R*,S*], где R* всегда определяется как центр отсчета, [R*,R*] обозначает центры с одинаковой хиральностью и [R*,S*] обозначает центры с разной хиральностью. Например, если хиральный центр с наименьшим номером в молекуле имеет S-конфигурацию и второй центр имеет R-конфигурацию, идентификатор стереоизомера должен определяться как S-[R*,S*]. При использовании символов “ Когда связь в положении “с” является простой связью, соединения формулы (I) и некоторые промежуточные соединения имеют по крайней мере два стереогенных центра в своей структуре. Когда R1 не является водородом, моноциклическое N-кольцо в формуле (I) имеет еще один стереогенный центр. Таким образом можно получить 8 стереохимически разных структур. Соединения формулы (I), полученные описанными ниже способами, можно синтезировать в форме рацемических смесей энантиомеров, которые могут быть отделены друг от друга при помощи методов разделения, известных в данной области. Рацемические соединения формулы (I) можно превратить в соответствующие диастереомерные соли, осуществляя взаимодействие с приемлемой хиральной кислотой. Указанные диастереомерные соли затем разделяют, например, селективной или фракционной кристаллизацией и выделяют из них энантиомеры путем щелочной обработки. Альтернативный метод разделения энантиомерных форм соединений формулы (I) включает применение жидкостной хроматографии с использованием хиральной стационарной фазы. Указанные чистые стереохимически изомерные формы можно также получить из соответствующих чистых стереохимически изомерных форм соответствующих исходных веществ при условии выполнения стереоспецифического взаимодействия. Если необходимо получить специфический стереоизомер, указанное соединение предпочтительно синтезируют стереоспецифическими методами получения. При осуществлении указанных методов преимущественно используют энантиомерно чистые исходные вещества. Соединения формулы (I) могут также существовать в таутомерной форме. Несмотря на то, что такие формы не отражены в полной мере в приведенной выше формуле, они входят в объем настоящего изобретения. Например, соединения формулы (I), в которой R5 означает Н, могут существовать в соответствующей таутомерной форме. В объем настоящего изобретения входят также производные соединения (обычно именуемые “пролекарствами”) фармакологически активных соединений по данному изобретению, которые расщепляются in vivo с образованием соединений по данному изобретению. Пролекарства обычно (но не всегда) оказывают менее сильное воздействие на рецептор-мишень по сравнению с соединениями, в которые они превращаются в результате расщепления. Пролекарства особенно пригодны в тех случаях, когда химические или физические свойства желаемого соединения затрудняют или делают неэффективным процесс его введения. Например, требуемое соединение может плохо растворяться, плохо переноситься через эпителий слизистой оболочки или иметь нежелательно короткий период полувыведения из плазмы. Пролекарства более подробно рассмотрены в статьях Stella, V.J. et al., “Prodrugs”, Drug Delivery Systems, 1985, pp. 112-176, and Drugs, 1985, 29, pp. 455-473. Пролекарственные формы фармакологически активных соединений по данному изобретению обычно представляют собой соединения формулы (I), их фармацевтически приемлемые кислотно- или основно-аддитивные соли, стереохимически изомерные формы и N-оксиды, имеющие кислотную группу, которая этерифицирована или амидирована. К таким этерифицированным кислотным группам относятся группы формулы -COORх, где Rх означает С1-6 алкил, фенил, бензил или одну из нижеследующих групп:
В данном описании изобретения “DMF” (ДМФА) означает N,N-диметилформамид, “DIPE” означает диизопропиловый эфир, “THF” (ТГФ) означает тетрагидрофуран, “MIBK” означает метилизобутилкетон, “DIPA” означает диизопропиламин. А. Получение промежуточных соединений Пример А1 а) Получение промежуточного соединения 1 d) Получение промежуточного соединения 4 е) Получение промежуточного соединения 5 Пример А2 а) Получение промежуточного соединения 6 Пример А3 а) Получение промежуточного соединения 10 ]бензимидазол-4(10Н)-она (промежуточное соединение 22). b) Получение промежуточного соединения 23 ]бензимидазол-4(10Н)-она (промежуточное соединение 23). с) Получение промежуточного соединения 24 |
||||||||||||||||||||||||||
| 10 | В1 | 2-бензил | ,4 )(В)] )(В)] |
|||||||||||||||||||||||
,4 )(В)];.Н2О (1:2) )(В)];.Н2О (1:2) |
||||||||||||||||||||||||||
| 12 | В1 | 2-бензил | ,4 )(В)] )(В)] |
|||||||||||||||||||||||
| 13 | В1 | 2-бензил | ,4 )(В)] )(В)] |
|||||||||||||||||||||||
| 14 | В1 | Н | ,4 )(А)]; (Е)-2-бутен диоат (2:3) )(А)]; (Е)-2-бутен диоат (2:3) |
|||||||||||||||||||||||
| 16 | В1 | 2-бензил | -СН2-СН2– | [А(2 ,4 ,4 )(В)] )(В)] |
||||||||||||||||||||||
| 17 | В1 | 2-бензил | -СН2-СН2– | [В(2 ,4 ,4 )(В)] )(В)] |
||||||||||||||||||||||
,4 )(В)] )(В)] |
||||||||||||||||||||||||||
| 20 | В1 | 2-бензил | ,4 )(В)] )(В)] |
|||||||||||||||||||||||
| 21 | В1 | 2-бензил | ,4 )(В)] )(В)] |
|||||||||||||||||||||||
| 22 | В1 | 2-бензил | ,4 )(В)] )(В)] |
|||||||||||||||||||||||
| 23 | В1 | 2-бензил | ,4 )(В)] )(В)] |
|||||||||||||||||||||||
,4 )(В)] )(В)] |
||||||||||||||||||||||||||
| 25 | В1 | 2-бензил | 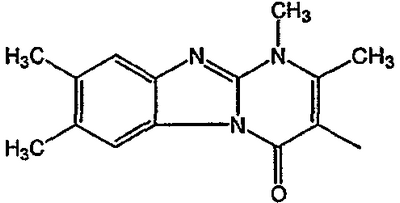 |
-СН2-СН2– | [(2 ,4 ,4 )(В)] )(В)] |
|||||||||||||||||||||
| 26 | В1 | 2-бензил | ,4 )(В)];.Н2О (1:1) )(В)];.Н2О (1:1) |
|||||||||||||||||||||||
| 27 | В1 | 2-бензил | ,4 )(В)] )(В)] |
|||||||||||||||||||||||
| 28 | В1 | 2-бензил | ,4 )(В)] )(В)] |
|||||||||||||||||||||||
| -СН2-СН2– | [(2 ,4 ,4 )(В)] )(В)] |
|||||||||||||||||||||||||
| 30 | В1 | 2-бензил | ,4 )(А)] )(А)] |
|||||||||||||||||||||||
| 31 | В1 | 2-бензил | ,4 )(В)] )(В)] |
|||||||||||||||||||||||
| 32 | В1 | 2-бензил | ,4 )(В)] )(В)] |
|||||||||||||||||||||||
| 33 | В1 | 2-бензил | ,4 )(В)] )(В)] |
|||||||||||||||||||||||
| 34 | В1 | 2-бензил | ,4 )(В)]; Н2О (1:1) )(В)]; Н2О (1:1) |
|||||||||||||||||||||||
,4 )(В)]; Н2О (1:1) )(В)]; Н2О (1:1) |
||||||||||||||||||||||||||
| 36 | В1 | 2-бензил | ,4 )(В)]; Н2О (1:1) )(В)]; Н2О (1:1) |
|||||||||||||||||||||||
| 37 | В1 | 2-бензил | -СН2-СН2– | [(2 ,4 ,4 )(В)] )(В)] |
||||||||||||||||||||||
| 38 | В1 | 2-бензил | -СН2-СН2– | [(2 ,4 ,4 )(В)]; Н2О (1:1) )(В)]; Н2О (1:1) |
||||||||||||||||||||||
| 39 | В1 | 2-бензил | -СН2-СН2– | [(2 ,4 ,4 )(В)]; Н2О (1:1) )(В)]; Н2О (1:1) |
||||||||||||||||||||||
| 40 | В1 | 2-бензил | -СН2-СН2– | [(2 ,4 ,4 )(В)] )(В)] |
||||||||||||||||||||||
,4 )(В)] )(В)] |
||||||||||||||||||||||||||
| 42 | В1 | 2-бензил | -СН2-СН2– | [(2 ,4 ,4 )(В)] )(В)] |
||||||||||||||||||||||
| 43 | В1 | 2-бензил | ,4 )(А)] )(А)] |
|||||||||||||||||||||||
| 44 | В1 | 2-бензил | 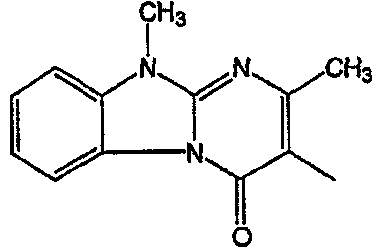 |
-СН2-СН2– | [А(2 ,4 ,4 )(А)] )(А)] |
|||||||||||||||||||||
| 45 | В1 | 2-бензил | 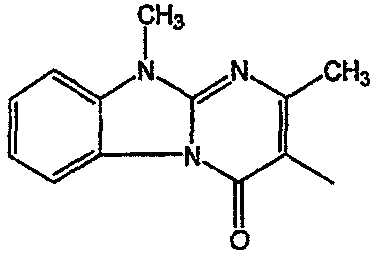 |
-СН2-СН2– | [В(2 ,4 ,4 )(А)] )(А)] |
|||||||||||||||||||||
| 46 | В1 | 2-бензил | -СН2-СН2– | [А(2 ,4 ,4 )(В)]; трифтор ацетат (1:1) )(В)]; трифтор ацетат (1:1) |
||||||||||||||||||||||
,4 )(В)]; трифтор ацетат (1:1) )(В)]; трифтор ацетат (1:1) |
||||||||||||||||||||||||||
| 48 | В1 | 2-бензил | -СН2-СН2– | [(2 ,4 ,4 )(А)] )(А)] |
||||||||||||||||||||||
| 49 | В1 | 2-бензил | 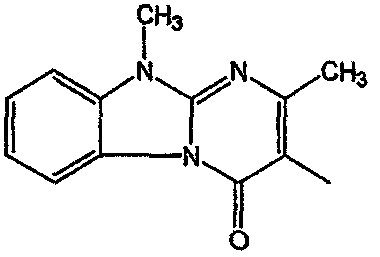 |
-СН2-СН2– | [(2 ,4 ,4 )(А)]; (-)-S(R*,R*)]-2,3-дигидрокси бутандиоат (1:2) )(А)]; (-)-S(R*,R*)]-2,3-дигидрокси бутандиоат (1:2) |
|||||||||||||||||||||
| 50 | В1 | 2-бензил | -СН2-СН2– | [(2 ,4 ,4 )(А)]; HCl(1:3).H2O (1:2) )(А)]; HCl(1:3).H2O (1:2) |
||||||||||||||||||||||
| 51 | В1 | 2-бензил | ,4 )(А)]; H2O (1:2) )(А)]; H2O (1:2) |
|||||||||||||||||||||||
| 52 | В1 | 2-бензил | -СН2-СН2– | [(2 ,4 ,4 )(А)] )(А)] |
||||||||||||||||||||||
| 53 | В1 | 2-бензил | ,4 )(А)] )(А)] |
|||||||||||||||||||||||
| -СН2-СН2– | [(2 ,4 ,4 )(А)]; (Е)-2-бутен диоат (1:1) )(А)]; (Е)-2-бутен диоат (1:1) |
|||||||||||||||||||||||||
| 55 | В1 | 2-бензил | -СН2-СН2– | [(2 ,4 ,4 )(А)]; (Е)-2-бутен диотат (1:1).Н2О(1:2) )(А)]; (Е)-2-бутен диотат (1:1).Н2О(1:2) |
||||||||||||||||||||||
| 2 | В1 | 2-бензил | -СН2-СН2– | [А(2 ,4 ,4 )(А)]; (Е)-2-бутен диоат (2:3).Н2О (1:1) )(А)]; (Е)-2-бутен диоат (2:3).Н2О (1:1) |
||||||||||||||||||||||
| 1 | В1 | 2-бензил | -СН2-СН2– | [В(2 ,4 ,4 )(А)]; (Е)-2-бутен диоат (2:3).Н2О (1:1) )(А)]; (Е)-2-бутен диоат (2:3).Н2О (1:1) |
||||||||||||||||||||||
| 56 | В1 | 2-бензил | -СН2-СН2-СН2– | [(2 ,4 ,4 )(В)] )(В)] |
||||||||||||||||||||||
| 57 | В1 | 2-бензил | 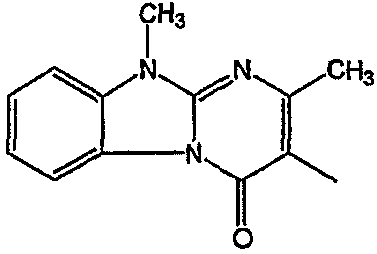 |
-СН2-СН2– | [А(2 ,4 ,4 )(А)] )(А)] |
|||||||||||||||||||||
| 58 | В1 | 2-бензил | -СН2-СН2– | [В(2 ,4 ,4 )(А)] )(А)] |
||||||||||||||||||||||
,4 )(А)] )(А)] |
||||||||||||||||||||||||||
| 60 | В1 | 2-бензил | -СН2-СН2– | [(2 ,4 ,4 )(В)] )(В)] |
||||||||||||||||||||||
| 109 | В1 | 2-бензил | -СН2– | [(2 ,4 ,4 )(В)] )(В)] |
||||||||||||||||||||||
| 152 | В1 | Н | -СН2-СН2– | |||||||||||||||||||||||
| 153 | В1 | Н | -СН2-СН2-СН2– | (Е)-2-бутен диоат (2:5) | ||||||||||||||||||||||
| Таблица 2 | |||||
,4 )(В)] )(В)] |
|||||
| 74 | В2 | 2-бензил | -CH=CH-S- | [(2 ,4 ,4 )(А)] )(А)] |
|
| 75 | В2 | 2-бензил | -CH=CH-S- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 76 | В2 | 2-бензил | -CH=CH-S- | [(2 ,4 ,4 )(А)]; (Е)-2-бутендиоат (1:2) этанолат (1:1) )(А)]; (Е)-2-бутендиоат (1:2) этанолат (1:1) |
|
,4 )(А)] )(А)] |
|||||
| 78 | В2 | -CH=CH-S- | [(2 ,4 ,4 )(В)] )(В)] |
||
| 79 | В2 | -CH=CH-S- | [(2 ,4 ,4 )(В)] )(В)] |
||
| 80 | В2 | 2-бензил | -CH=CH-CH=CH- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 81 | В2 | 2-бензил | -CH=CH-CH=CH- | [(2 ,4 ,4 )(А)] )(А)] |
|
| 82 | В2 | 2-бензил | -CH=CH-CH=CH- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 83 | В2 | 2-метилнафтил | -CH=CH-S- | [(2 ,4 ,4 )(А)] )(А)] |
|
| 84 | В2 | 2-метилнафтил | -CH=CH-S- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 85 | В2 | 2-метилнафтил | -CH=CH-S- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 86 | В2 | 2-метилнафтил | -CH=CH-S- | [(2 ,4 ,4 )(А)]; Н2О (1:1) этанолат (1:1) )(А)]; Н2О (1:1) этанолат (1:1) |
|
| 87 | В2 | 3-метил | -CH=CH-S- | А-транс | |
| 88 | В2 | 3-метил | -CH=CH-S- | В-транс | |
| 89 | В2 | 3-метил | -CH=CH-CH=CH- | [(3 ,4 ,4 )(В)] )(В)] |
|
,4 )(А)] )(А)] |
|||||
| 91 | В2 | 3-метил-(4-фторфенил) | -CH=CH-S- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 92 | В2 | 3-метил-(4-фторфенил) | -CH=CH-S- | [(2 ,4 ,4 )(А)] )(А)] |
|
| 93 | В2 | 3-метил-(4-фторфенил) | -CH=CH-S- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 94 | В2 | 3-метил | -CH=CH-CH=CH- | [(3 ,4 ,4 )(А)] )(А)] |
|
| 95 | В2 | 2-бензил | -CH=C(CH3)-N(CH3)- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 96 | В2 | 2-бензил | -CH=CH-N(CH3)- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 97 | В2 | 2-бензил | -CH=CH-CH=C(CH3)- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 98 | В2 | 2-бензил | -CH2-CH2-S- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 99 | В2 | 2-бензил | -СН2-С(СН3)=N-N(CH3)- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 100 | В2 | 2-бензил | -CH=C(CH3)-CH=CH- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 101 | В2 | 2-бензил | -C(CH3)=CH-C(CH3)=CH- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 102 | В2 | 2-бензил | -CH=C(Cl)-CH=C(Cl)- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 103 | В2 | 2-бензил | -CH=C(CF3)-CH=C(Cl)- | [(2 ,4 ,4 )(В)] )(В)] |
|
| 104 | В2 | 4-метил | -CH=CH-S- | ||
| 105 | В2 | 2-метил циклогексил | -CH=CH-CH=CH- | ||
| 106 | В2 | 2-бензил | -CH=CH-S- | [А(2 ,4 ,4 )(В)] )(В)] |
|
| 107 | В2 | 2-бензил | -CH=CH-S- | [В(2 ,4 ,4 )(В)] )(В)] |
|
,4 )(В)] )(В)] |
|||||
,4 )(В)] )(В)] |
|||||
| 121 | В2 | 2-бензил | Н | -CH=CH-CH=CH- | [(2 ,4 ,4 )(А)] )(А)] |
| 122 | В2 | Н | Н | -CH2-CH2-CH2-CH2– | |
| 123 | В2 | Н | Н | -CH2-CH2-CH2-S- | |
| 124 | В2 | Н | Н | -CH=CH-CH=CH- | |
| 125 | В2 | Н | Н | -CH2=CH2-S- | |
| 126 | В2 | Н | Н | -C(CH3)=CH-S- | |
| 127 | В2 | Н | Н | -CH=C(CH3)-CH=CH- | |
| 128 | В2 | Н | Н | -CH=CH-CH=C(CH3)- | |
| 129 | В2 | Н | Н | -CH2-C(CH3)=N-N(CH3)- | |
| 130 | В2 | Н | Н | -CH=CH-N(CH3)- | |
| 131 | В2 | Н | Н | -CH=C(CH3)-N(CH3)- | |
| 132 | В2 | Н | Н | -O-C(CH3)=CH- | (Е)-2-бутендиоат (1:2) |
| 133 | В2 | Н | Н | -C(CH3)=N-N(CH3)- | Н2О (1:1) |
| 134 | В2 | 2-бензил | Н | -CH=CH-CH=CH- | [(2 ,4 ,4 )(В)] )(В)] |
| 135 | В2 | 2-бензил | Н | -CH=CH-CH=CH- | [(2 ,4 ,4 )(А)] )(А)] |
| 136 | В2 | Н | Н | -CH=CH-S- | этандиоат (2:5).Н2О (2:1) |
| Таблица 6 | ||||||
,4 )(В)] )(В)] |
||||||
| 147 | В2 | -СН2– | Н | -NH2 | -СН3 | (Z)-2-бутендиоат (1:3) Н2О (1:1) |
| 148 | В2 | -СН2– | Н | -СН3 | ||
| 149 | В2 | -СН2– | Н | -СН3 | ||
| 151 | В2 | -СН2– | Н | -СН3 | HCl (1:3) H2O (1:2).2-пропанолат (2:1) | |
С. Фармакологические примеры
С1. Определение in vitro антагонистической активности в отношении Н1- и Н2-рецепторов гистамина
Исследования связывания рецептора с меченым лигандом выполняли in vitro для определения связывания выбранных соединений с меченым лигандом, используя препарат ткани, обогащенный конкретным рецептором, то есть Н1- или Н2-рецептором гистамина. Ткань, используемая для Н1-рецептора гистамина, представляла собой клетки яичника китайского хомячка (СНО), постоянно трансфецированные Н1-рецептором гистамина человека. Только дифенгидрамин испытывали с использованием клеток коры головного мозга морской свинки. Конкурентное ингибирование [3H]-пириламина испытуемыми соединениями исследовали, инкубируя меченый лиганд в низкой (нМ) концентрации с небольшим образцом препарата ткани (0,2-5 мл; 1-5 мг ткани) в забуференной среде, содержащей испытуемые соединения, растворенные в ДМСО, в диапазоне концентраций, отличающихся по крайней мере на 4 порядка величины от значения pIC50, установленного на основании кривой ингибирования. Антагонистическую активность в отношении Н2-рецептора гистамина испытывали по существу так же, как антагонистическую активность в отношении Н1-рецептора гистамина, используя клетки полосатого тела морской свинки и [125I]АРТ в качестве меченого лиганда в концентрации 0,1 нМ. Инкубацию производили в течение 150 минут при 22°С.
Все соединения по настоящему изобретению обладали антагонистической активностью в отношении Н1-рецептора гистамина, соответствующей значению pIC50, равному 5 или большей величине. Несколько соединений обладали антагонистической активностью в отношении Н1-рецептора гистамина, соответствующей значению pIC50, равному 6 или большей величине. Указанные соединения приведены в таблице 9. Кроме того, установлено, что коммерчески производимый типичный антагонист Н1-рецептора гистамина (дифенгидрамин) обладает лишь незначительно более высокой антагонистической активностью в отношении Н1-рецептора гистамина по сравнению с большинством соединений по данному изобретению. Далее установлено, что коммерчески производимые антагонисты Н2-рецептора гистамина (ранитидин и циметидин) характеризуются антагонистической активностью в отношении Н2-рецептора гистамина в диапазоне (умеренно высокой) активности соединений по данному изобретению в отношении Н2-рецептора гистамина. Некоторые соединения, приведенные в таблице 9, в том числе коммерчески производимые соединения, были также испытаны in vivo в отношении их способности снижать внутричерепное давление (ICP).
| Таблица 9 Результаты исследования модели антагонистической активности в отношении Н1- и Н2-рецепторов гистамина |
||
| Соединение № | Антагонистическая активность в отношении Н1-рецептора гистамина (pIC50) | Антагонистическая активность в отношении Н2-рецептора гистамина (pIC50) |
| 14 | 7,6 | |
| 94 | 7,0 | |
| 104 | 7,0 | |
| 46 | 6,9 | |
| 110 | 6,9 | |
| 1 (испытано также in vivo) | 6,7 | 6,0 |
| 6 | 6,7 | |
| 23 | 6,7 | |
| 78 | 6,7 | |
| 81 | 6,7 | |
| 82 | 6,7 | |
| 50 | 6,6 | |
| 55 | 6,6 | |
| 87 | 6,6 | |
| 12 | 6,5 | |
| 13 | 6,5 | |
| 15 (испытано также in vivo) | 6,5 | |
| 45 (испытано также in vivo) | 6,5 | |
| 48 | 6,5 | |
| 49 | 6,5 | |
| 53 | 6,5 | |
| 54 | 6,5 | |
| 83 | 6,5 | |
| 88 | 6,5 | |
| 20 | 6,4 | |
| 32 (испытано также in vivo) | 6,4 | |
| 47 (испытано также in vivo) | 6,4 | |
| 57 | 6,4 | |
| 58 | 6,4 | |
| 105 | 6,4 | |
| 29 | 6,3 | |
| 51 | 6,3 | |
| 84 | 6,3 | |
| 17 (испытано также in vivo) | 6,2 | |
| 27 | 6,2 | |
| 37 | 6,2 | |
| 2 (испытано также in vivo) | 6,1 | |
| 30 (испытано также in vivo) | 6,1 | |
| 35 | 6,1 | |
| 56 | 6,1 | |
| 89 | 6,1 | |
| 90 | 6,1 | |
| 9 (испытано также in vivo) | 6,0 | |
| 31 | 6,0 | |
| 41 | 6,0 | |
| 44 (испытано также in vivo) | 6,0 | |
| 102 | 6,0 | |
| Ранитидин (испытан также in vivo) | – | 5,5 |
| Циметидин | – | 5,9 |
| Дифенгидрамин (испытан также in vivo) | 7,2 | – |
С.2. Фармакология in vivo
Модель закрытой черепно-мозговой травмы (CHI)
Для испытания соединений по данному изобретению и коммерчески производимых соединений была использована клинически обоснованная модель травматического повреждения головного мозга у крыс. Вышеуказанная модель, имитирующая несколько клинических признаков травматического повреждения головного мозга, таких как повышенное внутричерепное давление, пониженное давление мозгового кровоснабжения, морфологические изменения, включающие диффузное поражение аксонов, некроз нервных клеток и контузию, нарушение ауторегуляции мозгового кровотока и уменьшение оксигенации головного мозга, была использована для исследования лекарственных средств, снижающих внутричерепное давление. Травму вызывали у интубированных, анестезированных изофлураном (1,5% изофлурана в смеси 30% О2 и 70% N2O) крыс Sprague-Dawley (380-400 г), которых помещали в стереотаксическом положении на стол, смонтированных на 4 пружинах. 400-граммовый стальной цилиндр, защищенный кремниевым диском с диаметром 9 мм, опускали в падении на незащищенный череп с высоты 70 см или 50 см (соответственно “тяжелая” и “средней тяжести” черепно-мозговая травма). Область нанесения удара была сцентрирована между брегмой и ламбдой. Внутричерепное давление регистрировали при помощи зонда с микродатчиком Кодмана, вводимого в теменную область коры головного мозга. В случае как тяжелой черепно-мозговой травмы, так и черепно-мозговой травмы средней тяжести внутричерепное давление повышалось сразу же после травмы и оставалось повышенным в течение нескольких дней. Модель тяжелой черепно-мозговой травмы была использована для оценки фармакологического действия лекарственных средств сразу же после травмы (метод отсеивания). Выживших и пришедших в себя после анестезии крыс исследовали по типу модели черепно-мозговой травмы средней тяжести. В фармакологических исследованиях были использованы животные с патологическим внутричерепным давлением от 12,5 до 35 мм Hg. Изменения внутричерепного давления, среднего артериального кровяного давления (МАВР) и давления мозгового кровоснабжения СРР (=МАВР-СРР) выражали в виде процентного значения от исходной величины в момент начала лечения.
Метод отсеивания, используемый для оценки соединений по данному изобретению
Четыре подвергаемых лечению группы по 3 крысы в каждой группе каждую неделю сравнивали с 3 животными, которым вводили физиологический раствор. Так как обычные статистические методы требуют большего числа животных, был использован последовательный метод. Последовательные методы включают несколько ступеней отбора. На каждой ступени выбирали как можно более однородную группу животных. Животных произвольно распределяли для введения лекарственных средств или физиологического раствора. Такой метод позволял принять решение о прекращении введения лекарственного средства, признании лекарственного средства активным или использовании новой группы животных на следующей ступени. Принимая во внимание биологически обоснованный уровень активности, который должен быть обнаружен, была определена и зафиксирована ожидаемая часть ложных положительных и отрицательных результатов. Был использован критерий последовательной оценки групп животных, основанный на двойной выборке. Трехступенчатый последовательный метод с использованием относительно небольшого числа животных на каждой ступени оказался оптимальным. Несмотря на изменчивость отдельных данных, указанный метод позволил состоятельно оценить стандартное лечение маннитом как активное, в то время как контрольные животные были отсеяны. Клинически обоснованные внутривенные дозы маннита (3 г в течение 45 минут) значительно снижали внутричерепное давление (среднее снижение составило примерно 20%).
| Таблица 10 Результаты метода отсеивания |
||
| Лечение (1) | Дельта-изменение в % (2) | Решение (3) |
| Соединение 9 | -12,4 | активное |
| Соединение 15 | -23,3 | активное |
| Соединение 17 | -8,9 | активное |
| Соединение 30 | -9,3 | активное |
| Соединение 32 | -13,9 | активное |
| Соединение 44 | -14,8 | активное |
| Соединение 45 | -13,1 | активное |
| Соединение 47 | -12,0 | активное |
| CD 10% | 5,1 | неактивное |
| CD 10% + 3H2T | 10,0 | неактивное |
| CD 20% | 19,1 | неактивное |
| CD 20% + HCl | 2,4 | неактивное |
| Маннит1 | -21,7 | активное |
| Маннит2 | -22,1 | активное |
| Маннит3 | -13,0 | активное |
| Маннит4 | -19,3 | активное |
| Маннит5 | -19,9 | активное |
(1) Испытуемые соединения вводили в виде болюса в дозе 1 мг/кг в течение 1 минуты с последующим вливанием 0,5 мг/кг/мин в течение 44 минут; растворители вводили в виде болюса в дозе 0,4 мл в течение 1 минуты с последующим вливанием 0,2 мл/мин в течение 44 минут; маннит вводили в виде вливания 67 мг/кг/мин в течение 45 минут.
(2) Дельта-изменение в % означает среднее изменение относительного внутричерепного давления от исходного уровня за период лечения.
(3) Решение основано на последовательной статистической оценке.
CD=гидроксипропил- -циклодекстрин, используемый в качестве растворителя.
-циклодекстрин, используемый в качестве растворителя.
Н2Т = винная кислота, используемая в качестве растворителя.
Маннит1-5: маннит оценивали 5 раз в отдельных испытаниях (положительные контрольные образцы). В таблице приведены результаты всех испытаний.
Дальнейшие исследования
В таблице 11 показаны изменения некоторых важных физиологических параметров у крыс, зарегистрированные во время лечения после тяжелой закрытой черепно-мозговой травмы. Лечение, которое начинали через 20 минут после тяжелой черепно-мозговой травмы, включало введение дозы, равной 0,5 мг/кг/мин, в течение 10 минут с последующим введением 0,1 мг/кг/мин в течение 50 минут.
| Таблица 11 Изменение важных физиологических параметров у крыс во время лечения после тяжелой закрытой черепно-мозговой травмы |
||||
| Растворитель (n=10) | Соединение 2 (n=10) | Соединение 1 (n=10) | Рацемат (соединение 1 и соединение 2) (n=10) | |
| ICP (%) | 1,6 (-9,4; 11,1) | -15,3 (-20,0; -9,5)* | -15,4 (-22,6; -11,5)* | -19,1 (-24,9; -10,8)* |
| МАВР (%) | -1,2 (-2,7; 3,7) | 18,8 (-2,0; 31,0)* | -3,6 (-11,9; -1,5) | 0,6 (-5,1; 8,5) |
| СРР (%) | -1,3 (-8,0; 5,8) | 24,2 (0,9; 43,6)* | -1,9 (-8,9; 0,4) | 7,5 (-2,4; 15,5) |
| ETCO2 (%) | 8,0 (-1,2; 12,9) | -4,4 (-8,9; 2,3)* | 2,2 (-0,8; 8,4) | 2,4 (-7,8; 3,8) |
| Частота сердечных сокращений (%) | -2,7 (-5,4; 3,9) | -9,6 (-21,8; 0,7) | -4,1 (-11,4; 1,9) | 5,6 (-11,7; 0,4) |
| Частота дыхания (%) | 3,6 (-4,3; 11,8) | 6,6 (-1,3; 14,6) | 5,3 (-3,3; 13,6) | 9,6 (3,0; 14,8) |
| Среднее изменение за весь период лечения, выраженное в виде % значения изменения от исходной величины. Приведенные значения являются средними величинами (95% C.I.) * = Значения, существенно отличающиеся от группы, получавшей растворитель (р<0,05, критерий Даннета) Растворитель: 10% гидроксипропил-бета-циклодекстрин, винная кислота, NaOH и маннит в пирогенной воде; рН 4; осмотическое давление 312-314 mOsm/кг; концентрация соединения 2 мг/мл Соединение: гидрат (1:1) (Е)-2-бутендиоата 3-[2-[4-(11,12-дигидро-6Н-бензимидазо[2,1-b][3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2-  ]бензимидазол-4(10Н)-она (2:3) ]бензимидазол-4(10Н)-она (2:3)Соединение 1: (В)[(2  ,4 ,4 )(А)] )(А)]Соединение 2: (А)[(2  ,4 ,4 )(А)] )(А)]Рацемат (соединение 1 и соединение 2): (2  ,4 ,4 )(А), то есть рацемическая смесь соединения 1 и соединения 2 )(А), то есть рацемическая смесь соединения 1 и соединения 2ICP: внутричерепное давление МАВР: среднее артериальное кровяное давление СРР: давление мозгового кровоснабжения ETCO2: конечное количество СО2, обмениваемого за одно дыхание |
||||
Воздействие соединения 2 на МАВР гораздо менее выражено при введении данного соединения в виде непрерывного вливания в количестве 0,1 мг/кг/мин. В данном случае отсутствует пик кровяного давления и не наблюдаются увеличения МАВР более чем на 20% (среднее увеличение МАВР в конце вливания составляет 9%, n=6). Максимальное снижение внутричерепного давления при указанной дозе сравнимо с величиной, наблюдаемой в том случае, когда вливанию предшествует введение “ударной дозы”, равной 5 мг/кг, в течение 10 минут, но время, необходимое для достижения такого эффекта, является более продолжительным (в среднем 30 минут).
Воздействие ранитидина и дифенгидрамина на внутричерепное давление
Ранитидин вливали крысам, используемым в качестве модели закрытой черепно-мозговой травмы, в дозе 2 мг/кг/мин в течение 6 минут после нанесения тяжелой черепно-мозговой травмы. Растворитель (NaCl+H2T) вводили в том же количестве. В каждой группе подвергали лечению 6 крыс. Ранитидин вызывал статистически значимое более выраженное снижение внутричерепного давления по сравнению с группой животных, которым вводили растворитель (снижение на 7,7% по сравнению с 0,5%, что является статистически значимым показателем при р=0,013). Процентное значение снижения внутричерепного давления высчитывали в виде % изменения ICP, зарегистрированного в начале лечения и в конце вливания. Существенного изменения кровяного давления не наблюдалось.
Дифенгидрамин вливали крысам, используемым в качестве модели закрытой черепно-мозговой травмы, в дозе 1 мг/кг/мин в течение 10 минут после нанесения тяжелой черепно-мозговой травмы. Лечению подвергали трех крыс. Дифенгидрамин вызывал 34% снижение внутричерепного давления без какого-либо значительного влияния на кровяное давление.
Сравнительные исследования с использованием агонистов
Для сравнения испытывали два коммерчески производимых агониста Н2-рецептора гистамина (димаприт и импромидин), которые вливали нетравмированным крысам в дозе 0,5 мг/кг/мин в течение 10 минут для димаприта и в дозах, увеличенных до 3,75 мг/кг/час, для импромидина. Не наблюдалось никакого эффекта. При введении димаприта в высокой дозе, равной 2 мг/кг/мин, в течение 10 минут и импромидина в виде болюса в дозе 0,5 мг/кг наблюдалось снижение кровяного давления и ICP, которые восстанавливались после лечения.
На основании полученных данных был сделан вывод о том, что антагонисты Н1- и/или Н2-рецепторов гистамина вызывают снижение ICP и при этом не оказывают существенного влияния на кровяное давление.
Эксперименты с использованием коммерчески производимых антагонистов Н1- и Н2-рецепторов гистамина
Несколько коммерчески производимых антагонистов Н1- и Н2-рецепторов гистамина вливали крысам, используемым в качестве модели закрытой черепно-мозговой травмы, в дозе 0,5 мг/кг/мин в течение 10 минут после нанесения тяжелой черепно-мозговой травмы. Растворитель (NaCl+H2T) вводили в том же количестве. В каждой группе подвергали лечению 6 крыс. Результаты изменения ICP и кровяного давления в течение первых 15 минут суммированы в таблице 12.
| Таблица 12 Действие коммерчески производимых антагонистов Н1- и Н2-рецепторов гистамина |
||
| Соединение | Воздействие на ICP | Воздействие на кровяное давление |
| Растворитель | 0 | 0 |
| Циклодекстрин | – | + |
| Алимемазин | – | – |
| Антазолин | — | — |
| Бромфенирамин | – | — |
| Хлорциклизин | – | 0 |
| Хлорфенирамин | – | + |
| Клемастин | – | — |
| Клемизол | – | – |
| Ципрогептадин | — | — |
| Диметинден | – | + |
| Дифенгидрамин | — | 0 |
| Дифенилпиралин | – | -/0 |
| Гидроксизин | – | 0 |
| Кетотифен | — | 0 |
| Лоратидин | – | + |
| Ниапразин | — | — |
| Оксатомид | – | – |
| Фенирамин | — | – |
| Прометазин | – | + |
| Пириламин (см.фиг.5) | — | 0 |
| Ритансерин | — | – |
| Тиотидин | — | -/0 |
| Золантидин | – | 0 |
| 0: никакого воздействия; -: снижение; –: значительное снижение; +: повышение | ||
Действие соединения 1 в зависимости от дозы
Результаты слепого, полностью рандомизированного исследования соединения 1, вводимого в разных дозах (0,125, 0,25, 0,5, 1 и 2 мг/кг/мин) в виде 10 минутного вливания крысам, используемым в качестве модели закрытой черепно-мозговой травмы, показывают, что в процессе лечения соединение 1 вызывает значительное снижение ICP в зависимости от дозы (фиг.1). Начиная с дозы 1 мг/кг/мин, соединение 1 вызывает статистически значимое более выраженное снижение ICP по сравнению с группой животных, которым вводили растворитель. Значительное воздействие на ICP в зависимости от дозы сохранялось в течение 10 минут после вливания (фиг.2).
Действие соединения 2, соединения 1 и рацемата (соединение 1 и соединение 2) на концентрацию гемоглобина и оксигенацию головного мозга
Спектроскопия в ближней инфракрасной области (NIRS) головного мозга крыс “in vivo” позволяет произвести неинвазивное количественное определение насыщения гемоглобина головного мозга кислородом (HbSat) и общей концентрации гемоглобина в головном мозге ([HbTot]). Указанный последним параметр является мерой объема мозговой крови (CBV). Кроме того, можно определить изменение окислительно-восстановительного состояния митохондриального фермента цитохром-оксидазы (CytOx), являющегося показателем оксигенации тканей.
Все соединения 2, 1 и рацемат (соединение 1 и соединение 2) не оказывают значительного воздействия на [HbTot] при введении через 24 часа после черепно-мозговой травмы средней тяжести в виде внутривенного вливания в дозе 0,5 мг/кг/мин в течение 10 минут с последующим вливанием 0,1 мг/кг/мин в течение 45 минут. Только соединение 2 вызывает небольшое, но статистически значимое снижение HbSat. Соединение 1 и рацемат (соединение 1 и соединение 2) не воздействуют на HbSat. При введении указанной дозы все соединения не оказывают воздействия на окислительно-восстановительное состояние CytOx. Полученные результаты показывают, что в созданных экспериментальных условиях сосудосуживающее действие на кровеносные сосуды головного мозга, если и имеет место, является весьма ограниченным, и оксигенация тканей не подвергается опасному воздействию.
Влияние анестезии на действие соединения 2
Эффект лечения соединением 2 (внутривенное вливание в дозе 0,1 мг/кг/мин в течение 30 минут) через 24 часа после травмы средней тяжести исследовали с использованием разных анестезирующих средств (изофлуран, хлоральгидрат, пентобарбитал). При использовании в качестве анестезирующего средства хлоральгидрата (внутрибрюшинное вливание 400 мг/кг) ICP снижается до 75% от исходного значения и МАВР (среднее артериальное кровяное давление) постепенно увеличивается до 110% от исходного значения (средние величины, n=6). Указанные воздействия сравнимы с результатами, наблюдаемыми при анестезии изофлураном. При использовании пентобарбитала (внутрибрюшинное вливание 60 мг/кг) соединение 2 вызывает значительное постепенное повышение МАВР до 141% от исходного значения в конце вливания, при этом ICP снижается до 64% от исходного значения (средние величины, n=6). Полученные результаты показывают, что аналогичные воздействия на ICP и МАВР наблюдаются при разных типах анестезии. То, что указанное соединение значительно снижает ICP при анестезии пентобарбиталом, имеет важное значение, так как барбитураты часто применяются для лечения субъектов с травматическим повреждением головного мозга. Благодаря тому, что барбитураты также снижают ICP, при использовании данного соединения можно получить важный дополнительный эффект.
Влияние повторного введения соединения 1 и маннита на повышенное внутричерепное давление у травмированных крыс
Соединение 1 вводили 2 раза с 20-минутными промежутками в виде внутривенного вливания в дозе 1 мг/кг/мин в течение 10 минут, начиная через 20 минут после нанесения тяжелой черепно-мозговой травмы.
Маннит вводили внутривенно с такими же временными параметрами, что и соединение 1, в дозе 0,125 г/кг/мин. Контрольные животные получали только растворитель (содержащий 10% НР- -CD, рН 4).
-CD, рН 4).
Вливание соединения 1 вызывало быстрое снижение внутричерепного давления (фиг.3). Данный эффект усиливался после окончания каждого периода вливания. Кровяное давление снижается во время введения соединения 1, но восстанавливается после окончания лечения. Такой результат отличается от воздействия, оказываемого маннитом, который вызывает снижение ICP и увеличение кровяного давления во время каждого вливания с последующим снижением кровяного давления после окончания каждой процедуры. Только у животных, которым вводили соединение 1, наблюдается четко выраженное различие между изменением кровяного давления и ICP. В отличие от этого, у животных, получавших маннит, происходят более или менее параллельные изменения кровяного давления и внутричерепного давления. Такой результат свидетельствует о том, что фармакологическое действие соединения 1 отличается от действия маннита.
Действие соединения 1 на повышение внутричерепного давления у кроликов в результате повреждения холодом коры головного мозга
У взрослых кроликов вызывали криогенные поражения с целью патологического изменения внутричерепного давления вследствие отека тканей. Прут из нержавеющей стали с диаметром 8 мм прикладывали к заранее определенным участкам обнаженного черепа кроликов, находящихся под глубоким наркозом, и охлаждали жидким азотом в течение 10 минут. Через один день животных снова анестезировали и постоянно регистрировали ICP и кровяное давление аналогично измерению подобных показателей у крыс. После стабилизации показателей в течение 15 минут соединение 1 вливали в дозе 2 мг/кг/мин в течение 10 минут. Растворитель (преклинический препарат, содержащий 10% НР- -CD, рН 4) вводили в дозе 2 мл/мин в течение 10 минут.
-CD, рН 4) вводили в дозе 2 мл/мин в течение 10 минут.
Во время вливания соединения 1 кровяное давление снижалось и, хотя не происходило экстренного снижения ICP, наблюдалось противодействие повышению ICP в отличие от животных, которым вводили растворитель (фиг.4). После окончания вливания лекарственного средства кровяное давление возвращалось к исходному значению и наблюдалось значительное снижение ICP, которое оставалось стабильным на протяжении всего периода регистрации.
Полученные результаты показывают, что данное соединение снижает ICP не только у грызунов, но и у других видов животных, а также при патологических повреждениях, отличающихся от закрытой черепно-мозговой травмы.
Действие соединения 1 на внутричерепное давление у нетравмированных животных
Крысы
Испытывали действие соединения 2, соединения 1 и рацемата (соединение 1 и соединение 2) на ICP, МАВР и СРР у анестезированных нетравмированных крыс. Указанные соединения вводили внутривенно в такой же дозе, что и травмированным крысам (0,5 мг/кг/мин в течение 10 минут с последующим введением 0,1 мг/кг/мин в течение 50 минут). Результаты сравнимы с величинами, полученными у травмированных животных.
Выводы
Результаты, полученные у травмированных животных, животных с повреждением головного мозга холодом и нетравмированных животных, показывают, что испытанные соединения являются активными в случае разных поражений и даже при отсутствии поражений. Область применения указанных соединений, по-видимому, включает разные патологические состояния, для которых характерно повышение внутричерепного давления.
Приложение 1
| Физико-химические характеристики | ||
| Соединение № | Темп. плавления и опт. вращение | |
| 1 | +36.16° (589 нм, с: 0.52540 мас./об.%, метанол, 20°С) | |
| 2 | 151.93°С | (*2) |
| 3 | 180.41°С | (*2) |
| 4 | 105.48°С | (*2) |
| 5 | 224.9°С | (*1) |
| 6 | 133.9°С | (*1) |
| 7 | 213.2°С | (*1) |
| 8 | 178.8°С | (*1) |
| 12 | 248.5°С | (*1) |
| 14 | 212.45°С | (*2) |
| 18 | 176.6°С | (*1) |
| 19 | 281.9°С | (*1) |
| 20 | 153.7°С | (*1) |
| 21 | 241.4°С | (*1) |
| 23 | 189.3°С | (*1) |
| 24 | 206.0°С | (*1) |
| 25 | 257.7°С | (*1) |
| 26 | 216°С | (*1) |
| 27 | 200.4°С | (*1) |
| 28 | 210.6°С | (*1) |
| 29 | 171.1°С | (*1) |
| 30 | 285.29°С | (*2) |
| 32 | 234°С | (*1) |
| 33 | 243.1°С | (*1) |
| 34 | 261.1°С | (*1) |
| 35 | 133.2°С | (*1) |
| 36 | 205.5°С | (*1) |
| 38 | 160.5°С | (*1) |
| 39 | 247.4°С | (*1) |
| 41 | 232.3°С | (*1) |
| 42 | 206.3°С | (*1) |
| 43 | 121.4°С | (*1) |
| 45 | 164.91°С | (*2) |
| 51 | 116.4°С | (*1) |
| 52 | 218.35°С | (*2) |
| 53 | 185.8°С | (*1) |
| 54 | 165.7°С | (*1) |
| 55 | 191.43°С | (*2) |
| 59 | 214.40°С | (*2) |
| 60 | 220.2°С | (*1) |
| 61 | 252.1°С | (*1) |
| 62 | 235.3°С | (*1) |
| 63 | 229.5°С | (*1) |
| 64 | 252.5°С | (*1) |
| 65 | 222.9°С | (*1) |
| 66 | 187.6°С | (*1) |
| 67 | 263.7°С | (*1) |
| 68 | 224.9°С | (*1) |
| 69 | 251.1°С | (*1) |
| 70 | 198.5°С | (*1) |
| 71 | 243.4°С | (*1) |
| 72 | 256.3°С | (*1) |
| 73 | 208.94°С | (*2) |
| 74 | 269.78°С | (*2) |
| 76 | 164.94°С | (*2) |
| 77 | 260.28°С | (*2) |
| 80 | 260.05°С | (*2) |
| 81 | 202.85°С | (*2) |
| 82 | 237.88°С | (*2) |
| 83 | 259.92°С | (*2) |
| 85 | 273.04°С | (*2) |
| 86 | Аморфный нет т.пл. | |
| 87 | 191.72°С | (*2) |
| 88 | 201.23°С | (*2) |
| 89 | 189.28°С | (*2) |
| 90 | 261.19°С | (*2) |
| 91 | 117.43°С | (*2) |
| 92 | 149.91°С | (*2) |
| 93 | 238.78°С | (*2) |
| 94 | 119.47°С | (*2) |
| 106 | 248.30°С | (*2) |
| 107 | 246.87°С | (*2) |
| 109 | 267.25°С | (*2) |
| 110 | 152.0°С | (*1) |
| 111 | 154.7°С | (*1) |
| 112 | 160.5°С | (*1) |
| 113 | 164.1°С | (*1) |
| 114 | 210.7°С | (*1) |
| 115 | 248.0°С | (*1) |
| 116 | 201.4°С | (*1) |
| 117 | 192.9°С | (*1) |
| 118 | 235.2°С | (*1) |
| 120 | 179.41°С | (*2) |
| 122 | 213.2°С | (*1) |
| 123 | 249.0°С | (*1) |
| 124 | 213.2°С | (*1) |
| 125 | 201.6°С | (*1) |
| 126 | 229.6°С | (*1) |
| 127 | 184.3°С | (*1) |
| 128 | 206.5°С | (*1) |
| 129 | 214.4°С | (*1) |
| 130 | 230.1°С | (*1) |
| 131 | 225.4°С | (*1) |
| 132 | 208.9°С | (*1) |
| 133 | 121.4°С | (*1) |
| 134 | 213.53°С | (*2) |
| 135 | 104.46°С | (*2) |
| 136 | 106.2°С | (*1) |
| 137 | 221.5°С | (*1) |
| 138 | 179.5°С | (*1) |
| 139 | 214.3°С | (*1) |
| 140 | 188.2°С | (*1) |
| 141 | 151.2°С | (*1) |
| 142 | 222.5°С | (*1) |
| 143 | 247.1°С | (*1) |
| 144 | 122.9°С | (*1) |
| 145 | 151.0°С | (*1) |
| 146 | 228.2°С | (*1) |
| 147 | 131.3°С | (*1) |
| 148 | 175.6°С | (*1) |
| 149 | 150.7°С | (*1) |
| 151 | 236.0°С | (*1) |
| 152 | 248.1°С | (*1) |
| 153 | 212.8°С | (*1) |
| Определение температуры плавления: | ||
| (*1): Температуры плавления определялись в аппарате для определения температуры плавления с использованием открытых капиллярных трубок. | ||
| (*2): Температуры плавления определялись DSC823e (Mettler-Toledo) (DSC: дифференциальный сканирующий калориметр). | ||
Приложение 2
Получение конечных соединений WO 02/100862)
Пример В1
Получение соединения 1 и соединения 2
Смесь промежуточного соединения 24 (0,021 моль), промежуточного соединения 5 (0,015 моль), Na2CO (0,021 моль) и KI (1 г) в MIBK (500 мл) перемешивали и кипятили с обратным холодильником в течение 72 часов. Растворитель выпаривали. Осадок распределяли в воде и CH2Cl2. Слои разделяли. Водный слой повторно экстрагировали CH2Cl2. Отделенный органический слой сушили (MgSO4), фильтровали и раствор выпаривали. Осадок очищали в стеклянной воронке с силикагелем (элюент: CH2CI2/(СН3ОН/NH3, 97/3 к 94/6). Фракции собирали и растворитель выпаривали. Осадок перекристаллизовывали из СН3CN, отфильтровывали и сушили. Эту фракцию (6,95 г) разделяли на энантиомеры над Chiralcel OD (элюент: гексан/(C2H5OH + 0,04% Et3N) 58/42). Чистые фракции собирали и растворитель выпаривали. Фракцию 1 растворяли в in 2-пропанол/этанол (95/5) и превращали в соль (Е)-2-бутендикарбоновой кислоты (2:3). Осадок отфильтровывали и сушили. Эту фракцию сушили. Выход: 2,2 г (A)[(2 ,4
,4 )(А)] 3-[2-(4-(11,12-дигидро-6H-бензимидазо[2,1-b] [3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2-a] бензимидазол-4 (10H)-он (соединение 2) (45%). Фракцию 2 растворяли в 2-пропанол/этаноле (95/5) и превращали в соль (Е)-2-бутендикарбоновой кислоты (2:3).Осадок отфильтровывали и сушили. Эту фракцию сушили. Выход: 2,1 г (B) [(2
)(А)] 3-[2-(4-(11,12-дигидро-6H-бензимидазо[2,1-b] [3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2-a] бензимидазол-4 (10H)-он (соединение 2) (45%). Фракцию 2 растворяли в 2-пропанол/этаноле (95/5) и превращали в соль (Е)-2-бутендикарбоновой кислоты (2:3).Осадок отфильтровывали и сушили. Эту фракцию сушили. Выход: 2,1 г (B) [(2 ,4
,4 )(А)] 3-[2-(4-(11,12-дигидро-6H-бензимидазо[2,1-b] [3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2-а] бензимидазол-4 (10H)-он(Е)-2-бутендиоата (2:3) гидрат (1:1) (соединение 1) (43%).
)(А)] 3-[2-(4-(11,12-дигидро-6H-бензимидазо[2,1-b] [3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2-а] бензимидазол-4 (10H)-он(Е)-2-бутендиоата (2:3) гидрат (1:1) (соединение 1) (43%).
Пример В2
Получение соединения 3 и соединения
Пример В3
Получение соединения 5
Смесь (0,01 мол), промежуточное соединение 13 (0,01 моль), Na2СО3 (0,025 моль)и KI (каталитическое количество) в MIBK (200 мл) перемешивали при 120°С. Реакционную смесь охлаждали и фильтровали с помощью дикалита. Фильтрат выпаривали. Осадок очищали на стеклянном фильтре с силикагелем (элюент: CH2CI2/СН3ОН 96/4). Чистые фракции собирали и растворитель выпаривали. Осадок (3,9 г) перекристаллизовывали из СН3CN. Продукт отфильтровывали и сушили. Выход: 2,3 г 6-[2-[4-(11,12-дигидро-6H-бензимидазо[2,1-b][3]бензазепин-6-илиден)-1-пиперидинил]этил]-7-метил-5H-тиазоло[3,2-а]пиримидин-5-она (соединения 5) (45,3%) (т.пл. 224,9°С).
Пример В4
Получение соединения 6
Смесь промежуточного соединения 16 (0,0023 моль), (0,0046 моль), Na2CO3 (0,0046 моль) и KI (0,0046 моль) в MIBK перемешивали в течение 24 часов. Реакционную смесь подвергали гидролизу водой и экстрагировали CH2Cl2. Осадок очищали колоночной хроматографией с силикагелем (элюент: CH2CI2/(CH3OH/NH3) 95/5), затем ВЭЖХ с сликагелем (элюент: СН2CI2/CH3OH/NH3) 97/3). Чистые фракции собирали и растворитель выпаривали. Выход: 0,250 г соединения 6 (23%) (т.пл: 133,9°С).
Пример В5
3. Соединение по п.1, отличающееся тем, что указанное соединение представляет собой 3-[2-[4-(11,12-дигидро-6Н-бензимидазо[2,1-b][3]бензазепин-6-ил)-2-(фенилметил)-1-пиперидинил]этил]-2,10-диметилпиримидо[1,2- ]бензимидазол-4(10Н)-он (Е)-2-бутендиоат (2:3) гидрат (1:1) и его стереоизомерные формы.
]бензимидазол-4(10Н)-он (Е)-2-бутендиоат (2:3) гидрат (1:1) и его стереоизомерные формы.
4. Соединение по п.2 или 3, отличающееся тем, что указанное соединение представляет собой (А) [(2 ,4
,4 )(А)]-энантиомер, (В)[(2
)(А)]-энантиомер, (В)[(2 ,4
,4 )(А)]-энантиомер или их смесь.
)(А)]-энантиомер или их смесь.
5. Соединение общей формулы (I) по любому из пп.1-4, для использования в качестве антагониста H1- и/или Н2-рецепторов гистамина.
6. Применение соединения по любому из пп.1-4 для получения лекарственного средства для лечения заболевания, опосредуемого H1- и Н2-рецептором гистамина.
7. Применение соединения по любому из пп.1-4 для получения лекарственного средства для иммуномодуляции у млекопитающего, подавления повышенной чувствительности и/или воспалительных реакций и лечения и/или предотвращения аллергических заболеваний и заболеваний желудочно-кишечного тракта.
8. Применение соединения по любому из пп.1-4 для получения лекарственного средства для иммуномодуляции у млекопитающего, подавления повышенной чувствительности и/или воспалительных реакций и лечения заболеваний желудочно-кишечного тракта.
9. Применение антагониста рецептора гистамина для получения лекарственного средства для снижения внутричерепного давления (ICP) у млекопитающего.
10. Применение антагониста рецептора гистамина для получения лекарственного средства для снижения и/или предотвращения повышенного внутричерепного давления (ICP) и/или лечения вторичной ишемии у млекопитающего.
11. Фармацевтическая композиция, включающая фармацевтически приемлемый носитель и терапевтически эффективное количество соединения определенного в любом из пп.1-4 в качестве антагониста гистаминового рецептора и/или для снижения внутричерепного давления (ICP) у млекопитающего.
12. Композиция по п.11, представленная в форме раствора или суспензии, пригодной для введения инъекцией или перфузией.
13. Способ получения соединения по любому из пп.1-4, отличающийся тем, что соединения реагируют согласно следующей реакции:
где все возможные заместители являются такими как они определены для формулы (I) и L представляет любую пригодную рекционноспособную уходящую группу, в частности галоген или сульфонилокси.
РИСУНКИ
