|
|
(21), (22) Заявка: 2003112460/04, 28.09.2001
(24) Дата начала отсчета срока действия патента:
28.09.2001
(30) Конвенционный приоритет:
29.09.2000 US 60/237,002
(43) Дата публикации заявки: 20.11.2004
(46) Опубликовано: 27.11.2007
(56) Список документов, цитированных в отчете о
поиске:
US 5801281 А, 01.09.1998. М.С. O’Sullivan et al. Tetrahedron Letters v.36, №20, 1995, p.3451-3452. RU 94031208 A1, 10.09.1996.
(85) Дата перевода заявки PCT на национальную фазу:
29.04.2003
(86) Заявка PCT:
US 01/30948 (28.09.2001)
(87) Публикация PCT:
WO 02/26721 (04.04.2002)
Адрес для переписки:
129010, Москва, ул. Б.Спасская, 25, стр.3, ООО “Юридическая фирма Городисский и Партнеры”, пат.пов. Е.Е.Назиной, рег. № 517
|
(72) Автор(ы):
ДЖАНДОМЕНИКО Кристен М. (US),
ЯНГ Вен (CA)
(73) Патентообладатель(и):
АНОРМЕД, ИНК. (CA)
|
(54) ЦИКЛИЧЕСКИЕ ПОЛИАМИНЫ, СОДЕРЖАЩИЕ В КОЛЬЦЕ N АТОМОВ АЗОТА, ЗАЩИЩЕННЫХ ПО ПРИНЦИПУ “ВСЕ, КРОМЕ ОДНОГО (N-1)”, И СПОСОБЫ ИХ ПОЛУЧЕНИЯ
(57) Реферат:
Описываются новые циклические полиамины общих формул
3), причем каждый атом азота отделен 2 или более атомами углерода, скорость реакции будет замедляться резко, стоит только защитить N-1 атомов азота, даже когда все атомы азота в циклическом полиамине первоначально химически эквивалентны. Указанные контролируемые реакции, таким образом, позволяют получать с превосходным выходом важные N-1 защищенные полиазамакроциклы при высокой селективности.
Данное изобретение относится, например, к эффективной дающей высокий выход N-1 защите циклических полиаминов, содержащих в сумме N атомов азота амина, где кольцо имеет от 9 до 20 членов кольца, и N равно от 3 до 6 атомам азота амина, разделенным 2 и более атомами углерода, с использованием фторированных сложных эфиров кислот и других структурно родственных защитных агентов (формула III). Полученные в результате защищенные амины, полученные указанным способом, являются полезными промежуточными соединениями для получения селективно N-замещенных защищенных циклических полиаминов. Защищенный селективно N-замещенный циклический полиамин легко поддается удалению защиты в мягких условиях с образованием селективно N-замещенных циклических полиаминов.
Более конкретно, данное изобретение раскрывает, наряду с прочим, тризащиту с высоким выходом 1,4,8,11-тетраазациклотетрадекана (циклама), 1,4,7,10- тетраазациклододекана (циклена) и дизащиту 1,4,7-триазациклононана с использованием агентов таких, как представленные формулой III.
Кроме того, данное изобретение относится к чрезвычайно эффективному и экономичному способу получения 1,1′-[1,4-фениленбис(метилен)]бис-1,4,8,11-тетраазациклотетрадекана из циклама с использованием защитных групп, таких как, но не ограничиваясь ими, трифторацетил, посредством последовательных реакций тризащиты, алкилирования и удаления защиты.
Другие аспекты изобретения раскрыты в более подробном описании и, в особенности, в формуле изобретения.
Фиг.1 изображает 13С ЯМР тритрифторацетилциклама.
Фиг.2 изображает 1Н ЯМР тритрифторацетилциклама.
Фиг.3 изображает 19F ЯМР тритрифторацетилциклама.
Данное изобретение относится к N-1 (т.е. все, кроме одного) защите циклических полиаминов, содержащих в сумме N атомов азота в амине на кольцевой системе, где кольцо имеет от 9 до 20 членов кольца и содержит от 3 до 6 атомов азота в амине, разделенных 2 или более атомами углерода, с использованием трифторацетила и других структурно родственных защитных агентов, которые представлены формулой III.
Предпочтительно, применимый циклический полиамин может быть представлен формулами I и II, где m и m’ представляют от 0 до 2, включительно, предпочтительно, от 0 до 1, включительно, атомов углерода; n, n’ и n” представляют от 1 до 3, включительно, предпочтительно, от 1 до 2, включительно, атомов углерода; m, m’, n, n’ и n” могут быть идентичными или различными для каждого конкретного соединения.
3,90-3,76 (шир.м, 4Н), 3,68-3,20 (м, 8Н), 3,10-2,65 (м, 4Н), 1,40-1,25 (м, 1Н). С14Н17F9N4О3 вычислено: С 36,53, Н 3,72, N 12,17, О 10,43; найдено: С 36,49, Н 3,71, N 12,11, О 10,59.
ПРИМЕР 2
Получение 1,4-бис(трифторацетил)-1,4,7-триазациклононана
1,4,7-триазациклононан (115,0 мг, 0,89 ммоль) растворяют в МеОН (2,0 мл). К этому прозрачному раствору добавляют NEt3 (0,13 мл, 0,89 ммоль) одной порцией с последующим добавлением этилового эфира трифторуксусной кислоты (0,43 мл, 13,56 ммоль) в течение 5 минут. Перемешивание продолжают в атмосфере N2 в течение 15 часов. Летучие вещества удаляют затем ротационным испарителем. Остаток растворяют в минимальном количестве СН2Cl2 (2,0 мл) и пропускают через короткую набивку силикагеля, элюируют 100% EtOAc. Элюент концентрируют, чтобы получить продукт в виде белого твердого вещества (267,0 мг, 94%). 1H ЯМР (300 МГц, CDCl3):  4,04-3,95 (м, 2Н), 3,80-3,72 (м, 2Н), 3,50-3,40 (м, 4Н), 3,0-2,90 (м, 4Н), 1/59 (с, 1Н). Масса, вычисленная для С10Н13F6N3O2: 321,2, найдено: М+1 322,1. 4,04-3,95 (м, 2Н), 3,80-3,72 (м, 2Н), 3,50-3,40 (м, 4Н), 3,0-2,90 (м, 4Н), 1/59 (с, 1Н). Масса, вычисленная для С10Н13F6N3O2: 321,2, найдено: М+1 322,1.
ПРИМЕР 3
Получение 1,4,8-трис(трифторацетил)-1,4,8,11-тетраазациклотетрадекана
Циклам (7,53 г, 37,58 ммоль) растворяют в лабораторном МеОН (30 мл). К этому прозрачному раствору добавляют NEt3 (5,20 мл, 37,58 ммоль) одной порцией с последующим порционным добавлением этилового эфира трифторуксусной кислоты (18,0 мл, 150,3 ммоль) в течение 5 минут. Реакционная смесь может быть охлаждена, чтобы поддержать температуру ниже 25°С. Перемешивание продолжают в атмосфере N2 в течение 5 часов. Летучие вещества удаляют затем в вакууме. Остаток растворяют в минимальном количестве СН2Cl2 (2,0 мл) и пропускают через короткую набивку силикагеля, элюируют 100% EtOAc. Элюент концентрируют, чтобы получить продукт в виде белого полутвердого вещества (17,05 г, 92,5%). 1Н ЯМР (200 МГц, CDCl3):  3,85-3,25 (м, 12Н), 2,80 (шир.с, 2Н), 2,74-2,50 (шир.с, 2Н), 2,30-1,90 (м, 2Н), 1,85-1,63 (м, 2Н), 1,25-0,60 (м, 1Н). 13С ЯМР (75,5 МГц, CDCl3): 3,85-3,25 (м, 12Н), 2,80 (шир.с, 2Н), 2,74-2,50 (шир.с, 2Н), 2,30-1,90 (м, 2Н), 1,85-1,63 (м, 2Н), 1,25-0,60 (м, 1Н). 13С ЯМР (75,5 МГц, CDCl3):  158,74-157,31 (м, С=О, вследствие конформации), 122,84-11,32 (кв, CF3, вследствие C-F связывания, JC-F264 Гц, дополнительный сплит вследствие конформации), 51,2-46,2 (м, СН2, ближайший к N), 29,4-27,8 (м, СН2). C16H21F9N4O3 вычислено: С 39,35, Н 4,33, N 11,47, О 9,83; найдено: С 39,19, Н 4,36, N 11,33, О 10,04. 158,74-157,31 (м, С=О, вследствие конформации), 122,84-11,32 (кв, CF3, вследствие C-F связывания, JC-F264 Гц, дополнительный сплит вследствие конформации), 51,2-46,2 (м, СН2, ближайший к N), 29,4-27,8 (м, СН2). C16H21F9N4O3 вычислено: С 39,35, Н 4,33, N 11,47, О 9,83; найдено: С 39,19, Н 4,36, N 11,33, О 10,04.
ПРИМЕР 4
Получение 1,1′-[1,4-фениленбис(метилен)]бистрис(трифторацетил)-1,4,8,11-тетраазатетрадекана
В круглодонную колбу загружают 1,4,8-трис(трифторацетил)-1,4,8,11-тетраазациклотетрадекан (3,70 г, 7,57 ммоль) и безводный СН3CN (20 мл). Смесь перемешивают при комнатной температуре, пока не получат раствор (10 минут). К этому раствору добавляют затем K2CO3 (98%, 1,57 г, 11,35 ммоль), KI (62,8 мг, 0,38 ммоль) и дихлорксилол (663,0 мг, 3,78 ммоль). Смесь нагревают при кипячении с обратным холодильником в атмосфере азота. ТСХ (1:1 EtOAc/гексан) используют для отслеживания течения реакции, которая завершается спустя 16 часов. Смесь охлаждают до комнатной температуры и фильтруют через спеченный стеклянный фильтр, чтобы удалить нерастворимую соль (промывают 20 мл СН3CN). Раствор затем концентрируют, чтобы получить слегка желтоватое твердое вещество. Твердое вещество подвергают перекристаллизации, используя 4/1 EtOH/H2O, чтобы получить очищенный продукт (3,47 г, 85%) в виде почти белого твердого вещества. 1Н ЯМР (300 МГц, CDCl3):  7,25-7,06 (м, 5Н), 3,80-3,20 (м, 28Н), 2,75 (шир.с, 4Н), 2,45-2,20 (м, 8Н), 1,90-1,60 (м, 4Н). 13С ЯМР (75,5 МГц, CDCl3): 7,25-7,06 (м, 5Н), 3,80-3,20 (м, 28Н), 2,75 (шир.с, 4Н), 2,45-2,20 (м, 8Н), 1,90-1,60 (м, 4Н). 13С ЯМР (75,5 МГц, CDCl3):  155,6-154,5 (м, С=О, м, благодаря конформации), 135,9-134,0 (м, ароматический С), 127,9-126,7 (м, ароматический С-Н), 118,0 (кв, JC-F287 Гц), 58,3-57,7 (м), 55,0-52,0 (м), 50,4-42,7 (м, благодаря конформации), 26,5-21,8 (м, благодаря конформации). Элементный анализ: для С40Н48F18N8О6 вычислено: С 44,53, Н 4,48, N 10,39, О 8,90; найдено: С 44,46, Н 4,40, N 10,26, О 9,11. 155,6-154,5 (м, С=О, м, благодаря конформации), 135,9-134,0 (м, ароматический С), 127,9-126,7 (м, ароматический С-Н), 118,0 (кв, JC-F287 Гц), 58,3-57,7 (м), 55,0-52,0 (м), 50,4-42,7 (м, благодаря конформации), 26,5-21,8 (м, благодаря конформации). Элементный анализ: для С40Н48F18N8О6 вычислено: С 44,53, Н 4,48, N 10,39, О 8,90; найдено: С 44,46, Н 4,40, N 10,26, О 9,11.
ПРИМЕР 5
Получение 1,1′-[1,4-фениленбис(метилен)]бис-1,4,8,11-тетраазациклотетрадекана, соединения XII:
4,0-3,28 (м, 10Н), 2,86 (шир.м, 2Н), 2,64-2,59 (м, 2Н), 2,48-1,99 (м, 2Н), 1,8-1,7 (м, 2Н), 1,1 (с, 1Н). 13С ЯМР (75,5 МГц, CDCl3):  159,4-157,7 (м, С=O), 123,9-111,8 (ткв, JC-F=249 Гц, 34 Гц, CF3CF2), 112,6-104,6 (мт, JC-F=308 Гц, CF2CF3), 50,3-44,4 (м, СН2, ближайший к N), 28,9-27,8 (м, CH2). C19H21N4F15O3 вычислено: С 35,75, Н 3,32, N 8,78, О 7,52; найдено: С 35,81, Н 3,37, N 8,55, О 7,74. 159,4-157,7 (м, С=O), 123,9-111,8 (ткв, JC-F=249 Гц, 34 Гц, CF3CF2), 112,6-104,6 (мт, JC-F=308 Гц, CF2CF3), 50,3-44,4 (м, СН2, ближайший к N), 28,9-27,8 (м, CH2). C19H21N4F15O3 вычислено: С 35,75, Н 3,32, N 8,78, О 7,52; найдено: С 35,81, Н 3,37, N 8,55, О 7,74.
ПРИМЕР 8
Получение производного мочевины 1,4,7-трис(трифторацетил)-1,4,7,10-тетраазациклододекана
1,4,7-трис(трифторацетил)-1,4,7,10-тетраазациклододекан (303,5 мг, 0,658 ммоль) растворяют в СН2Cl2 (5,0 мл). Фенилизоцианат (0,14 мл, 1,32 ммоль) добавляют одной порцией. Реакцию продолжают при комнатной температуре в течение 15 часов. После удаления всех летучих веществ остаток подвергают хроматографии, чтобы получить желательное производное мочевины (301,0 мг 79%). 1H ЯМР (CDCl3, 200 МГц):  7,38-7,26 (м, 5Н), 7,08-7,03 (м, 1Н), 4,03-3,28 (м, 16Н). МС вычислено для C21H22N5F9O4: 579,4, найдено: M+Na 602,5. 7,38-7,26 (м, 5Н), 7,08-7,03 (м, 1Н), 4,03-3,28 (м, 16Н). МС вычислено для C21H22N5F9O4: 579,4, найдено: M+Na 602,5.
ПРИМЕР 9
Получение моно-Cbz-трис(трифторацетил)циклама
Три-TFA-циклам растворяют в СН2С12 (10 мл) при комнатной температуре. Na2CO3 (566 мг, 5,34 ммоль) добавляют одной порцией с последующим медленным добавлением Cbz хлорида. Реакцию отслеживают ТСХ (1:1 этилацетат: гексан). Реакцию прекращают через 15 часов. Обычная обработка с последующей колоночной хроматографией с использованием силикагеля дает продукт (1,30 г, 94%) в виде белой пены. 1H ЯМР (CDCl3, 200 МГц):  7,31 (шир.м, 5Н), 5,02 (с, 2Н), 3,54-3,10 (м, 16Н), 2,04-1,54 (м, 4Н). Масса, вычисленная для C24H27F9N4O4: 622,5, найдено: М+1 (623,2). 7,31 (шир.м, 5Н), 5,02 (с, 2Н), 3,54-3,10 (м, 16Н), 2,04-1,54 (м, 4Н). Масса, вычисленная для C24H27F9N4O4: 622,5, найдено: М+1 (623,2).
ПРИМЕР 10
Получение монотозилтрис(трифторацетил)циклама
Три-TFA-циклам (3,31 г, 6,77 ммоль) растворяют в CH2Cl2 (30 мл). Триэтиламин (1,40 мл, 8,12 ммоль) добавляют одной порцией. Раствор охлаждают на водяной бане со льдом. TsCl (1,55 г, 8,12 ммоль) добавляют небольшими порциями в течение 5 минут. Реакцию продолжают при комнатной температуре в течение 8 часов. Обычная обработка и колоночная хроматография дают желательный продукт (3,47 г, 80%). 1H ЯМР (300 МГц, CDCl3):  7,5-7,48 (м, 2Н), 7,6-7,20 (м, 2Н), 3,67-3,30 (м, 12Н), 3,21 (шир.м, 2Н), 2,95 (шир.м, 2Н), 2,32 (с, 3Н), 2,20-1,70 (м, 4Н). 13С ЯМР (75,5 МГц, CDCl3): 7,5-7,48 (м, 2Н), 7,6-7,20 (м, 2Н), 3,67-3,30 (м, 12Н), 3,21 (шир.м, 2Н), 2,95 (шир.м, 2Н), 2,32 (с, 3Н), 2,20-1,70 (м, 4Н). 13С ЯМР (75,5 МГц, CDCl3):  158,4-156,4 (м, С=O), 144,8-144,7 (два с вследствие конформации), 134,2-133,8 (четыре с вследствие конформации кольца), 133,8, 127,7-127,5 (два с вследствие конформации), 122,3-110,8 (четыре с, вследствие C-F связывания, JC-F287 Гц), 51,8-45,0 (м вследствие конформации), 28,4-27,2 (м вследствие конформации), 21,6. 158,4-156,4 (м, С=O), 144,8-144,7 (два с вследствие конформации), 134,2-133,8 (четыре с вследствие конформации кольца), 133,8, 127,7-127,5 (два с вследствие конформации), 122,3-110,8 (четыре с, вследствие C-F связывания, JC-F287 Гц), 51,8-45,0 (м вследствие конформации), 28,4-27,2 (м вследствие конформации), 21,6.
ПРИМЕР 11
Получение моно-Cbz-циклама
Моно-Cbz-трис(трифторацетил)циклам (4,0 г, 6,4 ммоль) растворяют в лабораторном МеОН (50 мл). Добавляют К2CO3 (2,0 г, 14,5 ммоль) одной порцией. Смесь нагревают при кипячении с обратным холодильником в течение 15 часов. Большинство летучих веществ удаляют в вакууме и остаток забирают в CHCl3 (100 мл). Твердое вещество отфильтровывают и раствор концентрируют, чтобы получить моно-Cbz-циклам (1,82 г, 85%). 1H ЯМР (CDCl3, 200 МГц):  7,21-7,14 (м, 5Н), 4,98 (с, 2Н), 3,33 (т, 2Н), 3,26 (т, 2Н), 2,67 (т, 2Н), 2,60-2,51 (м, 10Н), 1,68 (шир.с, 3Н), 1,68-1,49 (м, 4Н). 7,21-7,14 (м, 5Н), 4,98 (с, 2Н), 3,33 (т, 2Н), 3,26 (т, 2Н), 2,67 (т, 2Н), 2,60-2,51 (м, 10Н), 1,68 (шир.с, 3Н), 1,68-1,49 (м, 4Н).
Цитирование документов здесь не имеет целью признание того, что какой-либо документ является предшествующим опытом. Все утверждения как в отношении данных или предоставления сведений, так и в отношении содержания этих документов основаны на информации, доступной для заявителей, и не являются каким-либо признанием корректности данных или содержания этих документов. Кроме того, все публикации и патенты, упомянутые в данном описании, приобщены к сему ссылкой. Различные модификации и изменения описанного способа и системы по изобретению должны быть очевидны специалисту, не выходя из объема действия и сущности изобретения. Хотя изобретение описано в связи с конкретными предпочтительными вариантами, следует понимать, что изобретение, как оно заявлено, не должно быть незаконно ограничено такими конкретными вариантами. Действительно, различные модификации осуществления изобретения, которые очевидны специалисту в данной или каких-либо родственных областях, как подразумевается, находятся в объеме представленной формулы изобретения.
Формула изобретения
1. Циклический полиамин общей формулы XIV
где у равен целому числу от 1 до 5,
р равен 0, и z равен целому числу от 3 до 11,
где m и m’ одинаковые и равны целому числу от 0 до 2, и
n и n’ одинаковые и равны целому числу от 1 до 2; и
где Е означает водород или фениламинокарбонил, бензилоксикарбонил или толуолсульфонил.
2. Соединение по п.1, где m=m’=n=n’=1; y=1 и z=3.
3. Бистетраазамакроцикл общей формулы XXI
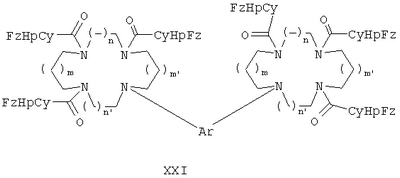
где Ar является 1,4-фениленбис(С1-2алкиленом);
a m и m’, n и n’, р, у и z имеют указанные выше значения
3) удаления ацильных групп, присоединенных на стадии 1, с помощью агента для снятия защитной группы, при этом получая соединение формулы Q-Ar-Q’.
8. Способ по п.7, где стадия 1 дополнительно включает добавление разбавителя к реакционной смеси, причем разбавитель содержит С1-12 алканол с прямой или разветвленной цепью.
9. Способ по п.7, включающий взаимодействие N-1 до (3×N) эквивалентов фторзамещенного ацилирующего агента на моль циклического полиамина, причем N представляет число атомов азота в кольце указанного циклического полиамина.
10. Способ по п.7, где указанный фторзамещенный ацилирующий агент формулы III является этилтрифторацетатом или метилпентафторпропионатом.
11. Способ по п.10, где указанный фторзамещенный ацилирующий агент является этилтрифторацетатом.
12. Способ по п.11, включающий взаимодействие указанного этилтрифторацетата с указанным циклическим полиамином в присутствии метанола при температуре от 10 до 40°С в течение между 1 и 24 ч.
13. Способ по п.7, где каждый m, m’, n и n’ в формуле 1 и VIII равен 1, и стадия 2 включает функционализацию оставшегося азота кольца путем взаимодействия указанного соединения, имеющего формулу VIII, с алкилирующим агентом на основе 1,4-фенилена формулы XI
где Lx и Lx‘ являются уходящими группами, представляющими галоген, при этом образуется соединение формулы Х
14. Способ по п.13, где алкилирующим агентом на основе 1,4-фенилена является 1,4-дихлорксилол или 1,4-дибромксилол.
15. Способ по п.13, где стадия 2 дополнительно включает добавление соединения, содержащего йодид анион.
16. Способ по п.13, где стадия 2 дополнительно включает добавление карбоната металла в качестве основания.
17. Способ по п.13, где стадия 2 дополнительно включает добавление алифатических или ароматических аминов, содержащих от 3 до 12 атомов углерода.
18. Способ по п.13, где алкилирующий агент на основе 1,4-фенилена растворяют в растворителе, выбранном из группы, состоящей из ацетонитрила, алканола с 1-12 атомами углерода, циклического простого эфира, толуола, N,N-диметилформамида и N,N-диметилацетамида или их смесей.
19. Способ по п.13, где алкилирующим агентом на основе 1,4-фенилена является 1,4-дихлорксилол, и он присутствует в количестве от 0,3 до 0,7 эквивалента, и добавляют от 0,015 до 2 эквивалентов KI и от 0,5 до 50 эквивалентов К2СО3 и реакцию проводят в присутствии ацетонитрила при температуре от 40 до 120°С в течение периода между 4 и 72 ч.
20. Способ по п.7, где агентом для снятия защитных групп является карбонат металла, гидроксид металла, кислота, аммиак, амин, гидразин или тиолат.
21. Способ по п.20, где агент для снятия защитных групп растворяют в растворителе, выбранном из группы, состоящей из полярного органического растворителя, воды и смеси полярного растворителя и воды.
22. Способ получения циклического полиамина общей формулы XV
где m и m’, n и n’ имеют указанные выше значения, а Е-фениламинокарбонил, бензилоксикарбонил или толуолсульфонил, включающий следующие стадии:
1) взаимодействие циклического полиамина формулы I
с 3-100 эквивалентами фторзамещенного ацилирующего агента формулы III на моль указанного циклического полиамина,
где Х представляет перфторзамещенный алкильный радикал CyHpFz, где у целое число равное от 1 до 5; р равно 0; и z целое число равное от 3 до 11;
Lv означает уходящую группу, представляющую алкоксигруппу;
при этом получая соединение формулы VIII
2) функционализацию оставшегося кольцевого азота заместителем Е, выбранным из фениламинокарбонила, бензилоксикарбонила или толуолсульфонила, получая соединение формулы XIV
и
3) удаления ацильных групп, присоединенных на стадии 1, с помощью агента для снятия защитной группы, при этом получая соединение формулы XV.
РИСУНКИ
|
|