|
|
(21), (22) Заявка: 2006107172/14, 07.03.2006
(24) Дата начала отсчета срока действия патента:
07.03.2006
(46) Опубликовано: 27.11.2007
(56) Список документов, цитированных в отчете о
поиске:
СТЕПАНОВА Н.А. Нарушения микроциркуляции и способы их коррекции у детей с тяжелой хирургической патологией. – Педиатрия, 1989, №5, с.54-63. RU 46164 U1, 27.06.2005. RU 2004115051 А, 20.11.2005. RU 2022521 C1, 15.11.1994. RU 2068648 С1, 10.11.1996. US 6866659 В2,15.03.2005. ВОЛОСОК Н.И., СТЕПАНОВА Н.А., МАЛКОЧ А.В. КОЛОМИЕЦ И.Ю. Биомикроскопия
Адрес для переписки:
690041, г.Владивосток, 41, ул. Балтийская, 43, ТОИ ДВО РАН, патентный отдел, Н.С. Василюк
|
(72) Автор(ы):
Обыденникова Тамара Николаевна (RU),
Усов Виктор Васильевич (RU),
Константинов Олег Григорьевич (RU),
Павлов Андрей Николаевич (RU)
(73) Патентообладатель(и):
Государственное образовательное учреждение высшего профессионального образования “Владивостокский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию” (ГОУ ВПО ВГМУ Федерального агентства здравоохранения и социального развития) (RU),
Тихоокеанский океанологический институт им. В.И. Ильичева Дальневосточного отделения Российской Академии наук (ТОИ ДВО РАН) (RU)
|
(54) СПОСОБ ОЦЕНКИ СОСТОЯНИЯ ПАЦИЕНТА И УСТРОЙСТВО ДЛЯ ОСУЩЕСТВЛЕНИЯ СПОСОБА
(57) Реферат:
Изобретение относится к медицине, а именно к хирургии, травматологии, реанимации и интенсивной терапии, а также к области медицинской оптики, и может быть использовано для диагностики состояния больного, в том числе и экспресс-диагностики с использованием инструментального наблюдения и анализа микроциркуляции крови в сосудах конъюнктивы глазного яблока. В качестве информативных морфометрических показателей используют общую удельную длину капилляров, удельную длину мельчайших капилляров и удельную длину больших сосудов. При уменьшении общей удельной длины капилляров не менее чем на 10% и/или удельной длины мельчайших капилляров не менее чем на 20% и/или увеличении удельной длины больших сосудов на 150-160% от величины средних показателей в норме равных, соответственно, 6,7; 5,3 и 0,3, делают вывод о наличии патологического процесса в организме. По динамике изменения данных показателей прогнозируют дальнейшее течение процесса. Способ осуществляют с использованием устройства, состоящего из высокоскоростной видеокамеры, на корпусе которой установлены два сверх ярких светодиода под углом 20-30 градусов относительно оптической оси системы переноса изображений. Видеокамера соединена с блоками управления, регистрации и анализа получаемых изображений, реализуемыми на основе аппаратно-программного комплекса на базе компьютера с процессором Pentium 2000, оснащенного интерфейсом USB2. Время обследования составляет 1-2 мин. Устройство позволяет осуществлять съемку конъюнктивы глаза пациента как в положении сидя, так и в положении лежа. Способ позволяет прогнозировать развитие заболевания и корректировать лечение до появления клинических признаков ухудшения. 2 н. и 2 з.п. ф-лы, 1 ил., 4 табл.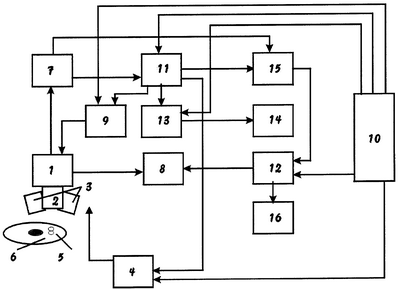
(56) (продолжение):
CLASS=”b560m”конъюнктивы в оценке состояния микроциркуляции при гломерулонефрите у детей. – Нефрология и диализ, т.1, 1999, №1. ТХОР В.Б. Использование цифровой обработки изображений для оценки состояния микроциркуляции у детей. – Информатика и кибернетика в педиатрии, 1990, с.182-185. CHEUNG A.T., RAMANUJAM S., GREER D.A., KUMAGAI L.F., AOKI T.T. Microvascular abnormalities in the bulbar conjunctiva of patients with type 2 diabetes mellitus. Endocr Pract. 2001 Sep-Oct; 358-63. TSILIMBARIS M.K. Transscleral ciliary body photodynamic therapy using phthalocyanine and a diode laser: functional and morphologic implications in albino rabbits. Ophthalmic Surg Lasers. 1997 Jun; 28(6): 483-94.
Изобретение относится к медицине, а именно – к хирургии, травматологии, реанимации и интенсивной терапии, и может быть использовано для диагностики состояния больного, в том числе и экспресс-диагностики.
Повреждения органов и тканей (травма, оперативное вмешательство, термические и лучевые поражения, гнойно-воспалительные заболевания, интоксикации и инфекционные процессы), как правило, сопровождаются нарушением микроциркуляции крови (Чернух А.М. Микроциркуляция в здоровом и больном организме. – М.: 3нание, 1974. – 62 с).
Известно, что при травматическом и токсическом поражении после кратковременного сужения микрососудов наступает расширение вен и артериол, что проявляется гиперемией и гипертермией [Чернух А.М., Александров П.Н., Алексеев О.В. Микроциркуляция. – М.: Медицина, 1984. – 456 с]. При нарушении свертывания крови могут образовываться микросгустки, которые также препятствуют микроциркуляции крови.
Микроциркуляторная система всегда на воздействие патогенного фактора реагирует как единый комплекс (Горчаков К.П., Поздинкова О.В. Структурная организация микрососудистого русла: норма, патология, коррекция. – Новосибирск, 1989, – 167 с; Казначеев В.П., Дзизинский А.А. Клиническая патология транскапиллярного обмена. – М.: Наука, 1975. – 280 с). Известно, что изменения в микроциркуляторном русле (МЦР) происходят раньше, чем возникают клинические проявления патологии. Поэтому исследование состояния МЦР конъюнктивы можно рассматривать как метод мониторинга состояния больного и последующего прогнозирования течения заболевания, что позволит оперативно назначать коррегирующее лечение еще до развития клинических проявлений осложнений (Мчедлишвили Г.И. Микроциркуляция крови: общие закономерности регулирования и нарушений. – Л., Медицина, 1989. – 290 с).
Основным методом качественной и количественной оценки состояния МЦР является метод биомикроскопии конъюнктивы глазного яблока.
Следует отметить, что большинство работ по оценке морфометрических параметров микроциркуляторного русла носят субъективный и качественный характер. Оценку основывают на различных описательных шкалах, в которых в формализованном виде делаются попытки объективизировать изменения, как правило, путем балльной оценки 7-10 критериев, таких как состояние микрососудов от артериол до венул, количество микрососудов на единицу площади, диаметр сосудов, состояние тонуса, наличие сладж синдрома, наличие анастомозов, наличие реканализированных сосудов, углы отхождения и деления, петлистость, извитость и пр., и последующего суммирования полученных баллов.
Известен метод оценки состояния детей с гломерулонефритом по биомикроскопии сосудов конъюнктивы. Способ основан на морфометрическом анализе полученных биомикрофотограмм. Специфическим и диагностически значимым признаком, по которому судят о состоянии больного, является резкое нарастание извитости капилляров, которое оценивают по коэффициенту извитости, определяемому как отношение средней линии, проведенной через нулевые значения периодов извитого сосуда, к его реальной длине, измеренной с помощью курвиметра (прибор для измерения длины кривых линий). Для осуществления способа используют модифицированный отечественный капилляроскоп М-70-А. Биомикроскопическое исследование проводилось через видоискатель и фиксировалось на цветной фотопленке. Оценка полученных изображений МЦР проводится исследователем вручную после получения фотографических изображений. Недостатком метода является дороговизна, необходимость оборудованного помещения, невозможность исследовать состояние МЦ у постели тяжелобольных, субъективная оценка получаемой информации (Н.И.Волосок, Н.А.Степанова, А.В.Малкоч, И.Ю.Коломиец. Биомикроскопия конъюнктивы в оценке состояния микроциркуляции при гломерулонефрите у детей. Ж. “Нефрология и диализ”, 1999, т.1, №1).
Известен способ оценки степени выраженности артериальной гипертензии на основе морфометрических показателей микроциркуляторного русла конъюнктивы, что проявляется уменьшением диаметра артериол, числа функционирующих капилляров (ЧФК) на единицу площади, увеличением степени их извитости, увеличением диаметра венул и их извитости на фоне прогрессирующего нарушения степени эндотелийопосредованной дилатации артериол. Биомикроскопию сосудов конъюнктивы глазного яблока проводили с использованием щелевой лампы “ЩЛ-2Б”, на которую с помощью переходного тубуса прикрепляли фотокамеру “Зенит-Е”. Съемку осуществляли на негативную фотопленку “Микрат-200”, фотографировали различные участки конъюнктивы темпорального отдела глаза (не менее 3 кадров). Освещение обеспечивала импульсная лампа-фотовспышка, свободно фиксированная на станине щелевой лампы. Негативы обрабатывали под визуальным контролем при свете красной лампы с помощью стандартных реактивов. Изготавливали черно-белые фотографии на контрастной фотобумаге. Морфометрические параметры артериол анализировали по фотоснимкам с помощью калиброметра “БОП-4”. (С.Н.Поливода, А.А.Черепок. Эндотелийопосредованные механизмы структурно-функциональной перестройки микроциркуляторного русла у пациентов с гипертонической болезнью. Украинский кардиологический журнал, 2002, №6).
Как правило, для исследования конъюнктивы глазного яблока используют устройства, выполненные на основе “щелевых ламп”. Щелевые лампы представляют собой устройства, основными компонентами которых являются оптическая система, включающая осветитель, выполненный, как правило, на основе галогенной лампы, микроскоп и устройство для фиксации головы пациента. В современных модификациях щелевых ламп, например серии SL, FS-3V и др., используют стереобинокулярные микроскопы, к одному из окуляров которого присоединяют фотоприставку или видеокамеру. Получаемое изображение регистрируют и выводят на монитор компьютера или сохраняют в его памяти.
Однако известные конструкции щелевых ламп обладают рядом существенных недостатков, а именно:
– свет от осветителя, попадая в зрачок, вызывает слезотечение и моргание как результат светового воздействия, что затрудняет визуальное наблюдение, фото- и видео – съемку и приводит к снижению точности исследования микроциркуляторного русла;
– для получения четкого и резкого снимка при использовании всех известных моделей щелевых ламп требуется такая фиксация головы пациента, чтобы ее перемещения не превышали, по крайней мере, характерного размера исследуемых сосудов 3-10 мкм. В то же время при обследовании пациентов с тяжелой патологией или находящихся в бессознательном состоянии фиксация камеры относительно глазного яблока или головы пациента тем или иным способом может быть затруднена или невозможна;
– результаты видеосъемки, в которой участвует оператор, наблюдающий за процессом, осуществляющий наводку на обследуемый участок конъюнктивы и обеспечивающий получение приемлемого по качеству изображения, несут отпечаток индивидуальных особенностей оператора – врача, что снижает их объективность.
Для исключения раздражения глаз в щелевой лампе перед направлением светового потока в область глаза его затеняют в пределах контура радужки. Для этого в фиксирующем устройстве предложено использовать налобник, снабженный направляющей, на которой установлены две подвижные каретки, снабженные надглазными элементами, которые устанавливают в такое положение, при котором их тень от источника света падает на глаз только в пределах радужки (п. РФ №2020863, опубл. 1994.10.15).
Известно устройство биомикроскопии сосудов глазного яблока, представляющее собой щелевую лампу и видеокамеру, совмещенную с одним из окуляров щелевой лампы для получения изображений сосудистой системы конъюнктивы глаза. Изображения, полученные видеокамерой, затем анализируются с помощью видеоанализатора “Мекос-Ц” для Windows-97. Из полученной видеопоследовательности оператором выбираются изображения с максимальными значениями частотно-контрастной характеристики, которые затем подвергаются морфологической обработке для подсчета общего числа капилляров на единицу площади, а также распределение их по размерам. Недостатками данного устройства является то, что оно неприменимо для больных, находящихся в тяжелом состоянии, находящихся в бессознательном состоянии или не способных самостоятельно передвигаться. Применение устройства также требует фиксации головы пациента, находящегося в сидячем положении. Этим резко ограничивается область применения устройства, особенно для анализа состояния ожоговых больных и больных в шоковом состоянии (“К методу исследования микроциркуляции в клинике”, Б.З.Сиротин, К.В.Жмеренецкий, В.И.Цыганков, Мат-лы н-практической конференции. – С-Пб., 2003).
Наиболее близкой к заявляемому устройству является система для мониторинга состояния микроциркуляции, включающая электрически связанные между собой видеокамеру с системой переноса изображений, оптический стенд с опорным источником облучения исследуемой зоны глаза спектром видимых световых волн, выполненный на базе щелевой лампы с галогеновым осветителем, а также систему управления, регистрации и анализа полученных изображений, выполненных на базе ЭВМ (ПМ №46164, опубл. 27.06.05).
Однако известному устройству, как и всем подобным устройствам на основе щелевых ламп, присущи и все их недостатки, перечисленные выше, а именно: известная система громоздка, стационарна, используется только для пациентов в положении сидя, требует фиксации головы пациента, что затрудняет ее применение в экстренных случаях для тяжелобольных пациентов, получение качественного изображения требует длительного времени, поскольку выбор участка конъюнктивы, установка освещения, наводка на резкость проводится оператором.
Таким образом, ни один из выше описанных способов и устройств не позволяет осуществить объективную, динамическую экспресс-оценку состояния пациента, не позволяет осуществить мониторирование изменений его состояния в процессе лечения, требует оборудованного рабочего места для исследования состояния пациента в процессе биомикроскопии конъюнктивы, что часто невозможно в случае тяжело больных пациентов.
Задача изобретения состоит в повышении оперативности и объективности способа за счет выявления новых объективных морфометрических параметров системы микроциркуляции бульбарной конъюнктивы и создании для этого мобильного портативного комплекса экспресс-съемки с автоматическим анализом микрососудистого русла конъюнктивы глазного яблока, применение которого максимально щадяще для пациента.
Поставленная задача достигается способом оценки состояния пациента путем биомикроскопического определения морфометрических показателей микроциркуляторного русла, при этом в качестве морфометрических показателей используют общую удельную длину капилляров, удельную длину мельчайших капилляров и удельную длину больших сосудов и при уменьшении общей удельной длины капилляров не менее чем на 10% и/или удельной длины мельчайших капилляров не менее чем на 20% и/или увеличении удельной длины больших сосудов на 150-160% от величины средних показателей в норме равных, соответственно, 6,7; 5,3 и 0,3, делают вывод о наличии патологического процесса, при этом удельная длина сосудов представляет собой величину отношения абсолютной длины сосудов, выраженной в миллиметрах, отнесенную к площади в один квадратный миллиметр.
Время наблюдения и частота съемки конъюнктивы глазного яблока зависят от тяжести состояния пациента. Так, при легкой и средней тяжести съемку осуществляют обычно через 2-3 часа, а при тяжелой степени поражения – через 0,5-1 час.
Поставленная задача решается также заявляемым устройством, состоящим из оптической системы, включающей видеокамеру с системой переноса изображений и осветитель, а также соединенной с ней системы управления, регистрации и анализа полученных изображений, при этом оптическая система связана с системой управления динамической обратной связью, обеспечивающей оптимизацию качества для каждого изображения, осветители представляют собой два конструктивно объединенных супер ярких белых светодиода, жестко закрепленных на видеокамере таким образом, что направление их световых потоков составляет угол не менее 20 градусов относительно оптической оси системы переноса изображений.
Блок-схема устройства для конъюнктивальной биомикроскопии глаза изображена на чертеже.
Устройство содержит видеокамеру 1 с системой 2 переноса изображений. На корпусе камеры 1 жестко закреплены два конструктивно связанных друг с другом осветителя 3. Для гашения бликов система 2 и осветители 3 могут быть снабжены поляризационными фильтрами (на чертеже не показаны). Осветители 3 соединены с блоком 4 управления яркостью и формируют световые пятна 5 на конъюнктиве 6. Видеокамера 1 соединена с буфером 7 изображений, блоком 8 отображения видеоинформации и блоком 9 управления передаточной характеристикой камеры. Блок 10 ввода параметров, а именно количество и качество изображений, пространственный спектр, яркостные и контрастные характеристики, связан с блоком 4 управления яркостью и блоком 11 предварительного анализа изображений, а также блоками 9, 11, блоком 12 морфологического анализа изображений и счетчиком 13 записанных кадров, который в свою очередь соединен с источником звукового сигнала 14. Буфер 7 изображений соединен с блоком 11 и блоком 15 записи изображений, который в свою очередь соединен с блоком 11. Блок 8 отображения видеоинформации соединен с видеокамерой 1 и блоком 12 морфологического анализа изображений, который соединен с блоком 16 записи результатов морфологического анализа изображений.
Взаимное расположение пятен 5 определяется расстоянием от видеокамеры 1 до конъюнктивы 6. При совмещении пятен 5 на приемной матрице видеокамеры 1 образуется резкое изображение области конъюнктивы, расположенной в световом пятне 5. Блок осветителей 3 установлен на корпусе видеокамеры 1 таким образом, что направление их световых потоков составляет угол не менее 20 градусов относительно оптической оси системы 2 переноса изображений, что позволяет исключить попадание света осветителей в зрачок глаза пациента.
Устройство работает следующим образом.
Видеокамеру 1 располагают вблизи от глаза пациента таким образом, чтобы на выбранном участке конъюнктивы 6 совместились световые пятна 5 от осветителей 3. Блок 11 предварительного анализа изображений определяет характеристики каждого изображения из последовательности, поступившей из буфера 7, и выдает управляющие сигналы на блок 9 управления передаточной характеристикой камеры 1 и блок 4 управления осветителями 3. При появлении в динамической последовательности изображений изображения, соответствующего заданным в блоке 10 параметрам качества: яркость, контраст, неравномерность яркости по полю изображения, уровень высокочастотных составляющих пространственного спектра, блок 11 предварительного анализа изображений направляет это изображение на блок 15 записи изображений и выдает сигнал счетчику 13 изображений для подсчета количества записанных изображений и сравнения с количеством, заданным в блоке 10. Счетчик 13 изображений при изменении своего состояния на короткое время включает источник 14 звукового сигнала для информирования оператора о ходе процесса записи и анализа. Блок 9 управления передаточной характеристикой камеры 1 и блок 4 управления осветителями 3 согласуют световой поток, попадающий на приемную матрицу видеокамеры 1 с ее передаточными характеристиками для получения изображений заданного качества. Блок 12 морфологического анализа осуществляет анализ записанных изображений конъюнктивы, поступающих из блока 15 записи изображений, рассчитывает характеристики микроциркуляции, а анализируемые изображения и результаты расчетов направляет на устройство 8 отображения и в блок 16 записи результатов.
Реализация заявляемого устройства осуществляется с использованием USB 2.0 видеокамеры высокого разрешения (1280×1024), преимущественно высокоскоростной (60 кадров/с и выше), например, USB-2.0 камера VEC-135 производства Санкт-Петербургской фирмы ЗАО “ЭВС”. Осветители выполняют на базе супер ярких белых светодиодов, например марки TL10W02-D.
Функциональные блоки 7÷9 и 10÷16 устройства реализуют в виде аппаратно-программного комплекса на базе портативного компьютера с процессором Pentium 2000, оснащенного интерфейсом USB2. Система в реальном времени заносит изображения с видеокамеры в оперативную память и отображает их на экране монитора. Программное обеспечение анализирует резкость, яркость и контрастность каждого изображения и корректирует передаточную характеристику камеры 1 таким образом, чтобы максимально использовать ее динамический диапазон. Каждое изображение подвергается процедуре Фурье-анализа для оценки его частотных и контрастных характеристик, и если они удовлетворяют параметрам, введенным в блок 10 параметров, сохраняется в памяти или на жестком диске компьютера. Это сопровождается изменением звукового сигнала. Записанное изображение и результаты предварительной обработки отображается в отдельном окне монитора. Этот процесс повторяется, пока не будет записано заданное в блоке 10 параметров количество изображений. После чего звуковой сигнал прекращается, что служит сигналом оператору для прекращения съемки конъюнктивы. Затем в блоке 12 морфологического анализа проводится детальный анализ серии записанных изображений, сохранение и отображение его результатов.
Таким образом, заявляемое устройство, включающее видеокамеру, осветитель и компьютер, позволяет отказаться от достаточно громоздкой системы на основе щелевой лампы, избежать фиксации головы пациента. Устройство портативно и мобильно, может быть легко доставлено в любое требуемое место, использоваться для исследования тяжелобольных пациентов, при этом значительно сокращается время получения морфометрических показателей.
Собственно процесс съемки конъюнктивы включает следующие стадии. В компьютер, например типа ноутбук, работающий под управлением операционной системы Windows XP, Windows 2000 или Linux с подключенной к нему видеокамерой загружается разработанная заявителем программа управления и обработки процессом измерений. Затем в интерактивном режиме вводится информация о пациенте и параметры управления процессом съемки (количество изображений, линейное увеличение камеры и т.п.). После этого при необходимости для обеспечения электробезопасности, если компьютер был подключен к сети, его отключают и переходят на автономное питание. Звуковой сигнал означает, что оператору можно приступать к съемке. Оператор в одну руку берет камеру 1, а другой рукой раздвигает веки пациента и располагает камеру 1 так, чтобы световые пятна 5 осветителей 3 совместились на участке конъюнктивы 6, съемка которого проводится. Далее он плавно перемещает камеру 1 в направлении оптической оси в обе стороны от этого положения на расстояние 3-5 мм, наблюдая за световыми пятнами осветителей. Прекращение звукового сигнала информирует оператора о завершении процесса измерений. После этого пациента оставляют в покое и приступают к анализу результатов экспресс-съемки, представленными на компьютере. Весь процесс записи и анализа снимков составляет не более 1-2 мин, что в несколько раз быстрее, чем с использованием известных устройств.
Для детального исследования определенной зоны можно увеличить размер снимка. На экран можно выводить сразу несколько любых изображений. Данные изображения затем могут быть отпечатаны на видеопринтере. Изображения и информация по пациенту хранятся в компьютере и могут быть записаны либо на дискету (например, для передачи пациенту), либо записываются на диски типа CD-R для создания своей компактной видеобиблиотеки.
Для определения морфометрических показателей конъюнктивы глазного яблока в норме на предлагаемом устройстве были проведены исследования конъюнктивы 126 практически здоровых лиц в возрасте 18-40 лет. Величина полученных средних показателей удельной длины всех сосудов и отдельных звеньев МЦР в норме с величиной стандартных отклонений представлена в таблице 1.
| Таблица 1 |
| Диаметр сосудов, мкм |
8-128 |
8-48 |
49-72 |
73-128 |
| Удельная длина сосудов МЦР |
6,7±0,5 |
5,3±0,4 |
1,1±0,08 |
0,3±0,03 |
Затем аналогичные исследования были проведены пациентам с тяжелой хирургической патологией, а именно:
1) больные с термическими ожогами (ИФ 31-60) – 12 человек, которым исследовали МЦ в период ожогового шока;
2) больные с интоксикационным синдромом вследствие острого панкреатита (отечная форма) с благоприятным течением заболевания – 9 человек.
Проведенный анализ полученных результатов показал, что клинически значимыми звеньями МЦР при исследовании бульбарной конъюнктивы являются общая удельная длина всех капилляров (8-128 мкм) МЦР, удельная длина мельчайших капилляров (8-48 мкм) и удельная длина больших сосудов (73-128 мкм). Именно величина этих морфометрических показателей МЦР наиболее ярко отражает изменения в состоянии пациента. Исследования в клинической практике влияния изменения удельной величины сосудов микроциркуляторного русла диаметром 49-72 мкм могут не приниматься во внимание при клинической оценке состояния пациента, поэтому далее их значения не приводятся.
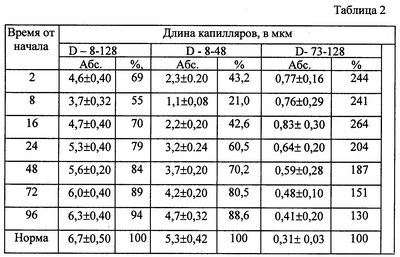
Так, у пациентов с термической травмой в период ожогового шока достоверно отмечено уменьшение общей удельной длины всех капилляров МЦР, удельной длины мельчайших капилляров (8-48 мкм) и увеличение удельной длины больших сосудов (73-128 мкм).
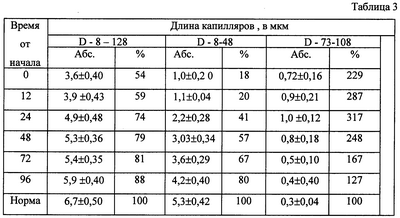
Такая же тенденция наблюдается и у пациентов с выраженным интоксикационным синдромом вследствие острого панкреатита (отечная форма) в острый период заболевания (таблица 3).
Мониторинг за состоянием пациентов показывает, что выраженность изменения этих показателей коррелирует с тяжестью состояния больного: чем больше отклонение от нормы, тем состояние больного тяжелее.
При купировании ожогового шока и явлений интоксикации происходит восстановление картины микроциркуляторного русла, хотя характеризующие ее показатели остаются достоверно ниже, чем в норме. Полученные данные показывают, что эти изменения сохраняются еще длительное время после ликвидации ожогового шока и купирования явлений интоксикации.
Кроме того, выявлено, что данный метод позволяет в процессе мониторирования выявлять в режиме реального времени изменения состояния МЦР, которые опережают на 6-8 часов клинические изменения состояния пациента. Это позволяет прогнозировать развитие заболевания и корректировать лечение до появления клинических признаков ухудшения.
Сущность изобретения поясняется приведенными ниже примерами.
Больной Ш., 52 лет, поступил в клинику с диагнозом: термический ожог ШАБ 18% поверхности тела (Индекс Франка – 34), легкий ожоговый шок спустя 2 часа после получения травмы. При транспортировке СМП больному вводились ненаркотические анальгетики. В стационаре проводилась инфузионная противошоковая терапия в расчетном объеме по формуле Эванса. Выполняли динамический контроль клинического анализа крови, измеряли почасовой диурез, выполняли термометрию. На фоне проводимого лечения через 24 часа больной вышел из состояния ожогового шока, что подтверждалось снижением гематокрита, повышением температуры тела до 37,6°С, адекватным диурезом; сатурация крови кислородом без респираторной поддержки составила 97%.
Контроль состояния микроциркуляции выполняли при помощи предлагаемой методики биомикроскопии бульбарной конъюнктивы с использованием заявляемого устройства. Выявлено, что при поступлении, спустя 2 часа после травмы, произошло значительное на 45% уменьшение удельной длины мельчайших и мелких капилляров, отмечено на 75% увеличение удельной длины более крупных сосудов, что соответствовало патофизиологическому состоянию шунтирования сосудов МЦР. При купировании явлений ожогового шока происходило постепенное увеличение длины функциональных капилляров МЦР и уменьшение удельной длины сосудов более крупного калибра.
Таким образом, проведенное исследование позволяет в режиме реального времени оценивать состояние МЦР, контролировать качество проводимых лечебных мероприятий.
Больная М., 42 лет, поступила в хирургическое отделение с диагнозом: острый панкреатит. У больной был выраженный болевой синдром в эпигастральной области, тошнота, рвота желудочным содержимым, не приносящая облегчения. Определяли выраженный лейкоцитоз (12,6·109/л), сгущение крови (гемоглобин 148 г/л; гематокрит 0,49). На УЗИ выявлено увеличение головки поджелудочной железы до 3,2 см и отечность парапанкреатической клетчатки.
Пациентке проводилась антибиотикотерапия, инфузионная дезинтоксикационная терапия, антиферментная терапия, цитостатики, сандостатин. На фоне проводимого лечения через 48 часов состояние пациентки значительно улучшилось: уменьшился болевой синдром, исчезли тошнота и рвота, лейкоцитоз снизился до 7,2·109/л, гематокрит до 0,321, амилаза до 64 ед. На УЗИ отмечено уменьшение головки поджелудочной железы до 2,3 см, исчез отек парапанкреатической клетчатки. В последующем отмечено благоприятное течение патологического процесса.
При биомикроскопии при помощи заявляемого устройства выявлено, что при поступлении до начала лечения удельная длина мелких и мельчайших капилляров была на 40% ниже значений нормы. В то же время отмечено достоверное на 85% увеличение удельной длины крупных сосудов, составляющих микроциркуляторное русло. Через 8 часов на фоне некоторого снижения явлений интоксикации отмечено увеличение длины функционирующих мелких и мельчайших капилляров, хотя длина крупных сосудов практически не изменилась. Через 24 часа и 48 часов на фоне стихания явлений воспалительного процесса в поджелудочной железе и купирования явлений интоксикации происходило дальнейшее увеличение удельной длины мелких и мельчайших капилляров и уменьшение удельной длины крупных сосудов. По данным УЗИ отек головки поджелудочной железы сохранялся в течение 7 дней. В эти же сроки все еще сохранялись выраженные нарушения в МЦР.
Больной П., 38 лет, поступил в клинику с диагнозом: термический ожог ШАБ ст 30% (12%) поверхности тела (индекс Франка 54), ожоговый шок средней степени тяжести спустя 4 часа после травмы. В стационаре проводилась инфузионная терапия под контролем изменений в клиническом анализе крови, почасового диуреза, термометрии, сатурации кислородом крови. На фоне инфузионной терапии состояние улучшилось, снизился гематокрит, восстановился диурез, сатурация крови кислородом достигла 96%.
На фоне клинического улучшения через 36 часов после начала лечения у больного отмечено в динамике ухудшение показателей, характеризующих состояние МЦР: произошло уменьшение удельной длины мелких и мельчайших капилляров и увеличение удельной длины крупных сосудов. Через 4 часа у больного появились признаки психоза, рвота с примесью измененной крови, температура тела снизилась до 36,7°С. Больному проведена коррекция лечения, увеличен объем инфузионной терапии, добавлены антиагреганты, антацидные препараты. На фоне скорректированной терапии через 12 часов наступила стабилизация состояния, что подтверждалось результатами биомикроскопии (таблица 4).
| Таблица 4 |
| Время после начала |
Длина капилляров, мкм |
| D – 8-128 |
D – 8-48 |
D – 73-108 |
|
| Абс. |
% |
Абс. |
% |
Абс. |
% |
| 2 |
5,0±0,41 |
75 |
3,26±0,19 |
51 |
0,62±0,15 |
198 |
| 8 |
4,7±0,32 |
75 |
1,52±0,04 |
29 |
0,88±0,3 |
281 |
| 16 |
5,0±0,4 |
74 |
2,3±0,2 |
43 |
0,79±0,3 |
253 |
| 24 |
5,6±0,4 |
83 |
3,0±0,2 |
57 |
0,73±0,2 |
233 |
| 30 |
5,7±0,2 |
85 |
2,7±0,2 |
62 |
0,66±0,2 |
212 |
| 36 |
5,0±0,4 |
75 |
2,0±0,2 |
39 |
0,79±0,2 |
253 |
| 42 |
5,3±0,4 |
79 |
2,6±0,3 |
50 |
0,66±0,2 |
210 |
| 48 |
5,3±0,2 |
80 |
3,0±0,2 |
57 |
0,64±0,2 |
203 |
| 60 |
5,1±0,38 |
76 |
3,3±0,2 |
62 |
0,48±0,29 |
153 |
| Норма |
6,7±0,53 |
100 |
5,0±0,43 |
100 |
0,31±0,04 |
100 |
Больной Е., 62 лет, поступил в кардиологическое отделение с диагнозом: ИБС. Инфаркт миокарда, передне-септальный, крупноочаговый, острый период, – через 2,5 часа после появления в покое интенсивных, постоянных, сжимающих болей за грудиной, с иррадиацией в левую лопатку, сопровождавшихся чувством нехватки воздуха, потливостью, страхом смерти. Прием нитроглицерина (4 таблетки под язык, дробно) эффекта не дал. Больной вызвал бригаду скорой медицинской помощи и после начала лечения (аспирин 0,25 внутрь, баралгин 5 мл в/в, гепарин 5000 ЕД в/в, метопролола тартрат 0,025 п/я) – был доставлен в приемное отделение ДВОМЦ.
При поступлении сохранялись неинтенсивные боли в левой половине грудной клетки («чувство наболевшего»), слабость. АД 140 и 85 мм рт.ст. На ЭКГ: ритм синусовый, ЧСС 84 удара в минуту, единичные желудочковые экстрасистолы; выпуклая элевация сегмента STV1-V3 до 4 мм в виде монофазной кривой, депрессия сегмента STIII, aVF до 2 мм.
В анализах (первые сутки нахождения в стационаре): лейкоцитов 8,4·109/л, креатинкиназа общая и МВ-фракция повышены; тропониновый тест положительный.
В отделении проводили терапию: ненаркотические анальгетики (кетопрофен),  -блокаторы (бисопролол по 5 мг/сут), инфузия перлинганита, инъекции низкомолекулярного гепарина (эноксапарин натрия по 0,8 мл×2 раза в день, подкожно), глюкозо-калиево-инсулиновую смесь (в/в капельно), ингибиторы ангиотензиопревращающего фермента (эналаприл по 5 мг×2 раза в сутки), ингаляции увлажненного кислорода. -блокаторы (бисопролол по 5 мг/сут), инфузия перлинганита, инъекции низкомолекулярного гепарина (эноксапарин натрия по 0,8 мл×2 раза в день, подкожно), глюкозо-калиево-инсулиновую смесь (в/в капельно), ингибиторы ангиотензиопревращающего фермента (эналаприл по 5 мг×2 раза в сутки), ингаляции увлажненного кислорода.
На фоне проводимого лечения к третьим суткам перестал рецидивировать болевой синдром за грудиной, эпизодов одышки не было. Гемодинамика стабильная: АД 130-140 и 80-85 мм рт.ст.
На ЭКГ – закономерная динамика крупноочагового инфаркта миокарда, формирование подострой стадии.
В анализах: лейкоцитоз 11,2·109/л, уровень активности креатинкиназы общей и МВ-фракции снизился.
При биомикроскопии при помощи заявленного устройства выявлено, что при поступлении до начала лечения удельная длина мелких и мельчайших капилляров была на 48% ниже нормы. Так же было отмечено достоверное на 116% увеличение удельной длины крупных сосудов, составляющих МЦР.
Через 24 и 48 часов на фоне терапии и стабилизации сердечной деятельности отмечено увеличение удельной длины мелких и мельчайших капилляров, а также уменьшение длины крупных сосудов.
Больной К., 29 лет. Поступил в пульмонологическое отделение с диагнозом внебольничная пневмония.
При поступлении больного беспокоили выраженные боли в правой половине грудной клетки, усиливающиеся при дыхании, на слабость, одышку, головокружение, выделение небольшого количества слизистой мокроты.
При обследовании выявлено – выраженный лейкоцитоз до 16,9·109/л с палочкоядерным сдвигом, повышение СРБ до 224 ед./л. На рентгенограмме органов грудной клетки выявлено почернение 9 и 10 сегментов правого легкого, ограниченный экссудативный плеврит. Пациенту проводилась антибиотикотерапия, инфузионная дезинтоксикационная терапия, противовоспалительные препараты, муколитики, антигистаминные средства.
На фоне проводимого лечения у пациента через 72 часа отмечено уменьшение выраженности болевых ощущений, слабости, одышки. Выявлено снижение лейкоцитоза до 12,8·109/л, снижение уровня МЦР до 148 ед./л.
На контрольной рентгенограмме органов грудной клетки через 10 дней после начала лечения отмечена положительная динамика – исчезновение выпота в плевральной полости, уменьшение полей затемнения в правом легком. В последующем отмечено благоприятное течение.
При биомикроскопии с использованием заявленного устройства выявлено, что до начала лечения длина мелких и мельчайших капилляров была на 54% ниже нормы, а удельная длина крупных капилляров была на 142% выше нормы.
Через 24 часа после начала лечения на фоне выраженной интоксикации достоверных изменений в МЦР выявлено не было. Через 48 часов отмечено увеличение удельной длины мелких и мельчайших капилляров, уменьшение удельной длины крупных капилляров отмечено только через 72 часа.
На 5-е сутки отмечено достоверное увеличение удельной длины мелких и мельчайших капилляров, уменьшение удельной длины крупных сосудов, что корректирует с позитивной динамикой клинической картины.
Изменения в МЦР сохранялись до 12 суток с момента поступления.
Таким образом, полученные данные свидетельствуют, что предлагаемый способ экспресс-диагностики состояния МЦР (методика и портативный аппаратно-программный комплекс) позволяет в режиме реального времени у постели больного получать информацию о состоянии МЦ у больных тяжелой патологией, позволяет осуществлять мониторинг состояния МЦР и на его основании прогнозировать изменение клинической картины, предпринимать лечебные мероприятия для предупреждения этих изменений.
При положительной динамике происходит постепенное увеличение длины мелких капилляров и уменьшение длины крупных. В том случае, если в результате мониторирования мы находим противоположную тенденцию, мы фиксируем ухудшение МЦ, что неизбежно ведет через 6-8 часов к ухудшению клинической картины, уже оцениваемое врачом ухудшение состояния.
Формула изобретения
1. Способ оценки состояния пациента на основе биомикроскопического определения морфометрических показателей микроциркуляторного русла, проводимого с помощью конъюнктивной микроскопии, отличающийся тем, что в качестве морфометрических показателей используют общую удельную длину капилляров, удельную длину мельчайших капилляров и удельную длину больших сосудов и при уменьшении общей удельной длины капилляров не менее чем на 10% и/или удельной длины мельчайших капилляров не менее чем на 20% и/или увеличении удельной длины больших сосудов на 150-160% от величины средних показателей в норме равных соответственно 6,7, 5,3 и 0,3, делают вывод о наличии патологического процесса в организме, связанного с нарушением микроциркуляции, при этом удельная длина сосудов представляет собой величину отношения абсолютной длины сосудов, выраженной в миллиметрах, отнесенную к площади в один квадратный миллиметр.
2. Устройство для конъюнктивальной микроскопии, состоящее из оптической системы, включающей цифровую видеокамеру с системой переноса изображений и осветитель, и связанной с ней системы управления, регистрации и анализа полученных изображений, отличающееся тем, что оптическая система связана с системой управления обратной связью, осветитель представляет собой два конструктивно объединенных сверх ярких белых светодиодов, жестко закрепленных на видеокамере таким образом, что направление их световых потоков составляет угол 20-30° относительно оптической оси системы переноса изображений.
3. Устройство по п.1, отличающееся тем, что система переноса изображений и осветители снабжены поляризационными фильтрами.
4. Устройство по п.1 или 2, отличающееся тем, что используют цифровую видеокамеру с разрешением не менее 1280×1024 и скоростью записи не ниже 60 кадров/с.
РИСУНКИ
|
|