|
|
(21), (22) Заявка: 2006108267/13, 17.03.2006
(24) Дата начала отсчета срока действия патента:
17.03.2006
(46) Опубликовано: 20.11.2007
(56) Список документов, цитированных в отчете о
поиске:
LIN ET AL. Enzyme Microb. Technol., 2000, v.27, pp.489-491. US 6,068,991, 17.02.1998. SU 1604163 A3, 30.10.1990.
Адрес для переписки:
117312, Москва, пр. 60-летия Октября, 7, корп.1, Центр “Биоинженерия” РАН
|
(72) Автор(ы):
Эльдаров Михаил Анатольевич (RU),
Редо Вадим Александрович (RU),
Жгун Александр Александрович (RU),
Зейналов Орхан Ахмед оглы (RU),
Скрябин Константин Георгиевич (RU)
(73) Патентообладатель(и):
Центр “Биоинженерия” РАН (RU)
|
(54) РЕКОМБИНАНТНАЯ ПЛАЗМИДА pETTvDAO2, ОБЕСПЕЧИВАЮЩАЯ СИНТЕЗ ОКСИДАЗЫ D-АМИНОКИСЛОТ (DAO) ДРОЖЖЕЙ Trigonopsis variabilis В КЛЕТКАХ Escherichia coli И РЕКОМБИНАНТНЫЙ ШТАММ Escherichia coli C41(DE3)/pETTvDAO2 – ПРОДУЦЕНТ DAO
(57) Реферат:
Изобретение относится к области биотехнологии, в частности к генетической инженерии, и может быть использовано в микробиологической промышленности при получении полусинтетических бета-лактамных антибиотиков нового поколения. Сконструирована рекомбинантная плазмидная ДНК pETTvDAO2, обеспечивающая высокий уровень экспрессии включенного в нее фрагмента ДНК, который кодирует оксидазу D-аминокислот дрожжей Trigonopsis variabilis, в клетках Escherichia coli. В результате трансформации штамма E.coli предложенной плазмидой и селекции трансформированных клонов получен новый рекомбинантный штамм E.coli C41(DE3)/pETTvDAO2 – продуцент оксидазы D-аминокислот, обеспечивающий высокий выход рекомбинантного фермента, который является одним из основных участников процесса энзиматической трансформации цефалоспорина С при получении антибиотиков из семейства цефалоспоринов. 2 н.п. ф-лы, 3 ил., 2 табл.
Настоящее изобретение относится к области биотехнологии и, в частности, к генетической инженерии и может быть использовано в микробиологической промышленности при получении полусинтетических цефалоспориновых антибиотиков нового поколения. Предлагаются рекомбинантная плазмидная ДНК pETTvDAO2, содержащая фрагмент ДНК, кодирующий оксидазу D-аминокислот дрожжей Trigonopsis variabilis, и обеспечивающая высокий уровень экспрессии фермента в клетках Escherichia coli, и рекомбинантный штамм E.coli С41(DE3)/pETTvDAO2 – продуцент оксидазы D-аминокислот.
Важнейшим промежуточным продуктом в производстве различных антибиотиков из семейства цефалоспоринов является 7-аминоцефалоспориновая кислота (7-АЦК) [1]. Конверсия цефалоспорина С (ЦефС) в 7-АЦК может осуществляться либо методом химического гидролиза, требующего использования крайне токсичных соединений и специальных условий инкубации при низких температурах, либо путем энзиматического превращения [2]. Наиболее распространен двухстадийный способ энзиматической трансформации, предусматривающий превращение ЦефС в глутарил-7-АЦК с помощью фермента оксидазы D-аминоксилот (DAO; EC-1.4.3.3), получаемого, например, из клеток микроорганизмов Aspergillus, Penicillium, Neurospora, Pseudomonas, Cephalosporium, Trigonopsis, и последующий гидролиз глутарил-7-АЦК с образованием 7-АЦК под действием специфической 7-бета-(4-карбоксилбутанамино) ацилазы (Gl7-ACA) из клеток бактерий рода Comamonas, Pseudomonas или Arthrobacter [1, 3].
Рост производства полусинтетических бета-лактамных антибиотиков нового поколения (согласно последним оценкам [2] сегодня рынок производства 7-АЦК составляет около 20 млрд. долларов США в год) определяет возрастающую потребность в ферментах, катализирующих превращение ЦефС в 7-АЦК, в том числе в значительных количествах качественных препаратов оксидазы D-аминокислот и, соответственно, стимулирует интерес к разработке эффективных и экономичных систем продукции этого фермента методами генетической инженерии.
Уровень техники
К настоящему времени установлены последовательности целого ряда природных генов, кодирующих DAO, сконструированы содержащие эти последовательности векторы экспрессии и предложены способы получения рекомбинантных форм фермента, в частности функционально активных DAO Trigonopsis variabilis [4], Rhodotorula gracilis [5] в клетках бактерий [6, 7] и дрожжей [8, 9].
Общими недостатками всех известных способов гетерологичной экспрессии DAO в клетках E.coli являются низкая жизнеспособность рекомбинантных штаммов-продуцентов и невысокий выход их биомассы даже при продолжительном культивировании на обогащенных средах, что обусловлено, в первую очередь, токсичностью функционально активной DAO для бактериальных клеток [10]. Токсическое действие DAO на клетки распространенных реципиентных штаммов E.coli связано с несколькими факторами: общим метаболическим стрессом сверхпродукции чужеродного белка, истощением пула D-аминокислот, необходимых для синтеза клеточной стенки, высвобождением побочного продукта реакции DAO – перекиси водорода [5-7]. Эти обстоятельства значительно затрудняют задачу масштабирования процессов получения DAO с помощью рекомбинантных штаммов E.coli и обеспечения физиологической стабильности продукции DAO при длительной ферментации и хранении бактериальных штаммов-продуцентов DAO [10]. Решение проблемы, связанной с токсичностью гетерологично экспрессируемой DAO для бактериальных клеток-хозяев, дополнительно осложняется тем, что для большинства используемых в E.coli промоторов характерен относительно высокий базальный уровень экспрессии [11, 12, 13]. Таким образом, задача создания новых стабильных и эффективных штаммов E.coli – продуцентов DAO, позволяющих успешно осуществлять масштабирование процессов ферментации, остается по-прежнему актуальной.
Раскрытие изобретения
С учетом особенностей экспрессии DAO в бактериальных клетках при решении задачи повышения выхода активной рекомбинантной DAO в E.coli весьма перспективной представляется разработка новых векторных конструкций, содержащих ген DAO, которые обеспечивали бы эффективный индуцибельный синтез фермента при низком базальном уровне экспрессии и поиск оптимальных с точки зрения стабильности и выхода биомассы систем экспрессии (комбинации “экспрессирующий вектор”/”штамм-реципиент”).
Эти аспекты и составили цель предлагаемого изобретения.
Поставленная цель была достигнута за счет того, что
1) в коллекции микроорганизмов был выявлен штамм Trigonopsis variabilis, эффективно синтезирующий фермент DAO (далее TvDAO);
2) из этого штамма получен ген TvDAO и последовательность ДНК, не содержащая интронов и кодирующая непрерывную полную аминокислотную последовательность фермента;
3) сконструирована рекомбинантная плазмидная ДНК pETTvDAO2, обеспечивающая высокий и стабильный выход TvDAO в клетках кишечной палочки в условиях индукции;
4) в результате трансформации экспрессирующей плазмидой pETTvDAO2 клеток штамма E.coli C43(DE3) получен рекомбинантный штамм Escherichia coli C43(DE3)/ pETTvDAO2 с высоким уровнем индуцируемого синтеза и стабильной продукцией активной DAO.
Штамм Trigonopsis variabilis, отобранный в качестве источника для выделения гена DAO, депонирован ранее во Всероссийской коллекции микроорганизмов под номером ВКМ Y-2601.
Последовательность гена TvDAO (SEQ ID №3), включающая нуклеотидную последовательность для полной аминокислотной последовательности фермента, получена методом полимеразной цепной реакции (ПЦР) с использованием в качестве матрицы хромосомной ДНК, выделенной из штамма Trigonopsis variabilis ВКМ Y-2601, а в качестве праймеров – синтетических олигонуклеотидов с нуклеотидными последовательностями SEQ ID №1 (праймер tv1) и SEQ ID№2 (праймер tv2), специфичными по отношению к ее N- и С-концевым областям. Для удаления интрона, содержащегося в последовательности, полученной путем ПЦР-амплификации с праймерами tv1/tv2, первичный ПЦР-продукт был подвергнут повторной ПЦР-амплификации с праймерами tv3 (SEQ ID №4) и tv5 (SEQ ID №5). Полученная в результате повторной амплификации последовательность SEQ ID №6, не содержавшая интрона, была использована далее для конструирования экспрессирующего вектора.
При создании рекомбинантной плазмиды для экспрессии DAO предварительно был получен промежуточный вектор pET-TetI (фиг.2), содержащий в качестве генетического маркера ген устойчивости к тетрациклину (TetR), которым был заменен ген бета-лактамазы в коммерческой плазмиде рЕТ21. Использование в качестве маркера гена устойчивости к тетрациклину, а не традиционно применяемого в подобных конструкциях гена устойчивости к ампициллину освобождает от необходимости последующей сложной очистки целевого белка для удаления примесей бета-лактамаз. Экспрессирующая рекомбинантная плазмида pETТvDAO2 сконструирована путем лигирования последовательности SEQ ID №6 в вектор pET-TetI по сайтам рестрикции NcoI и XhoI (фиг.3).
Для получения рекомбинантного штамма-продуцента TvDAO полученную плазмиду pETТvDAO2 вводили в клетки штамма-реципиента, в качестве которого был избран штамм Escherichia coli C41(DE3). Выбор штамма-реципиента обусловлен тем, что он а) несет ген РНК-полимеразы фага Т7, которая необходима для обеспечения эффективной транскрипции целевых генов, находящихся в векторной конструкции под контролем промотора фага Т7, б) дефектен по синтезу протеаз, что существенно повышает выход синтезируемых гетерологичных белков, и в) несет мутацию, снижающую уровень продукции Т7 полимеразы, что в свою очередь снижает базальный уровень экспрессии гена с промотора Т7 [14]. Отбор продуктивных и стабильных клонов-продуцентов среди тетрациклин-устойчивых трансформантов штамма C41(DE3) предложенной плазмидой проводили по признаку продукции функционально-активной DAO при культивировании на обычных селективных средах с добавлением индуктора изопропил-D-тиогалактозида (ИПТГ) или лактозы.
Полученный рекомбинантный штамм E.coli С41(DE3)/pETTvDAO2 характеризуется низким базальным уровнем экспрессии TvDAO и повышенным выходом функционально-активной оксидазы в условиях индукции, который в среднем примерно в 1,5 раза выше, чем у известных рекомбинантных штаммов кишечной палочки.
Таким образом, настоящее изобретение включает два объекта.
Первым объектом является рекомбинантная плазмида pETТvDAO2, обеспечивающая синтез оксидазы D-аминокислот Trigonopsis variabilis (TvDAO) в клетках Escherichia coli, которая состоит из кодирующего TvDAO фрагмента ДНК с нуклеотидной последовательностью SEQ ID №6 и NcoI/XhoI фрагмента размером 7,15 т.п.н. плазмиды pET-Tet, полученной путем замены гена бета-лактамазы в векторе рЕТ21 геном устойчивости к тетрациклину (TetR) в обратной ориентации.
Второй объект изобретения – рекомбинантный штамм Escherichia coli С41(DE3)/pETTvDAO2 – продуцент оксидазы D-аминокислот.
Краткое описание фигур.
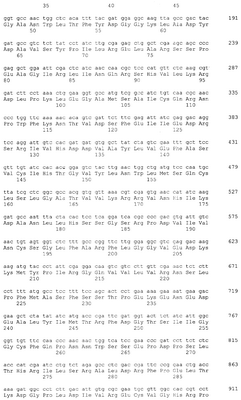
Фиг.1 – Сравнение нуклеотидных последовательностей гена TvDAO Trigonopsis variabilis (Query, номер доступа в Genbank Z80895) и ПЦР-фрагмента, полученного на геномной ДНК Trigonopsis variabilis ВКМ Y-2601 с праймерами tv1/tv2 (subject). Сиквенс с праймера tv1.
Фиг.2 – Физическая и генетическая карты векторов pET-TetD (А) и pET-TetI(Б). Обозначены положения индикаторных сайтов рестрикции, участки промотора и терминатора РНК-полимеразы фага Т7 (Т7 пром и Т7 терм), область начала репликации (ColE1 origin, f1 origin), ген устойчивости к тетрациклину (TetR), ген lac-репрессора (lacI).
Фиг.3 – Физическая и генетическая карты плазмиды pETTvDAO2. Обозначено положение гена TvDAO (заполнение черным), остальные обозначения, как на Фиг.2.
Осуществление изобретения
При осуществлении изобретения, помимо методов, подробно раскрытых в нижеследующих примерах, использовали хорошо известные специалистам методики, описанные в руководствах по молекулярной биологии и генетической инженерии [15, 16].
Пример 1. Культивирование штамма Trigonopsis variabilis ВКМ Y-2601 и определение активности оксидазы.
Культуру Trigonopsis variabilis выращивают в 5 мл жидкой среды YPD, содержащей 1% дрожжевой экстракт, 2% пептон, 2% глюкозу на качалке при 28°С в течение суток. Клетки собирают центрифугированием, когда плотность культуры достигает примерно 5 при 650 нм, промывают в буфере ТЕ (50 мМ Tris pH8,0 5 mM EDTA), суспендируют в этом же буфере (0.1 г влажных клеток на 200 мкл буфера) и замораживают до использования.
Для определения активности фермента DAO в культуре использовали колориметрический метод [17], основанный на детекции альфа-кетокислоты, образуемой в результате реакции. Сначала получают грубый экстракт, для чего замороженный осадок клеток разрушают на вортексе с помощью стеклянных бус (диаметр – 0,5 мм) с периодическим охлаждением на льду. Клеточный дебрис удаляют центрифугированием (13000 об/мин, 10 мин), 10-50 мкл полученного осветленного лизата инкубируют с 250 мкл 10 мМ D-аланина в 50 mM фосфатном буфере, pH 8.0, в течение 15 или 30 мин, реакцию останавливают добавлением 100 мкл насыщенного раствора 2,4 динитрофенилгидразина в 2N HCl. После 5 мин инкубации при комнатной температуре к раствору добавляют 300 мкл 3М NaOH и 2,5 мл дистиллированной воды и продолжают инкубацию в течение 10 мин при комнатной температуре, затем измеряют поглощение раствора при 550 нм и сравнивают результат со стандартной кривой, построенной с использованием пировиноградной кислоты. Удельную активность выражают в единицах фермента (мкмолей субстрата в мин при 25°С) на мг общего белка осветленного экстракта. Содержание общего белка определяют по методу Брэдфорда [15]. Рассчитанная таким образом удельная активность TvDAO в штамме Trigonopsis variabilis ВКМ Y-2601 составила 5 ед/мг белка.
Пример 2. Выделение геномной ДНК Trigonopsis variabilis ВКМ Y-2601.
К замороженной суспензии клеток добавляют 75 мкл 10% SDS до конечной концентрации 2% и 200 мкл промытых кислотой стеклянных бус (с диаметром 0,5 мм) и подвергают интенсивному встряхиванию на вортексе в течение 5 минут. Затем к суспензии добавляют 300 мкл насыщенного буфером ТЕ раствора фенола и встряхивают на вортексе 30 сек. Смесь центрифугируют, супернатант дважды экстрагируют насыщенным водой раствором хлороформа. Водную фазу отбирают и добавляют 5М раствор ацетата калия (рН 6,0) до конечной концентрации 1,5 М. Раствор центрифугируют, к супернатанту добавляют равный объем изопропанола. Осадок нуклеиновых кислот собирают центрифугированием, растворяют в 300 мкл 0,5 М ацетата калия, повторно осаждают добавлением 3 объемов этанола и растворяют в 100 мкл деионизованной воды при нагревании в течение 30 мин при 65°.
Пример 3. ПЦР-амплификация последовательности гена DAO Trigonopsis variabilis.
Первичная структура гена DAO Trigonopsis variabilis и его мРНК известны (номер доступа в GenBank Z80895). Это обстоятельство позволяет спроектировать “прямой” и “обратный” праймеры для ПЦР-амплификации требуемой области гена. В данном случае использовали праймеры, которые ограничивают последовательность, состоящую из двух экзонов и расположенного между ними интрона:
5′-TGATAGGCAAATC CGTGCTC-3′ “прямой” tv1-праймер (SEQID №1) и
5′-GTAAACACGTCGCAGTCGTC-3′ “обратный” tv2-праймер(SEQID №2)
Геномную ДНК Trigonopsis variabilis ВКМ Y-2601, выделенную, как описано в примере 2, денатурируют путем нагревания при 100°С в течение 5 минут, помещают в лед и подвергают 30 циклам ПЦР в 50 мкл смеси следующего состава:
5 мкл 10-кратного Taq-SE ПЦР-буфера (Сибэнзим);
5 мкл геномной ДНК (200 нг/мкл);
5 мкл 3 мкМ праймера tv1;
5 мкл 3 мкМ праймера tv2;
5 мкл 2,5 мМ dNTP каждого вида;
25 мкл деионизованной воды;
1 мкл Taq-SE полимеразы (5 ед/мкл, Сибэнзим).
Условия проведения ПЦР: 94°, 5′ (денатурация), 94°, 30  ; 50°, 30 ; 50°, 30  ; 72°,1′ (амплификация). После амплификации 5 мкл ПЦР смеси анализируют электрофорезом в 1% агарозном геле и выявляют гомогенный фрагмент размером около 1 тпн. Фрагмент выделяют из геля с помощью набора Wizard PCR Preps Kit и подвергают автоматическому секвенированию с использованием праймеров tv1, tv2. На основании данных секвенирования был сделан вывод о соответствии последовательности выделенного фрагмента ожидаемой (фиг.1) ; 72°,1′ (амплификация). После амплификации 5 мкл ПЦР смеси анализируют электрофорезом в 1% агарозном геле и выявляют гомогенный фрагмент размером около 1 тпн. Фрагмент выделяют из геля с помощью набора Wizard PCR Preps Kit и подвергают автоматическому секвенированию с использованием праймеров tv1, tv2. На основании данных секвенирования был сделан вывод о соответствии последовательности выделенного фрагмента ожидаемой (фиг.1)
Пример 4. Получение и клонирование последовательности ДНК, кодирующей полную аминокислотную последовательность DAO Trigonopsis variabilis.
Для получения ДНК-последовательности, кодирующей полную аминокислотную последовательность TV-DAO, из фрагмента, полученного путем ПЦР-амплификации с праймерами tv1/tv2 (SEQ ID №3), удаляют интрон, для чего его подвергают повторной ПЦР-амплификации с праймерами tv3/tv5, имеющими следующую структуру:
NcoI
5’catgccATGGCTAAAATCGTTGTTATTGGGGCCGGTGTTGCCGGTTTAAC-3′ tv5-праймер (SEQ ID №4)
XhoI
5’CCCTCGAGCGGCCGCTAAAGGTTTGGACGAGTAAGA-3′ tv3-праймер (SEQ ID №5)
Использованные праймеры ограничивают фрагмент гена DAO, включающий начало 2-го экзона, расположенного в положении +125 последовательности SEQID №3, и терминаторный кодон TAG, расположенный в положении +1170 той же последовательности, и добавляют к этой последовательности инициаторный кодон трансляции ATG и участок, кодирующий 8 аминокислот 1-го экзона. Праймеры несут также сайты для рестриктаз NcoI и XhoI, отсутствующие в кодирующей последовательности гена DAO. 1 нг ПЦР-фрагмента, полученного, как описано в примере 3, подвергают 25 циклам ПЦР-амплификации с праймерами tv5/tv3. Из агарозного геля выделяют фрагмент размером около 1 тпн и секвенируют. Нуклеотидная последовательность данного фрагмента представлена в SEQ ID №6.
Пример 5. Конструирование плазмид для экспрессии TvDAO в E.coli.
Конструирование рекомбинантных плазмид проводили в несколько стадий. В качестве базового вектора использовали плазмиду рЕТ21 (Novagen).
А) Конструирование плазмид pET TetD и pET TetI.
С целью удаления гена AmpR из плазмиды pET21 и замены его геном устойчивости к тетрациклину проводили конструирование плазмиды pET-Tet. Для этого сначала получали “вставку”, несущую ген устойчивости к тетрациклину: 2 мкг плазмидной ДНК pKRP12[18] гидролизовали рестриктазой PstI и выделяли из агарозного геля фрагмент размером 1200 п.н. Плазмиду рЕТ21 гидролизовали по сайту PstI и лигировали с полученной “вставкой”, используя следующую смесь: 1 мкл вектора (20 нг/мкл), 1 мкл фрагмента (50 нг/мкл), 2 мкл 5-кратного лигазного буфера (Gibco-BRL), 5 мкл воды и 1 мкл Т4 ДНК лигазы (1 ед/мкл, Сибэнзим). Смесь инкубировали в течение 14 часов при 12°, затем прогревали 15 мин при 65°, охлаждали во льду и 5 мкл смеси использовали для трансформации компетентных клеток штамма E.coli JM 109 [15]. Отбирали тетрациклин-устойчивые клоны, чувствительные к ампициллину. Дополнительную селекцию нужных клонов проводили с помощью рестриктного анализа препаратов плазмидной ДНК (по образованию фрагментов размером 1200, 1300, 4300 п.н. при гидролизе EcoRI+PstI). Отобранные клоны дополнительно анализировали для определения “ориентации” вставки маркера TetR путем совместного гидролиза рестриктазами ClaI+XhoI. Образование фрагментов размером 1,7 тпн и 5,6 тпн свидетельствует о “прямой” ориентации вставки маркера TetR, а фрагментов размером 2,7 тпн и 4, 6 тпн – об “обратной”. Отобранные клоны с “прямой” и “обратной” ориентацией маркера TetR были обозначены как pET_TetD и. pET_TetI соответственно и использованы в дальнейшей работе. Физические и генетические карты плазмид pET_TetD и. pET_TetI приведены на фиг.2.
Б) Получение рекомбинантных плазмид pETTvDAO1 и pETTvDAO2.
Полученный в примере 4 фрагмент с SEQ ID №6 гидролизуют рестриктазами NcoI и XhoI и лигируют с NcoI/XhoI фрагментом вектора pET TetD размером 7,15 т.п.н, используя следующие условия: 1 мкл вектора (20 нг/мкл), 1 мкл фрагмента (50 нг/мкл), 2 мкл 5-кратного лигазного буфера (Gibco-BRL), 5 мкл воды и 1 мкл Т4 ДНК лигазы (1 ед/мкл, Сибэнзим). Смесь инкубируют в течение ночи при 12°, затем прогревают 15 мин при 65° и охлаждают во льду. 5 мкл лигазной смеси используют для трансформации компетентных клеток штамма E.coli B21(DE3), после чего на селективной среде, содержащей тетрациклин (в концентрации 12 мкг/мл), выявляют устойчивые к антибиотику трансформанты.
Отбор “положительных” клонов среди полученных тетрациклин-устойчивых трансформантов штамма E.coli BL21(DE3) проводят по способности направлять синтез активной DAO. Для этого отдельные клоны выращивают в 5 мл среды LB (0,5% дрожжевой экстракт, 0,5% NaCl, 1% триптон, рН 7,2), содержащей 15 мкг/мл тетрациклина до плотности ОД600 1,0, далее добавляют индуктор ИПТГ до конечной концентрации 1 мМ и продолжают культивирование в течение ночи при температуре 23-25°С. Клетки собирают центрифугированием, суспендируют в 200 мкл буфера ТЕ, добавляют 100 мкл стеклянных бус диаметром 0,1 мм и интенсивно встряхивают на вортексе. Получают осветленные лизаты и определяют активность DAO, как описано в примере 1. Отбирают клоны с удельной активностью DAO в пределах 4-8 ед/мг белка. В контрольных (“отрицательных”) образцах активность отсутствует. Один из отобранных таким образом клонов по результатам секвенирования содержит вставку с SEQ ID №6 в нужной ориентации. Содержащуюся в этом клоне плазмиду обозначают как pETTv DAO1. Для получения вектора экспрессии TvDAO на основе плазмиды pET_TetI NcoI/XhoI фрагмент размером 1080 пн плазмиды pETTv DAO1, кодирующий ген TvDAO, переклонируют в вектор pET_TetI, и отбирают положительный клон, содержащий плазмиду с полной кодирующей последовательностью TvDAO (SEQ ID №6), которую обозначают как pETTv DAO2.
Пример 6. Получение рекомбинантного штамма – продуцента TvDAO.
Полученными рекомбинантными плазмидами рЕТTvDAO1 и рЕТTvDAO2 трансформируют штаммы E.coli BL21(DE3) [F-, ompT, hsdSB (rB-, mB-), dcm, gal,  DE3)], BL21(DE3)/plysS и C41(DE3). Штамм E.coli BL21(DE3)/plysS содержит дополнительную плазмиду с геном лизоцима фага Т7, являющегося ингибитором T7 полимеразы. Присутствие этой плазмиды обеспечивает дополнительный контроль экспрессии с промотора Т7 в условиях индукции. Штамм E.coli C41(DE3) является производным от BL21(DE3) и несет дополнительную мутацию, снижающую уровень транскрипции с Т7 промотора, позволяющую снижать базальный уровень продукции и улучшать сопряжение между транскрипцией и трансляцией целевых генов, находящихся под контролем Т7 промотора [12, 14]. DE3)], BL21(DE3)/plysS и C41(DE3). Штамм E.coli BL21(DE3)/plysS содержит дополнительную плазмиду с геном лизоцима фага Т7, являющегося ингибитором T7 полимеразы. Присутствие этой плазмиды обеспечивает дополнительный контроль экспрессии с промотора Т7 в условиях индукции. Штамм E.coli C41(DE3) является производным от BL21(DE3) и несет дополнительную мутацию, снижающую уровень транскрипции с Т7 промотора, позволяющую снижать базальный уровень продукции и улучшать сопряжение между транскрипцией и трансляцией целевых генов, находящихся под контролем Т7 промотора [12, 14].
Отдельные клоны трансформантов выращивают в условиях пониженной аэрации, оптимальных для продукции DAO, в 50 мл среды LB при температуре 30°С до примерно 2,0 ОЕ, после чего вносят индуктор ИПТГ до конечной концентрации 1 мМ и продолжают инкубацию, как описано в [6]. В конце культивирования определяют параметры роста культуры и активности фермента в бактериальных клетках. Результаты этих опытов представлены в таблице 1.
| Таблица 1 |
| Динамика накопления рекомбинантной DAO при культивировании различных штаммов E.coli – продуцентов |
| |
Рост культуры, ОП550 |
Уд. активность DAO, ед/мг белка |
Выход DAO, ед/мл |
| Штаммы-продуценты DAO |
До индукции |
После индукции |
До индукции |
После индукции |
|
| BL21(DE3)/pETTvDAO1 |
1,5 |
1,4 |
4 |
10 |
5 |
| BL21(DE3)/pETTvDAO2 |
1,6 |
1,8 |
5 |
12 |
6 |
| BL21(DE3)/pETTvDAO1/pLysS |
1,5 |
2,5 |
3 |
15 |
10 |
| BL21(DE3)/pETTvDAO2/pLysS |
1,7 |
3,5 |
2 |
17 |
12 |
| С41(DE3)/pETTvDAO1 |
1,6 |
5,4 |
2 |
19 |
20 |
| С41(DE3)/pETTvDAO2 |
1,7 |
7,2 |
1 |
23 |
25 |
| DH5a(pCDAAO20 [6] |
1,0 |
Н.о. |
Н.о. |
10,6 |
15,6 |
На основании полученных данных был сделан вывод о том, что наилучший результат как в плане накопления биомассы, так и в плане выхода активного фермента дает использование в качестве реципиента штамма C41(DE3), а в качестве вектора – плазмиды pETTvDAO2. Кроме того, было установлено, что клетки штамма C41(DE3), трансформированные экспрессирующим вектором pETTvDAO2, отличаются и наиболее высокой стабильностью при хранении.
Соответственно, для получения рекомбинантного штамма-продуцента TvDAO был отобран один из клонов, полученный в результате трансформации штамма E.coli C41(DE3) плазмидой pETTvDAO2.
Пример 7. Характеристика рекомбинантного штамма E.coli C41(DE3)/pETTvDAO2
Морфологические признаки
Клетки имеют продолговатую палочковидную форму, при делении не почкуются.
Культуральные признаки
Клетки хорошо растут на обычно используемых питательных средах. Время генерации составляет около 60 мин в жидкой LB-среде. На 2-2,5% питательном агаре “Difco” образуются круглые, гладкие, желтоватые колонии с ровными краями. При выращивании на жидких LB- и YT-средах образуется интенсивная ровная мутность.
Физиолого-биохимические признаки
Оптимальная температура культивирования – от 25 до 30°C, оптимум рН 7,6. Источником азота служат органические соединения (в виде триптона, дрожжевого экстракта).
Выход рекомбинантной TvDAO (по результатам определения активности в образцах биомассы штамма-продуцента, проведенного с учетом установленной ранее величины удельной активности TvDAO [6]) составляет около 150 мг/л при титре культуры 1×109 кл/мл.
Сопоставление полученного результата с данными, известными из литературы, позволяет заключить, что уровень продукции рекомбинантной TvDAO в штамме E.coli C41(DE3)/pETTvDAO2 в среднем в 1,5 раза превышает продуктивность известных штаммов-аналогов [3-6].
| Таблица 2 |
| Динамика накопления рекомбинантной DAO при культивировании различных штаммов E.coli – продуцентов |
| |
Рост культуры, ОП550 |
Уд. активность DAO, ед/мг белка |
Выход DAO, ед/мл |
| Штаммы-продуценты DAO |
До индукции |
После индукции |
До индукции |
После индукции |
|
| BL21(DE3)/pETTvDAO1 |
1,5 |
1,4 |
4 |
10 |
5 |
| BL21(DE3)/pETTvDAO2 |
1,6 |
1,8 |
5 |
12 |
6 |
| BL21(DE3)/pETTvDAO1/pLysS |
1,5 |
2,5 |
3 |
15 |
10 |
| BL21(DE3)/pETTvDAO2/pLysS |
1,7 |
3,5 |
2 |
17 |
12 |
| С41(DE3)/pETTvDAO1 |
1,6 |
5,4 |
2 |
19 |
20 |
| С41(DE3)/pETTvDAO2 |
1,7 |
7,2 |
1 |
23 |
25 |
| DH5a(pCDAAO20 [6] |
1,0 |
Н.о. |
Н.о. |
10,6 |
15,6 |
Список литературы.
1) Parmar A, Kumar H, Marwaha SS, Kennedy JF. 1998. Recent Trends in Enzymatic Conversion of Cephalosporin C to 7-Aminocephalosporanic Acid (7-ACA). Critical Reviews in Biotechnology 18:1-12.
2) Barber MS, Giesecke U, Reichert A, Minas W. 2004. Industrial enzymatic production of cephalosporin-based beta-lactams. Adv. Biochem. Eng Biotechnol. 88:179-215.
3) Pollegioni L, Caldinelli L, Molla G, Sacchi S, Pilone MS. 2004. Catalytic properties of D-amino acid oxidase in cephalosporin C bioconversion: a comparison between proteins from different sources. Biotechnol. Prog. 20:467-73.
4) Lin L, Chien HR, Wang W, Hwang T, Fu H, Hsu W. 2000. Expression of Trigonopsis variabilis D-amino acid oxidase gene in Escherichia coli and characterization of its inactive mutants. Enzyme Microb. Technol. 27:482-91.
5) Molla G, Vegezzi C, Pilone MS, Pollegioni L. 1998. Overexpression in Escherichia coli of a recombinant chimeric Rhodotorula gracilis d-amino acid oxidase. Protein Expr. Purif. 14:289-94.
6) Alonso J, Barredo JL, Diez B, Mellado E, Salto F, Garcia JL, Cortes E. 1998. D-amino-acid oxidase gene from Rhodotorula gracilis (Rhodosporidium toruloides) ATCC 26217. Microbiology 144 (Pt 4):1095-101.
7) Garcia Lopez et AL. Enzymatic process for the preparation of cephalosporanic 7$B(G)-(4-Carboxybutanamide) acid by means of the modified enzyme D-aminoacid oxidase of trigonopsis variabilis produced in escherichia coli. Патент США 6,635,458, 21 октября 2003 года.
8) Zheng H, Wang X, Chen J, Zhu K, Zhao Y, Yang Y, Yang S, Jiang W. 2005. Expression, purification, and immobilization of His-tagged D: -amino acid oxidase of Trigonopsis variabilis in Pichia pastoris. Appl. Microbiol. Biotechnol. 1-7.
9) Isoai A, Kimura H, Reichert A, Schorgendorfer K, Nikaido K, Tohda H, Giga-HamaY, Mutoh N, Kumagai H.2002. Production of D-amino acid oxidase (DAO) of Trigonopsis variabilis in Schizosaccharomyces pombe and the characterization of biocatalysts prepared with recombinant cells. Biotechnol Bioeng. 80(1):22-32.
10) Тишков В.И., Хороненкова С.В. 2005. ОКСИДАЗА DАМИНОКИСЛОТ: СТРУКТУРА, МЕХАНИЗМ ДЕЙСТВИЯ И ПРАКТИЧЕСКОЕ ПРИМЕНЕНИЕ. Биохимия, 70:51-67.
11) Novagene Inc. Product catalogue. (1999), pET System Manual. 11th Edition.
12) Dumon-Seignovert L., Cariot G., and Vuillard L. (2004). The toxicity of recombinant proteins in Escherichia coli: a comparison of overexpression in BL21(DE3), C41(DE3), and C43(DE3). Protein Expr. Purif. 37, 203-206.
13) Vethanayagam J, Flower A. 2005. Decreased gene expression from T7 promoters may be due to impaired production of active T7 RNA polymerase. Microbial Cell Factories 4:3.
14) Miroux B. and Walker J.E. (1996). Over-production of proteins in Escherichia coli: mutant hosts that allow synthesis of some membrane proteins and globular proteins at high levels. J Mol. Biol. 260, 289-298.
15) Ausubel FM. 1988. Current protocols in molecular biology.
16) Sambrook J, Maniatis T, Fritsch EF. 1989. Molecular cloning a laboratory manual Cold Spring Harbor, N.Y: Cold Spring Harbor Laboratory.
17) Khang YH, Kim IW, Hah YR, Hwangbo JH, Kang KK.(2003) Fusion protein of Vitreoscilla hemoglobin with D-amino acid oxidase enhancesactivity and stability of biocatalyst in the bioconversion process of cephalosporin C. Biotechnol Bioeng., 82(4), 480-8.
18) Reece, K.S., and G.J. Phillips. 1995. New plasmids carrying antibiotic resistance cassettes. Gene 165:141-142.





Формула изобретения
1. Рекомбинантная плазмида pETTvDAO2, обеспечивающая синтез оксидазы D-аминокислот Trigonopsis variabilis (TvDAO) в клетках Escherichia coli, которая состоит из кодирующего TvDAO фрагмента ДНК с нуклеотидной последовательностью SEQ ID №6 и NcoI/XhoI фрагмента размером 7,15 т.п. н плазмиды pET-TetI, полученной путем замены гена бета-лактамазы в векторе рЕТ21 геном устойчивости к тетрациклину (TetR) в обратной ориентации.
2. Рекомбинантный штамм Escherichia coli C41(DE3)/pETTvDAO2 – продуцент оксидазы D-аминокислот.
РИСУНКИ
|
|