|
|
(21), (22) Заявка: 2006113904/04, 24.04.2006
(24) Дата начала отсчета срока действия патента:
24.04.2006
(46) Опубликовано: 20.11.2007
(56) Список документов, цитированных в отчете о
поиске:
HSIU-PU DANIEL LEE ET AL. «Synthesis of deuterated methylenecyclohexanes, methylenedecalins and taraxasterols». Journal of Labelled Compounds and Radiopharmaceuticals, 1983, 20(12), 1395-1405. PAI P.P. ET AL. «Oxidation studies on taraxasterol, taraxasteryl acetate and taraxasterone», Indian Journal of Chemistry, Section B: Organic Chemistry
Адрес для переписки:
450075, РБ, г.Уфа, пр-кт Октября, 141, ИНК РАН, патентная группа
|
(72) Автор(ы):
Ахметова Внира Рахимовна (RU),
Шакурова Эльвира Рифовна (RU),
Халилова Алия Зуфаровна (RU),
Халилов Леонард Мухибович (RU)
(73) Патентообладатель(и):
Институт нефтехимии и катализа РАН (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ 3БЕТА-АЦЕТОКСИ-20-ОКСОНОРТАРАКСАСТ-21-ЕНА
(57) Реферат:
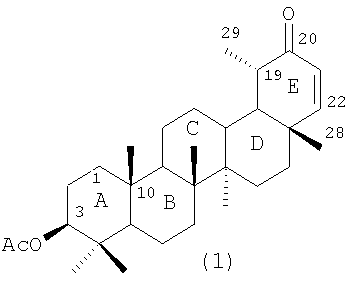
Изобретение относится к области органического синтеза, а именно к способу получения 3 -ацетокси-20-оксонортараксаст-21-ена формулы (1), который может найти применение в качестве противоопухолевого и противовоспалительного средства. Сущность способа заключается во взаимодействии 3 -ацетокси-20-оксонортараксаст-21-ена формулы (1), который может найти применение в качестве противоопухолевого и противовоспалительного средства. Сущность способа заключается во взаимодействии 3 -ацетокси-20-метилентараксастана с избытком озона в растворе хлороформа при комнатной температуре и перемешивании с последующим восстановлением перекисных продуктов озонирования Ме2S в течение 24 часов при перемешивании. Процесс ведут при мольном соотношении 3 -ацетокси-20-метилентараксастана с избытком озона в растворе хлороформа при комнатной температуре и перемешивании с последующим восстановлением перекисных продуктов озонирования Ме2S в течение 24 часов при перемешивании. Процесс ведут при мольном соотношении 3 -ацетокси-20-метилентараксастан:озон, равном 1:1.5 Выход целевого продукта составляет 93%. Технический результат – селективное получение соединения формулы (1) с высоким выходом. -ацетокси-20-метилентараксастан:озон, равном 1:1.5 Выход целевого продукта составляет 93%. Технический результат – селективное получение соединения формулы (1) с высоким выходом.
(56) (продолжение):
CLASS=”b560m”Including Medicinal Chemistry, 1977, 15B(12), 1134-1136. BARRERO A.F. ET AL. «A convenient synthesis of a ring functionalized podolactones. Revision of the structure of wentilactone B», Organic Letters, 2002, 4(8), 1379-1382. ALEJANDRO F.B. «First synthesis of the antifungal oldiolactone С from trans-communic acid: cytotoxic and antimicrobial activity in podolactone-related compounds», Journal of Organic Chemistry, 2002, 67(8), 2501-2508.
Предлагаемое изобретение относится к органической химии, в частности к способу получения 3 -ацетокси-20-оксонортараксаст-21-ена, имеющего формулу (1): -ацетокси-20-оксонортараксаст-21-ена, имеющего формулу (1):
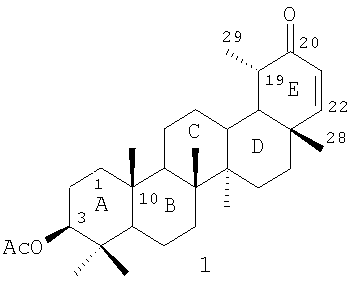
Пентациклические тритерпеноиды тараксастанового ряда могут найти применение в фармакологической промышленности в качестве потенциальных антибиотических препаратов, подавляющих развитие грамм-положительных бактерий (Bacillus subtilis, Escherichia coli, Pseudomonas purida), а также в качестве средств противоопухолевой и противовоспалительной активности.
Известен способ (Pai P.P., Kulkarni G.H. Oxidation studies on taraxasterol, taraxasteryl acetate and taraxastenone. Indian J.Chem. 1977. 15B. p.1134-1136) получения 20-оксопроизводных тараксастерилацетата, в частности 3 -ацетокси-20-оксонортараксастана (2) и 20-альдегидотараксастерилацетата (3) взаимодействием 3 -ацетокси-20-оксонортараксастана (2) и 20-альдегидотараксастерилацетата (3) взаимодействием 3 -ацетокси-20-метилентараксастана (тараксастерилацетат) (4) с реагентом Джонса по схеме: -ацетокси-20-метилентараксастана (тараксастерилацетат) (4) с реагентом Джонса по схеме:
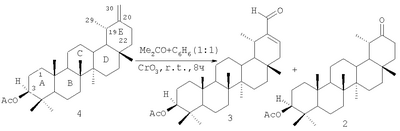
Известный способ не позволяет получать 3 -ацетокси-20-оксонортараксаст-21-ен (1) и приводит к смеси продуктов реакции 2 и 3. -ацетокси-20-оксонортараксаст-21-ен (1) и приводит к смеси продуктов реакции 2 и 3.
Известен способ (Pai P.P., Kulkarni G.H. Oxidation studies on taraxasterol, taraxasteryl acetate and taraxastenone. Indian J. Chem. 1977. 15B. p.1134-1136) получения 20-оксопроизводных нортараксастерилацетата, в частности 3 -ацетокси-20-оксонортараксастана (2) и 3 -ацетокси-20-оксонортараксастана (2) и 3 -ацетокси-20-гидрокситараксастерил-ацетата (5) взаимодействием 3 -ацетокси-20-гидрокситараксастерил-ацетата (5) взаимодействием 3 -ацетокси-20-метилентараксастана (4) с m-хлорпербензойной кислотой (m-CPBA) по схеме: -ацетокси-20-метилентараксастана (4) с m-хлорпербензойной кислотой (m-CPBA) по схеме:
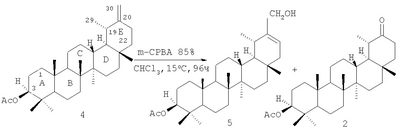
Известный способ не позволяет получать 3 -ацетокси-20-оксонортараксаст-21-ен (1) и приводит к смеси продуктов реакции 2 и 5. -ацетокси-20-оксонортараксаст-21-ен (1) и приводит к смеси продуктов реакции 2 и 5.
Предлагается новый способ синтеза 3 -ацетокси-20-оксонортараксаст-21-ена (1). -ацетокси-20-оксонортараксаст-21-ена (1).
Предлагаемый способ синтеза 3 -ацетокси-20-оксонортараксаст-21-ена (1) заключается во взаимодействии 3 -ацетокси-20-оксонортараксаст-21-ена (1) заключается во взаимодействии 3 -ацетокси-20-метилентараксастана (4) с 1.5 мольным избытком озона в присутствии хлороформа, при комнатной температуре и перемешивании. Образуется селективно 3 -ацетокси-20-метилентараксастана (4) с 1.5 мольным избытком озона в присутствии хлороформа, при комнатной температуре и перемешивании. Образуется селективно 3 -ацетокси-20-оксонортараксаст-21-ен (1). Реакция протекает по схеме: -ацетокси-20-оксонортараксаст-21-ен (1). Реакция протекает по схеме:
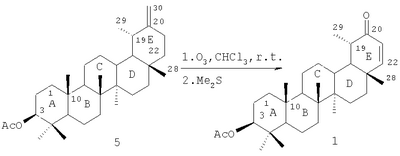
Целевой 3 -ацетокси-20-оксонортараксаст-21-ен(1) селективно образуется только в процессе озонолиза. При использовании других окислительных агентов (реактив Джонса, m-хлорпербензойная кислота) образование 3 -ацетокси-20-оксонортараксаст-21-ен(1) селективно образуется только в процессе озонолиза. При использовании других окислительных агентов (реактив Джонса, m-хлорпербензойная кислота) образование 3 -ацетокси-20-оксонортараксаст-21-ена (1) не происходит. Изменение соотношения исходных реагентов в сторону увеличения концентрации озона по отношению к 3 -ацетокси-20-оксонортараксаст-21-ена (1) не происходит. Изменение соотношения исходных реагентов в сторону увеличения концентрации озона по отношению к 3 -ацетокси-20-метилентараксастану (4) не приводит к существенному повышению выхода целевого 3 -ацетокси-20-метилентараксастану (4) не приводит к существенному повышению выхода целевого 3 -ацетокси-20-оксонортараксаст-21-ена (1). -ацетокси-20-оксонортараксаст-21-ена (1).
Существенные отличия предлагаемого способа:
В предлагаемом способе в качестве окислительного агента используется более дешевый и экологичный окислитель – озон, а в известном способе в качестве окислителя используются реактив Джонса (CrO3-H2SO4) и m-хлорпербензойная кислота (m-CPBA) и образование 3 -ацетокси-20-оксонортараксаст-21-ена (1) не происходит. -ацетокси-20-оксонортараксаст-21-ена (1) не происходит.
Преимущества предлагаемого способа:
Способ позволяет получать с высокой селективностью 3 -ацетокси-20-оксонортараксаст-21-ен (1). Разработанный авторами способ отличается высокой селективностью, простотой проведения эксперимента, сокращением времени эксперимента и применением более дешевого и экологичного окислителя озона, не приводящего к образованию вредных и побочных продуктов. -ацетокси-20-оксонортараксаст-21-ен (1). Разработанный авторами способ отличается высокой селективностью, простотой проведения эксперимента, сокращением времени эксперимента и применением более дешевого и экологичного окислителя озона, не приводящего к образованию вредных и побочных продуктов.
Способ поясняется примерами:
ПРИМЕР 1. Через раствор 0.28 г (0.59 ммоль) 3 -ацетокси-20-метилентараксастана (4) в 5 мл CHCl3 при перемешивании пропускают озоно-кислородную смесь при комнатной температуре (производительность озонатора 9.8 ммоль О3 за 1 ч) до поглощения 1.18 ммоль О3. Образовавшуюся смесь перекисных продуктов озонирования (проба на перекиси в присутствии 2%-ного раствора KJ и 1%-ного раствора крахмала) восстанавливают Me2S (0.88 ммоль) при комнатной температуре в течение 24 ч. Растворитель упаривают в вакууме и получают 0.26 г (93%) 3 -ацетокси-20-метилентараксастана (4) в 5 мл CHCl3 при перемешивании пропускают озоно-кислородную смесь при комнатной температуре (производительность озонатора 9.8 ммоль О3 за 1 ч) до поглощения 1.18 ммоль О3. Образовавшуюся смесь перекисных продуктов озонирования (проба на перекиси в присутствии 2%-ного раствора KJ и 1%-ного раствора крахмала) восстанавливают Me2S (0.88 ммоль) при комнатной температуре в течение 24 ч. Растворитель упаривают в вакууме и получают 0.26 г (93%) 3 -ацетокси-20-оксонортараксаст-21-ена (1) в виде белого кристаллического вещества с т.пл. 218-220°С. -ацетокси-20-оксонортараксаст-21-ена (1) в виде белого кристаллического вещества с т.пл. 218-220°С.
Спектральные характеристики 3 3 -ацетокси-20-оксонортараксаст-21-ена (1) -ацетокси-20-оксонортараксаст-21-ена (1) |
 |
Спектр ЯМР 1Н (CDCl3),  , м.д.: (J, Гц):0.91 с (6Н, Н23 и Н24), 0.86 с, (3Н, Н25), 0.99 c (3H, Н26), 0.96 с (3Н, Н27), 0.94 с (3Н, Н28), 1.08 д (3Н, Н29), 0.92-2.48 м (16Н, 8СН2), 2.05 с (3Н, ОС(О)СН3), 4.49 уш.с (1Н, Н3), 5.61 д (2Н, Н21′, Н21”) и 6.75 д (2Н, Н22′, Н22”). , м.д.: (J, Гц):0.91 с (6Н, Н23 и Н24), 0.86 с, (3Н, Н25), 0.99 c (3H, Н26), 0.96 с (3Н, Н27), 0.94 с (3Н, Н28), 1.08 д (3Н, Н29), 0.92-2.48 м (16Н, 8СН2), 2.05 с (3Н, ОС(О)СН3), 4.49 уш.с (1Н, Н3), 5.61 д (2Н, Н21′, Н21”) и 6.75 д (2Н, Н22′, Н22”). |
Спектр ЯМР 13С (CDCl3),  , м.д.: 80.94 с (С3), 21.17 с (ОС(О)СН3), 171.01 с (ОС=O), 27.82 и16.39 к (С23 и С24), 15.79 и 16.20 к (С25 и С26), 14.98 к (С27), 18.05 к (С28), 26.45 к (С29), 212.92 с (С20), 127.89 д (С21), 166.56 д (С22). , м.д.: 80.94 с (С3), 21.17 с (ОС(О)СН3), 171.01 с (ОС=O), 27.82 и16.39 к (С23 и С24), 15.79 и 16.20 к (С25 и С26), 14.98 к (С27), 18.05 к (С28), 26.45 к (С29), 212.92 с (С20), 127.89 д (С21), 166.56 д (С22). |
 – Спектры ЯМР зарегистрированы на спектрометре “Bruker АМХ-300” (рабочая частота для 1H – 300.13 МГц, 13С – 75 МГц), “Tesia BS-487” (для 1Н – 100 МГц), и на спектрометре “Jeol FX 90Q” (89.55 и 22.50 МГц), внутренний стандарт ТМС, растворитель CDCl3. – Спектры ЯМР зарегистрированы на спектрометре “Bruker АМХ-300” (рабочая частота для 1H – 300.13 МГц, 13С – 75 МГц), “Tesia BS-487” (для 1Н – 100 МГц), и на спектрометре “Jeol FX 90Q” (89.55 и 22.50 МГц), внутренний стандарт ТМС, растворитель CDCl3.
Формула изобретения
Способ получения 3 -ацетокси-20-оксонортараксаст-21-ена, имеющего формулу (1), -ацетокси-20-оксонортараксаст-21-ена, имеющего формулу (1),
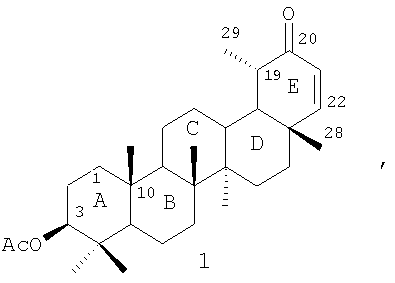
отличающийся тем, что 3 -ацетокси-20-метилентараксастан в растворе хлороформа взаимодействует с избытком озона в мольном соотношении 3 -ацетокси-20-метилентараксастан в растворе хлороформа взаимодействует с избытком озона в мольном соотношении 3 -ацетокси-20-метилентараксастан:озон, равном 1:1,5, при комнатной температуре и перемешивании, с последующим восстановлением перекисных продуктов озонирования Ме2S в течение 24 ч при перемешивании. -ацетокси-20-метилентараксастан:озон, равном 1:1,5, при комнатной температуре и перемешивании, с последующим восстановлением перекисных продуктов озонирования Ме2S в течение 24 ч при перемешивании.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 25.04.2008
Извещение опубликовано: 10.06.2010 БИ: 16/2010
|
|

 -ацетокси-20-оксонортараксаст-21-ена формулы (1), который может найти применение в качестве противоопухолевого и противовоспалительного средства. Сущность способа заключается во взаимодействии 3
-ацетокси-20-оксонортараксаст-21-ена формулы (1), который может найти применение в качестве противоопухолевого и противовоспалительного средства. Сущность способа заключается во взаимодействии 3




 3
3 , м.д.: (J, Гц):0.91 с (6Н, Н23 и Н24), 0.86 с, (3Н, Н25), 0.99 c (3H, Н26), 0.96 с (3Н, Н27), 0.94 с (3Н, Н28), 1.08 д (3Н, Н29), 0.92-2.48 м (16Н, 8СН2), 2.05 с (3Н, ОС(О)СН3), 4.49 уш.с (1Н, Н3), 5.61 д (2Н, Н21′, Н21”) и 6.75 д (2Н, Н22′, Н22”).
, м.д.: (J, Гц):0.91 с (6Н, Н23 и Н24), 0.86 с, (3Н, Н25), 0.99 c (3H, Н26), 0.96 с (3Н, Н27), 0.94 с (3Н, Н28), 1.08 д (3Н, Н29), 0.92-2.48 м (16Н, 8СН2), 2.05 с (3Н, ОС(О)СН3), 4.49 уш.с (1Н, Н3), 5.61 д (2Н, Н21′, Н21”) и 6.75 д (2Н, Н22′, Н22”).