Патент на изобретение №2310653
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-МЕТИЛ-5-(5-МЕТИЛ-2-ФУРИЛ)-4,10-ДИГИДРО-3H-ПИРИДАЗИНО[1,6-b]ИЗОХИНОЛИН-10-ОНА (ВАРИАНТЫ)
(57) Реферат:
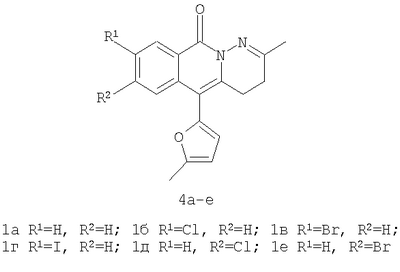
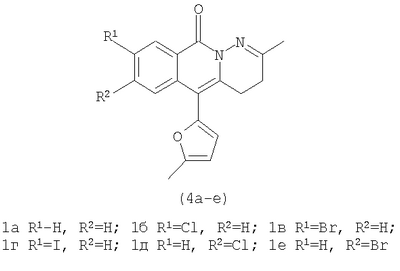
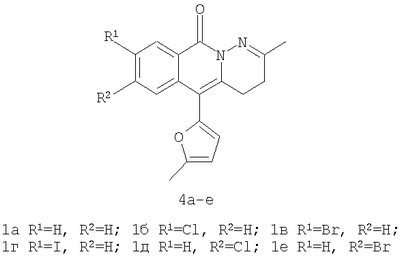
Изобретение относится к области органической химии – способу синтеза новых производных пиридазино[1,6-b]изохинолонов общей формулы 4а-е, представляющих интерес как вещества, обладающие потенциальной биологической активностью. Синтез осуществляется двумя вариантами. Первый вариант включает последовательность из трех химических реакций: а) алкилирование производных 2-ди(5-метил-2-фурил)метил-бензойной кислоты метил йодидом с образованием соответствующих сложных эфиров; б) гидразинолиз сложных эфиров с образованием соответствующих гидразидов; в) кислотно-катализируемая рециклизация гидразидов в производные пиридазино[1,6-b]изохинолона 4а-е. Второй вариант включает химическое превращение производных 4-(5-метил-2-фурил)-3-оксобутилизохромен-1-она в производные пиридазино[1,6-b]изохинолона 4а-е путем добавления гидразин гидрата при комнатной температуре в раствор соответствующего производного 4-(5-метил-2-фурил)-3-оксобутилизохромен-1-она в этиленгликоле с последующим кипячением полученной реакционной смеси. 2 н.п. ф-лы, 1 табл.
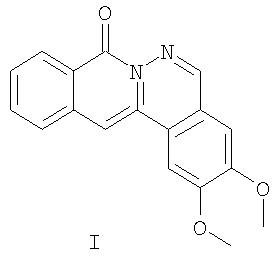
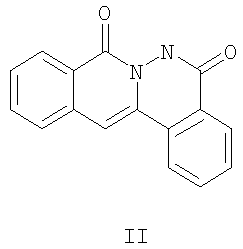
Изобретение относится к области органической химии – способу синтеза производных пиридазино[1,6-b]изохинолонов общей формулы 4а-е. Структура пиридазино[1,6-b]изохинолона общей формулы 4а-е имеет ряд фармакофорных составляющих: конденсированная гетероциклическая система, два атома азота со свободными электронными парами, конформационнофиксированная по отношению к цепочке двух атомов азота карбонильная группа, фурильный заместитель. Поэтому пиридазино[1,6-b]изохинолоны 4а-е рассматриваются как потенциальные биологически активные вещества. Вещества, содержащие в своей структуре пиридазино[1,6-b]изохинолиноновую систему, практически не изучены. В литературе имеется лишь два примера подобных веществ – I [S.Veeraraghavan, F.D.Popp, J.Heterocycl Chem, 1981, 18, 71] и II [Dusemund J., Archiv der Pharmazie, 1982, 315 (11), 925].
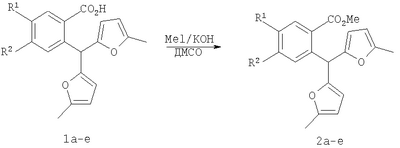
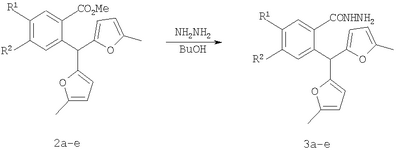
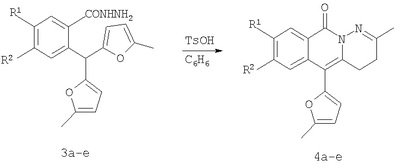
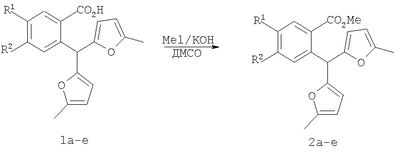
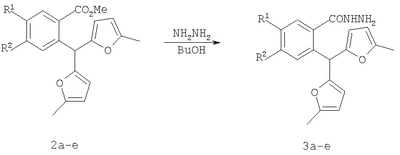
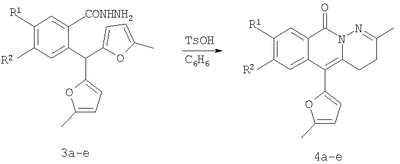
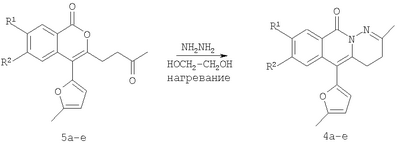
Вероятно, это связано с отсутствием приемлемых методов синтеза веществ этого класса. Известны способы синтеза различных бензанелированных гетероциклических IV систем на основе реакции рециклизации орто-функционализированных бензилфуранов III [В.Т.Абаев, А.В.Гутнов, А.В.Бутин, Химия гетероциклич. соедин., 1998, 603; А.V.Butin, Т.A.Stroganova, I.V.Lodina and G.D.Krapivin, Tetrahedron Lett., 2001, 42, 2031; В.Т.Абаев, А.А.Осипова, А.В.Бутин, Химия гетероциклич. соедин., 2001, 849; А.V.Gutnov, V.T.Abaev, A.V.Butin and A.S.Dmitriev, J. Org. Chem., 2001, 66, 8685; А.V.Butin, V.Т.Abaev, V.V.Mel Использование этой стратегия лежит в основе заявляемого способа синтеза производных пиридазино[1,6-b]изохинолона общей формулы 4а-е. Техническим результатом является синтез ранее недоступных производных пиридазино[1,6-b]изохинолона 4а-е для расширения арсенала веществ, обладающих потенциальной биологической активностью. Технический результат достигается реализацией любого из двух вариантов синтеза производных пиридазино[1,6-b]изохинолона 4а-е. Первый вариант включает последовательность из трех реакций. а) Алкилирование производных 2-ди(5-метил-2-фурил)метилбензойной кислоты 1а-е метил йодидом с образованием соответствующих сложных эфиров 2а-е при комнатной температуре в сухом диметилсульфоксиде при избытке метил йодида в присутствии гидроксида калия. б) Гидразинолиз сложных эфиров 2а-е с образованием соответствующих гидразидов 3а-е путем взаимодействия сложных эфиров общей формулы 2а-е с гидразином. в) Кислотно-катализируемая рециклизация гидразидов 3а-е в производные пиридазино[1,6-b]изохинолона 4а-е путем кипячения исходных гидразидов 3а-е в безводном растворе толуолсульфокислоты в бензоле. Второй вариант включает химическое превращение кетонов 5а-е, получаемых по известному методу из бензойных кислот 1a-e [V.T.Abaev, A.S.Dmitriev, A.V.Gutnov, S.A.Podelyakin, A.V.Butin, Journal of Heterocyclic Chemistry, 2006, 43, №4], в производные пиридазино[1,6-b]изохинолона 4а-е. Реакция осуществляется путем добавления гидразин гидрата при комнатной температуре в раствор соответствующего кетона 5а-е в этиленгликоле с последующим кипячением полученной реакционной смеси в течение 10-20 минут. Индивидуальность и строение синтезированных соединений 4а-е подтверждены данными ПМР спектроскопии и элементного анализа. Пример осуществления заявляемого способа синтеза производных 2-метил-5-(5-метил-2-фурил)-4,10-дигидро-3H-пиридазино[1,6-b]изохинолин-10-она 4а-е по первому варианту. Метил 2-ди(5-метил-2-фурил)метилбензоат (2а) К суспензии 2 г растертого в порошок гидроксида калия в 40 мл сухого диметилсульфоксида добавляют 2 г (6,76 ммоль) 2-ди(5-метил-2-фурил)метилбензойной кислоты, 2 см3 (12,12 ммоль) йодистого метила и перемешивают при комнатной температуре 20 минут. Затем суспензию отфильтровывают от гидроксида калия. Полученный раствор выливают в 500 см3 воды, рН эмульсии доводят до 5-6 разбавленным раствором соляной кислоты и экстрагируют несколько раз хлористым метиленом. Экстракт промывают водой, сушат над сульфатом натрия, добавляют петролейный эфир и чистят методом флэш-хроматографии на силикагеле. Очищенный раствор упаривают до 10-20 мл и оставляют кристаллизоваться при температуре ниже 0°С. Выход соединения 2а 1,8 г (86%). Тпл.=57-58°С. Найдено для С19H18О4, %: С 73.58; Н 5.81. Вычислено: С 73.53; Н 5.85. ПМР спектр (250 МГц, CDCl3): 2,24 (с, 6Н, СН3); 3,86 (с, 3Н, ОСН3); 5,83 (д, 2Н, J=3,3, 4-HFur); 5,86 (д, 2Н, J=3,3, 3-НFur); 6,52 (с, 1Н, СН); 7,27-7,34 (м, 2Н, НAr); 7,42-7,48 (м, 1Н, НAr); 7,89-7,92 (м, 1Н, НAr). 2-Ди(5-метил-2-фурил)метил-1-бензолкарбогидразид (3а) Смесь 1,8 г (5,81 ммоль) метил 2-ди(5-метил-2-фурил)метилбензоата, 9 мл бутанола и 9 мл гидразин гидрата кипятят 20 мин. Раствор выливают в 300 см3 воды. Выпавший осадок отфильтровывают и без очистки используют для дальнейших превращений. Выход технически чистого соединения 1,3 г (72%). 2-Метил-5-(5-метил-2-фурил)-4,10-дигидро-3H-пиридазино[1,6-b]изохинолин-10-он (4а) Смесь 1,3 г (4,19 ммоль) 2-ди(5-метил-2-фурил)метил-1-бензолкарбогидразида (2а) и 20 см3 15% раствора толуолсульфокислоты в бензоле кипят 10 минут. Полученный раствор выливают в 300 см3 воды. Взвесь экстрагируют несколько раз хлористым метиленом. Экстракт промывают водой и упаривают досуха. Целевой продукт выделяют из смеси методом колоночной хроматографии на силикагеле, в качестве элюента используют смесь этил ацетата и петролейного эфира в соотношении 1:4 по объему. Продукт кристаллизуют из смеси хлористого метилена и петролейного эфира при температуре ниже 0°С. Выход соединения 4а 0,5 г (41%). Тпл.=186-187°С. Найдено для C18H16N2O2, %: С 73.92; Н 5.56; N 9.57. Вычислено: С 73.96; Н 5.52; N9.58. ПМР спектр (300 МГц, CDCl3): 2,32 (с, 3Н, СН3); 2,32 (т, 2Н, J=7,6, СН2); 2,38 (с, 3Н, СН3); 2,85 (т, 2Н, J=7,6, СН2); 6,14 (д, 1Н, J=2,9, 4-HFur); 6,30 (д, 1Н, J=2,9, 3-Hfur); 7,36-7,39 (м, 1Н, НAr); 7,41-7,46 (м, 1Н, НAr); 7,55-7,60 (м, 1Н, НAr); 8,53-8,56 (м, 1Н, НAr). Пример осуществления заявляемого способа синтеза производных 2-метил-5-(5-метил-2-фурил)-4,10-дигидро-3H-пиридазино[1,6-b]изохинолин-10-она 4а-е по второму варианту 2-Метил-5-(5-мстил-2-фурил)-4,10-дигидро-3H-пиридазино[1,6-b]изохинолин-10-он (4а) Смесь 1 г (3,37 ммоль) 4-(5-метил-2-фурил)-3-оксобутилизохромен-1-она 5а, 50 мл этиленгликоля и 1 см3 гидразин гидрата перемешивают до полного расходования исходного вещества (20-30 минут, контроль методом тонкослойной хроматографии). Полученный раствор кипятят 10-15 минут с обратным холодильником. Реакционную смесь выливают в воду и экстрагируют хлористым метиленом. Экстракт промывают водой, сушат над сульфатом натрия и упаривают. Остаток чистят методом флэш-хроматографии на силикагеле (элюент – смесь этилацетата и петролейного эфира в соотношении 1:3 по объему). Очищенный раствор упаривают до 10-20 мл и оставляют кристаллизоваться при температуре ниже 0°С. Выход 0,7 г (69%). Заявляемыми вариантами получен ряд производных пиридазино[1,6-b]изохинолона 4б-е, выходы, температуры плавления и спектральные характеристики которых приведены в таблице 1. Физико-химические характеристики веществ 4а-е, полученных первым вариантом совпадают с аналогичными характеристиками веществ 4а-е, полученных вторым вариантом.
Формула изобретения
1. Способ синтеза гетероциклических соединений – производных пиридазино[1,6-b]изохинолона общей формулы 4а-е, включающий последовательность трех реакций: а) алкилирование производных 2-ди(5-метил-2-фурил)метилбензойной кислоты 1а-е метил йодидом с образованием соответствующих сложных эфиров 2а-е при комнатной температуре в сухом димстилсульфоксиде при избытке метил йодида в присутствии гидроксида калия, б) гидразинолиз сложных эфиров 2а-е с образованием соответствующих гидразидов 3а-е путем взаимодействия сложных эфиров общей формулы 2а-е с гидразином, в) кислотно-катализируемая рециклизация гидразидов 3а-е в производные пиридазино[1,6-b]изохинолонов 4а-е путем кипячения исходных гидразидов 3а-е в безводном растворе толуолсульфокислоты в бензоле. 2. Способ синтеза производных пиридазино[1,6-b]изохинолона общей формулы 4а-е включающий превращение кетонов 5а-е в производные пиридазино[1,6-b]изохинолона 4а-е путем добавления гидразин гидрата при комнатной температуре в раствор соответствующего кетона 5а-е в этиленгликоле с последующим кипячением полученной реакционной смеси в течение 10-20 мин.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 18.07.2008
Извещение опубликовано: 10.07.2010 БИ: 19/2010
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 chin and A.S.Dmitriev, Tetrahedron Lett., 2005, 46, 8439].
chin and A.S.Dmitriev, Tetrahedron Lett., 2005, 46, 8439].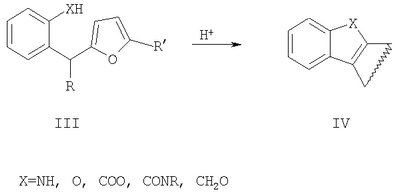
 (м.д.), КССВ (J, Гц)
(м.д.), КССВ (J, Гц)