|
|
(21), (22) Заявка: 2005117371/04, 03.11.2003
(24) Дата начала отсчета срока действия патента:
03.11.2003
(30) Конвенционный приоритет:
07.11.2002 IN 628/CAL/2002
(43) Дата публикации заявки: 20.01.2006
(46) Опубликовано: 20.11.2007
(56) Список документов, цитированных в отчете о
поиске:
JP 2000-026378 A1, 25.01.2000. WO 00/32551 А1, 08.06.2000. WO 01/47498 A2, 05.07.2001. WO 98/13335 A1, 08.06.2000. RU 2181358 C2, 20.04.2002. RU 2181287 C2, 20.04.2002.
(85) Дата перевода заявки PCT на национальную фазу:
07.06.2005
(86) Заявка PCT:
IB 03/04998 (03.11.2003)
(87) Публикация PCT:
WO 2004/041773 (21.05.2004)
Адрес для переписки:
129010, Москва, ул. Б.Спасская, 25, стр.3, ООО “Юридическая фирма Городисский и Партнеры”, пат.пов. Е.Е.Назиной, рег. № 517
|
(72) Автор(ы):
НАДКАРНИ Сунил Садананд (IN)
(73) Патентообладатель(и):
ТОРРЕНТ ФАРМАСЬЮТИКАЛЗ ЛТД (IN)
|
(54) СПОСОБ ПОЛУЧЕНИЯ ПОЛИМОРФНОЙ ФОРМЫ ГИДРОХЛОРИДА СЕРТРАЛИНА
(57) Реферат:
Изобретение относится к улучшенному способу получения формы V гидрохлорида сертралина, который обладает антидепрессивным действием. Способ включает стадии: а) растворение или суспендирование сертралин манделата в протонном растворителе или в смеси протонных растворителей; b) понижение рН раствора или суспензии добавлением водного раствора HCl или HCl в протонном растворителе с добавлением воды с образованием прозрачного раствора и с) выделение формы V гидрохлорида сертралина. В качестве протонного растворителя(ей), на стадии (а), как правило, выбираются растворители из группы, включающей спирт, воду или их смеси. Например, спиртовый растворитель, используемый на стадии (а), может быть выбран из группы, включающей метанол, этанол, н-пропиловый спирт, изопропиловый спирт, н-бутиловый спирт, трет-бутиловый спирт и изобутиловый спирт или их смеси. Предпочтителен изопропиловый спирт. При этом стадию (а) – растворения или суспендирования – осуществляют при нагревании и/или перемешивании в растворителе, как правило, при температуре в интервале от 20 до 90°С. Понижение рН на стадии (b) обычно осуществляют до интервала 1-3, предпочтительно 1-2. Выделение формы V гидрохлорида сертралина на стадии (с) осуществляют охлаждением содержимого стадии (b). При этом охлаждение осуществляют, давая возможность раствору самостоятельно достигнуть комнатной температуры или с помощью мягких охладителей, включающих холодную воду, воду, спирт или их смеси, где указанный спирт выбирают из группы, включающей одноатомные спирты, двухатомные спирты или их смеси. Изобретение также относится к способу получения фармацевтической композиции немедленного высвобождения из формы V гидрохлорида сертралина, включающий смешивание формы V гидрохлорида сертралина, полученного по п.1, с размером частиц меньше 20 мкм, составляющих не менее 90% частиц, с фармацевтически приемлемым разбавителем, носителем или эксципиентом. Предлагаемый способ позволяет упростить процесс получения за счет снижения общего количества стадий. 2 н. и 12 з.п. ф-лы, 2 ил., 1 табл.
Область изобретения
Изобретение относится к способу получения полиморфной формы V гидрохлорида (1S-цис)-4-(3,4-дихлорфенил)-1,2,3,4-тетрагидро-N-метил-1-нафталинамина, т.е. гидрохлорида сертралина. Гидрохлорид сертралина является средством для лечения депрессии, обсессивно-компульсивных нарушений и панических состояний (WO 00/32551).
Описание предшествующего уровня техники
Потребность в лекарствах, лишенных вредных и ограничивающих побочные эффекты от трициклических антидепрессантов, стимулирует поиск средств с повышенной избирательностью по отношению к специфическим механизмам действия, которые, как считается, являются существенными для антидепрессантной эффективности. Исследователи поставили своей целью найти селективные конкурентные ингибиторы повторного синаптосомального поглощения серотонина, и этот поиск привел к серии 1-метиламин-4-арилтетралинов, среди которых наиболее перспективным оказался аналог 4-(3,4-дихлорфенила). Испытание всех возможных стереоизомеров показало, что требуемая высокая селективность по серотонину проявляется у цис-1S,4S-изомера, т.е. гидрохлорида (1S-цис)-4-(3,4-дихлорфенил)-1,2,3,4-тетрагидро-N-метил-1-нафталинамина (I), известного как гидрохлорид сертралина
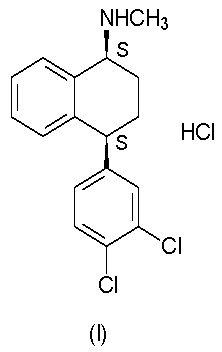
В литературе описаны различные полиморфные формы гидрохлорида сертралина. В свете современных потребностей фармацевтической промышленности очень важна полиморфная форма V (WO 00/32551). Следовательно, существует потребность в крупномасштабном производстве полиморфной формы V гидрохлорида сертралина с помощью эффективного и недорогого способа.
«Способ возгонки-конденсации» для получения формы V предложен в патенте США № 5248699. Однако указанный «способ возгонки-конденсации» не пригоден для применения в промышленном масштабе с учетом потребности в форме V гидрохлорида сертралина. Это обусловлено в первую очередь тем, что «способ возгонки-конденсации» требует специального оборудования, которое для возгонки исходного вещества должно одновременно включать высокий вакуум и температуру, а для того чтобы собрать продукт возгонки, требуется специальная аппаратура и умение. Более того, сложность задачи усугубляется еще и тем, что согласно WO 0032551 «способ возгонки-конденсации» оказался невоспроизводимым.
WO 0032551 и WO 0172684 для получения формы V гидрохлорида сертралина используют в основном гидрохлорид сертралина (схема 1) или сертралин основание (схема 2).
Схема 1
Сертралин манделат  Сертралин основание Сертралин основание  Сертралин·HCl Сертралин·HCl  Форма V сертралин·HCl Форма V сертралин·HCl
Схема 2
Сертралин манделат  Сертралин основание Сертралин основание  Форма V сертралин·HCl Форма V сертралин·HCl
Далее WO 0132601 раскрывает способы получения формы V сертралина·HCl из сертралина основания. Получение формы V сертралина·HCl, следуя WO 0132601, включает схему 3 или схему 4, как показано ниже:
Схема 3
Сертралин манделат  Сертралин основание Сертралин основание  Сертралин·HCl (Форма CSC 2) Сертралин·HCl (Форма CSC 2)  Форма V сертралин·HCl Форма V сертралин·HCl
Схема 4
Сертралин манделат  Сертралин основание Сертралин основание  Сертралин·HCl Сертралин·HCl  спиртовой сольват сертралина·HCl спиртовой сольват сертралина·HCl  форма V сертралин·HCl форма V сертралин·HCl
Согласно методикам, раскрытым в патентах США 5248699, США 4536518, WO 032551, сертралин основание получают из сертралин манделата в несколько стадий, требующих значительных затрат техники, рабочей силы и для завершения производственного цикла времени. Поэтому указанные способы являются коммерчески дорогостоящими.
Следовательно, существует необходимость в получении полиморфной формы V гидрохлорида сертралина с помощью простого, эффективного и недорогого способа.
Цели изобретения
Первым объектом настоящего изобретения является разработка эффективного и недорогого способа получения солей сертралина.
Вторым объектом настоящего изобретения является разработка эффективного и недорогого способа получения полиморфной формы V гидрохлорида сертралина.

Третьим объектом настоящего изобретения является получение формы V гидрохлорида сертралина, имеющей характеристическую рентгенограмму (XRPD).
Четвертым объектом изобретения является получение формы V гидрохлорида сертралина с характерным ИК спектром (ICR).
Пятым объектом изобретения является получение фармацевтической композиции с формой V гидрохлорида сертралина в качестве активного ингредиента.
Сущность изобретения
Настоящее изобретение предлагает способ получения соли сертралина, включающий стадии:
a) растворение или суспендирование сертралин манделата в растворителе;
b) понижение рН раствора или суспензии и
c) выделение соли сертралина.
Настоящее изобретение предлагает также способ получения формы V гидрохлорида сертралина, включающий стадии:
a) растворение или суспендирование сертралин манделата в растворителе;
b) понижение рН раствора или суспензии и
с) выделение формы V гидрохлорида сертралина.
Кроме того, настоящее изобретение предлагает способ получения фармацевтической композиции с формой V гидрохлорида сертралина в качестве активного ингредиента.
Подробное описание изобретения
Гидрохлорид сертралина формулы (I) существует в различных полиморфных формах, в частности, формах I-XVI, T1, CSC-1, CSC-2 и в аморфной форме. Кристаллизацию полиморфных форм обычно проводят путем растворения или плавления соединения с последующим постепенным или быстрым охлаждением полученного раствора или расплава. В растворе различные полиморфные формы идентичны, что следует из данных ЯМР и ИК (спектральные данные в растворе). С другой стороны, твердофазные методы, подобные рентгеновской дифракции или ИК спектроскопии (спектры в KBr), обнаруживают различия между полиморфными формами.
Настоящее изобретение предлагает новый способ получения формы V гидрохлорида сертралина из сертралин манделата.
Согласно настоящему способу, в отличие от способов уровня техники, нет необходимости превращать сертралин манделат в сертралин основание и затем в сертралин гидрохлорид. Многостадийные способы уровня техники, включающие промежуточную стадию превращения сертралин манделата в сертралин основание или сертралин гидрохлорид другой формы, (отличный от формы V) сертралин гидрохлорида, исключаются, поскольку настоящее изобретение обеспечивает непосредственное превращение сертралин манделата в форму V гидрохлорида сертралина. Таким образом, настоящее изобретение предлагает способ получения, который уменьшает число стадий и, следовательно, уменьшает затраты техники, рабочей силы и времени, необходимых для завершения производственного цикла. В результате настоящее изобретение предлагает простой одностадийный способ получения формы V гидрохлорида сертралина, который является эффективным и недорогим.
Способ настоящего изобретения для получения соли сертралина включает стадии:
d) растворение или суспендирование сертралин манделата в растворителе;
e) понижение рН раствора или суспензии и
f) выделение соли сертралина.
Согласно данному изобретению полиморфную форму V гидрохлорида сертралина получают способом, включающим
d) растворение или суспендирование сертралин манделата в растворителе;
e) понижение рН раствора или суспензии и
f) выделение формы V гидрохлорида сертралина.
Растворитель, используемый для растворения или суспендирования сертралин манделата, выбирают из группы, включающей протонные растворители или их смеси.
Растворитель, используемый для растворения или суспендирования сертралин манделата, выбирают из группы, состоящей из спирта, воды и их смесей. Спирты можно выбрать из метанола, этанола, н-пропанола, изопропанола, н-бутилового спирта, трет-бутилового спирта, изобутилового спирта и их смесей. Предпочтительным растворителем является изопропанол.
Растворение или суспендирование достигается путем нагревания и/или перемешивания. Нагревание можно осуществлять до 90°С. Предпочтительно сертралин манделат растворяют при 25-80°С и более предпочтительно при 25-30°С при перемешивании.
Величину рН можно понизить путем использования органических или неорганических кислот. Предпочтительными для понижения рН являются неорганические кислоты, например HCl, H2SO4, HNO3.
HCl применяют в виде газа или растворяют в растворителе. Растворителем может быть вода или органический растворитель или их смеси. Органический растворитель можно выбрать из спиртовых растворителей, например, метанола, этанола, н-пропанола, изопропилового спирта, н-бутанола или их смесей.
Предпочтительно рН понижают с помощью водного HCl.
После снижения рН до 1-3, предпочтительно 1-2, реакционная смесь может иметь вид прозрачного раствора или может оставаться суспензией. Прозрачный раствор необязательно можно получить нагреванием до 90°С.
Охлаждение осуществляют либо давая возможность раствору самостоятельно достигнуть комнатной температуры, либо с помощью мягкого охладителя, содержащего холодную воду, воду, спирты или их смеси. Спирт выбирают из группы, состоящей из одноатомного спирта, двухатомного спирта или их смесей. Затем полученное твердое вещество можно выделить с получением формы V.
Способ настоящего изобретения можно представить схемой 5.
Схема 5
Сертралин манделат  форма V сертралина·HCl форма V сертралина·HCl
Согласно предпочтительному воплощению способа настоящего изобретения сертралин манделат обрабатывают HCl в изопропиловом спирте. Доводят рН до 1-2 и добавляют воду, после чего нагревают реакционную массу до образования прозрачного раствора, который после охлаждения непосредственно дает форму V гидрохлорида сертралина.
Исходное соединение – сертралин манделат – можно получить по методике, описанной в патенте ЕР 30081. Предпочтительным является получение сертралин манделата высокой чистоты, поскольку оно не требует больших затрат времени и труда для повторных кристаллизаций. Согласно настоящему изобретению сертралин манделат получают способом, в котором не требуется очистка повторной кристаллизацией. Также отпадает необходимость получать дополнительную партию вещества, как описано в патенте ЕР 30081.
Фармацевтическая композиция может быть получена с использованием терапевтически эффективного количества полученной таким образом формы V гидрохлорида сертралина и фармацевтически приемлемого носителя.
Краткое описание чертежей
Фиг.1 показывает рентгенограмму соединения, полученного согласно настоящему изобретению;
фиг.2 показывает ИК-спектр соединения, полученного согласно настоящему изобретению. Это характерный спектр инфракрасного поглощения полиморфной формы V гидрохлорида сертралина формулы (I) в KBr.
Полиморфная форма V гидрохлорида сертралина формулы (I) характеризуется следующими данными.
Форма V гидрохлорида сертралина характеризуется порошковой рентгенограммой (XRPD), приведенной ниже в таблице 1:
| Таблица 1 |
| Серийный номер |
Угол дифракции ±0,2°
(два тета градусов) |
Параметр решетки (D)
(Ангстремы) |
| 1 |
5,2 |
17,119 |
| 2 |
10,9 |
8,122 |
| 3 |
14,1 |
6,259 |
| 4 |
16,3 |
5,433 |
| 5 |
17,1 |
5,181 |
| 6 |
19,0 |
4,671 |
| 7 |
19,7 |
4,506 |
| 8 |
20,9 |
4,256 |
| 9 |
22,0 |
4,046 |
| 10 |
23,0 |
3,860 |
| 11 |
23,5 |
3,776 |
| 12 |
25,3 |
3,517 |
| 13 |
25,9 |
3,437 |
| 14 |
29,0 |
3,075 |
Гидрохлорид сертралина, полученный по способу данного изобретения, можно охарактеризовать его порошковой рентгенограммой. Фиг.1 показывает типичную рентгенограмму формы V гидрохлорида сертралина. Основные пики наблюдаются около: 5,2±0,2, 10,9±0,2, 14,1±0,2, 16,3±0,2, 17,1±0,2, 19,0±0,2, 19,7±0,2, 20,9±0,2, 22,0±0,2, 23,0±0,2, 23,5±0,2, 25,3±0,2, 25,9±0,2 и 29,0±0,2 °2 тета.
ИК-спектр формы V гидрохлорида сертралина, полученного способом по изобретению, характеризуется следующими полосами:
773 см-1, 1011 см-1, 1032 см-1, 1054 см-1, 1134 см-1, 1330 см-1, 1561 см-1 и 1591 см-1, как показано на фиг.2.
ИК-фурье спектр был записан в твердом состоянии в виде KBr дисперсии на спектрофотометре Shimadzu FT IR 8700.
Фармацевтическая композиция формы V гидрохлорида сертралина может быть получена с использованием указанного выше химического соединения, удовлетворяющего следующим тестам:
Сер.
№ |
Тесты |
Пределы |
| 1. |
Сопутствующие вещества (%) (по данным ВЭЖХ). Общее количество известных и неизвестных примесей |
Не более 0,50 |
| 2. |
Сульфатированная зола (%) |
Не более 0,2 |
| 3. |
Тяжелые металлы (м.д.) |
Не более 20 |
| 4. |
Анализ (%) (Титрование) |
От 98,0 до 102,0; на
безводной основе |
| 5. |
Остаточный растворитель (м.д.)
(а) Изопропиловый спирт
(b) Метанол
(с) Ацетон
(d) Метиленхлорид |
Не более 2000
Не более 100
Не более 100
Не более 200 |
| 6. |
Полиморф по данным рентгенографии |
Значения 2 тета (D):
5,2 (17,119), 10,9 (8,122), 14,1 (6,259), 16,3 (5,433), 17,1 (5,181), 19,0 (4,671), 19,7 (4,506), 20,9 (4,256), 22,0 (4,046), 23,0 (3,860), 23,5 (3,776), 25,3 (3,517), 25,9 (3,437) и 29,0 (3,075) |
| 7. |
ИК (см-1) |
773, 1011, 1032, 1054, 1134, 1330, 1561 и 1591 |
| 8. |
Размер частиц (по ситовому анализу)
меньше 20 мкм |
Не менее 90,0% |
| 9. |
Предельное содержание микробов
всего аэробов (cfu/g)
(cfu/g – число колониеобразующих единиц на грамм)
Всего грибков (cfu/g)
E.coli |
Не более 1000
Не более 100
Должны отсутствовать |
В следующем разделе описаны предпочтительные воплощения в виде примеров, которые иллюстрируют способ настоящего изобретения. Однако примеры ни в коей мере не ограничивают объем настоящего изобретения.
ПРИМЕРЫ ПОЛУЧЕНИЯ
Получение сертралин манделата
из рацемического гидрохлорида сертралина
В литровую круглодонную колбу помещают 250 мл метиленхлорида, 250 мл воды и 50 г рацемического гидрохлорида сертралина при комнатной температуре. Добавляют 20% раствор гидроксида натрия (10 г раствора гидроксида натрия в 50 мл воды) до установления рН между 9 и 10, как определено по бумажному pH-индикатору. Перемешивают в течение 45 минут до образования прозрачного раствора. Слой метиленхлорида отделяют и водный слой экстрагируют дважды метиленхлоридом (50 мл на каждую экстракцию). Все метиленхлоридные слои объединяют и промывают водой до рН от 7 до 8. Все метиленхлоридные слои собирают и перегоняют в вакууме при 60°С и получают масло. К нему добавляют 200 мл метанола и нагревают до 50-55°С. Добавляют раствор D(-)-миндальной кислоты (23 г в 50 мл метанола) при 55-60°C. Повышают температуру до 60-65°С и выдерживают 10 мин. Через 1 ч массу охлаждают до 30-35°С и затем до 20-25°С, температуру выдерживают на этом уровне 30 мин и получают твердое вещество. Его отфильтровывают и 3 раза промывают ацетоном (по 25 мл каждый раз) и получают 28,0 г сертралин манделата в расчете на сухое вещество.
Получение формы V гидрохлорида сертралина из сертралин манделата
В 1-литровую четырехгорлую круглодонную колбу, снабженную мешалкой, карманом для термометра и водяным холодильником, помещают 25 г сертралин манделата при комнатной температуре. Затем добавляют 200 мл изопропилового спирта при перемешивании. Устанавливают рН раствора от 1 до 2, добавляя концентрированную HCl. Добавляют 5 мл воды и нагревают с обратным холодильником до образования прозрачного раствора. Раствор фильтруют через высокопроточный фильтр и охлаждают до комнатной температуры и получают 23 г белого твердого вещества, которое сушат и получают 13 г сухой формы V.
Фармацевтические композиции
Фармацевтические композиции формы V гидрохлорида сертралина должны предпочтительно иметь размер частиц менее 20 мкм и чистоту не менее 90%, когда готовятся в смеси с фармацевтически приемлемым разбавителем, носителем или эксципиентом. Уровень примесей в гидрохлориде сертралина в такой композиции не должен предпочтительно превышать 0,50% при содержании сульфатированной золы не более 0,2% и тяжелых металлов не более 20 м.д. Предпочтительно гидрохлорид сертралина, используемый в такой композиции, имеет тестовый показатель по титрованию между 98,0 и 102% на безводной основе.
Остаточные растворители в такой композиции предпочтительно находятся в следующих пределах:
| (а) изопропиловый спирт |
не более 2000 м.д. |
| (b) метанол |
не более 100 м.д. |
| (с) ацетон |
не более 100 м.д. |
| (d) метиленхлорид |
не более 200 м.д. |
Пределы по микробам в такой композиции предпочтительно следующие:
| всего аэробов (cfu/g) |
не более 1000 |
| всего грибков (cfu/g) |
не более 100 |
| E.coli |
должны отсутствовать |
В то время как настоящее изобретение было описано исходя из конкретных воплощений, специалистам в данной области будут очевидны возможные модификации и варианты, которые также включены в объем настоящего изобретения.
| Получение фармацевтической композиции немедленного высвобождения формы V гидрохлорида сертралина. |
| |
Ингредиенты |
мг на таблетку (в мг) |
| 1. |
Гидрохлорид сертралина (форма-V) эквивалент 100 г сертралина |
112,00 |
| 2. |
Микрокристаллическая целлюлоза |
44,100 |
| 3. |
Гликолят крахмалнатрия, тип А |
5,000 |
| 4. |
Гидрофосфат кальция, дигидрат |
50,000 |
| 5. |
Гидроксипропилцеллюлоза |
10,500 |
| 6. |
Полисорбат 80 |
7,500 |
| 7. |
Очищенная вода |
дост. количество |
| 8. |
Микрокристаллическая целлюлоза |
58,500 |
| 9. |
Гликолат крахмалнатрия, тип А |
10,000 |
| 10. |
Стеарат магния |
2,40 |
| |
Масса сердцевины: |
300 мг |
| 11. |
Гидромеллоза, 6 санти-Пуассон |
4,120 |
| 12. |
Пропиленгликоль |
0,630 |
| 13. |
Диоксид титана |
1,250 |
| 14. |
Очищенная вода |
дост. количество |
| |
Масса таблетки, покрытой оболочкой: |
306 мг |
Способ получения:
1. Просеивание гидрохлорида сертралина (Форма V), растворителя, агента, вызывающего дезинтеграцию, связующего вещества и необязательно других наполнителей через соответствующее сито и тщательное их перемешивание.
2. Получение водного раствора ПАВ и добавление полученного раствора к смеси, полученной на стадии 1; гранулирование смеси в соответствующем грануляторе.
3. Сушка гранул, полученных на стадии 2, и определение размера высушенных гранул через соответствующее сито.
4. Смешение смеси, полученной на стадии 3, со смазывающим веществом и необязательно другими наполнителями.
5. Прессование смеси, полученной на стадии 4, в таблетку подходящего размера.
6. Нанесение оболочки на прессованную таблетку.
Формула изобретения
1. Способ получения формы V гидрохлорида сертралина, включающий стадии
a) растворение или суспендирование сертралин манделата в протонном растворителе или в смеси протонных растворителей;
b) понижение рН раствора или суспензии добавлением водного раствора HCL или HCL в протонном растворителе с добавлением воды с образованием прозрачного раствора; и
c) выделение формы V гидрохлорида сертралина.
2. Способ по п.1, в котором протонный растворитель(и), используемые на стадии (а), выбраны из группы, включающей спирт, воду или их смеси.
3. Способ по п.2, в котором указанный спиртовый растворитель, используемый на стадии (а), выбран из группы, включающей метанол, этанол, н-пропиловый спирт, изопропиловый спирт, н-бутиловый спирт, трет-бутиловый спирт и изобутиловый спирт или их смеси.
4. Способ по п.3, в котором указанный спиртовый растворитель является изопропиловьм спиртом.
5. Способ по п.1, в котором указанная стадия (а) растворения или суспендирования осуществляется нагреванием и/или перемешиванием.
6. Способ по п.1, в котором указанную стадию (а) растворения или суспендирования сертралин манделата в растворителе осуществляют при температуре в интервале от 20 до 90°С.
7. Способ по п.6, в котором указанный интервал температур составляет от 25 до 80°С.
8. Способ по п.7, в котором указанный интервал температур составляет от 25 до 30°С.
9. Способ по п.1, в котором рН на стадии (b) понижают до интервала 1-3.
10. Способ по п.9, в котором рН понижают до интервала 1-2.
11. Способ по п.1, в котором выделение формы V гидрохлорида сертралина на стадии (с) осуществляют охлаждением содержимого стадии (b).
12. Способ по п.11, в котором охлаждение осуществляют, давая возможность раствору самостоятельно достигнуть комнатной температуры или с помощью мягких охладителей, включающих холодную воду, воду, спирт или их смеси.
13. Способ по п.12, в котором указанный спирт выбирают из группы, включающей одноатомные спирты, двухатомные спирты или их смеси.
14. Способ получения фармацевтической композиции немедленного высвобождения из формы V гидрохлорида сертралина, включающий смешивание формы V гидрохлорида сертралина, полученного по п.1, с размером частиц меньше 20 мкм, составляющих не менее 90% частиц, с фармацевтически приемлемым разбавителем, носителем или эксципиентом.
РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 04.11.2008
Извещение опубликовано: 27.07.2010 БИ: 21/2010
|
|