Патент на изобретение №2309931
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ (АДАМАНТ-1-ИЛМЕТИЛЕН)СОДЕРЖАЩИХ АРОМАТИЧЕСКИХ СОЕДИНЕНИЙ
(57) Реферат:
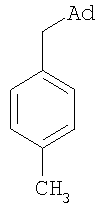
Изобретение относится к химии производных адамантана, а именно к новому способу получения (адамант-1-илметилен)содержащих ароматических соединений общей формулы, приведенной ниже, где R1=R2=R3=R4=H (1); R1=CH3, R2=R3=R4=H (2); R1=R3=R4=H, R2=CH3 (3); R1=R2=R4=H, R3=CH3 (4); R1=R3=H, R2=R4=CH3 (5); R1=R3=R4=CH3, R2=H (6); Ad – 1-адамантил, которые являются полупродуктами для синтеза биологически активных веществ. Сущность изобретения заключается в присоединении к производному адамантана ароматических соединений, причем в качестве производного адамантана используют 1,3-дегидроадамантан, а в качестве ароматических соединений используют соединения из ряда: толуол, о-, м-, п-ксилол, мезитилен, дурол при мольных соотношениях реагентов, равном 1:(2-4) в среде исходного ароматического соединения при их температуре кипения (110-197°С) в течение 60 мин. Техническим результатом является упрощение способа получения вышеопределенных соединений и их получение с высоким выходом.
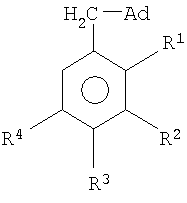
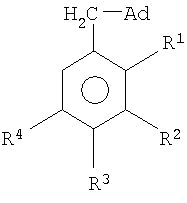
Изобретение относится к химии производных адамантана, а именно к новому способу получения (адамант-1-илметилен)содержащих ароматических соединений общей формулы
где R1=R2=R3=R4=H (1); R1=CH3, R2=R3=R4=H (2); R1=R3=R4=H, R2=CH3 (3); R1=R2=R4=H, R3=CH3 (4); R1=R3=H, R2=R4=CH3 (5); R1=R3=R4=CH3, R2=H (6); Ad – 1-адамантил, которые являются полупродуктами для синтеза биологически активных веществ. Известен способ получения производных адамантансодержащих ароматических соединений, состоящий во взаимодействии галогенпроизводных адамантана и ароматических углеводородов или их производных в присутствии кислот Льюиса (H.Stetter, M.Schwartz, A.Hirschom, Chem.Ber., 92, 1629 (1959). Основным недостатком данного метода являются трудности отделения полученного препарата от катализатора и очистка продукта. Кроме того, хлорид алюминия при попадании воды взрывоопасен. Недостатками данного метода являются многостадийность синтеза и сравнительно низкие выходы (26-86%). Упомянутые выше способы приводят к получению продукта присоединения адамантильного фрагмента к ароматическому кольцу. Существует способ получения адамантилсодержащих ароматических соединений на основе оксипроизводных адамантана в присутствии фосфорного ангидрида с последующим гидрированием на щелочном никеле [Л.А.Зосим, А.Г.Юрченко ЖОрХ, том XVI, вып.4 (1980)]. Недостатками данного метода являются сравнительно низкий выход (60%), приводящий к потерям дорогого сырья, многостадийность процесса. Недостатками данного метода являются сложность и низкая технологичность отдельных стадий, в частности стадии магнийорганического синтеза, представляющей опасность в пожарном отношении и предъявляющей высокие требования к чистоте исходных реагентов. Задачей предлагаемого изобретения является разработка технологичного малостадийного метода синтеза (адамант-1-илметилен)содержащих ароматических соединений, протекающего с высоким выходом по исходному адамантану. Техническим результатом является расширение арсенала химических соединений, получаемых с высоким выходом, и упрощение способа получения. Поставленный технический результат достигается в новом способе получения (адамант-1-илметилен)содержащих ароматических соединений общей формулы
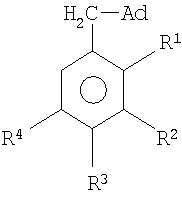
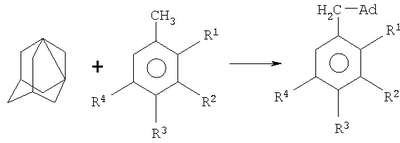
где R1=R2=R3=R4=H (1); R1=СН3, R2=R3=R4=H (2); R1=R3=R4=H, R2=СН3 (3); R1=R2=R4=H, R3=CH3 (4); R1=R3=H, R2=R4=CH3 (5); R1=R3=R4=CH3, R2=H (6); Ad – 1-адамантил, заключающийся в присоединении к производному адамантана ароматических соединений, причем в качестве производного адамантана используют 1,3-дегидроадамантан, а в качестве ароматических соединений используют соединения из ряда: толуол, о-, м-, п-ксилол, мезитилен, дурол при мольных соотношениях реагентов, равном 1:(2-4), в среде исходного ароматического соединения при их температуре кипения (110-197°С) в течение 60 мин. Сущностью метода является реакция присоединения 1,3-дегидроадамантана к ряду ароматических соединений где R1=R2=R3=R4=H (1); R1=СН3, R2=R3=R4=H (2); R1=R3=R4=H, R2=CH3 (3); R1=R2=R4=H, R3=CH3 (4); R1=R3=H, R2=R4=CH3 (5); R1=R3=R4=CH3, R2=H (6); Ad – 1-адамантил. Преимуществом данного метода является высокий (53-78%) выход, небольшая продолжительность реакции (60 мин), простота выделения продуктов, а также возможность получения практически любых гомологов данного ряда, многие из которых являются полупродуктами для синтеза биологически активных веществ. Способ осуществляется следующим образом. К 2-4-кратному мольному избытку ароматического соединения приливают раствор 1,3-дегидроадамантана в легкокипящем инертном растворителе (этиловый эфир), который затем удаляется из реакционной смеси отгонкой. Смесь 1,3-дегидроадамантана и ароматического соединения нагревают в течение 60 минут при температуре кипения ароматического соединения, после чего избыток его отгоняют. Реакция проводится в течение 60 мин. При уменьшении продолжительности реакции не достигается высокий выход основного продукта. Увеличение продолжительности реакции является нецелесообразным и экономически невыгодным. Найдено, что оптимальным условием проведения реакции присоединения ароматических соединений к 1,3-дегидроадамантану является ее осуществление при мольном соотношении 1,3-дегидроадамантан : ароматическое соединение 1:2-4. Меньший избыток приводил к некоторому снижению выхода целевых продуктов. Дальнейшее увеличение содержания ароматического соединения не влияло на выход целевых продуктов и являлось нецелесообразным. Синтезированные соединения после отгонки избытка исходных реагентов направляются на стадию очистки. Регенерированное ароматическое соединение не содержит каких-либо примесей и пригодно для повторного аналогичного синтеза. Изобретение иллюстрируется следующими примерами. Пример 1. 1-Бензиладамантан. Мольное соотношение 1,3-дегидроадамантана и толуола составляет 1:2.
К 5,52 г (0,06 моль) толуола в атмосфере сухого азота при комнатной температуре прикапывают раствор 4 г (0,03 моль) свежевозогнанного 1,3-дегидроадамантана в 20 мл эфира. Эфир отгоняют, смесь выдерживают 60 мин при температуре 110°С. По окончании реакции отгоняют избыток толуола. Продукт выделяют перегонкой. Выход 3,56 г (53%); т.пл. 42-43°С, т.кип. 164°С/2 мм рт.ст. Найдено, %: С 90,28; Н 9,75. С17Н22. Вычислено, %: С 90,20; Н 9,80. Масс-спектр, m/z (интенсивность, %): 226 (М+, 7%), 135 (Ad+, 100%), 91 (C7H7 +, 18%), 79 (C6H7 +, 15%), 41 (C3H5 +, 8%). Пример 2. о-(Адамантил-1-метил)толуол. Мольное соотношение 1,3-дегидроадамантана и о-ксилола составляет 1:2.
К 6,37 г (0,06 моль) о-ксилола в атмосфере сухого азота при комнатной температуре прикапывают раствор 4 г (0,03 моль) свежевозогнанного 1,3-дегидроадамантана в 20 мл эфира. Эфир отгоняют, смесь выдерживают 60 мин при температуре 144°С. По окончании реакции отгоняют избыток ксилола. Продукт выделяют перегонкой. Выход 4,30 г (60%); nD 20 1,5612, т.кип. 148-149°С/1 мм рт.ст. Найдено, %: С 90,03; Н 10,01. С18Н24. Вычислено, %: С 89,94; Н 10,06. ПМР-спектр Пример 3. м-(Адамантил-1-метил)толуол. Мольное соотношение 1,3-дегидроадамантана и м-ксилола составляет 1:2.
К 6,37 г (0,06 моль) м-ксилола в атмосфере сухого азота при комнатной температуре прикапывают раствор 4 г (0,03 моль) свежевозогнанного 1,3-дегидроадамантана в 20 мл эфира. Эфир отгоняют, смесь выдерживают 60 мин при температуре 139°С. По окончании реакции отгоняют избыток ксилола. Продукт выделяют перегонкой. Выход 5,06 г (70%); nD 20 1,5529, т. кип. 145-147°С/3 мм рт. ст. Найдено, %: С 90,03; Н 10,01. С18Н24. Вычислено, %: С 89,94; Н 10,06. Масс-спектр, m/z (интенсивность, %): 240 (M+, 28%), 136 (Ad+, 46%), 135 (Ad+, 100%), 107 ( ПМР-спектр Пример 4. п-(Адамантил-1-метил)толуол. Мольное соотношение 1,3-дегидроадамантана и п-ксилола составляет 1:2.
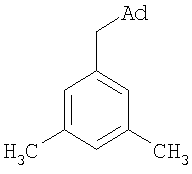
К 6,37 г (0,06 моль) п-ксилола в атмосфере сухого азота при комнатной температуре прикапывают раствор 4 г (0,03 моль) свежевозогнанного 1,3-дегидроадамантана в 20 мл эфира. Эфир отгоняют, смесь выдерживают 60 мин при температуре 138°С. По окончании реакции отгоняют избыток ксилола. Продукт выделяют перегонкой. Выход 4,92 г (68%); т. пл. 39-40,5°С, т. кип. 143-145°С/3 мм рт. ст. Найдено, %: С 90,03; Н 10,01. С18Н24. Вычислено, %: С 89,94; Н 10,06. Масс-спектр, m/z (интенсивность, %): 240 (M+, 58%), 136 (Ad+, 47%), 135 (Ad+, 100%), 107 (C8H11 +, 31%), 105 ( ПМР-спектр Пример 5. 1-(Адамантил-1-метил)-3,5-диметилбензол. Мольное соотношение 1,3-дегидроадамантана и мезитилена составляет 1:4.
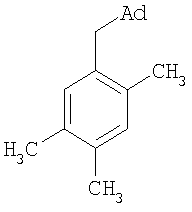
К 14,24 г (0,12 моль) мезитилена в атмосфере сухого азота при комнатной температуре прикапывают раствор 4 г (0,03 моль) свежевозогнанного 1,3-дегидроадамантана в 20 мл эфира. Эфир отгоняют, смесь выдерживают 60 мин при температуре 165°С. По окончании реакции отгоняют избыток мезитилена. Продукт выделяют перегонкой. Выход 4,70 г (62%); т. пл. 71-73°С, т. кип. 166°С/1 мм рт. ст. Найдено, %: С 89,79; Н 10,21. С19Н26. Вычислено, %: С 89,70; Н 10,30. ПМР-спектр Пример 6. 1-(Адамантил-1-метил)-2,4,5-триметилбензол. Мольное соотношение 1,3-дегидроадамантана и дурола (1,2,4,5-тетраметилбензола) составляет 1:4.
К 16,10 г (0,12 моль) 1,2,4,5-тетраметилбензола в атмосфере сухого азота при комнатной температуре прикапывают раствор 4 г (0,03 моль) свежевозогнанного 1,3-дегидроадамантана в 20 мл эфира. Эфир отгоняют, смесь выдерживают 60 мин при температуре 197°С. По окончании реакции отгоняют избыток 1,2,4,5-тетраметилбензола. Продукт выделяют перегонкой. Выход 6,27 г (78%); т.пл. 69-71°С, т.кип. 163°С/1 мм рт.ст. Найдено, %: С 89,56; Н 10,45. С20Н28. Вычислено, %: С 89,49; Н 10,51. ПМР-спектр Таким образом, вышеизложенные сведения свидетельствуют о выполнении при использовании заявленного изобретения следующей совокупности условий: – средство, воплощающее заявленное изобретение при его осуществлении, предназначено для применения в различных отраслях промышленности; – для заявленного изобретения в том виде, как оно охарактеризовано в независимом пункте нижеизложенной формулы изобретения, подтверждена возможность его осуществления с помощью вышеописанных в заявке или известных до даты приоритета средств и методов; – средство, воплощающее заявленное изобретение при его осуществлении способно обеспечить достижение технического результата. Следовательно, заявленное изобретение соответствует требованию «промышленная применимость». Выводы Разработан новый малостадийный способ получения (адамант-1-илметилен)содержащих ароматических соединений и их производных, позволяющий получать соединения заявляемой структурной формулы с достаточно высокими выходами. Структура полученных соединений подтверждена ПМР-спектроскопией и элементным анализом.
Формула изобретения
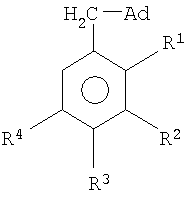
Способ получения (адамант-1-илметилен)содержащих ароматических соединений общей формулы
где R1=R2=R3=R4=H (1); R1=CH3, R2=R3=R4=H (2); R1=R3=R4=H, R2=CH3 (3); R1=R2=R4=H, R3=CH3 (4); R1=R3=H, R2=R4=CH3 (5); R1=R3=R4=CH3, R2=H (6), заключающийся в присоединении к производному адамантана ароматических соединений, отличающийся тем, что в качестве производного адамантана используют 1,3-дигидроадамантан, а в качестве ароматических соединений используют соединения из ряда: толуол, о-, м-, п-ксилол, мезитилен, дурол, при мольных соотношениях реагентов, равном 1:(2-4), в среде исходного ароматического соединения при их температуре кипения 110-197°С в течение 60 мин.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 12.07.2008
Извещение опубликовано: 10.07.2010 БИ: 19/2010
|
||||||||||||||||||||||||||

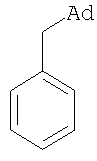
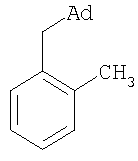
 , м.д.: 1,53 м, 1,92 с (15Н, Ad); 2,39 с (3Н, СН3); 2,40 с (2Н, СН3); 7,05 м (4Н, аром.).
, м.д.: 1,53 м, 1,92 с (15Н, Ad); 2,39 с (3Н, СН3); 2,40 с (2Н, СН3); 7,05 м (4Н, аром.).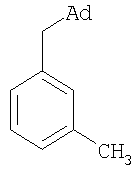
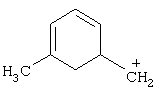 , 48%), 105 (
, 48%), 105 (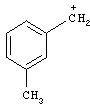 , 54%), 93 (
, 54%), 93 (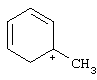 , 74%), 91 (C7H7 +, 50%), 79 (
, 74%), 91 (C7H7 +, 50%), 79 (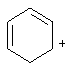 , 77%), 77 (C6H5 +, 54%), 67 (C5H7 +, 64%), 41 (C3H5 +, 77%).
, 77%), 77 (C6H5 +, 54%), 67 (C5H7 +, 64%), 41 (C3H5 +, 77%).