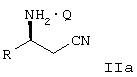Патент на изобретение №2309145
|
||||||||||||||||||||||||||
(54) РАЗДЕЛЕНИЕ 3-АМИНОАЛКИЛНИТРИЛОВ
(57) Реферат:
Изобретение относится к хиральным солям N-ацетил-альфа-аминокислот и оптически активных (
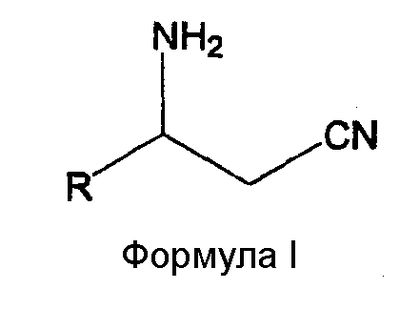
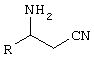
где R означает метил, этил, н-пропил, изопропил, н-бутил или изобутил, и Q означает N-ацетил-альфа-аминокислоту. Изобретение также относится к способу превращения рацемического 3-амино(С3-С7)алкилнитрила формулы I
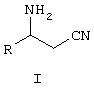
где R означает метил, этил, н-пропил, изопропил, н-бутил или изобутил, в соответствующий (R) изомер формулы IIa, который заключается во взаимодействии рацемического 3-амино-(С3-С7)алкилнитрила формулы I с N-ацетил-L-аминокислотой формулы Q в растворителе; к способу превращения R или S 3-амино-(С3-С7)алкилнитрила в рацемический 3-амино-(С3-С7)алкилнитрил, включающему взаимодействие R или S 3-амино-(С3-С7)алкилнитрила с водным аммиаком при температуре от около 30 до около 200°С. Изобретение также относится к составу для применения в качестве компоновочных блоков в синтезе оптически активных
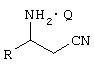
где R означает метил, этил, н-пропил, изопропил, н-бутил или изобутил, и Q означает N-ацетил-альфа-аминокислоту. 4 н. и 10 з.п. ф-лы.
Область изобретения Данное изобретение относится к способу получения оптически активных Более конкретно данное изобретение относится к хиральным солям N-ацетил-альфа-аминокислот оптически активных Уровень техники
Steer и др. в публикации “Применение В публикации “ Различные способы получения энантиочистых Учитывая низкую стоимость получения рацемических смесей Сущность изобретения Согласно одному аспекту данное изобретение относится к соединению формулы IIa или IIb где R означает метил, этил, н-пропил, изопропил, н-бутил или изобутил, и Q означает N-ацетил-L-аланин, N-ацетил-L-аргинин, N-ацетил-L-аспарагин, N-ацетил-L-аспарагиновую кислоту, N-ацетил-L-цистеин, N-ацетил-L-глутамин, N-ацетил-L-глутаминовую кислоту, N-ацетил-L-гистидин, N-ацетил-L-изолейцин, N-ацетил-L-лейцин, N-ацетил-L-лизин, N-ацетил-L-метионин, N-ацетил-L-фенилаланин, N-ацетил-L-пролин, N-ацетил-L-серин, N-ацетил-L-треонин, N-ацетил-L-триптофан, N-ацетил-L-тирозин, N-ацетил-L-валин, N-ацетил-D-аланин, N-ацетил-D-аргинин, N-ацетил-D-аспарагин, N-ацетил-D-аспарагиновую кислоту, N-ацетил-D-цистеин, N-ацетил-D-глутамин, N-ацетил-D-глутаминовую кислоту, N-ацетил-D-гистидин, N-ацетил-D-изолейцин, N-ацетил-D-лейцин, N-ацетил-D-лизин, N-ацетил-D-метионин, N-ацетил-D-фенилаламин, N-ацетил-D-пролин, N-ацетил-D-серин, N-ацетил-D-треонин, N-ацетил-D-триптофан, N-ацетил-D-тирозин, N-ацетил-D-валин. В предпочтительном воплощении Q выбран из группы, состоящей из N-ацетил-L-аланина, N-ацетил-L-цистеина, N-ацетил-L-изолейцина, N-ацетил-L-лейцина, N-ацетил-L-лизина и N-ацетил-L-валина. В другом предпочтительном воплощении Q означает N-ацетил-L-изолейцин. В еще одном предпочтительном воплощении Q означает N-ацетил-L-валин. Согласно другому предпочтительному воплощению R означает этил. Согласно другому аспекту данного изобретения предложен способ превращения рацемического 3-амино-(С3-С7)алкилнитрила формулы I где R означает метил, этил, н-пропил, изопропил, н-бутил или изобутил, в соответствующий (R) или (S) изомер формулы IIa или IIb, содержащий сочетание в растворителе рацемического 3-амино-(С3-С7)алкилнитрила формулы I с N-ацетил-L-аминокислотой формулы Q, где Q означает N-ацетил-L-аланин, N-ацетил-L-аргинин, N-ацетил-L-аспарагин, N-ацетил-L-аспарагиновую кислоту, N-ацетил-L-цистеин, N-ацетил-L-глутамин, N-ацетил-L-глутаминовую кислоту, N-ацетил-L-гистидин, N-ацетил-L-изолейцин, N-ацетил-L-лейцин, N-ацетил-L-лизин, N-ацетил-L-метионин, N-ацетил-L-фенилаланин, N-ацетил-L-пролин, N-ацетил-L-серин, N-ацетил-L-треонин, N-ацетил-L-триптофан, N-ацетил-L-тирозин, N-ацетил-L-валин, N-ацетил-D-аланин, N-ацетил-D-аргинин, N-ацетил-D-аспарагин, N-ацетил-D-аспарагиновую кислоту, N-ацетил-D-цистеин, N-ацетил-D-глутамин, N-ацетил-D-глутаминовую кислоту, N-ацетил-D-гистидин, N-ацетил-D-изолейцин, N-ацетил-D-лейцин, N-ацетил-D-лизин, N-ацетил-D-метионин, N-ацетил-D-фенилаламин, N-ацетил-D-пролин, N-ацетил-D-серин, N-ацетил-D-треонин, N-ацетил-D-триптофан, N-ацетил-D-тирозин или N-ацетил-D-валин, в растворителе, который выбран из группы, состоящей из этанола, н-пропанола, изопропанола, н-бутанола, трет-бутанола, метанола и воды или их смеси. В предпочтительном воплощении способа Q выбран из группы, состоящей из N-ацетил-L-аланина, N-ацетил-L-цистеина, N-ацетил-L-изолейцина, N-ацетил-L-лейцина, N-ацетил-L-лизина и N-ацетил-L-валина. В другом предпочтительном воплощении способа Q означает N-ацетил-L-изолейцин. В другом предпочтительном воплощении способа Q означает N-ацетил-L-валин. В другом предпочтительном воплощении R означает этил. Согласно другому аспекту изобретения предложен способ превращения R или S 3-амино-(С3-С7)алкилнитрила в рацемический 3-амино-(С3-С7)алкилнитрил, содержащий сочетание R или S 3-аминопентаннитрила с водным аммиаком при температуре от 30 до 200°С. Согласно другому аспекту изобретения рацемический амино-(С3-С7)алкилнитрил является R-3-аминопентаннитрилом. Согласно другому аспекту изобретения предложен состав, обогащенный соединением формулы IIa или IIb, как описано выше. Согласно другому аспекту изобретения предложено соединение формулы I
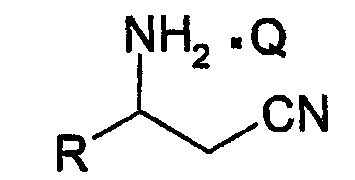
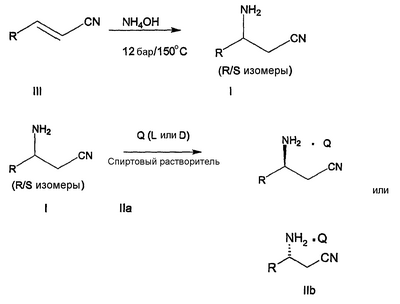
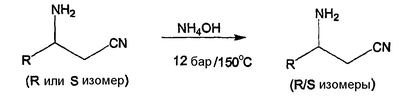
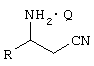
где R означает метил, этил, н-пропил, изопропил, н-бутил или изобутил, и Q означает N-ацетил-L-аланин, N-ацетил-L-аргинин, N-ацетил-L-аспарагин, N-ацетил-L-аспарагиновую кислоту, N-ацетил-L-цистеин, N-ацетил-L-глутамин, N-ацетил-L-глутаминовую кислоту, N-ацетил-L-гистидин, N-ацетил-L-изолейцин, N-ацетил-L-лейцин, N-ацетил-L-лизин, N-ацетил-L-метионин, N-ацетил-L-фенилаламин, N-ацетил-L-пролин, N-ацетил-L-серин, N-ацетил-L-треонин, N-ацетил-L-триптофан, N-ацетил-L-тирозин, N-ацетил-L-валин, N-ацетил-D-аланин, N-ацетил-D-аргинин, N-ацетил-D-аспарагин, N-ацетил-D-аспарагиновую кислоту, N-ацетил-D-цистеин, N-ацетил-D-глутамин, N-ацетил-D-глутаминовую кислоту, N-ацетил-D-гистидин, N-ацетил-D-изолейцин, N-ацетил-D-лейцин, N-ацетил-D-лизин, N-ацетил-D-метионин, N-ацетил-D-фенилаламин, N-ацетил-D-пролин, N-ацетил-D-серин, N-ацетил-D-треонин, N-ацетил-D-триптофан, N-ацетил-D-тирозин или N-ацетил-D-валин. Используемый здесь термин “разделение” имеет свое обычное значение, т.е. превращение рацемического 3-аминоалкилнитрила формулы I в продукт (т.е. состав), обогащенный соответствующим (R) или (S) изомером. Обогащенный состав – это состав, который содержит больший избыток или более высокую относительную долю одного стереоизомера по отношению к другому. Так, обогащенный состав обычно содержит более высокую относительную долю желаемого стереоизомера (например, энантиомера) по отношению к рацемату. В формулах здесь, если иначе не указано, связи амино-углерод имеют известные в технике стереохимические значения. Например, в формуле I связь амино-углерод, обозначенная прямой линией, представляет рацемат. Связь амино-углерод, обозначенная утолщенной линией, как в формуле IIa (смотри ниже), находится над плоскостью страницы. Связь амино-углерод, обозначенная прерывистой или пунктирной линией, как в формуле IIb (смотри ниже), находится за плоскостью страницы. Специалисты в этой области легко поймут, что символ · в формулах I, IIa и IIb означает солевую пару. Соль, образованная между оптически активной N-ацетил-альфа-аминокислотой, Q, и (R)-стереоизомером или (S)-стереоизомером субстрата где Q, R и связи амино-углерод имеют указанные выше значения. Конкретная образованная соль зависит, конечно, от стереохимии конкретной N-ацетил-альфа-аминокислоты, используемой для разделения Установлено, что оптически активные N-ацетил-альфа-аминокислоты, обозначенные здесь как Q, могут быть использованы для разделения рацемических Конкретный пример воплощения данного изобретения относится к способу, который описан выше, где L-N-ацетилвалин используют в качестве разделяющего агента и спирт, например этанол, используют в качестве растворителя для кристаллизации соли Подробное описание изобретения Обнаружено, что разделение рацемического 3-аминоалкилнитрила обработкой L-N-ацетил-аминокислотами может обеспечить высокопроизводительную реакцию разделения с очень высокой селективностью. В дополнение обнаружено, что этот подход обеспечивает дешевый/высокоэффективный способ синтеза представляющего интерес соединения, такого как R-3-аминопентаннитрил. Конкретные способы получения оптически активных Все исходные вещества коммерчески доступны, более того, их синтез будет очевиден для специалиста. Смотри, например, “Синтез N-ацетил-аминокислот”, Marshall, J.J. AM. Chem. Soc. 1956, 78, 4636. СХЕМА 1 На схеме R и Q имеют указанные ранее значения. Схема 1, приведенная выше, обеспечивает получение хиральной соли N-ацетил-аминокислоты и (R) или (S) 3-аминоалкилнитрила формулы IIa или IIb, начиная с соответствующего алкил-2-ен-нитрила формулы III. Алкил-2-ен-нитрил формулы III подвергают реакции с водным гидроксидом аммония, предпочтительно под давлением приблизительно 12 бар и при температуре приблизительно 150°С, чтобы получить рацемический 3-аминоалкил формулы I. Хиральную соль N-ацетил-альфа-аминокислоты и 3-аминоалкилнитрила формулы IIa или IIb затем получают взаимодействием рацемического 3-аминоалкилнитрила формулы I с подходящей хиральной N-ацетил-альфа-аминокислотой Q, предпочтительно в спиртовом или водном/спиртовом растворителе, при температуре от -20 до 120°С. Образование соли наиболее предпочтительно проводят, используя смесь этанол/вода в качестве растворителя и в пределах от 0,5 до 1,1 моль формулы Q на моль Предпочтительный способ получения хиральной соли N-ацетил-альфа-аминокислоты и 3-аминоалкилнитрила формулы IIa или IIb предусматривает взаимодействие 0,9 эквивалентов соответствующей хиральной N-ацетил-альфа-аминокислоты формулы Q с 1,0 эквивалентом рацемического 3-аминоалкилнитрила в водном этаноле. Более конкретно, рацемический 3-аминоалкилнитрил формулы I добавляют к хиральной N-ацетил-альфа-аминокислоте Q в водном этаноле при приблизительно 65 до 70°С. Реакционную смесь затем нагревают до кипения с возвращением флегмы, пока не получат гомогенный раствор. Реакционную смесь затем охлаждают до приблизительно 60°С и выдерживают при этой температуре в течение минимум 30 минут. Реакционную смесь затем охлаждают до 0°С и хиральную соль N-ацетил-альфа-аминокислоты и 3-аминоалкилнитрила формулы I, которая осаждается, отделяют и собирают фильтрованием. Фильтрат обогащен остающимся стереоизомером. Если фильтрат обогащен нежелаемым изомером, он может быть обработан, как описано выше, чтобы рацемизировать стереоизомер, и затем возвращен в цикл через процедуру разделения. Если он содержит желаемый стереоизомер, он может быть сконцентрирован выпариванием, чтобы извлечь его, необязательно с промежуточной экстракцией. Специалисту в этой области легко понятно, что указанная процедура обычно применима к любым Как предварительно отмечалось, для доведения до максимума атомной утилизации изобретение обеспечивает способ рацемизации нежелаемого изомера, как показано на схеме 2. Хиральный 3-амино-(С3-С7)алкилнитрил подвергают реакции с водным гидроксидом аммония при около 12 бар приблизительно при 120 до 150°С от 2 до 24 часов. Реакционную смесь затем концентрируют в вакууме, и полученный сырой рацемический 3-амино-(С3-С7)алкилнитрил может быть дополнительно отделен вакуумной перегонкой. СХЕМА 2 Полученная рацемическая смесь может быть затем разделена согласно известным процедурам, раскрытым здесь, то есть рацемическая смесь может быть подвергнута реакции с N-ацетил-аминокислотой, обозначенной здесь как Q, чтобы получить энантиомерно обогащенную соль формулы IIa или IIb в соответствии с условиями, описанными выше на схеме 1. ПРИМЕРЫ Пример I Синтез N-ацетил-L-валина L-Валин (200 г, 1,7 мол.экв.) растворяют в воде (500 мл), сопровождая добавлением NaOH (30%, 170 мл). Смесь охлаждают до 0-5°С, сопровождая добавлением уксусного ангидрида (32 мл, 1,4 экв.). Гидроксид натрия (30%, 34 мл) добавляют, поддерживая температуру 0-5°С. Чередующиеся добавления уксусного ангидрида и 30% NaOH повторяют шесть раз, поддерживая температуру (уксусный ангидрид, 6×32 мл; 30% NaOH 6×34 мл). После завершения всех добавлений смесь перемешивают в течение дополнительных двух часов при 0°С. Соляную кислоту (32%, 380 мл) добавляют, чтобы снизить рН ниже 3, поддерживая температуру 0°С. Полученную суспензию гранулируют в течение 12 часов, фильтруют и осадок на фильтре промывают HCl (0,1н., 100 мл). Влажный N-ацетил-L-валин сушат, получая 233 г (выход 86%). Пример II Разделение 3-аминопентаннитрила N-ацетил-L-валином N-ацетил-L-валин (145,4 г, 0,91 мол.экв.) объединяют с этанолом (1425 мл) и водой (75 мл) в колбе, снабженной мешалкой и конденсирующим устройством. Смесь нагревают до 65-70°С, сопровождая добавлением (шприцем) рацемического 3-аминопентаннитрила. Смесь выдерживают при кипении с возвращением флегмы до полного растворения. Смесь охлаждают до 60°С и выдерживают при этой температуре минимум 30 минут. Смесь охлаждают до 0°С и соль отделяют фильтрованием. Пример III Разделение 3-аминопентаннитрила N-ацетил-L-изолейцином. N-ацетил-L-изолейцин (157 г, 0,91 мол.экв.) объединяют с этанолом (250 мл) и водой (75 мл) в колбе, снабженной мешалкой и конденсирующим устройством. Смесь нагревают до 65-70°С, сопровождая добавлением рацемического 3-аминопентаннитрила. Смесь выдерживают при кипении с возвращением флегмы до полного растворения. Смесь охлаждают до 60°С и выдерживают при этой температуре минимум 30 минут. Смесь охлаждают до 0°С и соль отделяют фильтрованием (выход 70%, с максимум возможного выхода от 50% до 99,8%). Пример IV Рацемизация R-3-аминопентаннитрила R-3-аминопентаннитрил (197 г, 2,1 мол.экв.) объединяют с 30% водным раствором аммиака (930 мл, 14,7 моль.экв.) в подходящем работающим под давлением сосуде и смесь нагревают до 130°С. Через 6 часов смесь охлаждают и анализируют на завершение рацемизации. Смесь концентрируют в вакууме (15 мм рт. ст., 88°С) до 300 мл. Сырой продукт перегоняют в вакууме для дополнительной очистки, получая 160 г рацемической смеси (выход 77%, 95% GC чистота, 50/50% R/S). Пример V Превращение в свободное основание соли N-ацетил-L-валина с 3-аминопентаннитрилом Соль N-ацетил-L-валина с 3-аминопентаннитрилом (230 г) объединяют с дихлорметаном (713 мл). К смеси добавляют водный раствор гидроксида натрия (98 мл, 30% мас./мас.) и смесь перемешивают при 20-25°С в течение 1 часа. Нижнюю органическую фазу отделяют и верхнюю водную фазу промывают дополнительным дихлорметаном (2×180 мл). Органические слои объединяют, концентрируют и оптически активный 3-аминопентаннитрил отделяют перегонкой (выход 80%, 99,8%) Пример VI Получение соли L-ацетил-L-валина с 3-аминопентаннитрилом В 3-литровую колбу, снабженную мешалкой, термометром, капельной воронкой, масляной баней, загружают N-ацетил-L-валин (145,4 г), денатурированный этанол (денатурированный около 5% метанола и 3% циклогексана) (1425 мл) и воду (75 мл). Смесь нагревают при перемешивании до 65-70°С и добавляют 150 г 3-аминопентаннитрила. Раствор нагревают до кипения с возвращением флегмы (около 75°С) до получения полностью прозрачного раствора, который затем медленно охлаждают до 65°С. При постоянном перемешивании в смесь вносят в качестве затравки немного диастереомерно чистой соли L-ацетил-L-валина с 3-аминопентаннитрилом и перемешивают при 60°С в течение 1 часа. Густую суспензию затем охлаждают до 0°С в течение 3 часов и перемешивают при 0°С в течение 2 часов. Полученную соль отфильтровывают и промывают этанолом 2×75 мл. Оптическая чистота влажного продукта 89,8% (А%). Влажную соль загружают в 2-литровую колбу со стандартным оборудованием и добавляют 900 мл денатурированного этанола. Суспензию нагревают до кипения с возвращением флегмы, перемешивают в течение 1 часа при температуре кипения с возвращением флегмы и затем охлаждают до комнатной температуры в течение 2 часов. После более 2 часов перемешивания при комнатной температуре полученную соль отфильтровывают и промывают денатурированным этанолом 2×150 мл. Продукт сушат при 40°С, получая 118,3 г соли L-ацетил-L-валина с 3-аминопентаннитрилом, кристаллического твердого вещества белого цвета (оптическая чистота: 99,8%, выход: 60% от теоретического). Пример VII Получение соли L-ацетил-L-валина с 3-аминопентаннитрилом В 3-литровую колбу, снабженную мешалкой, термометром, капельной воронкой, масляной баней, загружают N-ацетил-L-валин (200,0 г), денатурированный этанол (денатурированный около 5% метанола и 3% циклогексана) (2000 мл) и воду (100 мл). Смесь нагревают при перемешивании до 65-70°С и добавляют 3-аминопентаннитрил (206,4 г) в течение 30 мин. Раствор нагревают до кипения с возвращением флегмы (около 75°С) до получения полностью прозрачного раствора, который затем медленно охлаждают до 65°С. При постоянном перемешивании в смесь вносят в качестве затравки немного диастереомерно чистой соли L-ацетил-L-валина с 3-аминопентаннитрилом и перемешивают при 60°С в течение 1 часа. Густую суспензию затем медленно охлаждают до 20°С в течение 3 часов и перемешивают при 20°С в течение 18 часов (в течение ночи). Суспензию с этого времени охлаждают до 5°С и перемешивают в течение 3 часов. Осажденную соль отфильтровывают и промывают денатурированным этанолом (3×100 мл) и сушат в вакуумной сушилке при 40°С С/10 мбар до достижения постоянной массы, получая соль L-ацетил-L-валина с 3-аминопентаннитрилом (228,7 г), кристаллическое твердое вещество белого цвета (выход 84,8%), имеющее оптическую чистоту 97,7%. Пример VIII Получение соли L-ацетил-L-изолейцина с 3-аминопентаннитрилом В колбу емкостью 250 мл, снабженную механической мешалкой, термометром, капельной воронкой, масляной баней, загружают 3-аминопентаннитрил (5 г), N-ацетил-L-изолейцин (8,8 г) и денатурированный этанол (денатурированный около 5% метанола и 3% циклогексана) (97 мл). Раствор нагревают до кипения с возвращением флегмы до получения полностью прозрачного раствора, который затем медленно охлаждают до 68°С. При постоянном перемешивании в смесь вносят в качестве затравки немного диастереомерно обогащенной соли L-ацетил-L-изолейцина с 3-аминопентаннитрилом и перемешивают при 65-70°С в течение 2 часов. Густую суспензию затем медленно охлаждают до комнатной температуры. Полученную соль отфильтровывают и промывают этанолом. Продукт сушат при 50°С, получая соль L-ацетил-L-изолейцина с 3-аминопентаннитрилом (7,3 г), кристаллическое твердое вещество белого цвета (оптическая чистота: 76% R; выход 112% от теоретического). Полученную соль загружают в колбу емкостью 250 мл со стандартным оборудованием и добавляют метил-этил-кетон (73 мл). Суспензию нагревают до кипения с возвращением флегмы, перемешивают в течение 1 часа при температуре кипения с возвращением флегмы и затем медленно охлаждают до 60°С. Полученную соль отфильтровывают и промывают метил-этил-кетоном. Продукт сушат при 50°С, получая соль L-ацетил-изолейцина с 3-аминопентаннитрилом (5,2 г), кристаллическое твердое вещество белого цвета (оптическая чистота: 98,2% R; выход 71,9% от теоретического). В данной заявке есть ссылки на различные публикации. Раскрытия указанных публикаций во всей их полноте приобщены тем самым к данной заявке для всех целей. Специалистам в данной области должно быть понятно, что различные модификации и изменения могут быть сделаны в данном изобретении, не выходя из сферы действия и сущности изобретения. Другие воплощения изобретения будут очевидны специалистам в этой области из рассмотрения описания и осуществления на практике изобретения, раскрытого здесь. Подразумевается, что описание и примеры следует рассматривать только в качестве примеров, истинный объем и суть изобретения указаны следующей формулой изобретения.
Формула изобретения
1. Соединение формулы IIa
где R означает метил, этил, н-пропил, изопропил, н-бутил или изобутил; Q означает N-ацетил-L-аланин, N-ацетил-L-аргинин, N-ацетил-L-аспарагин, N-ацетил-L-аспарагиновую кислоту, N-ацетил-L-цистеин, N-ацетил-L-глутамин, N-ацетил-L-глутаминовую кислоту, N-ацетил-L-гистидин, N-ацетил-L-изолейцин, N-ацетил-L-лейцин, N-ацетил-L-лизин, N-ацетил-L-метионин, N-ацетил-L-фенилаланин, N-ацетил-L-пролин, N-ацетил-L-серин, N-ацетил-L-треонин, N-ацетил-L-триптофан, N-ацетил-L-тирозин, N-ацетил-L-валин, N-ацетил-D-аланин, N-ацетил-D-аргинин, N-ацетил-D-аспарагин, N-ацетил-D-аспарагиновую кислоту, N-ацетил-D-цистеин, N-ацетил-D-глутамин, N-ацетил-D-глутаминовую кислоту, N-ацетил-D-гистидин, N-ацетил-D-изолейцин, N-ацетил-D-лейцин, N-ацетил-D-лизин, N-ацетил-D-метионин, N-ацетил-D-фенилаламин, N-ацетил-D-пролин, N-ацетил-D-серин, N-ацетил-D-треонин, N-ацетил-D-триптофан, N-ацетил-D-тирозин, N-ацетил-D-валин. 2. Соединение по п.1, где Q выбран из группы, состоящей из N-ацетил-L-аланина, N-ацетил-L-цистеина, N-ацетил-L-изолейцина, N-ацетил-L-лейцина, N-ацетил-L-лизина и N-ацетил-L-валина. 3. Соединение по п.2, где Q означает N-ацетил-L-изолейцин. 4. Соединение по п.2, где Q означает N-ацетил-L-валин. 5. Соединение по любому из пп.1-4, где R означает этил. 6. Способ превращения рацемического 3-амино-(С3-С7)алкилнитрила формулы I
где R означает метил, этил, н-пропил, изопропил, н-бутил или изобутил, в соответствующий (R) изомер формулы IIa,
который заключается во взаимодействии рацемического 3-амино-(С3-С7)алкилнитрила формулы I с N-ацетил-L-аминокислотой формулы Q в растворителе, где Q означает N-ацетил-L-аланин, N-ацетил-L-аргинин, N-ацетил-L-аспарагин, N-ацетил-L-аспарагиновую кислоту, N-ацетил-L-цистеин, N-ацетил-L-глутамин, N-ацетил-L-глутаминовую кислоту, N-ацетил-L-гистидин, N-ацетил-L-изолейцин, N-ацетил-L-лейцин, N-ацетил-L-лизин, N-ацетил-L-метионин, N-ацетил-L-фенилаламин, N-ацетил-L-пролин, N-ацетил-L-серин, N-ацетил-L-триптофан, N-ацетил-L-триптофан, N-ацетил-L-тирозин, N-ацетил-L-валин, N-ацетил-D-аланин, N-ацетил-D-аргинин, N-ацетил-D-аспарагин, N-ацетил-D-аспарагиновую кислоту, N-ацетил-D-цистеин, N-ацетил-D-глутамин, N-ацетил-D-глутаминовую кислоту, N-ацетил-D-гистидин, N-ацетил-D-изолейцин, N-ацетил-D-лейцин, N-ацетил-D-лизин, N-ацетил-D-метионин, N-ацетил-D-фенилаламин, N-ацетил-D-пролин, N-ацетил-D-серин, N-ацетил-D-треонин, N-ацетил-D-триптофан, N-ацетил-D-тирозин или N-ацетил-D-валин, где растворитель выбран из группы, состоящей из этанола, н-пропанола, изопропанола, н-бутанола, трет-бутанола, метанола и воды или их смеси. 7. Способ по п.6, где Q выбран из группы, состоящей из N-ацетил-L-аланина, N-ацетил-L-цистеина, N-ацетил-L-изолейцина, N-ацетил-L-лейцина, N-ацетил-L-лизина и N-ацетил-L-валина. 8. Способ по п.7, где Q означает N-ацетил-L-изолейцин. 9. Способ по п.7, где Q означает N-ацетил-L-валин. 10. Способ по любому из пп.6-9, где R означает этил. 11. Способ превращения R или S 3-амино-(С3-С7)алкилнитрила в рацемический 3-амино-(С3-С7)алкилнитрил, включающий взаимодействие R или S 3-амино-(С3-С7)алкилнитрила с водным аммиаком при температуре от около 30°С до около 200°С. 12. Способ по п.11, где рацемический амино-(С3-С7)алкилнитрил является R-3-аминопентаннитрилом. 13. Состав для применения в качестве компоновочных блоков в синтезе оптически активных 14. Соединение формулы I
где R означает метил, этил, н-пропил, изопропил, н-бутил или изобутил; Q означает N-ацетил-L-аланин, N-ацетил-L-аргинин, N-ацетил-L-аспарагин, N-ацетил-L-аспарагиновую кислоту, N-ацетил-L-цистеин, N-ацетил-L-глутамин, N-ацетил-L-глутаминовую кислоту, N-ацетил-L-гистидин, N-ацетил-L-изолейцин, N-ацетил-L-лейцин, N-ацетил-L-лизин, N-ацетил-L-метионин, N-ацетил-L-фенилаланин, N-ацетил-L-пролин, N-ацетил-L-серин, N-ацетил-L-треонин, N-ацетил-L-триптофан, N-ацетил-L-тирозин, N-ацетил-L-валин, N-ацетил-D-аланин, N-ацетил-D-аргинин, N-ацетил-D-аспарагин, N-ацетил-D-аспарагиновую кислоту, N-ацетил-D-цистеин, N-ацетил-D-глутамин, N-ацетил-D-глутаминовую кислоту, N-ацетил-D-гистидин, N-ацетил-D-изолейцин, N-ацетил-D-лейцин, N-ацетил-D-лизин, N-ацетил-D-метионин, N-ацетил-D-фенилаламин, N-ацетил-D-пролин, N-ацетил-D-серин, N-ацетил-D-треонин, N-ацетил-D-триптофан, N-ацетил-D-тирозин или N-ацетил-D-валин.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 19.10.2008
Извещение опубликовано: 27.07.2010 БИ: 21/2010
|
||||||||||||||||||||||||||

 -аминоалкилнитрилов, а именно соединению формулы IIa
-аминоалкилнитрилов, а именно соединению формулы IIa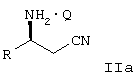 ,
, ,
,
 -аминокислотам в том, что они содержат концевую аминогруппу и концевую карбоксильную группу, они также имеют два атома углерода, которые разделяют указанные функциональные концевые группы. Как таковые,
-аминокислотам в том, что они содержат концевую аминогруппу и концевую карбоксильную группу, они также имеют два атома углерода, которые разделяют указанные функциональные концевые группы. Как таковые,