|
|
(21), (22) Заявка: 2005128437/15, 30.08.2005
(24) Дата начала отсчета срока действия патента:
30.08.2005
(43) Дата публикации заявки: 20.03.2007
(46) Опубликовано: 27.10.2007
(56) Список документов, цитированных в отчете о
поиске:
WO 9111394 А1, 08.08.1991. SU 1632493 А1, 07.03.1991. SU 403154 А2, 15.03.1974. SU 1820871 A3, 07.06.1993. RU 94006699 А1, 27.09.1995. RU 2084761 С1, 20.07.1997. RU 2162459 С1, 27.01.2001. WO 2004101446 А1, 25.11.2004. US 5558783 А, 24.09.1996. US 6264844 А, 24.07.2001.
Адрес для переписки:
630090, г.Новосибирск, пр. Акад. Лаврентьева, 5, Институт катализа им. Г.К. Борескова, патентный отдел, Т.Д. Юдиной
|
(72) Автор(ы):
Аникеев Владимир Ильич (RU),
Белобров Николай Степанович (RU),
Ермакова Анна (HU),
Микенин Павел Евгеньевич (RU),
Питеркин Рудольф Николаевич (RU),
Просвирнин Рудольф Шакирович (RU)
(73) Патентообладатель(и):
Институт катализа им. Г.К. Борескова Сибирского отделения Российской Академии наук (RU)
|
(54) СПОСОБ ОСУЩЕСТВЛЕНИЯ РЕАКЦИЙ ОКИСЛЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
(57) Реферат:
Изобретение относится к области химической технологии, экологии, а более подробно к способам проведения химических реакций, в частности окисления в сверхкритических средах-флюидах (или растворителях). Способ осуществления реакций окисления органических соединений включает подачу топлива и окислителя через устройство смешивания в каталитический пакет. Полученные продукты окисления с выхода каталитического пакета направляют в объем смешения на лопасти мешалки и в продукты окисления после каталитического пакета подают реагенты, содержащие органические соединения и окислитель. Полученные продукты реакции подают в трубчатую часть реактора для их полного окисления, при этом окисление органических соединений проводят в сверхкритической воде. В качестве окислителя используют нитрат аммония, смесь нитрата аммония и воздуха, смесь нитрата аммония и кислорода или смесь нитрата аммония и перекиси водорода. Часть окислителя подают непосредственно в трубчатую часть реактора. Изобретение позволяет повысить эффективность процесса окисления органических соединений. 5 з.п. ф-лы, 2 ил., 2 табл.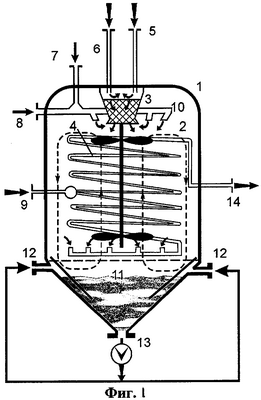
Изобретение относится к области химической технологии, экологии, а более подробно к способам проведения химических реакций, в частности окисления в сверхкритических средах-флюидах (или растворителях), обеспечивающих многократное увеличение скорости химического процесса и контролируемую его селективность.
Многие жидкости в сверхкритическом состоянии вблизи критической точки, как среды для проведения химических реакций, обладают рядом особых свойств, которые позволяют с высокой скоростью осуществлять реакции дегидратации и гидролиза, синтеза, гидрирования и окисления большого числа органических и неорганических веществ. Такое состояние жидкости может быть результатом изменения ее структурных свойств в сверхкритических условиях. В частности, для воды в сверхкритическом ее состоянии вблизи критической точки характерно образование высокой концентрации ионов Н+ и ОН–, что обеспечивает свойства основного или кислотного катализа.
Среди сверхкритических растворителей, наиболее пригодных для проведения в них химических превращений и практического использования, следует выделить воду, СО2, гексан, аммиак, ряд предельных и непредельных углеводородов. Наиболее высоким сохраняется интерес к сверхкритической воде, находящейся вблизи своего критического состояния, как к среде для осуществления химических реакций. Поскольку осуществлять химические превращения в воде или другой жидкой среде мы просто вынуждены, так как именно в воде, чаще всего в стоках, содержатся малые примеси различных органических и неорганических веществ. И на сегодняшний день практически нет альтернативных и эффективных путей их удаления, кроме как проводить химические превращения с участием этих соединений в той среде, в которой они растворены. Среди реакций, на которые следует серьезно обратить внимание для их проведения в сверхкритической воде (СКВ), надо выделить окисление, дегидратацию, гидролиз и гидрирование.
Известны способы осуществления процессов окисления различного класса органических соединений в сверхкритической воде и устройства-реактора, в которых осуществляются эти реакции [Р.Е.Savage, S.Gopalan, T.I.Mizan, Ch.J.Martino, E.E.Brock. Reactions at supercritical conditions: Applications and fundamentals. AIChE Journal, 1995, 41, 1723-1778; US Pat. 5723045, Mar. 3, 1998].
К основным недостаткам таких способов осуществления химических реакций в сверхкритических растворителях можно отнести низкие скорости химических реакций (если это не окислительные реакции), не выбраны параметры, контролирующие и управляющие скоростью и селективностью химических превращений, реакции проводятся при температурах и давлениях, далеких от оптимальных, организация осуществления химических реакций в реакторах не обеспечивает требуемых степеней превращений. Нагрев растворителя для перевода его в сверхкритическое состояние производится вместе с растворенным в нем реагентом, в результате, растворенный реагент проходит вместе с водой много стадий нагревания, сопровождаемое различными скоростями химических превращений и селективностью. В итоге, по достижении флюидом своего сверхкритического состояния реагент частично прореагирует.
Наиболее близкими являются изобретения, в которых предлагаются различные реакторы и процессы окисления отходов и материалов в сверхкритической воде [US Pat. 5558783, Sep.24, 1996; US Pat. 5591415, Jan. 7, 1997; US Pat. 6264844, Jul. 24, 2001].
В этих патентах предлагается использовать проточный трубчатый реактор (Us Pat. 6264844, Jul. 24, 2001), выполненный в виде прямой трубы, для процессов окисления в СКВ (недостатки: сложно поддерживать изотермичность реакционной смеси, состав меняется по длине реактора): проточный реактор в виде сосуда высокого давления (реактор смешения) (US Pat. 5591415, Jan.7, 1997). К недостаткам такого типа реактора, как и практически любого реактора смешения, можно отнести трудности в достижении больших времен контакта реакционной смеси, что приводит к достижению невысоких степеней превращения.
Известен способ осуществления реакций окисления горючих материалов в сверхкритической воде (WO 01/96247, 20.12.2001). Здесь в качестве окислителя используется перекись водорода, воздух, кислород или их комбинации.
Известен способ осуществления реакций окисления горючих материалов в докритической воде, принятый нами за прототип [WO 91/11394, Aug. 8, 1991]. Здесь, в качестве окислителя используются воздух, кислород, кислородосодержащий газ, перекись водорода, азотная кислота и перхлорат.
К недостаткам способа осуществления химических реакций окисления прототипа можно отнести следующее: давление ниже критического при температуре выше сверхкритической температуры воды.
Изобретение решает задачу высокоэффективного осуществления реакций окисления органических соединений в сверхкритической воде в реакторах при проведении процессов, во-первых, уничтожения и утилизации токсичных и вредных веществ, во-вторых, синтеза новых соединений.
Задача решается способом осуществления реакций окисления органических соединений, по которому топливо и окислитель через устройство смешения подают в каталитический пакет, полученные продукты окисления с выхода каталитического пакета направляют в объем смещения на лопасти мешалки, в продукты окисления после каталитического пакета подают реагенты, содержащие органические соединения и окислитель, полученные продукты реакции подают в трубчатую часть реактора для их полного окисления, при этом окисление органических соединений проводят в сверхкритической воде.
В качестве окислителя используют нитрат аммония, или смесь нитрата аммония и воздуха, или смесь нитрата аммония и кислорода, или смесь нитрата аммония и перекиси водорода.
Часть окислителя можно подавать непосредственно в трубчатую часть реактора.
Основные идеи практической реализации осуществления химических реакций окисления в сверхкритических флюидах, в частности воде, предложенные в настоящем изобретении, заключаются в том, что, во-первых, в качестве окислителя органических соединений используются растворимые в воде неорганические соли нитрата аммония или в сочетании с кислородом, воздухом, перекисью водорода или перхлоратом; во-вторых, предложенная конструкция реактора позволяет достигать гарантированного полного окисления целевых органических соединений.
Принципиальная схема устройства, отражающего основные признаки изобретения, представлена на Фиг.1, где 1 – корпус реактора смешения, 2 – трубчатый реактор вытеснения, 3 – каталитический пакет, 4 – мешалка, 5 – подача топлива, 6, 7 и 9 – подача окислителя, 8 – устройство подачи реагентов, 10 – устройство смешения и ввода реакционной смеси, 11 – устройство ввода реакционной смеси в трубчатый реактор, 12 – устройство ввода орошающей воды, 13 – устройство вывода орошающей воды, 14 – устройство вывода продуктов реакции.
Предложенный реактор для проведения процессов полного, селективного окисления в сверхкритической воде в присутствии окислителя представляет собой последовательное сочетание объема смешения высокого давления 1 и трубчатого объема вытеснения 2, расположенного в центральной части объема смешения реактора.
Предлагаемый способ осуществляют следующим образом.
Топливо 5 и окислитель 6 поступают в устройство смешения, затем в каталитический пакет 3, где происходит окисление топлива с выделением тепла. Продукты окисления с выхода каталитическою пакета направляются на лопасти мешалки 4, вращая ее, тем самым обеспечивая изотермичность и хорошее перемешивание внутри объема реактора. В струю горячего газа после каталитического пакета подаются водные отходы 7, содержащие органические и неорганические соединения, и окислитель 8. В результате хорошего перемешивания и высокой температуры, близкой к критической температуре воды, органические отходы окисляются. Образующиеся неорганические соли выпадают из сверхкритического раствора и вследствие хорошей циркуляции потока в объеме реактора попадают в воду на дне объема реактора, в которой они растворяются и выводятся из реактора. Орошающая вода поступает через вводы 12 в нижнюю часть реактора и циркулируется насосом 13. Очищенные от солей продукты реакции через распределительный приемник 11 поступают в трубчатую часть реактора 2, где происходит полное окисление всех исходных реагентов. При необходимости, для достижения 100% степени превращения, в трубчатую часть реактора вводится дополнительное количество окислителя 9. Такое парциальное введение окислителя позволяет снизить избыток кислорода в объеме реактора и тем самым приводит к снижению коррозии стенок реактора. Продукты реакции выходят из реактора через выход 14.
Ниже приведены примеры осуществления способа.
Пример 1.
Окисление глицерина нитратом аммония в присутствии кислорода в СКВ.
Топливо (ацетон) и окислитель (кислород) в избытке поступают в каталитический пакет 3, где происходит полное окисление топлива с выделением тепла. В струю горячего газа после каталитического пакета подают водный раствор глицерина 7 и растворенный в воде окислитель (нитрат аммония) 8.
Реакция окисления глицерина в присутствии двух окислителей протекает в две стадии:
С3Н8О3+0.5O2=3СH3СООН
СН3СООН+4 NH4NO3=4N2+2СО2+10Н2O
Продукты реакции из объема смешения через распределительный приемник 11 поступают в трубчатую часть реактора, где происходит полное окисление уксусной кислоты (промежуточный продукт).
Пример 2.
Окисление диметилформамида нитратом аммония в СКВ.
Топливо (ацетон) 5 и окислитель (воздух или кислород) 6 в количестве, необходимом только для полного окисления топлива, подают в каталитический пакет 3, где происходит полное окисление топлива с выделением тепла. В струю продуктов полного окисления топлива после каталитического пакета подают водный раствор диметилформамида 7 и растворенный в воде нитрат аммония (окислитель) 8.
Превращения диметилформамида происходят в несколько стадий, две из которых являются гидролизом и прямым окислением:
C3H7ON+Н2O=C2H7N+НСООН
C2H7N+2H2O=NH3+2СH3OH
НСООН+NH4NO3=N2+СО2+3Н2О
СН3ОН+3NH4NO3+3N2+СО2+8Н2O
Продукты реакции из объема смешения через распределительный приемник 11 поступают в трубчатую часть реактора, где происходит полное окисление реактантов.
Пример 3.
Окисление сложной смеси органических соединений смесью нитрата аммония и воздуха в СКВ.
Топливо (ацетон) и окислитель (воздух) в избытке поступают в каталитический пакет 3, где происходит полное окисление топлива с выделением тепла. В струю горячего газа после каталитического пакета подают водный раствор нижеприведенной смеси органических соединений 7 и растворенный в воде окислитель (нитрат аммония) 8.
Состав отходов изменяется в пределах:
| Диметилформамид |
65-75% |
| Уксусная кислота |
15-25% |
| Этанол |
4-10% |
| Толуол |
2-5% |
| Неидентифицированные примеси |
до 2% |
| Вода |
до 8% |
Неорганические отходы содержат около 25% нитрата аммония и примеси других солей, в основном сульфатов.
В ходе проведенных исследований отбирают пробы раствора на анализ, по результатам которого оценивают степень окисления органических веществ (показатель «химическое потребление кислорода») и степень разложения нитрата аммония по показателям «содержание нитратов NO3 – и содержание аммонийного азота в катионе NH4 +».
Результаты представлены в таблице 1.
| Таблица 1. |
| Показатели |
На входе |
На выходе |
Степень превращения, % |
Температура, °С |
Давление, МПа |
| В реакторе |
После реактора |
|
| Содержание нитроэфиров, мг/л |
194 |
нет |
100 |
634 |
577 |
24,2 |
ХПК, мг
О2/л |
40372 |
308,3 |
99,2 |
То же |
| Азот аммиака, мг/л |
5936 |
58,8 |
99,0 |
То же |
| Содержание нитратов, мг/л |
26106 |
592,9 |
97,7 |
То же |
| Содержание сульфатов, (SO4 =), мг/л |
223,8 |
19,2 |
91,4 |
То же |
| Значение РН |
4,05 |
6,54 |
– |
То же |
На Фиг.2 представлен график, который демонстрирует стабильность в поведении параметров процесса при окислении воздухом сточных вод с производства смеси нитроглицерина и динитрата диэтиленгликоля в присутствии ацетона и нитрата аммония.
Пример 4.
Окисление нитроэфиров смесью окислителей нитрата аммония и перекиси водорода. Топливо (ацетон) 5 и окислитель (воздух или кислород) 6 в количестве, необходимом только для полного окисления топлива, подают в каталитический пакет 3, где происходит полное окисление топлива с выделением тепла. В струю продуктов полного окисления топлива после каталитического пакета подают водный раствор смеси нитроэфиров и нитрата аммония 7 и 30% перекиси водорода (окислитель) 8. Непрореагировавшие реагенты и продукты реакции из объема смешения реактора через распределительный приемник 11 поступают в трубчатую часть реактора, где происходит их полное окисление.
Результаты превращений приведены в таблице 2.
| Таблица 2. |
| Показатели |
На входе |
На выходе |
Степень превращения, % |
Температура, °С |
Давление, МПа |
| В реакторе |
После реактора |
|
ХПК, мг
О2/л |
95277,8 |
103,5 |
99,89 |
652 |
434
437 |
25,2
27,8 |
| Азот аммиака, мг/л |
3206,4 |
231,4 |
92,8 |
То же |
| Содержание нитратов (NO3 –), мг/л |
9728,0 |
0,86 |
99,99 |
То же |
| Содержание нитритов (NO2 –), мг/л |
23,49 |
0,49 |
97,9 |
То же |
| Содержание сульфатов, (SO4 =), мг/л |
нет |
нет |
— |
То же |
| Значение РН |
3,85 |
7,24 |
— |
То же |
Пример 5.
Синтез терефталевой кислоты путем окисления пара-ксилола.
Синтез терефталевой кислоты осуществляют при окислении пара-ксилола перекисью водорода в сверхкритической воде без катализатора, при температуре 270-500°С и давлении 221-300 бар. Почти 100%-ная конверсия пара-ксилола наступает через 15-20 мин, достигается селективность процесса выше 90%.
Топливо 5 и окислитель 6 в количестве, необходимом только для полного окисления топлива, поступают в устройство смешения, затем в каталитический пакет 3, где происходит окисление топлива с выделением тепла. В струю горячего газа после каталитического пакета подают пара-ксилол 7 и 30% перекись водорода (окислитель) 8. Непрореагировавшие реагенты и продукты реакции из объема смешения реактора через распределительный приемник 11 поступают в трубчатую часть реактора. Для достижения полного окисления в трубчатую часть реактора вводят дополнительное количество окислителя 9. Продукты реакции – терефталиевая кислота – выходят из реактора через выход 14.
Таким образом, приведенные примеры показывают, что изобретение позволяет высокоэффективно осуществлять химические реакции в сверхкритической воде и может быть использовано для уничтожения и утилизации токсичных и вредных веществ и отходов, синтеза новых соединений.
Формула изобретения
1. Способ осуществления реакций окисления органических соединений, отличающийся тем, что топливо и окислитель через устройство смешивания подают в каталитический пакет, полученные продукты окисления с выхода каталитического пакета направляют в объем смешения на лопасти мешалки и в продукты окисления после каталитического пакета подают реагенты, содержащие органические соединения и окислитель, полученные продукты реакции подают в трубчатую часть реактора для их полного окисления, при этом окисление органических соединений проводят в сверхкритической воде.
2. Способ по п.1, отличающийся тем, что в качестве окислителя используют нитрат аммония.
3. Способ по п.1, отличающийся тем, что в качестве окислителя используют смесь нитрата аммония и воздуха.
4. Способ по п.1, отличающийся тем, что в качестве окислителя используют смесь нитрата аммония и кислорода.
5. Способ по п.1, отличающийся тем, что в качестве окислителя используют смесь нитрата аммония и перекиси водорода.
6. Способ по п.1, отличающийся тем, что часть окислителя подают непосредственно в трубчатую часть реактора.
РИСУНКИ
|
|