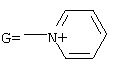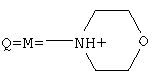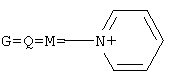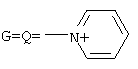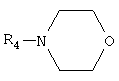Патент на изобретение №2308466
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
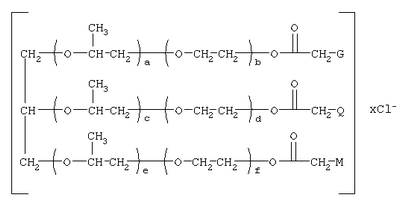
(54) [(ГЕТЕРИЛОНИО)(АММОНИО)МЕТИЛКАРБОНИЛОКСИПОЛИ(АЛКИЛЕНОКСИ)] ПРОПАН ХЛОРИДЫ, ОБЛАДАЮЩИЕ ФУНГИЦИДНОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ
(57) Реферат:
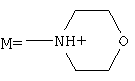
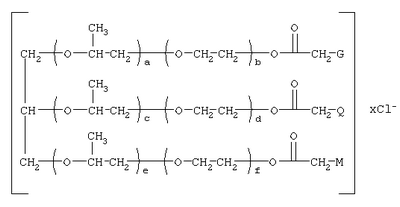
Изобретение относится к соединениям, обладающим фунгицидной активностью, а именно к [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропанхлоридам, общей формулы: где: при b+d+f=10, x=3; при G=Q=M=-N+H2CH2CH2NH2, а+с+е=49, b+d+f=9, x=3; при G=Q=M=-N+H2CH2CH2NH2, а+с+е=55, b+d+f=10, x=3; при G=Q=-N+H2CH2CH2NH2, M=-Cl, a+c+e=49, b+d+f=9, x=2; при G=Q=-N+H2CH2CH2NH2, М=-Cl, а+с+е=55, b+d+f=10, x=2; при G=Q=M=-N+H2CH2CH2OH, а+с+е=49, b+d+f=9, х=3; при G=Q=M=-N+H2CH2CH2OH, а+с+е=55, b+d+f=10, x=3; при
Изобретение относится к органической химии, а именно к синтезу неизвестных ранее [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропанхлоридов, обладающих фунгицидной активностью, которые могут быть использованы для борьбы с грибковыми поражениями пчел в ветеринарии и сельском хозяйстве. Особенностью предлагаемого ряда соединений является то, что они одновременно содержат сложноэфирные и полиоксиалкильные (полиоксиэтильные и/или полиоксипропильные) группировки. Известны четвертичные аммониевые соединения, содержащие сложноэфирные группировки с алифатическими длинноцепочечными радикалами, представляющие собой N,N-диметил-N-алкил-N-[алкоксикарбонилметил]аммоний хлориды, формулы:
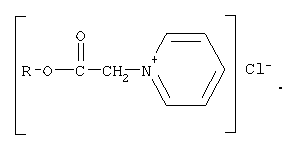
Известны четвертичные гетерилониевые соединения, содержащие сложноэфирную группировку и гетерилониевый фрагмент гетероциклического амина – пиридина, являющиеся N-[алкилоксикарбонилметил]пиридиний хлоридами, формулы:
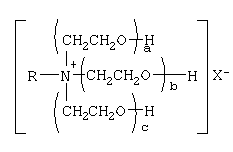
Известны так же четвертичные аммониевые соединения, содержащие один или несколько полиоксиэтильных фрагментов. Такими, например, являются четвертичные аммониевые соединения, включающие в структуру аммонийного катиона три полиоксиэтильных фрагмента и имеющие общую формулу:
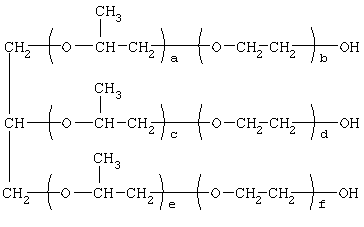
Наиболее близкими по структуре к предлагаемым соединениям являются N-[изононилфеноксиполи(этиленокси)карбонилметил]аммоний хлориды общей формулы: [Патент 1531416 РФ. МКИ С 07 С 87/30. Опубл. 10.04.1995. Фахретдинов П.С., Романов Г.В. и др. Способ получения ингибиторов коррозии углеродистых сталей в минерализованных сероводородсодержащих водных средах, проявляющих фунгистатическое, бактериостатическое и дезинфицирующее действие] Недостатком соединений, заявляемых в этом известном решении, является то, что они, проявляя бактеристатическое и фунгистатическое действие, не обладают при этом фунгицидной активностью. Технический результат настоящего изобретения – синтез новых [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропанхлоридов, обладающих фунгицидной активностью, и способ их получения. Разработанные нами [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропанхлориды содержат от одного до трех одинаковых или разных гетерилониевых и/или аммониевых центров, а также одновременно включают в свою структуру сложноэфирные и полиоксиалкильные (полиоксиэтильные и/или полиоксипропильные) фрагменты общей формулы: где: при а+с+е = общая степень оксипропилирования, равная 49; b+d+f = общая степень оксиэтилирования, равная 9; х=3; при а+с+е = общая степень оксипропилирования, равная 55; b+d+f = общая степень оксиэтилирования, равная 10; х=3; при
а+с+е = общая степень оксипропилирования, равная 49; b+d+f = общая степень оксиэтилирования, равная 9; х=3; при
а+с+е = общая степень оксипропилирования, равная 55; b+d+f = общая степень оксиэтилирования, равная 10; х=3; при а+с+е = общая степень оксипропилирования, равная 49; b+d+f = общая степень оксиэтилирования, равная 9; х=3; при а+с+е = общая степень оксипропилирования, равная 55; b+d+f = общая степень оксиэтилирования, равная 10; х=3; при G=Q=М=-N+H2CH2CH2NH2; а+с+е = общая степень оксипропилирования, равная 49; b+d+f = общая степень оксиэтилирования, равная 9; х=3; при G=Q=М=-N+H2CH2CH2NH2; а+с+е = общая степень оксипропилирования, равная 55; b+d+f = общая степень оксиэтилирования, равная 10; х=3; при G=Q=-N+H2CH2CH2NH2; М=-Cl а+с+е = общая степень оксипропилирования, равная 49; b+d+f = общая степень оксиэтилирования, равная 9; х=2; при G=Q=-N+H2CH2CH2NH2; М=-Cl а+с+е = общая степень оксипропилирования, равная 55; b+d+f = общая степень оксиэтилирования, равная 10; х=2 при G=Q=М=-N+Н2CH2СН2ОН; а+с+е = общая степень оксипропилирования, равная 49; b+d+f = общая степень оксиэтилирования, равная 9; х=3; при G=Q=М=-N+Н2СН2СН2ОН; а+с+е = общая степень оксипропилирования, равная 55; b+d+f = общая степень оксиэтилирования, равная 10; х=3. при
а+с+е = общая степень оксипропилирования, равная 49; b+d+f = =общая степень оксиэтилирования, равная 0; х=3; при
а+с+е = общая степень оксипропилирования, равная 55; b+d+f = общая степень оксиэтилирования, равная 0; х=3. Заявляемые нами [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропанхлориды являются новыми, не известными ранее соединениями, обладающими фунгицидной активностью. Известен способ получения аммониевых соединений, содержащих сложноэфирные и полиоксиэтильные группировки, например, N-[изононилфеноксиполи(этиленокси)карбонилметил]аммоний хлоридов, общей формулы: где: R1=R2=СН3, алкил фракции С7-С9; R3 = алкил фракции С7-С9, алкил фракции С10-С16, алкил фракции С15-C18; n=3, 10; путем взаимодействия монохлоруксусной кислоты со спиртовой компонентой, которой являются изононилфеноксиполиэтиленгликоли, общей формулы:
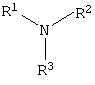
где: n=3, 10; и последующей обработкой аминами, общей формулы:
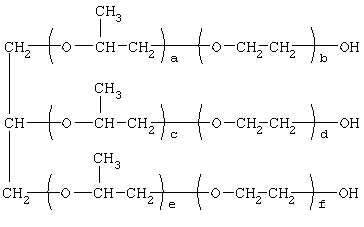
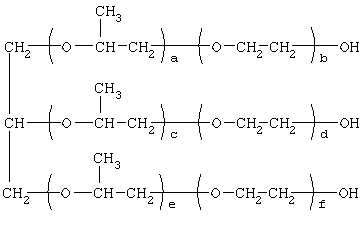
где: R1=R2=СН3, алкил фракции С7-С9; R3 = алкил фракции С7-С9, алкил фракции С10-C16 или алкил фракции C15-C18 [Патент 1531416 РФ. МКИ С 07 С 87/30. Опубл. 10.04.1995] Для заявляемых нами [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропанхлоридов предлагается способ их получения путем взаимодействия 1,2,3-трис[гидроксиполи(алкиленокси)]пропанов, формулы:
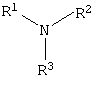
где: а+с+е = общая степень оксипропилирования, равная 49-55; b+d+f = общая степень оксиэтилирования, равная 0-10, с монохлоруксусной кислотой в присутствии кислотных катализаторов в среде кипящего органического растворителя, с азеотропным удалением образовавшейся воды и с последующей обработкой при нагревании полученного продукта алифатическими аминами в, общей формулы:
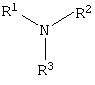
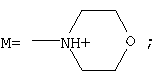
где: R1=R2=H; R3=СН2СН2NH2, СН2СН2ОН; или смесью гетероциклических аминов – ряда морфолина, формулы:
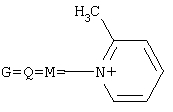
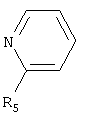
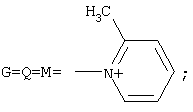
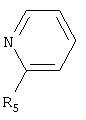
где R4=Н; и ряда пиридинов, формулы:
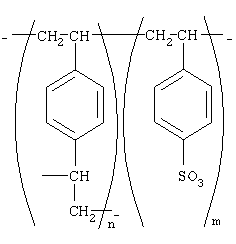
где R5=Н, СН3. Обработку аминосоединениями продукта взаимодействия гидроксильного производного пропана с монохлоруксусной кислотой ведут при температуре 60-90°С. В случае, когда для обработки продукта взаимодействия гидроксильного производного пропана с монохлоруксусной кислотой используют аминосоединения алифатического ряда, выдерживаются мольные соотношения реагентов – гидроксильное производное пропана:монохлоруксусная кислота:алифатические амины=1:3,0-3,2:2,0-3,1 соответственно. В случае, когда для обработки продукта взаимодействия производного пропана с монохлоруксусной кислотой используют гетероциклические аминосоединения пиридинового ряда, выдерживаются мольные соотношения реагентов – гидроксильное производное пропана:монохлоруксусная кислота: пиридины=1:3,0-3,2:3,0-3,1 соответственно. В случае, когда для обработки продукта взаимодействия гидроксильного производного пропана с монохлоруксусной кислотой используют смеси гетероциклических аминосоединений – морфолина и пиридина, выдерживаются мольные соотношения реагентов – гидроксильное производное пропана:монохлоруксусная кислота:морфолин:пиридин=1:3,0-3,2:1,0-2,1:1,0-2,1 соответственно, при этом суммарное количество морфолина и пиридина составляет 3,0-3,2 моля. В качестве исходных 1,2,3-трис[гидроксиполи(алкиленокси)] пропанов, наряду с индивидуальными соединениями, можно использовать выпускаемые нефтехимической промышленностью различные оксиэтилированные и/или оксипропилированные глицерины, в том числе: Лапрол 3003 (ТУ 2226-022-10488057-95) с общей степенью оксипропилирования, равной 49-55, и общей степенью оксиэтилирования, равной 0; Лапрол 3603-2-12 (ТУ 2226-015-10488057-94) с общей степенью оксипропилирования, равной 49-55, и общей степенью оксиэтилирования, равной 9-10; Лапрол 5003-2-15 (ТУ 2226-006-10488057-94) с общей степенью оксипропилирования, равной 66-76, и общей степенью оксиэтилирования, равной 15-18. Монохлоруксусная кислота используется в виде индивидуального соединения или технического продукта по ТУ 2431-288-05763441-99. В качестве кислотного катализатора используют Н+ – форму катионообменной смолы КУ-2-8, которая представляет собой твердые, ограничено набухающие высокомолекулярные полисульфокислоты сополимера стирола с дивинилбензолом, общей формулы:
и выпускается в различных модификациях, отличающихся количеством дивинилбензола в сополимере. Например, марки катионита КУ-2-8 и КУ-2-10 содержат 8% и 10% дивинилбензола соответственно. [Салдадзе К.М., Пашков А.Б., Титов B.C. Ионообменные высокомолекулярные соединения. Под ред. Салдадзе К.М., Москва: Гос. научн.-техн. изд. хим. лит., 1960, с.112-114]. Катионообменная смола КУ-2-8 выпускается по ГОСТ 20298-74. Н+-форма катионообменной смолы КУ 2-8 используется в качестве кислотного катализатора при взаимодействии гидроксильного производного пропана с монохлоруксусной кислотой в количестве 3,0-5,0% масс от веса исходного гидроксильного производного пропана. В качестве органического растворителя при взаимодействии гидроксильного производного пропана с монохлоруксусной кислотой используют ароматический углеводородный растворитель, например, толуол, ксилол, нефрас А-120/200. Под условным обозначением Нефрас А-120/200 нефтехимической промышленностью выпускается сольвент нефтяной тяжелый по ТУ 38-101809-90, получаемый из продуктов каталитического риформинга, содержащий смесь ароматических углеводородов С8-С9 (ксилолы, пропилбензолы, метилэтилбензолы, мезитилен, псевдокумол и др.) Предлагаемый способ получения новых, не известных ранее соединений [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропанхлоридов имеет некоторое сходство со способом получения других рядов четвертичных аммониевых соединений, например N-[изононилфеноксиполи(этиленокси)карбонилметил] аммоний хлоридов [Патент 1531416 РФ. МПК С07С 87/30. Опубл. 10.04.1995]. Но и различия этих двух способов являются существенными. В известном способе в качестве спиртовой компоненты используют изононилфеноксиполиэтиленгликоли, общей формулы:
а в качестве аминосоединений – длинноцепочечные алифатические третичные амины типа N,N,N-триалкиламинов фракции c7-С9, N,N-диметил-N-алкиламинов фракции С10-C16 или фракции C15-C18. В предлагаемом способе в качестве спиртовой компоненты используют гидроксилсодержащие производные пропана, представляющие собой 1,2,3-трис[гидроксиполи(алкиленокси)]пропаны, общей формулы:
где: а+с+е=общая степень оксипропилирования, равная 49-55; b+d+f=общая степень оксиэтилирования, равная 0-10, Для обработки продукта взаимодействия гидроксилсодержащего производного пропана с монохлоруксусной кислотой используют алифатические аминосоединения, формулы:
где: R1=R2=H; R3=CH2CH2NH2, CH2CH2OH; или гетероциклические ряда пиридинов, формулы
где R5=Н, СН3. или смесь гетероциклических аминов ряда морфолина, формулы
где R4=Н; и пиридина. Обработку аминосоединениями продукта взаимодействия гидроксильного производного пропана с монохлоруксусной кислотой ведут при температуре 60-90°С. В случае, когда для обработки продукта взаимодействия гидроксильного производного пропана с монохлоруксусной кислотой используют аминосоединения алифатического ряда, выдерживаются мольные соотношения реагентов – гидроксильное производное пропана:монохлоруксусная кислота: алифатические амины=1:3,0-3,2:2,0-3,1 соответственно. В случае, когда для обработки продукта взаимодействия производного пропана с монохлоруксусной кислотой используют гетероциклические аминосоединения пиридинового ряда, выдерживаются мольные соотношения реагентов – гидроксильное производное пропана:монохлоруксусная кислота: пиридины=1,0:3,0-3,2:3,0-3,1 соответственно. В случае, когда для обработки продукта взаимодействия гидроксильного производного пропана с монохлоруксусной кислотой используют смеси гетероциклических аминосоединений – морфолина и пиридина, выдерживаются мольные соотношения реагентов – гидроксильное производное пропана: монохлоруксусная кислота: морфолин: пиридин=1:3,0-3,2:1,0-2,1:1,0-2,1 соответственно, при этом суммарное количество морфолина и пиридина составляет 3,0-3,2 моля. Приведенные данные подтверждают, что предлагаемый способ с использованием в качестве исходных гидроксилсодержащих продуктов не использовавшихся ранее 1,2,3 – трис[гидроксиполи(алкиленокси)] пропанов, а в качестве аминосоединений – алифатических аминов, гетероциклических аминов ряда морфолинов и пиридинов вышеуказанных формул позволяет получать неизвестные ранее [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропанхлориды, обладающие фунгицидной активностью. Таким образом, заявляемые [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропанхлориды являются новыми и способ их получения является так же новым. Предлагаемый способ получения заявляемых соединений является несложным, не требующим особых условий и специального оборудования и может быть осуществлен практически на любом химическом производстве. Приводим конкретные примеры выполнения изобретения. Пример 1. Трис[(2-метилпиридинио)метилкарбонилоксиполи(этиленокси)поли(2-метилэтиленокси)]пропантрихлорид с общей степенью оксипропилирования, равной 49, и общей степенью оксиэтилирования, равной 9. Смесь 110.0 г (3.3·10-2 г·моля) 1,2,3-трис[гидроксиполи(2-метил-этиленокси)]пропана с общей степенью оксипропилирования, равной 49, и общей степенью оксиэтилирования, равной 9, 9.4 г (9.9·10-2 г·моля) монохлоруксусной кислоты, 220.0 мл толуола; 3.3 г (3,0% масс от веса гидроксильного производного пропана) Н+-формы катионообменной смолы КУ-2-8 (в качестве кислотного катализатора) кипятят с ловушкой Дина-Старка и обратным холодильником до полного прекращения выделения воды и снижения кислотного числа реакционной массы до величин, меньших и равных 2 мг КОН/г. Величины кислотного числа в пробах определяют обычным титрованием спиртовым раствором КОН. Время реакции 15-16 часов. От реакционной массы отфильтровывают катализатор в вакууме, удаляют органический растворитель (толуол) и не вступившую в реакцию монохлоруксусную кислоту. Смешивают полученный продукт реакции с 9.2 г(9.9·10-2 г·моля) 2-метилпиридина и при перемешивании выдерживают при температуре 60-90°С в течение 8-10 часов. Контроль реакции ведут титрометрически, определяя содержание свободных аминов потенциометрическим титрованием спиртовым раствором соляной кислоты. Реакцию прекращают при остаточном содержании свободных аминов менее 0,2%. Отгоняют в вакууме растворитель. Выход 125,3 г (99,0% от теор.) вязкой светло-желтой жидкости. ИК-спектр: Пример 2. Трис[(2-метилпиридинио)метилкарбонилоксиполи(этиленокси)поли(2-метилэтиленокси)]пропантрихлорид с общей степенью оксипропилирования, равной 55, и общей степенью оксиэтилирования, равной 10. Получен аналогично примеру 1 из 130.0 г (3.5·10-2 г·моля) 1,2,3-трис[гидроксиполи(этиленокси)поли(2′-метилэтиленокси)]пропана с общей степенью оксипропилирования, равной 55 и общей степенью оксиэтилирования, равной 10; 10.6 г (11.1·10-2 г·моля) монохлоруксусной кислоты; 260.0 мл нефраса А-120/200; 6.5 г (5,0% масс от веса гидроксильного производного пропана) Н+-формы катионообменной смолы КУ-2-8 (в качестве кислотного катализатора); 10.4 г(11.1·10-2 г·моля) 2-метилпиридина. Выход 146.4 г (99.5% от теор.) вязкой светло-оранжевой жидкости. ИК-спектр: Пример 3. [(Пиридинио)метилкарбонилоксиполи(этиленокси)поли(2′-метилэтиленокси)]-бис[(морфолинио)метилкарбонилоксиполи(этиленокси)поли(2′-метилэтиленокси)] пропантрихлорид с общей степенью оксипропилирования, равной 49, и общей степенью оксиэтилирования, равной 9. Получен аналогично примеру 1 из 120.0 г (3.6·10-2 г·моля) 1,2,3-трис[гидроксиполи(этиленокси)поли(2′-метилэтиленокси)]пропана с общей степенью оксипропилирования, равной 49, и общей степенью оксиэтилирования, равной 9; 10.2 г (10.1·10-2 г·моля) монохлоруксусной кислоты; 240 мл ксилола; 3.6 г (3,0% масс от веса гидроксильного производного пропана) Н+-формы катионообменной смолы КУ-2-8 (в качестве кислотного катализатора); 6.3 г (7.2·10-2 г·моля) морфолина и 2.8 г (3.6·10-2 г·моля) пиридина. Выход 136.4 г (99.8% от теор.) вязкой жидкости красного цвета. ИК-спектр: Пример 4. [(Пиридинио)метилкарбонилоксиполи(этиленокси)поли(2′-метилэтиленокси)]-бис[(морфолинио)метилкарбонилоксиполи(этиленокси)поли(2′-метилэтиленокси)]пропантрихлорид с общей степенью оксипропилирования, равной 55, и общей степенью оксиэтилирования, равной 10. Получен аналогично примеру 1 из 135.0 г (3.6·10-2 г·моля) 1,2,3-трис[гидроксиполи(этиленокси)поли(2′-метилэтиленокси)]пропана с общей степенью оксипропилирования, равной 55, и общей степенью оксиэтилирования, равной 10, 11.0 г (12.0·10-2 г·моля) монохлоруксусной кислоты; 270.0 мл толуола; 6.8 г (5,0% масс от веса гидроксильного производного пропана) H+-формы катионообменной смолы КУ 2-8 (в качестве кислотного катализатора); 6.9 г (8.0·10-2 г·моля) морфолина и 3.2 г (4.0·10-2 г·моля) пиридина. Выход 151.7 г (99.6% от теор.) вязкой жидкости красного цвета. ИК-спектр: Пример 5. Трис[(пиридинио)метилкарбонилоксиполи(этиленокси)поли(2-метилэтиленокси)]пропан трихлорид с общей степенью оксипропилирования, равной 49, и общей степенью оксиэтилирования, равной 9. Получен аналогично примеру 1 из 110.0 г (3.3·10-2 г·моля) 1,2,3-трис[гидроксиполи(этиленокси)поли(2-метилэтиленокси)]пропана с общей степенью оксипропилирования, равной 49, и общей степенью оксиэтилирования, равной 9; 9.4 г (9.9·10-2 г·моля) монохлоруксусной кислоты; 220.0 мл толуола; 3.3 г (3,0% масс от веса гидроксильного производного пропана) H+– формы катионообменной смолы КУ-2-8 (в качестве кислотного катализатора); 7.8 г (9.9·10-2 г·моля) пиридина. Выход 123.9 г (99.0% от теор.) вязкой жидкости светло-красного цвета. ИК-спектр: Пример 6. Трис[(пиридинио)метилкарбонилоксиполи(этиленокси)поли(2-метилэтиленокси)] пропантрихлорид с общей степенью оксипропилирования, равной 55, и общей степенью оксиэтилирования, равной 10. Получен аналогично примеру 1 из 130.0 г (3.5·10-2 г·моля) 1,2,3-трис[гидроксиполи(этиленокси)поли(2′-метилэтиленокси)]пропана с общей степенью оксипропилирования, равной 55, и общей степенью оксиэтилирования, равной 10; 10.6 г (11.0·10-2 г·моля) монохлоруксусной кислоты; 260.0 мл ксилола; 6.5 г (5,0% масс от веса гидроксильного производного пропана) Н+-формы катионообменной смолы КУ-2-8 (в качестве кислотного катализатора); 8.8 г (11.00·10-2 г·моля) пиридина. Выход 145.1 г (99.5% от теор.) вязкой жидкости светло-красного цвета. ИК-спектр: Пример 7. Трис[(2-аминоэтиламмонио)метилкарбонилоксиполи(этиленоки)поли(2′-метилэтиленокси)]пропантрихлорид с общей степенью оксипропилирования, равной 49, и общей степенью оксиэтилирования, равной 9. Получен аналогично примеру 1 из 180.0 г (5.4·10-2 г·моля) 1,2,3-трис [гидроксиполи(этиленокси)поли(2-метилэтиленокси)] пропана с общей степенью оксипропилирования, равной 49, и общей степенью оксиэтилирования, равной 9; 15.3 г (16.2·10-2 г·моля) монохлоруксусной кислоты; 360 мл толуола; 5.4 г (3,0% масс от веса гидроксильного производного пропана) Н+-формы катионообменной смолы КУ-2-8 (в качестве кислотного катализатора); 9.7 г (16.2·10-2 г·моля) этилендиамина. Выход 200.1 г (99.7% от теор.) вязкой жидкости серого цвета. ИК-спектр: Пример 8. Трис[(2-аминоэтиламмонио)метилкарбонилоксиполи(этиленокси)поли(2′-метилэтиленокси)]пропантрихлорид с общей степенью оксипропилирования, равной 55, и общей степенью оксиэтилирования, равной 10. Получен аналогично примеру 1 из 200.0 г (5.4·10-2 г·моля) 1,2,3-трис [гидроксиполи(этиленокси)поли(2-метилэтиленокси)] пропана с общей степенью оксипропилирования, равной 55, и общей степенью оксиэтилирования, равной 10; 16.2 г (17.1·10-2 г·моля) монохлоруксусной кислоты, 360.0 мл ксилола; 10.0 г (5,0% масс от веса гидроксильного производного пропана) Н+-формы катионообменной смолы КУ-2-8 (в качестве кислотного катализатора); 10.3 г (17.2·10-2 г·моля) этилендиамина. Выход 220.2 г (99.4% от теор.) вязкой жидкости серого цвета. ИК-спектр: Пример 9. Бис[(2-аминоэтиламмонио)метилкарбонилоксиполи(этиленокси)поли(2′-метилэтиленокси)] [хлорацетилоксикарбонилоксиполи(этиленокси)поли(2′-метилэтиленокси)]пропандихлорид с общей степенью оксипропилирования, равной 49, и общей степенью оксиэтилирования, равной 9. Получен аналогично примеру 1 из 250.0 г (7.5·10-2 г·моля) 1,2,3-трис[гидроксиполи(этиленокси)поли(2′-метилэтиленокси)]пропана с общей степенью оксипропилирования, равной 49, и общей степенью оксиэтилирования, равной 9; 21.3 г (22.5·10-2 г·моля) монохлоруксусной кислоты; 500.0 мл нефраса А-120/200; 7.5 г (3,0% масс от веса гидроксильного производного пропана) Н+-формы катионообменной смолы КУ-2-8 (в качестве кислотного катализатора); 9.0 г (15.0·10-2 г·моля) этилендиамина. Выход 274.6 г (99.0% от теор.) вязкой жидкости серого цвета. ИК-спектр: Пример 10. Бис[(2-аминоэтиламмонио)метилкарбонилоксиполи(этиленокси)поли(2′-метилэтиленокси)] [хлорацетилоксикарбонилоксиполи(этиленокси)поли(2′-метилэтиленокси)]пропандихлорид с общей степенью оксипропилирования, равной 55, и общей степенью оксиэтилирования, равной 10. Получен аналогично примеру 1 из 300.0 г (8.1·10-2 г·моля) 1,2,3-трис[гидроксиполи(этиленокси)поли(2′-метилэтиленокси)]пропана с общей степенью оксипропилирования, равной 55, и общей степенью оксиэтилирования, равной 10; 24.4 г (25.8·10-2 г·моля) монохлоруксусной кислоты; 600.0 мл толуола; 15.0 г (5,0% масс от веса гидроксильного производного пропана) H+-формы катионообменной смолы КУ-2-8 (в качестве кислотного катализатора); 10.6 г (17.7·10-2 г·моля) этилендиамина. Выход 325.2 г (99.7% от теор.) вязкой жидкости серого цвета. ИК-спектр: Пример 11. Трис[(2-гидроксиэтиламмонио)метилкарбонилоксиполи(этиленокси)поли(2-метилэтиленокси)]пропантрихлорид с общей степенью оксипропилирования, равной 49, и общей степенью оксиэтилирования, равной 9. Получен аналогично примеру 1 из 73.0 г (2.2·10-2 г·моля) 1,2,3-трис [гидроксиполи(этиленокси)поли(2-метилэтиленокси)] пропана с общей степенью оксипропилирования, равной 49, и общей степенью оксиэтилирования, равной 9; 6.2 г (6.6·10-2 г·моля) монохлоруксусной кислоты; 150 мл нефраса А-120/200; 2.2 г (3,0% масс от веса гидроксильного производного пропана) Н+-формы катионообменной смолы КУ-2-8 (в качестве кислотного катализатора); 4.0 г (6.6·10-2 г·моля) 2-гидроксиэтиламина. Выход 81.6 г (99.9% от теор.) вязкой жидкости желтого цвета. ИК-спектр: Пример 12. Трис[(2-гидроксиэтиламмонио)метилкарбонилоксиполи(этиленокси)поли(2-метилэтиленокси)]пропантрихлорид с общей степенью оксипропилирования, равной 55, и общей степенью оксиэтилирования, равной 10. Получен аналогично примеру 1 из 75.0 г (2.0·10-2 г·моля) 1,2,3-трис [гидроксиполи(этиленокси)поли(2-метилэтиленокси)] пропана с общей степенью оксипропилирования, равной 55, и общей степенью оксиэтилирования, равной 10; 6.1 г (6.4·10-2 г·моля) монохлоруксусной кислоты; 150.0 мл толуола; 3.8 г (5,0% масс от веса гидроксильного производного пропана) H+-формы катионообменной смолы КУ-2-8 (в качестве кислотного катализатора); 3.9 г (6.4·10-2 г·моля) 2-гидроксиэтиламина. Выход 82.6 г (99.7% от теор.) вязкой жидкости серого цвета. ИК-спектр: Пример 13. [(Морфолинио)метилкарбонилоксиполи(2′-метилэтиленокси)]-бис[(Пиридинио)метилкарбонилоксиполи(2′-метилэтиленокси)]пропантрихлорид с общей степенью оксипропилирования, равной 49. Получен аналогично примеру 1 из 73.0 г (2.5·10-2 г·моля) 1,2,3-трис[гидроксиполи (2′-метилэтиленокси)] пропана с общей степенью оксипропилирования, равной 49, 7.1 г (7.5·10-2 г·моля) монохлоруксусной кислоты, 150 мл ксилола; 2,2 г (3,02% масс от веса гидроксильного производного пропана) Н+-формы катионообменной смолы КУ-2-8 (в качестве кислотного катализатора); 2,2 г (2.5·10-2 г·моля) морфолина и 3.9 г (5.0·10-2 г·моля) пиридина. Выход 84.3 г (99.9% от теор.) вязкой жидкости красного цвета. ИК-спектр: Пример 14. [(Морфолинио)метилкарбонилоксиполи(2′-метилэтиленокси)]-бис[(Пиридинио)метилкарбонилоксиполи(2′-метилэтиленокси)]пропантрихлорид с общей степенью оксипропилирования, равной 55. Получен аналогично примеру 1 из 75,0 г (2,3·10-2 г·моля) 1,2,3-трис[гидроксиполи (2-метилэтиленокси)] пропана с общей степенью с общей степенью оксипропилирования, равной 55, 6,9 г (7,3·10-2 г·моля) монохлоруксусной кислоты, 150,0 мл нефраса А-120/200; 3,8 г (5,0% масс от веса гидроксильного производного пропана) Н+-формы катионобменной смолы КУ-2-8 (в качестве кислотного катализатора); 2,2 г (2,5·10-2 г·моля) морфолина и 3,8 г (4,8·10-2 г·моля) пиридина. Выход 85,1 г.(99,7% от теор.) вязкой жидкости красного цвета. ИК-спектр: Определение фунгицидной активности. Фунгицидную активность предлагаемых соединений исследовали на примере возбудителя аскосфероза (болезни расплода пчел) – Ascosphaera apis, штамм ВГ-8. Испытания проводили по общепринятой в микробиологии методике серийных разведении [Методы экспериментальной химиотерапии/ Под ред. Першина Г.Н. М.: Медицина, 1973. С.318-320; Ведьмина Е.А., Фурер Н.М. Руководство по микробиологии, клинике и эпидемиологии, клинике и эпидемиологии инфекционных болезней. М.: Медицина, 1964, С.608-610] Для опытов использовали взвесь грибов с грибковой нагрузкой 200000 грибковых тел в 1 мл физиологического раствора. Грибковую взвесь разливали в пробирки, содержащие определенные концентрации исследуемых препаратов, в пропорции – 1 часть грибковой взвеси на 1 часть раствора препарата. В качестве эталона сравнения использовали структурный аналог – “Препарат Ф-761” (Патент РФ № 1531416), строение которого приведено выше. В качестве контроля используют то же количество стерильного физиологического раствора. Экспозиции при этом составляют 5, 10, 30, 60 и 120 мин. После экспозиции проводят посев опытных и контрольных материалов на элективную питательную среду – сусло-агар. Инкубацию проводят в термостате при температуре 37°С и наблюдение ведут в течение 14 суток. Результаты исследований фунгицидной активности заявляемых соединений и эталона сравнения представлены в табл.1 Данные табл.1 свидетельствуют, что заявляемые соединения проявляют фунгицидную активность в отношении возбудителя аскоросфероза Ascosphaera apis. Минимальные фунгицидные концентрации этих препаратов составляют 0,25-2,0% при экспозиции 2 часа, в то время, как структурный аналог “Препарат Ф-761”, проявляя фунгицистатическое действие, фунгицидной активностью не обладает. Представленные данные подтверждают преимущества предлагаемых [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропантрихлоридов перед структурным аналогом по фунгицидной активности. Таким образом, предлагаемые [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропантрихлориды являются новыми, обладающими фунгицидной активностью. Предлагаемые соединения могут быть использованы для борьбы с грибковыми поражениями пчел в ветеринарии и сельском хозяйстве.
Формула изобретения
1. [(Гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропан хлориды, формулы
где при а+с+е=общая степень оксипропилирования, равная 49; b+d+f=общая степень оксиэтилирования, равная 9; х=3;
при а+с+е=общая степень оксипропилирования, равная 55; b+d+f=общая степень оксиэтилирования, равная 10; х=3;
при
а+с+е=общая степень оксипропилирования, равная 49: b+d+f=общая степень оксиэтилирования, равная 9; х=3;
при
а+с+е=общая степень оксипропилирования, равная 55; b+d+f=общая степень оксиэтилирования, равная 10;
при а+с+е=общая степень оксипропилирования, равная 49; b+d+f=общая степень оксиэтилирования, равная 9; х=3;
при а+с+е=общая степень оксипропилирования, равная 55; b+d+f=общая степень оксиэтилирования, равная 10; х=3; при G=Q=M=-N+H2CH2CH2NH2; а+с+е=общая степень оксипропилирования, равная 49; b+d+f=общая степень оксиэтилирования, равная 9; х=3; при G=Q=M=-N+H2CH2CH2NH2; а+с+е=общая степень оксипропилирования, равная 55; b+d+f=общая степень оксиэтилирования, равная 10; х=3; при G=Q=-N+H2CH2CH2NH2; М=-Cl; а+с+е=общая степень оксипропилирования, равная 49; b+d+f=общая степень оксиэтилирования, равная 9; х=2; при G=Q=-N+H2CH2CH2NH2; М=-Cl; а+с+е=общая степень оксипропилирования, равная 55; b+d+f=общая степень оксиэтилирования, равная 10; х=2; при G=Q=M=-N+H2CH2CH2OH; а+с+е=общая степень оксипропилирования, равная 49; b+d+f=общая степень оксиэтилирования, равная 9; х=3; при G=Q=M=-N+H2CH2CH2OH; а+с+е=общая степень оксипропилирования, равная 55; b+d+f=общая степень оксиэтилирования, равная 10; х=3;
при
а+с+е=общая степень оксипропилирования, равная 49; b+d+f=общая степень оксиэтилирования, равная 0; х=3;
при
а+с+е=общая степень оксипропилирования, равная 55; b+d+f=общая степень оксиэтилирования, равная 0; х=3. 2. Соединения по п.1, обладающие фунгицидной активностью. 3. Способ получения соединений по п.1, заключающийся во взаимодействии 1,2,3-трис[гидроксиполи(алкиленокси)]пропана, формулы
где а+с+е=общая степень оксипропилирования, равная 49-55; b+d+f=общая степень оксиэтилирования, равная 0-10; с монохлоруксусной кислотой в кипящем органическом растворителе в присутствии кислотных катализаторов с азеотропным удалением образовавшейся воды и с последующей обработкой при нагревании полученного продукта аминосоединениями – алифатическими аминами, общей формулы
где R1=R2=H; R3=CH2CH2NH2, СН2СН2OH; при мольных соотношениях реагентов – гидроксильное производное пропана:монохлоруксусная кислота:алифатические амины=1:3,0-3,2:2,0-3,1 соответственно; или гетероциклическими аминами ряда пиридинов, формулы
где R5=H, СН3; при мольных соотношениях реагентов – гидроксильное производное пропана монохлоруксусная кислота: пиридины=1:3,0-3,2:3,0-3,1 соответственно; или смесью гетероциклических аминов ряда морфолина, формулы
где R4=H;
где R5=H; при мольных соотношениях реагентов – гидроксильное производное пропана:монохлоруксусная кислота:морфолины:пиридины=1:3,0-3,2:1,0-2,1:1,0-2,1 соответственно, при этом суммарное количество морфолина и пиридина составляет 3,-3,2 моля. 4. Способ по п.3, отличающийся тем, что в качестве кислотного катализатора используют H+ – форму катионообменной смолы КУ-2-8, взятую в количестве 3-5% от веса исходного гидроксильного производного пропана. 5. Способ по п.3, отличающийся тем, что в качестве органического растворителя используют ароматический углеводородный растворитель, например толуол, ксилол, нефрас А-120/200.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 07.07.2007
Извещение опубликовано: 20.02.2009 БИ: 05/2009
|
||||||||||||||||||||||||||||||||||||||||||||||||||||

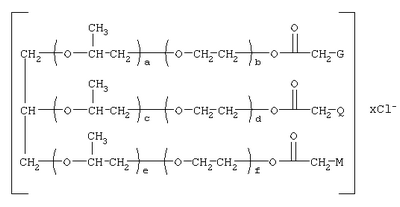
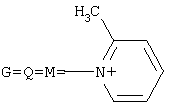 , а+с+е=49, b+d+f=9, x=3; при
, а+с+е=49, b+d+f=9, x=3; при 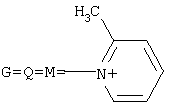 , а+с+е=55, b+d+f=10, x=3; при
, а+с+е=55, b+d+f=10, x=3; при 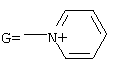 ,
, 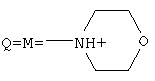 , а+с+е=49, b+d+f=9, х=3; при
, а+с+е=49, b+d+f=9, х=3; при 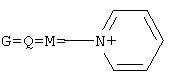 , а+с+е=49, b+d+f=9, x=3; при
, а+с+е=49, b+d+f=9, x=3; при 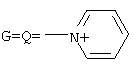 ,
, 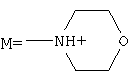 , а+с+е=49, b+d+f=0, х=3; при
, а+с+е=49, b+d+f=0, х=3; при 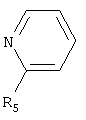 , где: R5=Н, СН3 или смесью морфолина и пиридина при мольных соотношениях реагентов – гидроксильное производное пропана:монохлоруксусная кислота:алифатические амины=1:3,0-3,2:2,0-3,1 соответственно или гидроксильное производное пропана:монохлоруксусная кислота: пиридин=1:3,0-3,2:3,0-3,1 соответственно или гидроксильное производное пропана:монохлоруксусная кислота:морфолин:пиридин=1:3,0-3,2:1,0-2,1:1,0-2,1 соответственно. При этом суммарное количество морфолина и пиридина составляет 3,-3,2 моля. Технический результат – синтез новых [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропанхлоридов, обладающих фунгицидной активностью, и способ их получения. 2 н. и 3 з.п. ф-лы, 1 табл.
, где: R5=Н, СН3 или смесью морфолина и пиридина при мольных соотношениях реагентов – гидроксильное производное пропана:монохлоруксусная кислота:алифатические амины=1:3,0-3,2:2,0-3,1 соответственно или гидроксильное производное пропана:монохлоруксусная кислота: пиридин=1:3,0-3,2:3,0-3,1 соответственно или гидроксильное производное пропана:монохлоруксусная кислота:морфолин:пиридин=1:3,0-3,2:1,0-2,1:1,0-2,1 соответственно. При этом суммарное количество морфолина и пиридина составляет 3,-3,2 моля. Технический результат – синтез новых [(гетерилонио)(аммонио)метилкарбонилоксиполи(алкиленокси)]пропанхлоридов, обладающих фунгицидной активностью, и способ их получения. 2 н. и 3 з.п. ф-лы, 1 табл.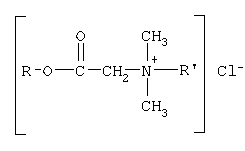
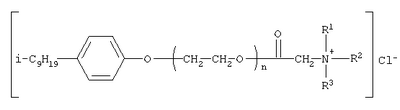
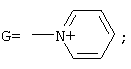
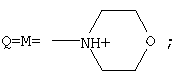
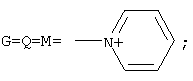
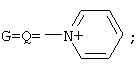
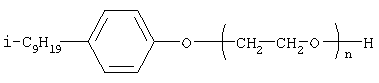
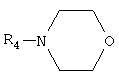
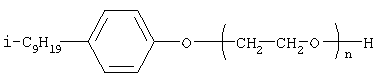
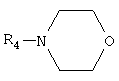
 (C=O)=1748 см-2;
(C=O)=1748 см-2;