|
|
(21), (22) Заявка: 2006105761/14, 27.02.2006
(24) Дата начала отсчета срока действия патента:
27.02.2006
(46) Опубликовано: 20.10.2007
(56) Список документов, цитированных в отчете о
поиске:
МИНКИН Л.И. и др. Применение хлоргексидинсодержащих препаратов для лечения заболеваний пародонта (литературный обзор). – Пародонтология. – М., 1997, №4, с.29-33. RU 2122865 С1, 10.12.1998. RU 2143905 С1, 10.01.2000. ГИЛЬМАН Л.М. Использование бактерицидных покрытий на основе полигексаметиленгуанидина в бальнеотехнических системах. – Вопр.
Адрес для переписки:
141400, Московская обл., г. Химки, ул. Парковая, 12, кв.106, Л.С. Лазаренко
|
(72) Автор(ы):
Щипский Александр Васильевич (RU),
Афанасьев Василий Владимирович (RU),
Ефимов Константин Михайлович (RU),
Поликарпов Николай Александрович (RU),
Дмитрук Иван Борисович (RU)
(73) Патентообладатель(и):
Общество с ограниченной ответственностью “Международный институт эколого-технологических проблем” (RU)
|
(54) СПОСОБ ЛЕЧЕНИЯ ГНОЙНО-ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ ЧЕЛЮСТНО-ЛИЦЕВОЙ ОБЛАСТИ
(57) Реферат:
Изобретение относится к медицине, а именно к стоматологии, и может быть использовано для лечения гнойно-воспалительных заболеваний челюстно-лицевой области. Для этого обрабатывают воспалительный очаг 0,05-0,1% водным раствором полигексаметиленгуанидина гидрохлорида. Способ обеспечивает эффективное лечение за счет использования нового антисептического средства при отсутствии нежелательных резорбтивных и местных реакций. 7 табл., 1 ил.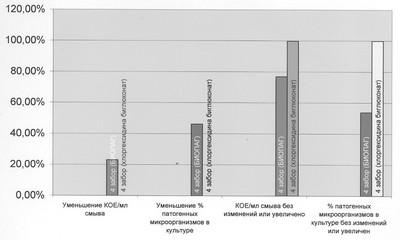
(56) (продолжение):
CLASS=”b560m”курортологии, физиотерапии и лечеб. физ. культуры. – М., 1993, №6, с.35-39. МУРАТОВА Н.М. Токсиколого-гигиенические аспекты действия полигексаметиленгуанидин гидрохлорида – нового препарата полигуанидинового ряда. – М., 1994. SOKOLOWA N.F. “[The antimicrobial effectiveness of hand antiseptics]”, Z Gesamte Hyg. 1990 Feb; 36(2):81-82.
Изобретение относится к области медицины, а именно к стоматологии, и может быть использовано для лечения воспалительных заболеваний челюстно-лицевой области (ЧЛО).
Кроме того, связь органов ЧЛО с ЛОР-органами, глазницей, черепом может привести к развитию медиастинита, флегмоны шеи и орбиты, тромбоза пещеристого синуса и др., а в случае их неадекватной терапии – к тяжелым гнойно-септическим осложнениям с летальным исходом.
В практике хирургической стоматологии для промывания гнойно-воспалительных очагов после хирургической обработки применяют антисептические препараты различных групп, а также растворы антибиотиков как в чистом виде, так и в виде комплексных препаратов (смотри таблицу 1).
Данные препараты должны отвечать определенным критериям: обладать высокой антибактериальной активностью, не должны вызывать раздражение и повреждение тканей, резорбтивное действие в виде аллергических, токсических и др. реакций, не препятствовать росту грануляций и формированию эпителия.
Хлоргексидина биглюконат имеет следующую структурную формулу:
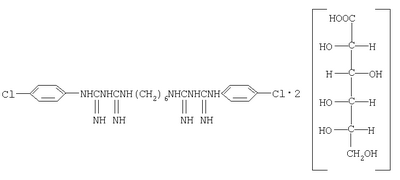
| Брутто формула: C34H54O14N10Cl2 |
M=701 |
Хлоргексидина биглюконат является антисептическим и дезинфицирующим средством. Код АТХ D 08 АС 02.
Хлоргексидина биглюконат (синонимы гибитан, гексикон, гибиспарт, пливасепт, фервекс) разработан в конце 40-х г (впервые появился в продаже в Великобритании в 1953 г.) и относится к катионоактивным бисбигуанидам. Препарат является одним из самых хорошо изученных и широко применяемых в стоматологической практике антисептиков. Проявляет бактерицидную активность в отношении большинства грамположительных и грамотрицательных аэробных и анаэробных бактерий, трепонем, гонококков, трихомонад. Наряду с этим хлоргексидина биглюконат обладает слабой фунгицидной активностью и не действует на кислостойкие формы бактерий.
Задачей изобретения является повышение эффективности лечения гнойно-воспалительных заболеваний челюстно-лицевой области через усиление антибактериальной эффективности антисептической обработки воспалительного очага при отсутствии нежелательных резорбтивных и местных реакций.
Для решения поставленной задачи в способе лечения гнойно-воспалительных заболеваний челюстно-лицевой области, включающем обработку тканей воспалительного очага водным раствором антисептика, в качестве водного раствора антисептика используют 0,05-0,1% раствор полигексаметиленгуанидина гидрохлорида (БИОПАГА).
Сущность изобретения поясняется следующим образом. Полимерные дезинфицирующие препараты семейства полигексаметиленгуанидинов (ПГМГ) способны одновременно воздействовать на грибковую и бактериальную, аэробную и анаэробную микрофлору. Полимерная природа препаратов позволяет образовывать на поверхности биоцидную пленку, сохраняющую антимикробное действие до 1,5 лет (по сравнению с несколькими часами при использовании обычных дезинфектантов). ПГМГ экологически безопасны, не летучи, без запаха, не агрессивны по отношению к различным материалам, устойчивы к высоким температурам (до +200°С), не содержат окислителей хлора, ртути, альдегидов и фенолов. В силу своих характеристик данные препараты нашли применение в быту, пищевой промышленности, для дезинфекции помещений и изделий медицинского назначения перед их утилизацией и т.п.
Одним из представителей ПГМГ является полигексаметиленгуанидина гидрохлорид, выпускаемый Институтом эколого-технологических проблем (ИЭТП) в виде 20% водного раствора согласно ТУ 9392-009-41547288-2000 под торговой маркой БИОПАГ. По данным экспериментальных исследований препарат обладает низкой токсичностью и относится к III классу умеренно опасных веществ при введении в желудок и к IV классу малоопасных веществ при нанесении на кожу, не вызывает аллергических реакций, не раздражает слизистые оболочки, не накапливается в организме. Обладает широким спектром биоцидной активности: антимикробной, вируцилидной, фунгицидной. Эффективно воздействует на грамположительную и грамотрицательную микрофлору. Как и другие представители полигексаметилегуанидинов, БИОПАГ благодаря полимерной природе обладает пролонгированным дезинфицирующим эффектом.
Полигексаметиленгуанидина гидрохлорида (БИОПАГ) имеет следующую структурную формулу:
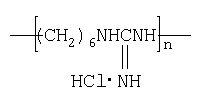
n=30-50
В клинической практике БИОПАГ в качестве антисептика до настоящего времени не применялся, неизвестна его антибактериальная эффективность при воспалительных заболеваниях челюстно-лицевой области.
В случае применения раствора ПГМГ гидрохлорида менее 0,05% не будет наблюдаться достаточного антисептического действия. Если же раствор будет превышать более 0,1%, то это приведет к неоправданно высокому расходу антисептика.
Для оценки преимущества БИОПАГА по сравнению с хлоргексидина биглюконатом нами проведены рандомизированные контролируемые испытания клинического применения данных препаратов в качестве антисептиков для лечения гнойно-воспалительных заболеваний челюстно-лицевой области.
Исследования проводили в 2 этапа.
В связи с тем что БИОПАГ в качестве антисептика применялся в клинической практике впервые, существовала предварительная необходимость определить оптимальную для этих целей концентрацию препарата (1 этап). Для этой цели культивировали и идентифицировали микрофлору из содержимого гнойно-воспалительных очагов 42 пациентов с различными воспалительными заболеваниями челюстно-лицевой области (смотри таблицу 2), произвольно встречающимися в условиях неспециализированной стоматологической клиники. Забор материала и его транспортировку в микробиологическую лабораторию производили по установленным стандартам до начала проведения антибактериальной терапии выявленного заболевания.
В микробиологической лаборатории проводили десятикратное разведение проб и их посев на жидкие и плотные питательные среды для культивирования строго анаэробных и факультативно-анаэробных микроорганизмов: питательную среду для контроля стерильности, Schaedler anaerobe agar (Oxoid, England) с 5% крови, среду Висмут Блер, Hektoen enteric agar, среду Хэнеля (Haenel agar), маннитол-солевой агар, а также среды Чапека и Сабуро. Культивирование микроорганизмов производили в термостате и микроанаэростате с газовой смесью из 95% азота и 5% углекислого газа. После подсчета колоний выросших микроорганизмов производили их изоляцию на скошенный агар для дальнейших исследований. Выделенные культуры идентифицировали по соответствующим методикам с использованием систем API-20 E, API-20 Staph, API-20 А, а также автоматизированной системы для идентификации микроорганизмов Vitek (BioMerieux, Франция).
Выявленные клинические штаммы микроорганизмов протестировали различными концентрациями БИОПАГА и хлоргексидина биглюконата для определения минимально подавляющих концентраций (МПК) с использованием метода серийных разведении в жидких средах (питательная среда для контроля стерильности и трипказо-соевый бульон (TSB) (BioMerieux, Франция), жидкая среда Чапека). Для объективности результатов исследований повторяли 2-4 раза.
В результате исследований клинического материала выделили 17 родов бактерий, один вид дрожжеподобного гриба и один вид плесневого гриба. Среди них следующие микроорганизмы: Peptococcus spp. (Peptococcus niger; Peptococcus asaccharolyticus); Peptostreptococcus spp. (Peptostreptococcus anaerobius); Streptococcus spp. (Streptococcus pyogenes; Streptococcus intermedius); Staphilococcus spp (Staphilococcus aureus; Staphilococcus warneri; Staphilococcus hominis; Staphilococcus haemoliticus; Staphilococcus cohnii; Staphilococcus epidermidis; Staphilococcus capitis;); Enterococcus spp. (Enterococcus gallunarum; Enterococcus faecium); Propionbacterium achnes; Fusobacterium necrophorum; Eubacterium spp. (Eubacterium lentum; Eubacterium saburreum); Actinomyces israelii; Bacteroides spp. (Bacteroides distasonis; Bacteroides fragilis; Bacteroides oralis; Bacteroides melaninogenicus); Eikenella corrodens; Veillonella parvula; Klebssiella oxytoca; Edvardsiella tarda; Escherichia coli; Proteus morganii; Aspergillus niger; Candida albicans. Всего в 45 заборах обнаружили 138 культур микроорганизмов в виде монокультуры или чаще в виде различных ассоциаций микроорганизмов. В 10 заборах (22,2%) культура была представлена 1 видом, в 8 (17,8%) – 2 видами, в 13 – 3 видами (28,9%), в 9 – 4 видами (20,0%), в 5 – 5 видами (11,1%) и в 1 случае (2,2%) культура была представлена 6 различными видами микроорганизмов. Чаще всего высевались анаэробные микроорганизмы: в 60% случаев различные штаммы Peptococcus; в 56% случаев – Bacteroides; в 38% случаев различные штаммы Peptostreptococcus; в 24% – разновидности Streptococcus. Veillonella parvula встречалась в 22% случаях, остальные – реже.
Сравнительный анализ полученных значений МПК БИОПАГА и хлоргексидина биглюконата, проведенный с помощью классического метода робастной оценки Хьюбера, показал, что БИОПАГ проявлял антибактериальную активность при меньших концентрациях, чем хлоргексидина биглюконат (р<0,001) (смотри таблицу 3).
Фунгицидная активность БИОПАГА также была выше по сравнению с хлоргексидина биглюконатом. Так, на Aspergillus niger и Candida albicans эффективно воздействии соответственно 0,005% (0,05 мг/мл) и 0,002% (0,02 мг/мл) растворы БИОПАГА и лишь 0,02% (0,2 мг/мл) и 0,01% (0,1 мг/мл) растворы хлоргексидина биглюконата.
Пример 1. Больная X, 38 лет, обратилась в поликлинику челюстно-лицевого госпиталя с жалобами на периодические болевые ощущения в области верхней челюсти слева, заложенность носового дыхания и слизисто-гнойные выделения из носа. В анамнезе неоднократное лечение отоларингологом без ощутимого результата. На обзорной рентгенограмме придаточных пазух носа наблюдалось негомогенное средней интенсивности затемнение левого верхнечелюстного синуса, в верхнем отделе – тень повышенной плотности неправильной формы. Каналы 24 зуба запломбированы некачественно, имелись очаги разрежения кости в области верхушек.
На основании клинических и рентгенологических данных установили диагноз: левосторонний хронический одонтогенный верхнечелюстной синусит, возможно аспергиллез. Хронический периодонтит 24 и 26 зубов.
28.09.04 после соответствующей подготовки в челюстно-лицевом стационаре провели радикальную гайморотомию. При этом удалили полипозноизмененную слизистую оболочку верхнечелюстного синуса, крупные полипы, пломбировочный материал и два конгломерата грязно-зеленого цвета. Операционный материал отправили на патогистологическое и микробиологическое исследование. Патогистологическое заключение: гипертрофический гайморит с обострением. По данным микробиологического исследования в содержимом синуса выявлен Aspergillus niger в большом количестве. Тестирование колонии различными концентрациями БИОПАГА и хлоргексидина выявило фунгицидный эффект при воздействии 0,005% (0,05 мг/мл) и 0,02% (0,2 мг/мл) растворами данных препаратов соответственно.
Послеоперационный период протекал без осложнений, пациентка выписана из стационара через 7 дней после операции под амбулаторное наблюдение. Исходя из результатов микробиологического исследования в поликлинике верхнечелюстной синус промывали раствором БИОПАГА, другое лечение не проводили. После проведенного хирургического и антисептического лечения имевшиеся ранее жалобы отсутствовали, прекратились выделения из носа, восстановилось в полном объеме носовое дыхание, что свидетельствовало о выздоровлении пациентки. Срок динамического наблюдения составил больше 1 года.
Выбор оптимальной для клинического использования концентрации БИОПАГА осуществили на основании подсчета количества значений МПК, оказавших бактерицидный эффект на большинство выявленных у пациентов штаммов микроорганизмов (смотри таблицы 4; 5). Обнаружили, что БИОПАГ в концентрации 0.500 мг/мл (0.05% раствор) оказывал бактерицидный эффект в 82% случаев, т.е. на большинство микроорганизмов, а 0.1% раствор БИОПАГА воздействовал на микрофлору практически со 100% эффективностью.
Следовательно, БИОПАГ в концентрации 0,500-0,100 мг/мл (0.05-0,1% раствор) обладает более выраженными антибактериальными и фунгицидными биглюконата и может применяться в клинической практике в указанных концентрациях в качестве антисептика для лечения гнойно-воспалительных заболеваний челюстно-лицевой области.
Клиническая эффективность и безопасность 0,05% раствора БИОПАГА была изучена при лечении 14 пациентов с хроническим одонтогенным (перфоративным) верхнечелюстным синуситом (2 этап) посредством промывания верхнечелюстного синуса. Контрольную группу составили 6 пациентов с хроническим одонтогенным (перфоративным) верхнечелюстным синуситом, лечение которых провели с помощью 0,05% раствора хлоргексидина биглюконата (смотри таблицу 6). Анатомо-топографические особенности перфоративного гайморита позволили применить у всех пациентов унифицированную методику забора материала для микробиологических исследований. Для изучения антибактериального эффекта антисептиков в динамике забор материала у пациентов осуществляли четыре раза. 1 забор проводили до начала обработки верхнечелюстного синуса антисептиком с целью установления исходного уровня обсемененности, остальные 3 забора – через 60 мин, 3 дня и 7 дней после начала терапии. Забор и транспортировку материала в микробиологическую лабораторию осуществляли согласно стандартам с использованием “двойного слепого метода”, согласно которому микробиолог и пациент не знали название применяемого антисептика.
Посев материала провели на специальные питательные среды с целью определения общего микробного числа микроорганизмов, а также количественного уровня потенциально патогенных микроорганизмов в общей культуре. Принадлежность культур к потенциально патогенным микроорганизмам определяли по активности ДНКазы и РНКазы в виде зон просветления вокруг колоний от 2 мм и более (Jeffries CD., Holtman D.F., Guse D. / Rapid method for determining the activiti of microorganisms on nucleic acids /. J.Bacteriology, 1957, v.73, №4, p.50-591).
После применения 0.05% раствора БИОПАГА уменьшение количества КОЕ/мл по сравнению с исходным уровнем выявили в материале 2 забора у 57.14% пациентов; 3 забора у 64.29% пациентов и в 46.15% случаев в материале 4 забора. В контрольной группе результаты соответственно составили: 83.33%; 100.00% и 75.00% (смотри таблицу 7). Статистически достоверное различие (р<0.02) между антисептиками обнаружено лишь при сравнении результатов 3 забора.
При анализе воздействия антисептиков на потенциально патогенную микрофлору синуса обнаружили противоположную тенденцию. Так, под действием 0.05% БИОПАГА уменьшение доли патогенной микрофлоры в общей культуре по сравнению с исходным уровнем произошло в материале 2 забора у 50.00% пациентов; в материале 3 забора у 35.71% пациентов и в 53.85% случаев в материале 4 забора. После применения хлоргексидина биглюконата результаты соответственно составили: 33.33%; 20.00% и 25.00% (Таб.7). По мере увеличения сроков лечения тенденция: “хлоргексидин сильнее воздействует на общий состав микрофлоры, БИОПАГ – на ее патогенную составляющую” получила статистическое подтверждение (р<0.01). Так, под влиянием 0.05% раствора БИОПАГА в общей культуре 4 забора у 46.15% пациентов произошло уменьшение доли патогенной микрофлоры по сравнению с показателями 3 забора. В контрольной группе положительный эффект не наблюдали (смотри таблицу 7; чертеж).
Вне зависимости от применявшегося антисептика все пациенты отмечали уменьшение или исчезновение выделений из верхнечелюстного синуса и улучшение носового дыхания, уменьшение или исчезновение болевых ощущений в области верхнечелюстного синуса. БИОПАГ не обладал отрицательными вкусовыми качествами, тогда как применение хлоргексидина биглюконата у всех пациентов сопровождалось неприятным привкусом.
Применение БИОПАГА не приводило к ухудшению общего состояния пациентов, не вызывало раздражения слизистой оболочки полости рта и зева и аллергических реакций, что свидетельствовало об отсутствии у данного препарат побочных и токсических эффектов.
| Таблица 1 |
| Препараты, применяемые для промывания (ирригации) гнойных ран в челюстно-лицевой области (Ушаков Р.В., Царев В.Н. Российский стоматологический журнал, 2003, №6, стр.40-44). |
| Группа |
Препарат |
Концентрация |
| Окислители |
Перекись водорода |
3% |
| Галогены |
Иодантипирин |
5% |
| |
Иодопирон |
0,1-1% |
| Декаметоксин |
Декаметоксин |
0,025-0,5% |
| |
Хлорамин Б |
2% |
| Красители |
Этакридина лактат (риванол) |
0,1-0,2% |
| Катионные детергенты |
Бензалкония хлорид |
1% |
| Бигуаниды |
Хлоргексидина глюконат |
0,05% |
| |
Пливасепта глюконат |
5% |
| Соединения металлов |
Колларгол |
0,2-1% |
| |
Протаргол |
7,8-8,3% серебра |
| Производные хиноксалина |
Диоксидин |
0,1-0,5% |
| Препараты растительного и животного происхождения |
Новоиманин |
0,01% |
| |
Лизоцим |
0,05% |
| Антибиотики |
Грамицидин С |
0,01-0,02% |
| Таблица 2 |
| Общая характеристика обследованных пациентов с воспитательными заболеваниями челюстно-лицевой области (1-й этап) |
| Заболевание |
Пациенты |
Заборы |
Мужчины |
Женщины |
| Обострение хронического одонтогенного верхнечелюстного синусита |
6 |
8 |
2 |
4 |
| Нагноение радикулярной кисты |
15 |
16 |
7 |
8 |
| Обострение хронического периодонтита. Острый гнойный периостит |
8 |
8 |
5 |
3 |
| Флегмона. Абсцесс. Лимфаденит |
6 |
6 |
4 |
2 |
| Кисты неодонтогенного происхождения |
5 |
5 |
2 |
3 |
| Обострение хронического сиаладенита |
1 |
1 |
1 |
0 |
| Пародонтит |
1 |
1 |
0 |
1 |
| ВСЕГО: |
42 |
45 |
21 |
21 |
| Таблица 3 |
| Сравнительный анализ методик статистической обработки значений МПК БИОПАГА и хлоргексидина биглюконата |
| Антисептик |
Бактериостатический эффект |
Бактерицидный эффект |
| |
Стандартная |
Метод |
Стандартная |
Метод |
| |
методика |
Хьюбера |
методика |
Хьюбера |
| БИОПАГ |
0.092±0.036 |
0.056±0.009 |
0.245±0.082 |
0.091±0.017 |
| |
(0.009±0.004%) |
(0.006±0.001%) |
(0.025±0.008%) |
(0.009±0.002%) |
| Хлоргексидин |
0.086±0.033 |
0.080±0.006 |
0.216±0.070 |
0.180±0.017 |
| биглюконат |
(0.009±0.003%) |
(0.008±0.001%) |
(0.022±0.007%) |
(0.018±0.002%) |
| Примечание: 0.092±0.036, где 0.092 среднее арифметическое значение, выраженное в мг/мл; ±0.036 – среднеквадратическое отклонение. |
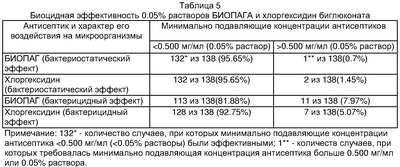
| Таблица 4 |
| Анализ биоцидной активности БИОПАГА и хлоргексидина биглюконата |
| Антисептик и характер его воздействия на микроорганизмы |
Минимально подавляющие концентрации антисептиков, выраженные в мг/мл |
| 0.001 |
0.002 |
0.003 |
0.010 |
0.020 |
0.030 |
0.040 |
0.050 |
0.100 |
0.200 |
0.300 |
0.400 |
0.500 |
1.000 |
2.000 |
| БИОПАГ (бактериостатический эффект) |
6* |
3 |
12 |
45 |
16 |
1 |
0 |
1 |
35 |
4 |
0 |
9 |
0 |
1 |
0 |
| Хлоргексидин (бактериостатический эффект) |
7 |
3 |
12 |
36 |
15 |
0 |
0 |
4 |
43 |
7 |
0 |
5 |
0 |
2 |
0 |
| БИОПАГ(бактерицидный эффект) |
0 |
0 |
6 |
14 |
44 |
1 |
1 |
2 |
17 |
5 |
0 |
23 |
0 |
10 |
1 |
| Хлоргексидин (бактерицидный эффект) |
2 |
1 |
7 |
14 |
32 |
0 |
0 |
1 |
35 |
8 |
0 |
28 |
0 |
6 |
1 |
| Примечание: 6* – количество случаев, при которых данная концентрация антисептика являлась минимально подавляющей |
| Таблица 6 |
| Общая характеристика пациентов с хроническим одонтогенным верхнечелюстным синуситом (2-й этап) |
| Антисептик |
пациенты |
мужчины |
Женщины |
1 посещение |
2 посещение |
3 посещение |
ВСЕГО |
| 1 забор |
2 забор |
3 забор |
4 забор |
Все заборы |
| БИОПАГ |
14 |
10 |
4 |
14 |
14 |
14 |
13 |
55 |
| Хлоргексидин биглюконат |
6 |
5 |
1 |
6 |
6 |
5 |
4 |
21 |
| ВСЕГО: |
20 |
15 |
5 |
20 |
20 |
19 |
17 |
76 |
| Таблица 7 |
| Сравнительный анализ эффективности антимикробной обработки верхнечелюстного синуса 0.05% растворами БИОПАГА и хлоргексидина биглюконата |
| (полный или частичный эффект) |
(отсутствие эффекта или прогресснрованне) |
| Уменьшение КОЕ/мл смыва |
Уменьшение % потенциально патогенных микроорганизмов в общей культуре |
КОЕ/мл смыва без изменении или увеличено |
% потенциально патогенных микроорганизмов в общей культуре без изменений или увеличился |
| По сравнению с исходным показателем – 1 забора (состояние перед введением 0.05% раствора антисептика) |
| Данные 2 забора (через 60 мин после 1-го введения 0,05% р-ра БИОПАГА) (n=14) |
| 8 (57,14%) |
7 (50,00%) |
6 (42,86%) |
7 (50,00%) |
| Данные 2 забора (через 60 мин после 1-го введения 0,05% р-ра хлоргексидина) (n=6) |
| 5 (83,33%) |
2 (33,33%) |
1 (16,67%) |
4 (66,67%) |
| Данные 3 забора (через 3 дня после 1-го введения 0,05% р-ра БИОПАГА) (n=14) |
| 9 (64,29%) |
5 (35,71%) |
5 (35,71%) |
9 (64,29%) |
| Данные 3 забора (через 3 дня после 1-го введения 0,05% р-ра хлогексидина) (n=5) |
| 5 (100,00%) |
1 (20,00%) |
0 |
4 (80,00%) |
| Сравнительные данные 4 забора (состояние через 7 дней после 1-го введения и 4 дня после 2-го введения 0,05% р-ра БПОПАГА) (n=13) |
| 6 (46,15%) |
7 (53,85%) |
8 (61,54%) |
6 (46,15%) |
| Данные 4 забора (через 7 дней после 1-го введения и 4 дня после 2-го введения 0,05% р-ра хлоргексидина)(n=4) |
| 3 (75,00%) |
1 (25,00%) |
1 (25,00%) |
3(75,00%) |
| По сравнению с показателем 2 забора (состояние через 60 мин после первого введения 0.05% р-ра антисептика) |
| Данные 3 забора (через 3 дня после 1-го введения 0,05% р-ра БИОПАГА) (n=14) |
| 6 (42,86%) |
3(21,43%) |
10(71,43%) |
12(85,71%) |
| Данные 3 забора (через 3 дня после 1-го введения 0,05% р-ра хлоргексидина) (n=5) |
| 3 (60,00%) |
2 (40,00%) |
2 (40,00%) |
3 (60,00%) |
| Данные 4 забора (через 7 дней после 1-го введения и 4 дня после 2-го введения 0,05% р-ра БИОПАГА) (n=13) |
| 3 (23,08%) |
6(46,15%) |
9 (69,23%) |
11 (84,62%) |
| Данные 4 забора (через 7 дней после 1-го введения и 4 дня после 2-го введения 0,05% р-ра хлоргексидина) (n=4) |
| 2 (50,00%) |
2 (50,00%) |
2(50,00%) |
2(50,00%) |
| По сравнению с показателем 3 забора (состояние через 3 дня после первого введения 0.05% р-ра антисептика) |
| Данные 4 забора (через 7 дней после 1-го введения н 4 дня после 2-го введения 0,05% р-ра БИОПАГА) (n=13) |
| 3 (23,08%) |
6 (46,15%) |
10(76,92%) |
7 (53,85%) |
| Данные 4 забора (через 7 дней после 1-го введения н 4 дня после 2-го введения 0,05% р-ра хлоргексидина) (n=4) |
| 0 |
0 |
4(100,00%) |
4(100,00%) |
| Примечание: 8 (57.14%) – встречаемость признака в абсолютном и процентном соотношении к общему количеству микрофлоры. |
Формула изобретения
Способ лечения гнойно-воспалительных заболеваний челюстно-лицевой области, включающий обработку воспалительного очага водным раствором антисептика, отличающийся тем, что в качестве водного раствора антисептика используют 0,05-0,1%-ный раствор полигексаметиленгуанидина гидрохлорида.
РИСУНКИ
|
|