|
(21), (22) Заявка: 2006113959/02, 25.04.2006
(24) Дата начала отсчета срока действия патента:
25.04.2006
(46) Опубликовано: 27.09.2007
(56) Список документов, цитированных в отчете о
поиске:
СТЕНДЕР А.А. Прикладная электрохимия. – Харьков: Харьковский университет, 1961, с.244. SU 876759 А, 30.10.1981. RU 2154119 C1, 10.08.2000. GB 2025461 А, 23.01.1980.
Адрес для переписки:
119991, Москва, Ленинский пр-кт, 49, Институт металлургии и материаловедения им. А.А. Байкова РАН, директору Ю.К.Ковнеристому
|
(72) Автор(ы):
Ковнеристый Юлий Константинович (RU),
Бурханов Юрий Сергеевич (RU),
Бурханов Геннадий Сергеевич (RU),
Шаталов Валентин Васильевич (RU),
Мельников Сергей Александрович (RU),
Паршин Анатолий Павлович (RU)
(73) Патентообладатель(и):
Институт металлургии и материаловедения им. А.А. Байкова РАН (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ МЕТАЛЛОВ
(57) Реферат:
Изобретение относится к области электрохимии, в частности к электролитическому получению металлов из их сульфидов. Электролиз ведут с использованием раствора электролита и положительного электрода, содержащего сульфид получаемого металла, порошок вещества, являющегося акцептором атомов серы, и порошок вещества, являющегося объемным токосъемником с электронной проводимостью. Способ является экологически безопасным и экономически эффективным.
Изобретение относится к области электрохимии, в частности к электролизному получению металлов, твердых растворов, химических соединений; изготовлению аккумуляторов и нормальных элементов.
Большая часть природных минералов меди, цинка, ртути, никеля и кобальта является сульфидными соединениями (Свойства элементов: Справ. изд./ Под ред. М.Е. Дрица, М: Металлургия, 1985, 672 с.). Получение металлов из водных растворов солей связано с осуществлением ряда технологических операций по получению этих солей из соответствующих сульфидов, которые экологически опасны. Поэтому целесообразно получать металлы непосредственно из их сульфидов, а не из их окислов и солей. Известен способ анодного разложения сульфидов металлов, например, для сульфидов никеля и меди (В.В.Стендер. Прикладная электрохимия. Харьков. Изд. Харьковского университета, 1961, стр.244). Недостатком этого процесса является то, что он оказался малопроизводительным с выходом некачественного металла.
Техническим результатом данного изобретения является разработка экологически безопасного и экономически эффективного способа получения металлов из их сульфидов электролизом нового типа.
Технический результат достигается тем, что предложен способ получения металлов, включающий электролиз с использованием нерасходуемого раствора электролита и положительного электрода, содержащего сульфид получаемого металла, при этом положительный электрод дополнительно содержит порошок вещества, являющегося акцептором атомов серы, и порошок вещества, являющегося объемным токосъемником с электронной проводимостью. В предлагаемом электролизном способе получения металлов из их сульфидов используется объемный насыпной положительный электрод, состоящий из смеси порошков и обладающий поэтому развитой внутренней поверхностью. Одним из компонентов этой смеси порошков является порошок с электронной проводимостью, который играет роль объемного токосъемника.
В качестве такого порошка используется, в частности, порошок кокса или угля. Эти два фактора интенсификации процесса разложения сульфидов используются при получении меди. Для увеличения эффективности процессов электролизного получения цинка, ртути, никеля и кобальта из их сульфидов используется дополнительный компонент смеси порошков – Cu2S, который играет роль акцептора атомов серы при их отрыве от сульфида восстанавливаемого металла.
Пример №1. Получение меди из Cu2S известным способом.
Электролиз происходил в насыщенном водном растворе CuSO4 (p) при комнатной температуре. Использовался объемный положительный электрод из смеси порошка Cu2S и дробленого кокса.
Осуществлялись следующие токообразующие реакции:
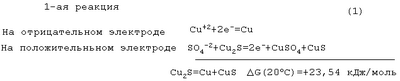
Термодинамический потенциал реакции  G (20°C) рассчитывался из термодинамических потенциалов сульфидов меди Cu2S и CuS [M.X.Карапетьянц, М.Л.Карапетьянц. Основные термодинамические константы неорганических и органических веществ. М.: Химия, 1968, с.470]. G (20°C) рассчитывался из термодинамических потенциалов сульфидов меди Cu2S и CuS [M.X.Карапетьянц, М.Л.Карапетьянц. Основные термодинамические константы неорганических и органических веществ. М.: Химия, 1968, с.470].
Из этой величины термодинамического потенциала реакции следует, что минимальное напряжение электролиза равно 0.15 В.
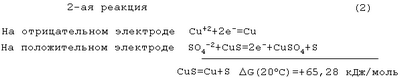
Рассчитанное минимальное напряжение этой электролизной реакции равно 0,41 В.
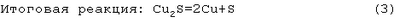
При практической реализации рассмотренных реакций установлены следующие характеристики процесса электролиза:
| U [B] |
0.2 |
0.3 |
0.5 |
0.6 |
0.8 |
0.9 |
| j [A/м2] |
0 |
6 |
12 |
18 |
23 |
37 |
Достигнутые плотности тока j свидетельствуют о высокой производительности предложенного процесса производства меди и его сульфидов, которая соизмерима с производительностью традиционных процессов электролиза.
При увеличении напряжения и межэлектродного расстояния происходило возрастание плотности восстанавливаемого металла.
Пример №2. Получение цинка из ZnS
При производстве цинка обычно используют технологически трудоемкий и экологически вредный процесс получения ZnO из ZnS с последующим восстановлением Zn углеродом или получения ZnSO4 из ZnO и H2SO4. Кроме того, получаемый таким образом цинк содержит заметное количество примесей и поэтому требуется дополнительная операция по его очистке.
В данной работе осуществлен процесс получения цинка из его сульфида в насыщенном водном растворе ZnCl2 (p) при комнатной температуре. Объемный положительный электрод изготавливался из смеси порошков сульфидов цинка ZnS и меди Cu2S в соотношении 1 моль ZnS – 1 моль Cu2S. В качестве объемного токосъемника добавлялся толченый кокс или уголь. Молекулы Cu2S являлись акцепторами атомов серы при их отрыве от ZnS.
Опыты осуществлялись при визуальном контроле над процессом электролизного осаждения цинка на отрицательном электроде и многократном взвешивании этого электрода до и после процесса.
Токообразующая реакция данного процесса: 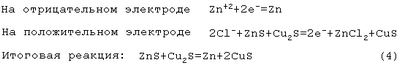
Термодинамический потенциал этой реакции  G (20°С)=+158.38 кДж/моль. G (20°С)=+158.38 кДж/моль.
Рассчитанное минимальное напряжение электролиза равно 1,0 В.
Приведем электрические параметры процесса, осуществленного в лабораторном опыте.
| U [B] |
1.2 |
1.3 |
1.4 |
1.5 |
| j [A/м2] |
0 |
16 |
20 |
40 |
Достигнутые величины плотности тока (при соизмеримых напряжениях) значительно больше, чем при электролизе меди из Cu2S. Причина этого увеличения плотности тока – введение акцепторов атомов серы в положительный электрод в виде порошка Cu2S.
Удовлетворительное качество получаемого металла (его плотность и химическая чистота) достигались при межэлектродном расстоянии >1-2 см.
В данном процессе отсутствует возможность загрязнения медью получаемого цинка (даже при высоком напряжении электролиза). Действительно, при U>1,7 В термодинамически разрешенной является токообразующая реакция с образованием CuCl2
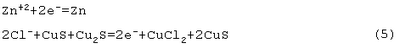
Однако, ZnS взаимодействует с CuCl2 по следующей самопроизвольной реакции:
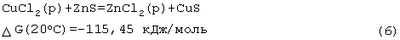
Термодинамически такая реакция разрешена при комнатной температуре.
Поэтому медь не появляется на отрицательном электроде.
Пример 3. Возможность получения никеля и кобальта из их сульфидов.
Предлагается новый процесс получения никеля из сульфидов, например из природного соединения NiS. Для осуществления этого процесса положительный электрод изготавливается из смеси порошков NiS и Cu2S (в соотношении: 1 моль NiS – 1 моль Cu2S) и порошка дробленого кокса. Возможно использование двух электролитов: или NiCl2 (p), или NiSO4 (р). Выбор между этими электролитами может быть сделан только в ходе опытов, в которых будут установлены условия достижения максимальной плотности тока.
Токообразующая реакция предложенного процесса (на примере использования NiCl2 (р)):
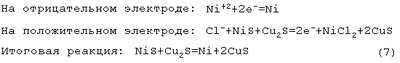
Термодинамический потенциал этой реакции  G (20°C) равен: G (20°C) равен:
 G (200°C)=-50,62 кДж/моль. G (200°C)=-50,62 кДж/моль.
Исходя из этой величины  G (20°С) для величины ЭДС, образующейся в ходе осуществления предложенного процесса получения Ni из NiS, получаем: ЭДС=0,3 В. G (20°С) для величины ЭДС, образующейся в ходе осуществления предложенного процесса получения Ni из NiS, получаем: ЭДС=0,3 В.
Однако величина плотности тока этого процесса, по-видимому, является очень маленькой и, соответственно, ничтожной производительность такого процесса производства никеля.
Поэтому, чтобы процесс стал производительным, необходима внешняя ЭДС. Возможно, что заметная плотность тока может достигаться при малом напряжении, необходимом лишь для «перегонки» на отрицательный электрод мелкодисперсного никеля, возникающего в ходе самопроизвольной реакции (7) внутри положительного электрода.
Заметим, что медь не может возникнуть на отрицательном никелевом электроде, так как не может возникнуть в растворе соль меди из-за существования следующей самопроизвольной реакции:
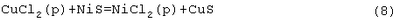
Термодинамический потенциал этой реакции равен:  G (20°C)=-113,01 кДж/моль. G (20°C)=-113,01 кДж/моль.
Анализ возможности получения никеля из NiS полностью относится к получению кобальта из CoS.
Формула изобретения
Способ получения металлов, включающий электролиз с использованием раствора электролита и положительного электрода, содержащего сульфид получаемого металла, отличающийся тем, что положительный электрод дополнительно содержит порошок вещества, являющегося акцептором атомов серы, и порошок вещества, являющегося объемным токосъемником с электронной проводимостью.
|