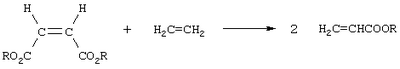Патент на изобретение №2307119
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ АКРИЛОВОЙ КИСЛОТЫ
(57) Реферат:
Изобретение относится к органическому синтезу и касается усовершенствованного способа получения эфиров акриловой кислоты, заключающегося в том, что эфиры малеиновой кислоты с алифатическими спиртами C1-C4 подвергают взаимодействию с этиленом в присутствии катализатора метатезиса при температуре от 20°С до 140°С, давлении этилена от 101325 Па до 506625 Па. Способ позволяет синтезировать акрилаты с высокой селективностью без применения жестких условий реакции и токсичных реагентов. 6 з.п. ф-лы, 8 табл.
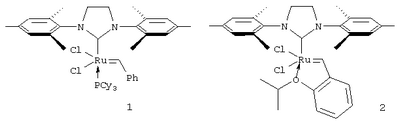
Область техники, к которой относится изобретение Изобретение относится к органическому синтезу и касается способа получения эфиров акриловой кислоты с алифатическими спиртами C1-C4. Уровень техники Известен двухстадийный способ получения акриловой кислоты (акрилатов). На первой стадии осуществляют синтез акриловой кислоты окислением пропилена кислородом воздуха в присутствии катализаторов на основе молибдена. Реакция проводится при температуре 370-425°С, конверсия пропилена составляет 17-26%, выход акриловой кислоты 45-61% (GB 1244184, 1968). На второй стадии проводится этерификация акриловой кислоты спиртами в присутствии кислого катализатора и ингибиторов полимеризации (US 6025520, 2000; US 2004/0019235 A1, 2001; WO 02/055473 A1, 2002). Реакция осуществляется при температуре 90-130°С и мольном соотношении спирт: акриловая кислота = 1:0.5-1:2. Недостатками такого способа получения акрилатов являются жесткие условия (высокая температура) синтеза акриловой кислоты, а также низкая селективность ее получения и невысокая конверсия пропилена. Известен способ синтеза акрилатов карбонилированием ацетилена в присутствие спиртов в условиях реакции Реппе. Реакцию ведут в спирте в присутствии бромида никеля и соединений меди или ртути при 190°С по давлением окиси углерода около 50 атм (GB 824520, 1959). Недостатком этого метода является работа с токсичными соединениями. Известен способ получения акрилатов двухстадийным гидролизом акрилонитрила до акриловой кислоты с последующей ее этерификацией спиртами (RU 2108391, 1998) – прототип. Первая стадия получения акриловой кислоты осуществляется при 90-100°С в растворе 50% серной кислоты течение около 1 часа. В результате получается сульфат акриламида, последующий гидролиз которого ведут при 190°С. Этерификация полученной акриловой кислоты также происходит в присутствие серной кислоты. Акрилонитрил, необходимый для этого процесса, синтезируют окислительным аммонолизом пропилена в присутствии катализатора (молибдаты или фосформолибдаты висмута, молибдаты или вольфраматы теллура и церия, оксиды сурьмы, урана, олова и железа) (US 2004/0248734 A1, 2004). Процесс проводят при 400-485°С. Недостатком данного способа синтеза акрилатов являются жесткие условия получения акрилонитрила (высокая температура), работа с токсичными соединениями, умеренные или низкие выходы продуктов. Раскрытие изобретения Задача, решаемая данным изобретением, состоит в разработке эффективного способа получения акрилатов. Технический результат состоит в получении акрилатов с высокой селективностью без применения жестких условий реакции и токсичных реагентов в ходе осуществления реакции метатезиса малеатов. Технический результат достигается тем, что малеаты подвергают взаимодействию с этиленом в присутствии катализатора метатезиса при температуре от 20°С до 140°С и давлении этилена от 101325 Па (1 атм) до 506625 Па (5 атм) В качестве катализатора метатезиса применяют карбеновые комплексы рутения, содержащие имидазольные лиганды, такие как катализатор Граббса второго поколения (1) или катализатор Ховейды второго поколения (2). Оптимальное соотношение малеат: катализатор составляет от 10000:1 до 25000:1 (соответствует от 0.01 до 0.004 мол.%). При этом сохраняются как достаточно высокое его число оборотов (1740-2780), так и высокий выход акрилатов (11-25%). Увеличение выхода акрилатов за счет снижения скорости образования фумаратов удается достигнуть проведением реакции в отсутствие растворителя. В случае получения метил- и этилакрилатов реакцию можно вести с их отгонкой как при атмосферном, так и при пониженном давлении, которое составляет от 6 кПа до 12 кПа. В обоих случаях также достигается дополнительный технический результат – увеличение выхода целевого продукта за счет увеличения срока жизни (действия) катализатора. Выход акрилатов может быть также повышен путем барбатирования этилена через реакционную смесь со скоростью 1-10 л/ч. Осуществление изобретения Получение акрилатов осуществляют по реакции метатезиса (этенолиза) диалкилмалеатов с этиленом, уравнение которой представлено ниже. Продуктами этой реакции являются акрилаты, которые образуются с селективностью, близкой к 100%. Для осуществления заявленного способа малеаты подвергают взаимодействию с этиленом в присутствии катализатора метатезиса при температуре от 20°С до 140°С и давлении этилена от 101325 Па (1 атм) до 506625 Па (5 атм). Оптимальными условиями являются: температурный интервал 40°С-60°С и давление этилена 101325 Па. При более низких температурах скорость реакции мала, а при повышении температуры значительно возрастает скорость разложения катализатора. Разложению катализатора также способствует увеличение давления этилена, что показано на примере метатезиса диэтилмалеата в присутствии 0.01 мол.% комплекса (2) при 50°С. При давлении этилена 101325 Па и 506625 Па этилакрилат был получен с выходами 17.4% и 9.8% соответственно. Наиболее предпочтительным катализатором является комплекс (2). Так, например, этенолиз диэтилмалеата при 50°С в присутствии 0.01 мол.% (2) приводит к этилакрилату с выходом 17.4%, в то время как в аналогичных условиях, но в присутствии 0.01 мол.% комплекса (1), выход этилакрилата составляет 4.5%. Оптимальное содержание катализатора – 0.004-0.01 мол.%. Увеличение содержания катализатора приводит к более высокому выходу акрилатов, однако при этом существенно снижается его число оборотов (таблица 1).
Выбор оптимальных температурных условий реакции определяется спиртовым заместителем малеата. В случае синтеза этилакрилата из диэтилмалеата оптимальной температурой этенолиза является 50°С (таблицы 2 и 3). Оптимальной температурой этенолиза дибутилмалеата является 40°С (таблицы 4 и 5). Для диметилмалеата также наиболее предпочтительно проводить этенолиз при температуре около 40-50°С (таблицы 6 и 7).
По сравнению с метатезисом диэтилмалеата, в реакции с дибутилмалеатом катализатор действует более продуктивно – максимально достигнутое число его оборотов в этом случае составило 2540 (в присутствии 0.01 мол.% комплекса 2, таблица 5). Близкое значение продуктивности катализатора было получено и в реакции с диметилмалеатом – 2630 оборотов (таблица 7). Для диэтилмалеата в присутствие того же количества катализатора (2) его продуктивность составила 1740 оборотов (таблица 3). Следует отметить, что увеличение температуры от 40 до 90°С в реакции этенолиза как диэтил-, так и дибутилмалеата приводит к существенному снижению его продуктивности. При этом частота оборотов катализатора в обоих случаях возрастает в 1.5-2 раза. Этот результат связан с уменьшением времени жизни катализатора (таблицы 3 и 5). В случае этенолиза диметилмалеата изменение температуры влияет лишь на время жизни катализатора и его продуктивность. Влияние температуры на частоту оборотов катализатора здесь незначительно (таблиц 6 и 7). Помимо давления этилена и температуры на время жизни катализатора также в значительной степени влияет образующийся в процессе реакции акрилат. По мере его накопления скорость разложения катализатора возрастает. В связи с этим, для увеличения выхода продукта, можно отгонять его из реакционной смеси. Реакционная установка для проведения синтеза акрилатов с отгонкой продукта из реакционной смеси представляет собой колбу Кляйзена с 10-см дефлегматором, в которую помещают смесь малеата с катализатором. Вместо колбы Кляйзена может использоваться двухгорлая колба подходящего объема (зависит от количества реакционной смеси), к которой подсоединяют капилляр для ввода этилена и насадку для перегонки с 10-см дефлегматором, нисходящим холодильником и охлаждаемым приемником. Нагрев реакционной смеси обеспечивают с помощью термостата или масляной бани. Ввод этилена в реакционную смесь осуществляют через стеклянный или металлический капилляр. С целью уменьшения потерь акрилата, связанных с уносом из установки током этилена, приемник охлаждают до -30°С. В качестве охлаждающей смеси может использоваться любая подходящая, например, лед – CaCl2, сухой лед – ацетон, жидкий азот – спирт и другие. Поскольку акрилаты при атмосферном давлении кипят выше оптимальной температуры для проведения метатезиса, реакцию проводят в вакууме, благодаря чему температура кипения акрилатов снижается. Давление в установке определяется используемым малеатом и подбирается так, что бы продукт реакции кипел около 30°С, а исходный олефин около 125-130°С. В этих условиях достигается быстрое и эффективное удаление образующегося акрилата из реакционной смеси с минимальным переносом реагента. Для синтеза этилакрилата, температура кипения которого при атмосферном давлении 100°С, оно составляет 6 кПа. Получение метилакрилата (т.кип. 80°С) проводят при давлении 12 кПа. Время реакции составляет около 6 часов и обусловлено временем жизни катализатора. Метатезис диэтилмалеата в описанной установке в присутствии 0.004 мол.% комплекса (2) приводит к этилакрилату с выходом 19.2%, что соответствует числу оборотов катализатора 4800 TON (число продуктивных каталитических циклов, осуществляемых одной молекулой катализатора). Полученный продукт, судя по данным ГЖХ, содержит менее 0.3% диэтилмалеата. Кубовый остаток по данным ГЖХ содержит менее 0.9% этилакрилата, непрореагировавший диэтилмалеат и диэтилфумарат, присутствующий в коммерческом диэтилмалеате. Массовый баланс составляет 97.8%. В аналогичных условиях метилакрилат был получен с выходом 10.0%, что соответствует 2500 оборотов катализатора. Падение продуктивности в этом случае по сравнению с синтезом этилакрилата, вероятно, связано с низкой растворимостью этилена в диметилмалеате. По данным ГЖХ полученный продукт содержит менее 0.8% диметилмалеата. Кубовый остаток состоит из непрореагировавшего диметилмалеата, диметилфумарата, присутствующему в коммерческом диметилмалеате и менее 0.4% метилакрилата. Массовый баланс составляет 96.8%. Применение предложенного метода для синтеза более тяжелых эфиров акриловой кислоты неэффективно, так как из-за их более высоких температур кипения (по сравнению с метил- и этилакрилатом) для отгонки продукта из реакционной смеси требуется давление менее 2.5 кПа. В этих условиях растворимость этилена в субстрате очень низкая и скорость реакции мала. Благодаря достаточно низкой температуре кипения метилметакрилата, его синтез с отгонкой можно осуществлять также при атмосферном давлении, что существенно упрощает осуществление заявленного способа, а также при этом значительно сокращается его время (с 6 часов до 30 минут). Реакцию ведут в установке, в которой вместо вакуумного насоса к выходу из прибора подсоединяется ловушка, охлаждаемая до -30°С. Температуру реакционной смеси во время проведения эксперимента поддерживают около 120°С. При меньшей температуре удаление образующегося метилакрилата неэффективно, а при большей существенно сокращается время жизни катализатора. Дефлегматор в установке для синтеза метилакрилата при атмосферном давлении должен быть минимальным или отсутствовать вовсе. В противном случае скорость отгонки снижается, что способствует сокращению времени жизни катализатора. Продуктивность катализатора в этом случае ниже, чем при проведении реакции в вакууме. Она возрастает с увеличением скорости подачи этилена в реакционную смесь (таблица 8), однако при этом также снижаются чистота получаемого продукта и массовый баланс реакции.
Для всех малеатов селективность реакции по акрилатам как при осуществлении способа без отгонки продукта, так и с его отгонкой, близка к 100%. Изобретение иллюстрируется следующими примерами. Пример 1. Метатезис малеатов с этиленом проводят по стандартным методикам в условиях, исключающих попадание влаги и воздуха в реакционную систему используя реакторы Шленка, подсоединенные к вакуумной и этиленовой линиям. Этилен полимеризационной чистоты (ГОСТ 25070-87) перед использованием высушивают, последовательно пропуская через колонны, наполненные окисью алюминия и цеолитом 13Х, прокаленными при 400°С. Коммерческие диэтилмалеат (97%, фирмы “Aldrich”), диметилмалеат (96%, фирмы “Acros”) и дибутилмалеат (97%, фирмы “Acros”) очищают перегонкой в вакууме и высушивают над молекулярными ситами А4. Анализ реакционных смесей ведут методом ГЖХ, отбирая 0.1 мл реакционной смеси и обрабатывая ее 1 мл винилэтилового эфира с целью дезактивирования активных каталитических частиц. При вычислении выхода продукта используются калибровочные коэффициенты, полученные из анализа искусственных смесей соответствующих акрилатов, малеатов и фумаратов с последующим пересчетом отношений площадей на хроматограмме к массовым соотношениям составных компонентов. В колбу Шленка на 25 мл, снабженную магнитной мешалкой, помещают 11.91 г (69.2 ммоль) диэтилмалеата и замораживают жидким азотом, после чего вакуумируют до 0.1 Па. Операцию дегазации повторяют два раза. Вакуум перекрывают, реакционной смеси дают нагреться до комнатной температуры и в реакционную колбу вводят этилен, создавая давление 101325 Па, после чего смесь нагревают до 50°С. Далее в реакционную смесь вводят суспензию 4.70 мг катализатора (2) в 1.00 г (5.8 ммоль) диэтилмалеата. Контроль за ходом реакции осуществляют методом ГЖХ через 10, 20, 30, 45, 60 минут после начала эксперимента и далее через каждые 30 минут до завершения реакции (таблицы 1, 2 и 3, примеры 2). Пример 2. Метатезис диэтилмалеата с этиленом проводят по примеру 1, но при температуре 40°С. Результаты представлены в таблицах 2 и 3, примеры 1. Пример 3. Метатезис диэтилмалеата с этиленом проводят по примеру 1, но при температуре 60°С. Результаты представлены в таблицах 2 и 3, примеры 3. Пример 4. Метатезис диэтилмалеата с этиленом проводят по примеру 1, но при температуре 70°С. Результаты представлены в таблицах 2 и 3, примеры 4. Пример 5. Метатезис диэтилмалеата с этиленом проводят по примеру 1, но при температуре 80°С. Результаты представлены в таблицах 2 и 3, примеры 5. Пример 6. Метатезис диэтилмалеата с этиленом проводят по примеру 1, но при температуре 90°С. Результаты представлены в таблицах 2 и 3, примеры 6. Пример 7. Метатезис диэтилмалеата с этиленом проводят по примеру 1, но используя 9.40 мг катализатора (2) (таблица 1, пример 1). Пример 8. Метатезис диэтилмалеата с этиленом проводят по примеру 1, но используя 3.13 мг катализатора (2) (таблица 1, пример 3). Пример 9. Метатезис диэтилмалеата с этиленом проводят по примеру 1, но используя 1.88 мг катализатора (2) (таблица 1, пример 4). Пример 10. Метатезис диэтилмалеата с этиленом проводят по примеру 1, но используя 6.37 мг катализатора (1). Выход этилакрилата составил 4.5%. Пример 11. Метатезис диэтилмалеата с этиленом при давлении этилена выше атмосферного проводят в автоклаве Parr объемом 75 мл, используя те же реактивы, что в примере 1. Анализ реакционной смеси и вычисление выхода этилакрилата осуществляют по примеру 1. В продутый этиленом автоклав помещают 11.91 г (69.2 ммоль) диэтилмалеата. Реакционную смесь нагревают до 50°С и в реактор сразу вводят суспензию 4.70 мг катализатора (2) в 1.00 г (5.8 ммоль) диэтилмалеата, после чего давление этилена в автоклаве увеличивают до 506625 Па. Реакционную смесь перемешивают при 50°С в течение 2 часов. Контроль за ходом реакции осуществляют методом ГЖХ. Выход этилакрилата составил 9.8%. Пример 12. Метатезис дибутилмалеата с этиленом проводят по примеру 1, используя 16.12 г (70.6 ммоль) дибутилмалеата. Катализатор добавляют в 1.00 г (4.4 ммоль) дибутилмалеата. Результаты эксперимента представлены в таблицах 4 и 5, примеры 3. Пример 13. Метатезис дибутилмалеата с этиленом проводят по примеру 12, но при температуре 23°С. Результаты эксперимента представлены в таблицах 4 и 5, примеры 1. Пример 14. Метатезис дибутилмалеата с этиленом проводят по примеру 12, но при температуре 40°С. Результаты эксперимента представлены в таблицах 4 и 5, примеры 2. Пример 15. Метатезис дибутилмалеата с этиленом проводят по примеру 12, но при температуре 60°С. Результаты эксперимента представлены в таблицах 4 и 5, примеры 4. Пример 16. Метатезис дибутилмалеата с этиленом проводят по примеру 12, но при температуре 70°С. Результаты эксперимента представлены в таблицах 4 и 5, примеры 5. Пример 17. Метатезис дибутилмалеата с этиленом проводят по примеру 12, но при температуре 80°С. Результаты эксперимента представлены в таблицах 4 и 5, примеры 6. Пример 18. Метатезис дибутилмалеата с этиленом проводят по примеру 12, но при температуре 90°С. Результаты эксперимента представлены в таблицах 4 и 5, примеры 7. Пример 19. Метатезис диметилмалеата с этиленом проводят по примеру 1, используя 9.81 г (68.1 ммоль) диметилмалеата. Катализатор добавляют в 1.00 г (6.9 ммоль) диметилмалеата. Результаты эксперимента представлены в таблицах 6 и 7, примеры 2. Пример 20. Метатезис диметилмалеата с этиленом проводят по примеру 19, но при температуре 40°С. Результаты эксперимента представлены в таблицах 6 и 7, примеры 1. Пример 21. Метатезис диметилмалеата с этиленом проводят по примеру 19, но при температуре 60°С. Результаты эксперимента представлены в таблицах 6 и 7, примеры 3. Пример 22. Метатезис диметилмалеата с этиленом проводят по примеру 19, но при температуре 70°С. Результаты эксперимента представлены в таблицах 6 и 7, примеры 4. Пример 23. Метатезис диметилмалеата с этиленом проводят по примеру 19, но при температуре 80°С. Результаты эксперимента представлены в таблицах 6 и 7, примеры 5. Пример 24. Метатезис диэтилмалеата с этиленом в условиях отгонки образующегося этилакрилата проводят в установке с объемом перегонной колбы 25 мл. В установку помещают 12.91 г (75 ммоль) диэтилмалеата и 1.88 мг (0.003 ммоль, 0.004 мол.%) катализатора (2). Реакционную смесь замораживают жидким азотом и вакуумируют через выход из аллонжа до 0.1 Па. Далее вакуум перекрывают и реакционной смеси дают нагреться до комнатной температуры. Операцию дегазации повторяют два раза, после чего в реакционную смесь через металлический каппиляр вводят ток аргона. Установку помещают в масляную баню с температурой 60-65°С, вакуумируют до 6 кПа и ток аргона сменяют на ток этилена. Приемник охлаждают до -30°С с помощью смеси спирт – жидкий азот. Реакцию ведут в течение 6 часов. Получают 2.89 г этилакрилата в виде бесцветной жидкости. Выход 19.2%. Продукт, судя по данным ГЖХ, содержит менее 0.3% диэтилмалеата. Кубовый остаток представляет собой смесь диэтилмалеата, диэтилфумарата и, судя по данным ГЖХ, содержит менее 0.9% этилакрилата. Масса кубового остатка 10.16 г. Массовый баланс составляет 97.8%. Пример 25. Синтез метилакрилата ведут по примеру 24, используя 10.81 г (75 ммоль) диметилмалеата. Давление в реакционной установке поддерживают 12 кПа. По окончании реакции получают 1.30 г метилакрилата в виде бесцветной жидкости. Выход 10.0%. Продукт, судя по данным ГЖХ, содержит менее 0.8% диметилмалеата. Кубовый остаток представляет собой смесь диметилмалеата, диметилфумарата и, судя по данным ГЖХ, содержит менее 0.4% метилакрилата. Масса кубового остатка 9.38 г. Массовый баланс составляет 96.8%. Пример 26. Получение метилакрилата по реакции метатезиса диметилмалеата с этиленом в условиях отгонки образующегося продукта при атмосферном давлении ведут в установке с объемом перегонной колбы 15 мл, не содержащей дефлегматор и включающей ловушку, подсоединенную к выходу из аллонжа вместо вакуумного насоса. В описанную установку помещают 9.81 г (68.1 ммоль) диметилмалеата. Шлиф, через который подсоединяют капилляр для ввода этилена, закрывают септой. Перегонную колбу с помещенным в нее малеатом замораживают жидким азотом и вакуумируют до 0.1 Па. Далее вакуум перекрывают и реакционной смеси дают нагреться до комнатной температуры. Операцию дегазации повторяют два раза, после чего через септу вводят металлический капилляр до дна перегонной колбы и установку заполняют этиленом, очищенным по примеру 1. Скорость потока этилена устанавливают 4.3 л/ч. Реакционную смесь нагревают с помощью масляной бани до 120°С, после чего с помощью шприца через септу в установку вводят суспензию 4.70 мг катализатора (2) в 1.00 г (6.9 ммоль) диметилмалеата. Реакцию ведут в течение 30 минут. Приемник и ловушку охлаждают до -30°С с помощью смеси спирт – жидкий азот. Массовый баланс, выход и чистота продукта представлены в таблице 8. Кубовый остаток, судя по данным ГЖХ, содержал менее 1% метилакрилата. Пример 27. Метилакрилат синтезируют по примеру 26, но при скорости потока этилена 7.0 л/ч. Массовый баланс, выход и чистота продукта представлены в таблице 8. Кубовый остаток, судя по данным ГЖХ, содержал менее 0.1% метилакрилата. Пример 28. Метилакрилат синтезируют по примеру 26, но при скорости потока этилена 10.0 л/ч. Массовый баланс, выход и чистота продукта представлены в таблице 8. Кубовый остаток, судя по данным ГЖХ, содержал только диметилмалеат и диметилфумарат, присутствующий в коммерческом диметилмалеате. Промышленная применимость Производство акрилатов по реакции метатезиса олефинов представляет интерес для промышленности благодаря низкой себестоимостью и доступности исходных соединений, а также мягкости условий и высокой селективности реакции. Предложенный в изобретении метод позволяет получать акрилаты, исходя из малеатов и этилена. При этом существенно упрощается технология получения этих соединений за счет применения более мягких условий реакции, нетоксичных реагентов, исключения из процесса легкополимеризующихся акрилонитрила и акриловой кислоты, а также исключения стадий их получения, протекающих в жестких условиях. Селективность получения акрилатов по заявленному способу близка к 100%.
Формула изобретения
1. Способ получения эфиров акриловой кислоты, заключающийся в том, что эфиры малеиновой кислоты с алифатическими спиртами С1-С4 подвергают взаимодействию с этиленом в присутствии катализатора метатезиса при температуре от 20 до 140°С, давлении этилена от 101325 до 506625 Па. 2. Способ по п.1, отличающийся тем, что в качестве катализатора метатезиса используют катализатор Ховейды второго поколения. 3. Способ по п.1, отличающийся тем, что соотношение эфир малеиновой кислоты: катализатор составляет от 10000:1 до 25000:1. 4. Способ по п.1, отличающийся тем, что взаимодействие эфиров малеиновой кислоты и этилена осуществляют в отсутствии растворителя. 5. Способ по п.1, отличающийся тем, что взаимодействие метилового или этилового эфира малеиновой кислоты осуществляют одновременно с отгонкой образующегося эфира акриловой кислоты. 6. Способ по п.1, отличающийся тем, что взаимодействие с этиленом осуществляют путем его барбатирования со скоростью потока 1-10 л/ч. 7. Способ по п.1, отличающийся тем, что взаимодействие выполняют при температуре от 40 до 60°С.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||