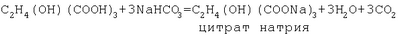Патент на изобретение №2306135
|
||||||||||||||||||||||||||
(54) СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЗАДЕРЖАНИЯ ПОСЛЕДА И ЭНДОМЕТРИТА У ЖИВОТНЫХ ПЕНООБРАЗУЮЩИМ ПРЕПАРАТОМ
(57) Реферат:
Изобретение относится к ветеринарной медицине. Способ включает введение во влагалище или матку пенообразующего препарата следующего состава, г (%): калий йодистый – 1,5 (5,8), фурацилин – 0,5 (1,9), левомицетин, левомицетин стеарат или бициллин – 1,5 (5,8), натрий бикарбонат – 9,1 (35,2), крахмал картофельный – 4,9 (18,9), кислота лимонная – 7,0 (27,0), стеарат кальция – 0,2 (0,7), 20%-ный спиртовой свежий раствор эмульгатора – 1,2 (4,7). Способ эффективен при профилактике и лечении задержания последа и эндометрита у животных.
Предлагаемее изобретение относится к ветеринарной медицине, конкретно к способам профилактики и лечения задержаний последов и эндометритов у коров. Известны разработанные в СКЗНИВИ В.Ф.Шаталовым, Е.Е.Нехаевым, широко опробированные в практике, но не защищенные охранным документом свечи маточные пенообразующие (3). В их состав входят лекарственные вещества (например, бриллиантовый зеленый, фурацилин и др.), наполнитель (крахмал картофельный), пенообразующие вещества (лимонная кислота, натрия бикарбонат), стабилизаторы пены (кальция стеарат 20%-ный спиртовой раствор эмульгатора МГД-2). Основные недостатки их следующие: а) пенообразующие вещества находятся в соотношении почти 1:1, дают при взаимодействии с влагой жидкость кислой реакции (рН 4,5-5), губительно действующей на больные клетки больного органа; б) лекарственные вещества действуют губительно на немногие виды микроорганизмов. Эти недостатки ликвидированы в предлагаемом составе свечей. Цель изобретения – повышение бактериостатического и бактериолитического действия препарата. Поставленная цель достигается тем, что в состав препарата введен широкого действия антибиотик левомицетин при следующем соотношении компонентов, г (%): калий йодистый – 1,5 (5,8), фурацилин – 0,5 (1,9), левомицетин – 1,5 (5,8), натрий бикарбонат – 9,1 (35,2), крахмал картофельный – 4,9 (8,9), кислота лимонная – 7,0 (27,0), стеарат кальция – 0,2 (0,7), 20%-ный спиртовой свежий раствор эмульгатора МГД-2 или другого равнозначного – 1,2 (4,7), при этом вместо левомицетина может быть левомицетин стеарат, бициллин, стрептомицин + пенициллин в лечебной дозе, к тому же пенообразующий препарат в виде свечи или смеси сухих веществ должен быть герметически упакован. Технология приготовления препарата: – все входящие в состав кристаллические вещества измельчают до аморфного состояния, просеивают через сито с ячейками до 0,5 мм; – при измельчении калия йодистого добавляют крахмал картофельный в соотношении 2:1; – в смеситель вносят смесь калия йодистого с крахмалом картофельным, фурацилин, левомицетин, натрия бикарбонат, остаток крахмала картофельного, кислоту лимонную, стеарат кальция; – однородную сухую смесь перемешивают с 20%-ным свежим спиртовым раствором эмульгатора до получения однородной равномерно овлажненной смеси. После суточного высушивания тонким слоем при температуре 20-25°С сухую смесь просеивают через сито с ячейками до 0,5 мм, комочки измельчают и высыпают в смесь; – полученный исходный материал можно расфасовывать в гнезда ленты полиэтиленовой или прессовать свечи. Учитывая гигроскопичность калия йодистого и др. ингридиентов, смесь сухих веществ и свечи пенообразующие герметически закрывают, хранят их в темном сухом месте при температуре до 25°С до 2-х лет. Фармакодинамика компонентов препарата: – калий йодистый – белый кристаллический порошок без запаха, хорошо растворим в воде (1:0,75), гигроскопичен, не содержит свободного йода, не раздражает нервные окончания тканей, не оказывает бактерицидного действия. После быстрого всасывания изменяется в организме с образованием различных соединений йода, входящих в состав гормонов щитовидной железы, регулирующих белковый обмен веществ, активизирующих деятельность защитных и буферных систем организма, действующих бактерицидно, противовоспалительно (2, с.323); – фурацилин – желтый или зеленовато-желтый порошок, мало растворимый в воде 1:4200 (1, с.299), но лучше в изотоническом (0,9%-ном) растворе натрия хлористого 1:420 (2, с.433), в жидкой среде действует губительно на грамположительные и на грамотрицательные бактерии (1, с.300; 2, с.433); – левомицетин – белый или со слабым желтовато-зеленоватым оттенком кристаллический порошок – антибиотик широкого спектра действия, эффективен в отношении многих грамположительных и грамотрицательных бактерий, действует губительно на штаммы бактерий, устойчивых к пенициллину, стрептомицину, сульфаниламидным препаратам. Механизм его антимикробного действия связан с нарушением синтеза белков микроорганизмом. Левомицетин легко всасывается, максимальная его концентрация в крови создается через 2-3 часа, удерживается после однократного введения со свечой или раствором в течение 4-5 часов. Выводится левомицетин из организма в основном с мочой. Таким образом левомицетин действует на микроорганизмы непосредственно или опосредованно через организм животного; – натрий бикарбонат (м.м.84) – белый кристаллический порошок без запаха, хорошо растворим в воде 1:12 с образованием щелочного раствора, при взаимодействии с кислотами образует пенистые растворы с выделением углекислоты (СО2). После всасывания в кровь животного натрия бикарбонат входит в состав буферных систем, нейтрализует кислые вещества обмена и воспалительного очага, смягчает действие недоокисленных ядовитых и вредных веществ воспалительного эксудата, оказывает противовоспалительное и противопаразитарное действие (2-й, с.341-343); – крахмал картофельный – белый мучнистый, без запаха и вкуса, мелкоструктурный, скрепящий между пальцами нерастворимый в холодной воде порошок. В препарате используется как вещество, адсорбирующееся на поверхностях гигроскопических веществ, как формообразующееся вещество (2, с.196); – кислота лимонная (м.м. 192, 13) – крупнокристаллический порошок, хорошо растворимый в воде, при взаимодействии с натрием бикарбонатом во взятом в прописи соотношении образует пенистый раствор щелочной реакции (рН 7,5-8,0). Взаимодействие лимонной кислоты и бикарбоната натрия в водной среде будет протекать следующим образом: Цитрат натрия (лимоннокислый натрий) имеет щелочную реакцию, взаимодействует с кислыми веществами воспалительного очага и нейтрализует их при взаимодействии с кальцием крови капилляров, образует соли, предотвращающие ее свертывание, и этим способствует притоку артериальной крови в воспаленный участок или орган; – стеарат кальция и эмульгатор МГД-2 или другой равнозначный используются в препарате (пенообразующей свече) как формообразующее вещество и как вещества, предотвращающие быстрый распад пенистой массы. Таким образом вещества препарата оказывают как местное, так и общее действие, активизируя деятельность гормональных, буферных и др. систем организма. Предварительные эксперименты оценки деятельности препарата дали вполне обнадеживающие результаты после введения в полость больного органа (влагалища, матки) свечей или смесей сухих веществ. Литература 1. Машковский М.Д. Лекарственные вещества. М., “Медицина”, 1987 г., т.1-й, стр.365, т.2-й, стр.106, 112, 132, 299, 343, 390. 2. Мозгов И.Е. Фармакология. М., “Сельхозиздат”, 1954 г., с.196, 323, 341, 346, 433, 480. 3. Шаталов В.Ф., Нехаев Е.Е. и др. Рекомендации по диагностике, лечению и профилактике эндометритов у коров. Новочеркасск, 1939 г., с.12.
Формула изобретения
Способ профилактики и лечения задержания последа и эндометрита у животных пенообразующим препаратом, включающий введение во влагалище или матку пенообразующего препарата, отличающийся тем, что вводимый препарат содержит, г (%): калий йодистый – 1,5 (5,8), фурацилин – 0,5 (1,9), левомицетин, левомицетин стеарат или бициллин – 1,5 (5,8), натрий бикарбонат – 9,1 (35,2), крахмал картофельный – 4,9 (18,9), кислоту лимонную – 7,0 (27,0), стеарат кальция – 0,2 (0,7), 20%-ный спиртовой свежий раствор эмульгатора – 1,2 (4,7).
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 13.09.2008
Извещение опубликовано: 27.07.2010 БИ: 21/2010
|
||||||||||||||||||||||||||