Патент на изобретение №2304581
|
|||||||||||||||||||||||||||||||||
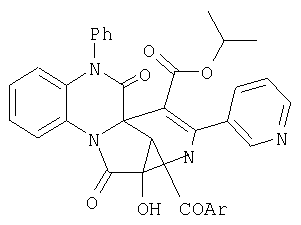
(54) ИЗОПРОПИЛ 12-АРОИЛ-2-ГИДРОКСИ-1,6-ДИОКСО-4-(3-ПИРИДИНИЛ)-7-ФЕНИЛ 1,3,6,7-ТЕТРАГИДРО-2,5
(57) Реферат:
Изобретение относится к области органической химии, а именно к новым индивидуальным соединениям класса 2,5
где Ar = фенил или n-метоксифенил
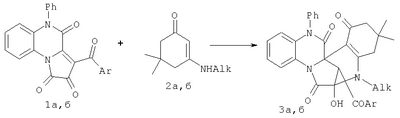
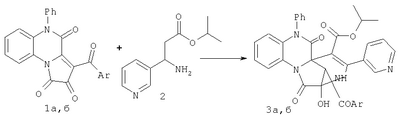
Изобретение относится к области органической химии, а именно к новым индивидуальным соединениям класса 2,5 Известны структурные аналоги заявленных соединений, получаемые взаимодействием 3-ароил-5-фенилпирроло[1,2- где Ar=4-BrC6Н4 и Alk=СН2СН=СН2 (3а) или Ar=4-МеОС6Н4 и Alk=CH2Ph (3б). К недостаткам данного способа относится невозможность получения изопропил 12-ароил-2-гидрокси-1,6-диоксо-4-(3-пиридинил)-7-фенил-1,3,6,7-тетрагидро-2,5 Задачей изобретения является разработка простого способа синтеза не описанных в литературе изопропил 12-ароил-2-гидрокси-1,6-диоксо-4-(3-пиридинил)-7-фенил-1,3,6,7-тетрагидро-2,5 Поставленная задача осуществляется путем кипячения 3-ароил-5-фенилпирроло[1,2- где Ar=Ph (1a, 3а) или Ar=p-СН3ОС6Н4 (1б, 3б). Процесс ведут при температуре 99-101°С, а в качестве растворителя используют абсолютный диоксан. Из патентной и технической литературы не были выявлены способы получения изопропил 12-ароил-2-гидрокси-1,6-диоксо-4-(3-пиридинил)-7-фенил-1,3,6,7-тетрагидро-2,5 Изобретение иллюстрируется следующими примерами. Пример 1. Изопропил 12-бензоил-2-гидрокси-1,6-диоксо-4-(3-пиридинил)-7-фенил-1,3,6,7-тетрагидро-2,5 К раствору 1.8 г (0.0045 моль) 3-бензоил-5-фенилпирроло[2,1- Найдено, %: С 69.98; Н 4.81; N 9.30. Вычислено, %: С 69.99; Н 4.79; N 9.33. Пример 2. Изопропил 2-гидрокси-1,6-диоксо-12-n-метоксибензоил-4-(3-пиридинил)-7-фенил-1,3,6,7-тетрагидро-2,5 К раствору 1.9 г (0.0045 моль) 3-n-метоксибензоил-5-фенилпирроло[2,1- Найдено, %: С 68.59; Н 4.77; N 8.89. Вычислено, %: С 68.56; Н 4.79; N 8.88. Соединения (3а, б) – бесцветные кристаллические вещества, легкорастворимые в ДМСО и ДМФА, труднорастворимые в обычных органических растворителях, нерастворимые в воде и алканах; устойчивы при хранении в обычных условиях. В ИК спектрах соединений (3а, б), снятых в виде пасты в вазелиновом масле, присутствуют полосы валентных колебаний групп ОН и NH в виде широкой полосы в области 3130-3140 см-1, лактамной карбонильной группы С1=О и изопропоксикарбонильной группы в области 1716-1720 см-1, лактамной карбонильной группы С6=О в области 1680-1685 см-1, ароильной группы в области 1668-1670 см-1. В спектрах 1Н ЯМР растворов соединений (3а, б) в ДМСО-d6, кроме сигналов протонов ароматических заместителей и связанных с ними групп, присутствуют дублеты протонов двух метильных групп (0.47-0.48 м.д. и 0.72-0.73 м.д.) и мультиплет протона (4.48 м.д.) изопропильного фрагмента, синглет метинового протона Н12 (4.97-5.03 м.д.), уширенный синглет протона гидроксильной группы (7.33 м.д.). Из группы сигналов ароматических протонов в сильное поле (6.32 м.д.) смещается дублет протона Н8, экранированного Предлагаемый способ прост в осуществлении, одностадиен и позволяет получить не описанные в литературе изопропил 12-ароил-2-гидрокси-1,6-диоксо-4-(3-пиридинил)-7-фенил-1,3,6,7-тетрагидро-2,5 Пример 3. Фармакологическое исследование изопропил 12-ароил-2-гидрокси-1,6-диоксо-4-(3-пиридинил)-7-фенил-1,3,6,7-тетрагидро-2,5 Исследование противомикробной активности соединений (3а, б) проводили методом двукратных серийных разведений согласно общепринятым методам (Методы экспериментальной химиотерапии, под ред. Г.Н.Першина, М., Мед., 1971). В качестве тест-культур использовали музейные штаммы: золотистый стафилококк (St aureus), 906; кишечная палочка (Е. Coli), 25922. Готовили серийные разведения препаратов в питательной жидкой среде. Максимальная концентрация составила 1000 мк/мл или 0.1%. Приготовленную по стандарту мутности микробную взвесь (25×104 в 1 мл) вносили в приготовленные серийные разведения препаратов. После 18-20-часового термостатирования при 37°С регистрировали ингибирующее действие, через 7 суток – бактерицидное действие препаратов.
Проведенные исследования показали (табл.1): обнаружено ингибирующее действие соединения 3а в отношении золотистого стафилококка в концентрации 1000.0 мкг/мл, в отношении кишечной палочки – в концентрации <1000.0>500.0 мкг/мл. Бактерицидными свойствами в испытанных концентрациях соединение За не обладает. Соединение 3б не обладает антимикробным действием в испытанных концентрациях.
Формула изобретения
1. Изопропил 12-ароил-2-гидрокси-1,6-диоксо-4-(3-пиридинил)-7-фенил-1,3,6,7-тетрагидро-2,5
где Ar фенил или n – метоксифенил. 2. Способ получения изопропил 12-ароил-2-гидрокси-1,6-диоксо-4-(3-пиридинил)-7-фенил-1,3,6,7-тетрагидро-2,5 3. Способ по п.2, отличающийся тем, что процесс ведут при температуре 99-101°С. 4. Способ по любому из пп.2 и 3, отличающийся тем, что в качестве растворителя используют абсолютный диоксан.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 04.07.2008
Извещение опубликовано: 20.05.2010 БИ: 14/2010
|
|||||||||||||||||||||||||||||||||

 ]quinoxaline-1,2,4-triones», Mendeleev Communications, 2005, 4, 163-164. CHRISTELLE P. ET ALL, «One-pot stereoselective synthesis of dimethanodibenzo[e,i][1,4]diazecines by a zinc-acetic acid promoted cascade reaction », Tetrahedron, 1999, 55, №30, 9233-9244.
]quinoxaline-1,2,4-triones», Mendeleev Communications, 2005, 4, 163-164. CHRISTELLE P. ET ALL, «One-pot stereoselective synthesis of dimethanodibenzo[e,i][1,4]diazecines by a zinc-acetic acid promoted cascade reaction », Tetrahedron, 1999, 55, №30, 9233-9244.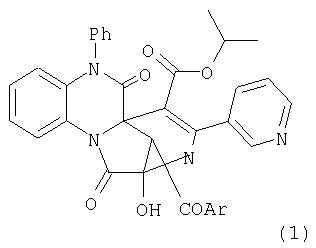
 -электронами бензольного кольца заместителя у атома азота N7, а в слабое поле – синглет протона Н2
-электронами бензольного кольца заместителя у атома азота N7, а в слабое поле – синглет протона Н2 (8.45-8.56 м.д.) и дублет протона Н6
(8.45-8.56 м.д.) и дублет протона Н6