Патент на изобретение №2303025
|
||||||||||||||||||||||||||||||||||
(54) 2,2,5,5-ТЕТРАБРОМ-1,6-ДИ-(41-МЕТИЛФЕНИЛ)-1,3,4,6-ГЕКСАНТЕТРАОН (I), ОБЛАДАЮЩИЙ ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ
(57) Реферат:
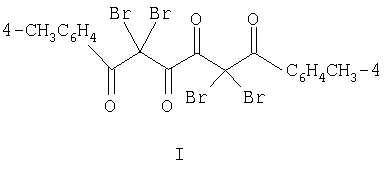
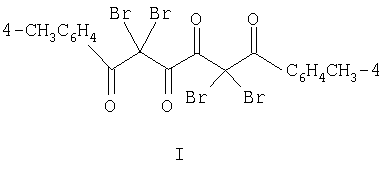
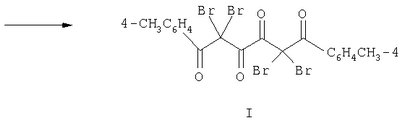
Изобретение относится к новому 2,2,5,5-тетрабром-1,6-ди-(41-метилфенил)-1,3,4,6-гексантетраону формулы (I)
который обладает противомикробной активностью. Соединение (I) получают взаимодействием 3,4-дигидрокси-1,6-ди-(41-метилфенил)-2,4-гексадиен-1,6-диона с бромом в среде хлороформа. Соединение (I) обладает противомикробной активностью по отношению к золотистому стафилококку с МПК 0,0075-0,06 мкг/мл, к кишечной палочке 0,12-0,32 мкг/мл при острой токсичности ЛД50 2960 мг/мл. 1 табл.
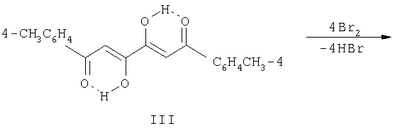
Изобретение относится к области органической химии, к производным поликарбонильных соединений, а именно к новым биологически активным веществам – 2,2,5,5-тетрабром-1,6-ди-(41-метилфенил)-1,3,4,6-гексантетраону формулы (I):
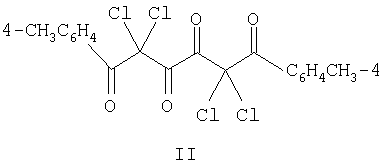
который может найти применение в медицине в качестве лекарственного противомикробного препарата. Ближайшим структурным аналогом заявляемому соединению является 1,6-ди-(41
обладающий противомикробной активностью. В качестве эталона сравнения нами взяты противомикробные препараты – диоксидин [Машковский М.Д. Лекарственные средства. М.: Новая волна, 2000, Т.2, с.298-299] и флуконазол [там же, с.361-362], широко применяемые в лечебной практике. Цель данного изобретения – синтез не описанного ранее 2,2,5,5-тетрабром-1,6-ди-(41-метилфенил)-1,3,4,6-гексантетраона, обладающего противомикробным действием. Поставленная цель достигается получением 2,2,5,5-тетрабром-1,6-ди-(41-метилфенил)-1,3,4,6-гексантетраона реакцией 3,4-дигидрокси-1,6-ди-(41 Пример получения заявляемого соединения (I) К смеси 0,64 г (0,002 моль) 3,4-дигидрокси-1,6-ди-(41-метилфенил)2,4-гексадиен-1,6-диона и 1 г натрия карбоната в 80 мл хлороформа прикапывают 1,28 г (0,008 моль) брома в 20 мл хлороформа. Перемешивают на магнитной мешалке в течение 2 ч до обесцвечивания раствора. Раствор отфильтровывают и упаривают. Сухой остаток перекристаллизовывают из толуола. Получают 0,82 г (64%) кристаллического соединения (I) с Тпл. 203-204 (разл). C18H8Br6О4. ИК спектр, Полученное соединение (I) представляет собой желтое кристаллическое вещество, растворимое в диметилсульфоксиде и диметилформамиде, труднорастворимое в хлороформе, толуоле, нерастворимое в гексане и воде. Заявленное соединение было исследовано на наличие у него противомикробной активности. Определение бактериостатической активности проводили методом двукратных серийных разведений в жидкой питательной среде [Руководство по экспериментальному (доклиническому) изучению новых фармакологических веществ. – М., 2000, с.264-273]. Для всех исследуемых соединений были определены МПК в отношении фармакопейных штаммов: S. aureus ATCC 6538-Р, E.coli ATCC 25922, С. albicans ATCC 885-653, Р. aerugenosa ATCC 9027. Посевы производили в мясопептонный бульон, рН 7,0 с различной концентрацией испытуемых соединений. Культуры выращивали в пробирках на скошенной агаризированной среде (мясопептонный агар). Для определения противомикробной активности использовалась 18-20-часовая культура. Для приготовления рабочей взвеси микробов производили смыв выросшей культуры изотоническим раствором натрия хлорида и устанавливали плотность микробной взвеси по стандарту мутности 5 единиц. Далее из полученной микробной взвеси (500 млн. м.т./мл. готовили рабочий раствор бактерий с концентрацией 5 млн. м.т./мл. Данную взвесь микробов вносили в количестве 0,1 мл в пробирки с серийными разведениями изучаемого препарата. Таким образом, микробная нагрузка при определении ПМА составила 250 000 м.т./мл. Изучаемое соединение в количестве 0,05 г растворяли в 5 мл диметилсульфоксида, 1 мл полученного разведения 1:100 соединяли с 4 мл мясопептонного бульона (1:500). Далее готовили ряд серийных разведений соединения с двукратно уменьшающей концентрацией. Учет результатов производили через 18-20 ч выдержки контрольных и опытных пробирок в термостате при температуре 37°С. Минимальную подавляющую концентрацию (МПК) устанавливали по отсутствию признаков роста на питательной среде: последняя пробирка с задержкой роста (прозрачный бульон) соответствует МПК препарата в отношении данного штамма. Бактериостатический эффект исследуемых соединений сравнивали с действием диоксидина [Падейская Е.Н., Инф. и антимикроб, терап., 2001, №5, с.105-155]. Противогрибковая активность сопоставлялась с действием флуконазола [Rex J.Y., Wals Т.J., Sobel J.D. et all, Clin. Infect/ Dis., 2000, V.30, №4, р.662-668]. Острую токсичность (ЛД50) заявленного соединения изучали на белых лабораторных мышах обоего пола массой 19-20 г. Исследуемое соединение вводили однократно в желудок в виде крахмальной слизи в объеме 1480, 2960, 4440, 5920, 7400 мг/кг соответственно, наблюдение за животными проводили в течение 10 суток. Статистическую обработку результатов проводили по Прозоровскому В.В. сравнением средней смертельной дозы (ЛД50) при Р=0,05 [Прозоровский В.В., Прозоровская М.П., Демченко В.М. Фармакол. и токсикол., 1978, №4, с.497-502]. Результаты исследований представлены в таблице. Как видно из таблицы, соединение (I) превышает по противомикробной активности диоксидин к S.aureus не менее чем в 8330 раза, E.coli – не менее чем в 32,5 раза, P.aerugenosa одинакова. Соединение (I) по противогрибковой активности к C.albicans сопоставим с активностью флуконазола. Соединение (I) по классификации Измерова Н.Ф.[Измеров Н.Ф. Параметры токсикометрии промышленных ядов при однократном введении, М., Медицина, 1977, с.197] относится к классу практически нетоксичных препаратов. Таким образом, 2,2,5,5-тетрабром-1,6-ди-(41-метилфенил-1,3,4,6-гексан-тетраон) (I) проявляет выраженную противомикробную активность и является практически нетоксичным. Следовательно, заявляемое соединение (I) может найти применение в медицине в качестве противомикробного лекарственного средства.
Формула изобретения
2,2,5,5-тетрабром-1,6-ди-(41-метилфенил)-1,3,4,6,-гексантетраон формулы
обладающий противомикробной активностью.
|
||||||||||||||||||||||||||||||||||

 , см-1 (кристаллы): 1760 (СО), 1710 (СО). Спектр ПМР,
, см-1 (кристаллы): 1760 (СО), 1710 (СО). Спектр ПМР,  , м. д. CBCl3: 2.44 с (6Н, 2СН3), 7.23 д., 7.92 д. (8Н, 2С6Н4).
, м. д. CBCl3: 2.44 с (6Н, 2СН3), 7.23 д., 7.92 д. (8Н, 2С6Н4).