|
|
(21), (22) Заявка: 2005114081/15, 11.05.2005
(24) Дата начала отсчета срока действия патента:
11.05.2005
(43) Дата публикации заявки: 20.11.2006
(46) Опубликовано: 10.07.2007
(56) Список документов, цитированных в отчете о
поиске:
АХМЕДЖАНОВА С.Б. и др. Определение гистамина и серотонина в цельной крови методом высокоэффективной жидкостной хроматографии. Лабораторное дело. 1991, №11, с.10-13. RU 2244307 С2 10.01.2005. JP 2001272395 05.10.2001. СТЕПАНОВА Н.В. и др. Хроматографический метод определения серотонина и гистамина в одной пробе биологического материала. Лабораторное
Адрес для переписки:
656038, г.Барнаул, пр-кт Ленина, 40, ГОУ ВПО АГМУ Росздрава, Отдел интеллектуальной собственности
|
(72) Автор(ы):
Брюханов Валерий Михайлович (RU),
Витчуткина Елена Александровна (RU),
Зверев Яков Федорович (RU),
Лампатов Вячеслав Витальевич (RU),
Жариков Александр Юрьевич (RU)
(73) Патентообладатель(и):
Государственное образовательное учреждение высшего профессионального образования “Алтайский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию” (ГОУ ВПО АГМУ Росздрава) (RU)
|
(54) СПОСОБ ОПРЕДЕЛЕНИЯ ГИСТАМИНА В ПЛАЗМЕ КРОВИ
(57) Реферат:
Изобретение относится к области медицины, а именно к патофизиологии, фармакологии и токсикологии, и может быть использовано для определения гистамина в плазме крови у больных в условиях различных неблагоприятных воздействий, включая побочное действие лекарственных средств. Сущность способа: определение гистамина методом высокоэффективной жидкостной хроматографии (ВЭЖХ) осуществляют в надосадочной жидкости, полученной в результате осаждения белков плазмы ацетонитрилом. Для осуществления ВЭЖХ используют хроматографическую колонку Pronto SIL-120-5-C18AQ 2×75 мм с размером частиц 5 мкм, в качестве элюэнта используют смесь 0,1 М раствора дигидрофосфата натрия и ацетонитрила при градиенте концентрации последнего от 0 до 50%, при скорости подачи потока элюента 90 мкл/мин, объеме элюирования 1500 мкл, температура хроматографической колонки 35°С, причем детекцию проводят при длине волны 210 нм. Использование способа позволяет повысить точность определения гистамина в плазме крови за счет определения количественных и качественных характеристик гистамина в плазме крови. 1 табл., 2 ил.
(56) (продолжение):
CLASS=”b560m”дело. 1989, №7, с.28-30. LIU W. et al. Simultaneous analysis of histamine and noradrenaline in human plasma by high performance liquid chromatography/electrochemical detection. Se. Pu. 1999, Jan; 17(1), p.80-82, реф. Найдено из БД PubMed, PMID 12548839. [Найдено 19.10.2006]. [он-лайн]. HARSING L.G. Jr. et al. Determination of histamine concentrations in plasma by liquid chromatography/electrochemistry. Clin. Chem. 1986 Oct; 32(10), p.1823-1827, реф. Найдено из БД PubMed, PMID 3093119. [Найдено 19.10.2006]. [он-лайн].
Изобретение относится к медицине, а именно к патофизиологии, фармакологии и токсикологии, и может быть использовано для определения гистамина в плазме крови больных в условиях различных неблагоприятных воздействий, включая побочное действие лекарственных средств.
В настоящее время существует несколько способов определения гистамина в биологических пробах, однако использование этих способов сопряжено с рядом недостатков, что делает процедуру определения длительной, а данные количественного определения неточными.
Известен способ определения гистамина в плазме крови, основанный на реакции образования с о-фталиевым альдегидом сильно флюоресцирующего соединения, которое определяют на спектрофлюориметре при длине волны 450 нм и возбуждении при 365 нм (Shore P.A., Burkhalter A., Cohn V.H., Jr., J. Pharmcol. Exp. Ther. – 1959. – V.127. – P.182).
Недостатками известного способа являются трудоемкость, связанная с многостадийностью и рядом последовательно проводимых химических реакций и физико-химических определений, а также высокая стоимость применяемых химических реактивов.
Однако известный способ малоэффективен, так как имеет низкую точность количественного определения.
Авторы предлагают высокоэффективный способ, позволяющий быстро и высокоточно определять качественные и количественные характеристики гистамина в биологических пробах методом высокоэффективной жидкостной хроматографии.
Техническим результатом заявляемого способа является повышение эффективности за счет точного и быстрого определения качественных и количественных характеристик гистамина в плазме крови.
Технический результат достигается тем, что используют жидкостную хроматографию, в качестве элюэнта – смесь 0,1 М раствора дигидрофосфата натрия и ацетонитрила при градиенте концентрации последнего от 0 до 50% и скорости подачи потока элюента 90 мкл/мин, объеме элюирования 1500 мкл, температура хроматографической колонки 35°С, детекцию проводят при длине волны 210 нм.
Способ проиллюстрирован фигурами 1, 2 и таблицей.
Способ осуществляют поэтапно следующим образом:
1. Забор крови.
Для определения используют венозную кровь, которую забирают из локтевой вены широкой сухой иглой в стеклянную пробирку, куда предварительно добавлен в качестве антикоагулянта гепарин из расчета 1,75 мл гепарина на 17 мл забираемой венозной крови. Покачиванием или легким встряхиванием пробирки кровь перемешивают с антикоагулянтом.
2. Подготовка пробы.
Для определения используют венозную кровь, консервированную гепарином. Кровь центрифугируют при 8000 об/мин в течение 20 минут для осаждения форменных элементов. Затем к 1 мл полученной плазмы добавляют 2 мл 100% ацетонитрила для осаждения белков плазмы. Полученную суспензию сразу тщательно перемешивают стеклянной палочкой для формирования равномерного осадка. Затем пробу центрифугируют при 8000 об/мин в течение 15 минут для формирования плотного осадка. Для исследования забирают надосадочную жидкость.
3. Хроматографирование пробы.
Полученную надосадочную жидкость хроматографируют, используя в качестве подвижной фазы (элюэнта) смесь 0,1 М раствора дигидрофосфата натрия и ацетонитрила при градиенте концентрации последнего от 0 до 50%. Скорость подачи потока элюэнта составляет 90 мкл/мин, объем элюирования 1500 мкл, температура хроматографической колонки 35°С. Детекцию проводят при длине волны 210 нм.
Используемое оборудование.
Для проведения определения используют высокоэффективный жидкостный хроматограф «Милихром А-02» (ЗАО Институт хроматографии «Эконова», Новосибирск, Россия) с УФ-детектором и хроматографической колонкой Pronto SIL-120-5-C18AQ 2×75 мм с размером частиц 5 мкм.
Для центрифугирования используют центрифугу марки “Центрифуга лабораторная медицинская ОПн-8 ШХ 2.779.040» производства АО ТНК «Дастан», г.Бишкек.
Используемые стандартные образцы и реактивы.
В качестве стандартного образца используют кристаллический порошкообразный гистамин фирмы «Fluka», USA.
В качестве элюэнта и реактива для осаждения белков использовали ацетонитрил для хроматографии фирмы «Fluka», USA.
Для приготовления фосфатного буфера использовались порошкообразные кристаллические натрия фосфат однозамещенный и калия фосфат двузамещенный химически чистые для анализа фирмы «Sigma», USA.
Гистамин в плазме идентифицируют путем сопоставления времени удерживания пика, полученного на хроматограмме анализируемой пробы, со временем удерживания стандартного образца. Для подтверждения полученных результатов добавляют стандартный раствор гистамина в анализируемую пробу и наблюдают увеличение предполагаемого пика гистамина, сравнивают спектры поглощения в УФ-области стандартного образца и обнаруженного гистамина в плазме, записанные при остановленном потоке элюэнта во время выхода вещества из колонки.
Количественное определение гистамина в плазме проводят путем построения градуировочного графика, хроматографируя серию разведений стандартного образца гистамина в воде. Концентрацию гистамина в плазме вычисляют по формуле: С=W(R)×D/V, где W(R) – вычисленное по градуировочной зависимости количество вещества в пике, D – разведение пробы, V – объем пробы (2 мкл).
Заявленный способ обладает высокой эффективностью, не требует проведения многочисленных предварительных химических реакций и не предусматривает использование большого количества химических реактивов.
Способ определения гистамина в плазме крови
| Таблица |
| Статистическая обработка шести параллельных определений |
| № пробы |
Содержание гистамина в мкг/мл |
Статистические показатели |
| 1 |
32,46 |
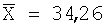
S=1,21
Sx=0,49
 Х=1,26 Х=1,26
а=±3,67% |
| 2 |
33,85 |
| 3 |
35,72 |
| 4 |
34,14 |
| 5 |
35,53 |
| 6 |
33,85 |
Относительная погрешность определения гистамина в плазме крови не превысила 3,67%.
Формула изобретения
Способ определения гистамина в плазме крови путем высокоэффективной жидкостной хроматографии (ВЭЖХ), отличающийся тем, что определение гистамина проводят в надосадочной жидкости, полученной в результате осаждения белков плазмы ацетонитрилом, ВЭЖХ осуществляют на хроматографической колонке Pronto SIL-120-5-C18AQ 2×75 мм с размером частиц 5 мкм, в качестве элюэнта используют смесь 0,1 М раствора дигидрофосфата натрия и ацетонитрила при градиенте концентрации последнего от 0 до 50%, при скорости подачи потока элюента 90 мкл/мин, объеме элюирования 1500 мкл, температура хроматографической колонки 35°С, детекцию проводят при длине волны 210 нм.
РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 12.05.2007
Извещение опубликовано: 27.07.2008 БИ: 21/2008
|
|