|
|
(21), (22) Заявка: 2004137709/04, 23.12.2004
(24) Дата начала отсчета срока действия патента:
23.12.2004
(43) Дата публикации заявки: 10.06.2006
(46) Опубликовано: 10.07.2007
(56) Список документов, цитированных в отчете о
поиске:
Г.И.ЖУНГИЕТУ и др. Препаративная химия индола. – Кишинев: Штиинца, 1975, с.179. Известия АН, серия Химическая, 51(1), 2002, с.185-186. Химия гетероциклических соединений. №2, 1974, с.211-213. J. Med. Chem. V.37, 1994, p.3141-3153.
Адрес для переписки:
125047, Москва, Миусская пл., 9, РХТУ им. Д.И. Менделеева, патентный отдел
|
(72) Автор(ы):
Семенов Борис Борисович (RU),
Новиков Кирилл Александрович (RU),
Качала Вадим Вадимович (RU)
(73) Патентообладатель(и):
Российский химико-технологический университет им. Д.И. Менделеева (РХТУ им. Д.И. Менделеева) (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ 3-ИНДОЛИЛФЕНИЛМЕТИЛ 2-ЗАМЕЩЕННЫХ ЦИКЛИЧЕСКИХ АЛЬФА-КЕТОНОВ
(57) Реферат:
Изобретение относится к способу получения новых 3-индолилфенилметил 2-замещенных циклических  -кетонов общей формулы: -кетонов общей формулы:
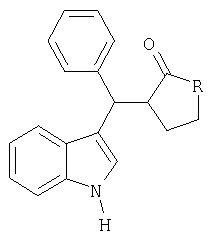
где R означает число атомов углерода от одного до двух, с аннелированным бензольным кольцом или замещенной метилиденовой группой, которая представляет собой 2-метилпропилиден или 2-фенилметилиден, и заключается в том, что  -фенил-нор-грамин подвергают взаимодействию с циклическим кетоном формулы: -фенил-нор-грамин подвергают взаимодействию с циклическим кетоном формулы:
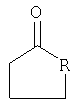
где R указан выше, в кипящем изопропиловом спирте в присутствии в качестве основания ацетата натрия или пиридина, или триэтиламина, или щелочи, или хирального амина. 3 табл.
Настоящее изобретение относится к области химии гетероциклических соединений, обладающих потенциальной биологической активностью, в частности к способу получения 3-индолилфенилметил 2-замещенных циклических  -кетонов. -кетонов.
Известно, что 2-алкилзамещенные  -инданоны предложены как ингибиторы ацетилхолинестеразы, что может явиться терапевтическим эффектом для лечения болезни Альцгеймера [Y.Yamamoto, Y.Ishihara, I.D.Kuntz, J. Med. Chem., 1994, 37, 3141-3153]. -инданоны предложены как ингибиторы ацетилхолинестеразы, что может явиться терапевтическим эффектом для лечения болезни Альцгеймера [Y.Yamamoto, Y.Ishihara, I.D.Kuntz, J. Med. Chem., 1994, 37, 3141-3153].
Наиболее близким является способ получения 2-(1H-индол-3-илметил)циклопентанона алкилированием енаминов циклических кетонов грамином (N-(1H-индол-3-илметил)-N,N-диметиламином), в присутствии в качестве катализатора кислот (п-толуолсульфокислоты), с последующим гидролизом образующихся енаминов. [Г.И.Жунгиету, В.А.Будылин, А.Н.Кост. Препаративная химия индола. Кишинев, Штиинца, 1975, стр.179].
Недостатком способа, принятого за прототип, является невозможность диастереонаправленного синтеза получения 3-индолилфенилметил 2-замещенных циклических  -кетонов (ввиду отсутствия двух хиральных центров). -кетонов (ввиду отсутствия двух хиральных центров).
Задачей изобретения является разработка способа диастереонаправленного 3-индолилфенилметил 2-замещенных циклических  -кетонов. -кетонов.
Поставленная задача решается способом получения 3-индолилфенилметил 2-замещенных циклических  -кетонов, имеющих несколько хиральных центров с противоположной конфигурацией асимметрических атомов углерода, путем алкилирования циклических кетонов (имеющих Е-конфигурацию енолятов) грамином, в присутствии основания и органического растворителя, причем в качестве грамина используют -кетонов, имеющих несколько хиральных центров с противоположной конфигурацией асимметрических атомов углерода, путем алкилирования циклических кетонов (имеющих Е-конфигурацию енолятов) грамином, в присутствии основания и органического растворителя, причем в качестве грамина используют  -фенил-нор-грамин, в качестве органического растворителя используют этиловый или изопропиловый спирт, а в качестве основания используют ацетат натрия или пиридин, или триэтиламин, или щелочи, или амины, в том числе и хиральные (хинин или цинхонин, или анабазин). -фенил-нор-грамин, в качестве органического растворителя используют этиловый или изопропиловый спирт, а в качестве основания используют ацетат натрия или пиридин, или триэтиламин, или щелочи, или амины, в том числе и хиральные (хинин или цинхонин, или анабазин).
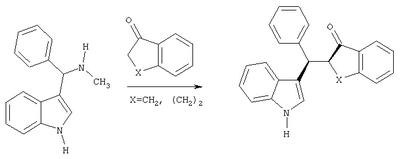
Пример 1 (по прототипу)
Смесь 1. 805 г 1-морфолиноциклопентена, 2.06 г грамина и 12 мг п-толуолсульфокислоты нагревают в инертной атмосфере 30 мин при 130-135°С. Смесь охлаждают, добавляют 4 мл диоксана, 0.5 мл воды и кипятят 1 ч. Растворитель упаривают в вакууме, остаток растворяют в хлористом метилене, промывают разбавленной уксусной кислотой, раствором соды и водой. После удаления растворителя остаток хроматографируют на колонке с окисью алюминия. Выход 2-(1H-индол-3-илметил)циклопентанона 1,613 г (64%), т.пл. 61-62°С (из смеси бензол-петролейный эфир). Г.И.Жунгиету, В.А.Будылин, А.Н.Кост. Препаративная химия индола. Кишинев, Штиинца, 1975, стр.179.
Пример 2
(2S*)-2-[(R*)-1H-индол-3-ил(фенил)метил]-2,3-дигидро-1H-инден-1-он
К кипящему раствору 1.0 г  -фенил-нор-грамина (0.42 ммоля) в 10 мл изопропанола добавляют раствор 0.1 ммоля триэтиламина в 1 мл Н2О и 0.625 ммоля 1-инданона. -фенил-нор-грамина (0.42 ммоля) в 10 мл изопропанола добавляют раствор 0.1 ммоля триэтиламина в 1 мл Н2О и 0.625 ммоля 1-инданона.
Нагревают при температуре кипения в токе инертного газа до исчезновения исходного соединения. Контроль по ТСХ (Silufol UV-254, система EtOAc-CCl4 (1:4)). Реакционную смесь охлаждают до комнатной температуры. Выпавший осадок отфильтровывают и перекристаллизовывают из водного спирта. Т.пл. 246°С (из EtOH). m/z (IОТН (%)): 337 [М]+ (14), 206 [IndCHPh]+ (100). Найдено (%): С, 85.64; Н, 5.71; N, 4.01. C24H19NO. Вычислено (%): С, 85.43; Н, 5.68; N, 4.15.
Пример 3
(2S*)-2-[(R*)-1H-индол-3-ил(фенил)метил]-3,4-дигидро-1(2H)-нафталенон
К кипящему раствору 1.0 г  -фенил-нор-грамина (0.42 ммоля) в 10 мл изопропанола добавляют раствор 0.1 ммоля ацетата натрия в 1 мл Н2О и 0.625 ммоля 1-тетралона. -фенил-нор-грамина (0.42 ммоля) в 10 мл изопропанола добавляют раствор 0.1 ммоля ацетата натрия в 1 мл Н2О и 0.625 ммоля 1-тетралона.
Нагревают при температуре кипения в токе инертного газа до исчезновения исходного соединения. Контроль по ТСХ (Silufol UV-254, система EtOAc-CCl4 (1:4)). Реакционную смесь охлаждают до комнатной температуры. Выпавший осадок отфильтровывают и перекристаллизовывают из спирта.
Белые кристаллы, Т.пл. 138-139°С (водн. i-PrOH). Масс-спектр m/z (Iотн., %): 351 [M]+ (17), 206 [IndCHPh]+ (100); Найдено, %: С 85.63; Н 6.04; N 3.87. C25H21NO. Вычислено, %: С 85.44; Н 6.02; N 3.99.
Пример 4
(2S*)-2-[(R*)2-[1H-индол-3-ил(фенил)метил]-5-[2-метилпропилиден]циклопентанон
К кипящему раствору 1.0 г  -фенил-нор-грамина (0.42 ммоля) в 10 мл изопропанола добавляют раствор 0.1 ммоля пиридина в 5 мл Н2О и 0.625 ммоля [2-метилпропилиден]циклопентанона. Нагревают при температуре кипения в токе инертного газа до исчезновения исходного соединения. Контроль по ТСХ (Silufol UV-254, система EtOAc-CCl4 (1:4)). Реакционную смесь охлаждают до комнатной температуры. Выпавший осадок отфильтровывают и перекристаллизовывают из спирта. Белые кристаллы, Т.пл. 231°С (водн. i-PrOH). Масс-спектр m/z (I отн., %): 343 [М]+ (27), 206 [IndCHPh]+ (100); Найдено, %: С 84.01; Н 7.54; N 3.97. C24H25NO. Вычислено, %: С 83.93; Н 7.34; N 4.08. -фенил-нор-грамина (0.42 ммоля) в 10 мл изопропанола добавляют раствор 0.1 ммоля пиридина в 5 мл Н2О и 0.625 ммоля [2-метилпропилиден]циклопентанона. Нагревают при температуре кипения в токе инертного газа до исчезновения исходного соединения. Контроль по ТСХ (Silufol UV-254, система EtOAc-CCl4 (1:4)). Реакционную смесь охлаждают до комнатной температуры. Выпавший осадок отфильтровывают и перекристаллизовывают из спирта. Белые кристаллы, Т.пл. 231°С (водн. i-PrOH). Масс-спектр m/z (I отн., %): 343 [М]+ (27), 206 [IndCHPh]+ (100); Найдено, %: С 84.01; Н 7.54; N 3.97. C24H25NO. Вычислено, %: С 83.93; Н 7.34; N 4.08.
Пример 5
(2S*)-2-[(R*)2-[1H-индол-3-ил(фенил)метил]-5-12-метилпропилиден]циклопентанон
К кипящему раствору 1.0 г  -фенил-нор-грамина (0.42 ммоля) в 10 мл изопропанола добавляют раствор 0.1 ммоля цинхонина в 5 мл Н2О и 0.625 ммоля [2-метилпропилиден]циклопентанона. Нагревают при температуре кипения в токе инертного газа до исчезновения исходного соединения. Контроль по ТСХ (Silufol UV-254, система EtOAc-CCl4 (1:4)). Реакционную смесь охлаждают до комнатной температуры. Выпавший осадок отфильтровывают и перекристаллизовывают из спирта. Белые кристаллы, Т.пл. 231°С (водн. i-PrOH). Масс-спектр m/z (I отн., %): 343 [М]+ (27), 206 [IndCHPh]+ (100); Найдено, %: С 84.01; Н 7.54; N 3.97. C24H25NO. Вычислено, %: С 83.93; Н 7.34; N 4.08. -фенил-нор-грамина (0.42 ммоля) в 10 мл изопропанола добавляют раствор 0.1 ммоля цинхонина в 5 мл Н2О и 0.625 ммоля [2-метилпропилиден]циклопентанона. Нагревают при температуре кипения в токе инертного газа до исчезновения исходного соединения. Контроль по ТСХ (Silufol UV-254, система EtOAc-CCl4 (1:4)). Реакционную смесь охлаждают до комнатной температуры. Выпавший осадок отфильтровывают и перекристаллизовывают из спирта. Белые кристаллы, Т.пл. 231°С (водн. i-PrOH). Масс-спектр m/z (I отн., %): 343 [М]+ (27), 206 [IndCHPh]+ (100); Найдено, %: С 84.01; Н 7.54; N 3.97. C24H25NO. Вычислено, %: С 83.93; Н 7.34; N 4.08.
Пример 6
(2S*)-2-[(R*)2-[1H-индол-3-ил(фенил)метил]-5-[2-фенилметилиден]циклопентанон.
К кипящему раствору 1.0 г  -фенил-нор-грамина (0.42 ммоля) в 10 мл изопропанола добавляют раствор 0.1 ммоля гидроксида натрия в 5 мл Н2О и 0.625 ммоля [2-фенилметилиден]циклопентанона. Нагревают при температуре кипения в токе инертного газа до исчезновения исходного соединения. Контроль по ТСХ (Silufol UV-254, система EtOAc-CCl4 (1:4)). Реакционную смесь охлаждают до комнатной температуры. Выпавший осадок отфильтровывают и перекристаллизовывают из спирта. Белые кристаллы, Т.пл. >300°С (водн. i-PrOH). Масс-спектр m/z (I отн., %): 377 [М]+ (14), 206 [IndCHPh]+ (100); Найдено, %: С 86.31; Н 6.54; N 3.67. С27Н23NO. Вычислено, %: С 85.91; Н 6.14; N 3.71. -фенил-нор-грамина (0.42 ммоля) в 10 мл изопропанола добавляют раствор 0.1 ммоля гидроксида натрия в 5 мл Н2О и 0.625 ммоля [2-фенилметилиден]циклопентанона. Нагревают при температуре кипения в токе инертного газа до исчезновения исходного соединения. Контроль по ТСХ (Silufol UV-254, система EtOAc-CCl4 (1:4)). Реакционную смесь охлаждают до комнатной температуры. Выпавший осадок отфильтровывают и перекристаллизовывают из спирта. Белые кристаллы, Т.пл. >300°С (водн. i-PrOH). Масс-спектр m/z (I отн., %): 377 [М]+ (14), 206 [IndCHPh]+ (100); Найдено, %: С 86.31; Н 6.54; N 3.67. С27Н23NO. Вычислено, %: С 85.91; Н 6.14; N 3.71.
Как видно из приведенных примеров (см. табл.1-3), разработанный способ позволяет диастереонаправленно получать производные циклических  -кетонов. -кетонов.
Полученные соединения могут быть использованы при синтезе “лекарственно подобных” производных индола по реакции Фишера.
Характерной особенностью данного класса соединений является способность регулировать “калиевые” потоки в сердечном цикле, переполяризации мембранного потенциала после каждого сокращения. Управляемое ингибирование фермента ацетилхолинестеразы, что важно для лечения болезней, связанных с ацетилхолинестерол истощением, в частности болезни Альцгеймера.
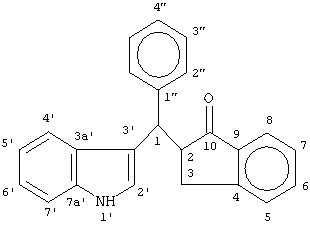
| Таблица 1. |
| Хим. сдвиги 1H 13C NMR для (2R*)-2-[(S*)-1H-индол-3-ил(фенил)метил]-2,3-дигидро-1H-инден-1-она и (2S*)-2-[(S*)-1H-индол-3-ил(фенил)метил]-2,3-дигидро-1H-инден-1-она |
| |
13С |
1Н |
13С |
1Н |
| Нумерация атомов |
R*S* |
S*S* |
| 1 |
42.0 |
5.05 |
46.7 |
4.90 |
| 2 |
51.2 |
3.65 |
45.4 |
5.18 |
| 3 |
29.5 |
3.50 3.00 |
32.9 |
4.20 3.92 |
| 4 |
153.9 |
– |
148.7 |
– |
| 5 |
126.6 |
7.43 |
125.5 |
7.60 |
| 6 |
134.6 |
7.54 |
133.9 |
7.67 |
| 7 |
127.2 |
7.33 |
127.2 |
7.45 |
| 8 |
122.9 |
7.63 |
123.1 |
7.74 |
| 9 |
136.5 |
– |
138.9 |
– |
| 10 |
206.6 |
– |
193.5 |
– |
| 1 |
– |
10.97 |
– |
10.93 |
| 2′ |
122.9 |
7.48 |
122.9 |
7.54. |
| 3′ |
116.2 |
– |
116.8 |
– |
| 3a’ |
126.6 |
– |
127.0 |
– |
| 4′ |
118.8 |
7.06 |
119.3 |
6.95 |
| 5′ |
118.2 |
6.83 |
117.9 |
6.77 |
| 6′ |
121.0 |
7.03 |
120.8 |
6.97 |
| 7′ |
111.3 |
7.37 |
111.2 |
7.30 |
| 7а’ |
136.5 |
– |
136.5 |
– |
| 1″ |
141.3 |
– |
140.7 |
– |
| 2″ |
128.8 |
7.13 |
128.9 |
6.95 |
| 3″ |
127.7 |
7.07 |
127.7 |
7.04 |
| 4″ |
126.1 |
7.03 |
126.8 |
6.85 |
Таблица 2
Хим. сдвиги ЯМР 1Н и 13С (2S*)-2-[(R*)-1H-индол-3-ил(фенил)метил]-3,4-дигидро-1(2H)-нафталенона |
 |
| Нумерация Атомов |
 , м.д. 13С , м.д. 13С |
 , м.д. 1Н , м.д. 1Н |
| 1 |
40.9 |
5.22 |
| 2 |
52.4 |
3.45 |
| 3 |
26.5 |
2.30 1.85 |
| 4 |
28.3 |
3.10 |
| 5 |
126.8 |
– |
| 6 |
128.7 |
7.22 |
| 7 |
126.7 |
7.25 |
| 8 |
133.2 |
7.45 |
| 9 |
127.9 |
7.96 |
| 10 |
143.1 |
– |
| 11 |
197.3 |
– |
| 1′ |
– |
8.05 |
| 2′ |
121.6 |
7.26 |
| 3′ |
117.8 |
– |
| 3а’ |
127.0 |
– |
| 4′ |
119.7 |
7.28 |
| 5′ |
119.3 |
6.95 |
| 6′ |
122.1 |
7.13 |
| 7′ |
111.0 |
7.33 |
| 7а’ |
1358 |
– |
| 1″ |
140.7 |
– |
| 2″ |
129.2 |
7.36 |
| 3″ |
128.2 |
7.24 |
| 4″ |
126.3 |
7.16 |
Таблица 3.
Хим. сдвиги 1H 13С NMR для (2R*)-2-[(S*)-1H-индол-3-ил(фенил)метил]-5-[(E)-2-метилпропилиден]циклопентанона. |
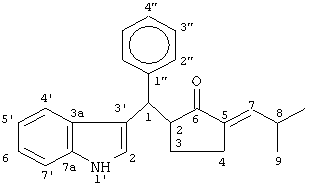 |
| Нумерация Атомов |
13C |
1Н |
| 1 |
41.3 |
4.70 |
| 2 |
52.9 |
3.23 |
| 3 |
23.8 |
2.13 1.49 |
| 4 |
23.9 |
2.38 |
| 5 |
135.4 |
– |
| 6 |
205.7 |
– |
| 7 |
141.2 |
6.19 |
| 8 |
28.2 |
2.40 |
| 9 |
21.4 21.5 |
0.98 0.94 |
| 1′ |
– |
|
| 2′ |
122.5 |
7.41 |
| 3′ |
116.7 |
– |
| 3а’ |
126.7 |
– |
| 4′ |
118.7 |
7.08 |
| 5′ |
118.0 |
6.81 |
| 6′ |
120.8 |
7.00 |
| 7′ |
111.2 |
7.32 |
| 7а’ |
136.3 |
– |
| 1″ |
142.6 |
– |
| 2″ |
128.8 |
7.22 |
| 3″ |
127.8 |
7.18 |
| 4″ |
125.9 |
7.11 |
Формула изобретения
Способ получения 3-индолилфенилметил 2-замещенных циклических  -кетонов общей формулы -кетонов общей формулы
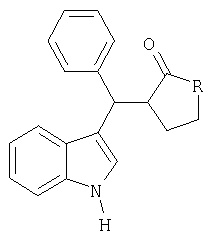
где R означает число атомов углерода от одного до двух, с аннелированным бензольным кольцом или замещенной метилиденовой группой, которая представляет собой 2-метилпропилиден или 2-фенилметилиден, заключающийся в том, что  -фенил-нор-грамин подвергают взаимодействию с циклическим кетоном формулы -фенил-нор-грамин подвергают взаимодействию с циклическим кетоном формулы
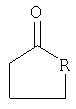
где R определен выше,
в кипящем изопропиловом спирте в присутствии в качестве основания ацетата натрия, или пиридина, или триэтиламина, или щелочи, или хирального амина, такого как цинхонина.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 24.12.2006
Извещение опубликовано: 10.04.2009 БИ: 10/2009
|
|

 -кетонов общей формулы:
-кетонов общей формулы:



 , м.д. 13С
, м.д. 13С

