Патент на изобретение №2300563
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ СУСПЕНЗИОННОГО КУЛЬТИВИРОВАНИЯ КЛЕТОК МЛЕКОПИТАЮЩИХ
(57) Реферат:
Изобретение относится к биотехнологии и может быть использовано при производстве питательных сред для суспензионного культивирования клеток. Питательная среда содержит натрий хлористый, калий хлористый, магний сернокислый, натрий фосфорнокислый двузамещенный, калий фосфорнокислый однозамещенный, кальций хлористый, натрий двууглекислый, L-аргинин, L-глутамин, L-тирозин, L-триптофан, L-цистин, пантотенат кальция, пиридоксаль HCl, тиамин, мезо-инозит, никотинамид, рибофлавин, фолиевую кислоту, глюкозу, ферментативный гидролизат мышечных белков, ферментативный гидролизат лактальбумина, сыворотку крупного рогатого скота, амфотерицин, бензилпенициллина натриевую соль, канамицина сульфат и дистиллированную воду. Изобретение позволяет получить качественную и экономически выгодную питательную среду. 2 табл.
(56) (продолжение): CLASS=”b560m”Под ред. Г.П. ПИНАЕВА. Методы культивирования клеток. Сборник научных трудов. – М.: НАУКА, 1988, с.47-57.
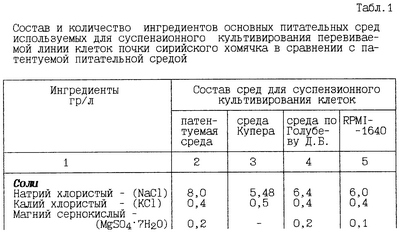
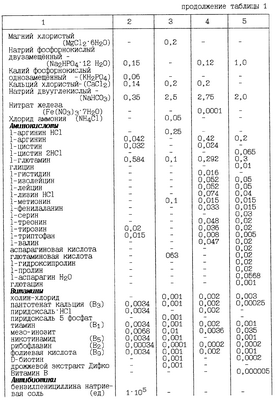
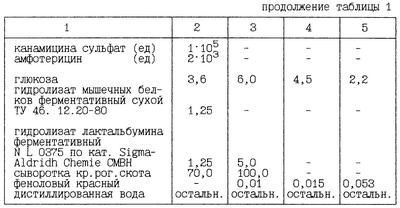
Область техники, к которой относится изобретение. Область биотехнологии, сфера питательных сред, суспензионного культивирования клеток почки сирийского хомячка (ВНК – 21). Уровень техники. Из литературных данных известны прописи питательных сред для суспензионного культивирования клеток: – среда Купера (Методические рекомендации по работе с клеточными культурами и средами /Под ред.А.А.Сомниной.- Ленинград.- 1975. – стр.38-40), – специальная среда для культивирования клеток ВНК-2.1 (Голубев Д.Б., Сомнина А.А., Медведева М.Н. Руководство по применению клеточных культур в вирусологии.- Л.: Медицина, 1976. стр.19), – среда Мак-Коя для суспензионного культивирования RPMI – 1640 (Животная клетка в культуре (Методы и применение в биотехнологии / Под ред. проф. Дьяконова Л.П., проф. Ситькова В.И. – М.: Компания Спутник, 2000. стр.53- 55). В состав перечисленных питательных сред входят: неорганические соли, аминокислоты, витамины, углеводы. Из указанных аналогов наиболее близким к заявляемому изобретению (прототипом) является среда RPMI-1640 (табл.1). В представленной таблице к существенным отличительным признакам патентуемой питательной среды относятся те, что среда дополнительно содержит гидролизат мышечных белков ферментативный сухой и гидролизат лактальбумина ферментативный и только пять аминокислот вместо 20 аминокислот в прототипе. Раскрытие изобретения. (1) Сведения, раскрывающие сущность изобретения. (1.1) Сущность изобретения: подобран состав компонентов питательной среды, включающий: гидролизат мышечных белков ферментативный сухой и гидролизат лактальбумина ферментативный; аминокислоты – аргинин, глутамин, тирозин, триптофан и цистин, обеспечивающий накопление клеток, при суспензионном культивировании перевиваемой линии ВНК-21 до 3,5·106 кл./см3. (1.2.) Техническим результатом заявляемого изобретения является создание экономически выгодной питательной среды для суспензионного культивирования клеток ВНК-21 в условиях массового биопроизводства при изготовлении культуральных вакцин. Технический результат достигнут введением в состав питательной среды оптимального количественного соотношения компонентов, представленных в таблице 2. Осуществление изобретения. Изобретение относится к композиции в которую входят ингредиенты в соотношениях количества граммов на 1 литр дистиллированной воды, указанных в таблице 2. Способ получения композиции следующий: навески отдельных компонентов берут, соблюдая правила взвешивания для весов соответствующего класса. Учитывая объем приготавливаемой смеси, допускается взвешивание солей, гидролизатов, глюкозы на весах 3-го класса; навески отдельных аминокислот, витаминов и антибиотиков – на аналитических весах 2-го класса с соблюдением точности до второго знака после запятой. Процесс приготовления питательной среды заключается в приготовлении солевой основы среды, которой является раствор Хенкса, и растворении в нем антибиотиков, солей, глюкозы, гидролизата мышечных белков ферментативного сухого и гидролизата лактальбумина ферментативного по 1,25 г/л с конечной концентрацией суммы гидролизатов в питательной среде, равной 0,25%, пяти аминокислот, сыворотки, витаминов, бикарбоната натрия. Растворение компонентов питательной среды ведут в дистиллированной воде, имеющей температуру 35-40°С, при непрерывном перемешивании. В начале растворяют антибиотики и навески солей поочередно NaCl, KCl, MgSO4·7H2O, Na2HPO4·12H2O (развести в горячей воде), KH2PO4 до полного растворения предыдущей навески, вносят навеску глюкозы 3,6 г/л среды. Дополнительно к механическому перемешиванию осуществляют перемешивание сжатым воздухом, т.е. барботированием в течение 10 минут. После растворения навесок убирают барботирование. В глюкозосолевой раствор осторожно, тонкой струйкой при механическом перемешивании вносят хлористый кальций (CaCl2) в виде 40%-ного раствора и вновь барботируют. Из указанного в табл.2 количества гидролизата мышечных белков ферментативного сухого и гидролизата лактальбумина ферментативного готовят 10%-ный раствор и вносят его в полученный глюкозосолевой раствор, и растворяют в течение 10 минут перемешиванием и барботированием. Отдельно растворяют аминокислоты. Растворение навесок проводят последовательно согласно прописи питательной среды в таблице 2. L-цистин и l-тирозин растворяют отдельно в небольшом количестве дистиллированной воды при нагревании до кипения с добавлением по каплям концентрированной соляной кислоты (d=1,19) до полного просветления раствора. Сначала растворяют l-цистин, затем l-тирозин. Если при внесении l-тирозина раствор помутнел, необходимо вновь вносить по каплям концентрированную HCl, до полного растворения навески. Вместо l-цистина можно использовать l-цистин HCl и растворять l-цистин HCl просто в кипящей воде. Все витамины, кроме рибофлавина и фолиевой кислоты, последовательно растворяют в небольшом количестве дистиллированной воды комнатной температуры. При этом каждую последующую навеску растворяют только после полного растворения предыдущей. Рибофлавин и фолиевую кислоту растворяют отдельно в небольшом количестве дистиллированной воды комнатной температуры с добавлением по каплям 20%-ного раствора NaOH до полного растворения навесок. Сначала растворяют рибофлавин, затем фолиевую кислоту, при растворении которой необходимо вновь по каплям вносить 20%-ный р-р NaOH до полного просветления раствора. В глюкозосолевой раствор вносят растворы аминокислот, витаминов, сыворотку, натрий двууглекислый и перемешивают. После внесения в среду всех необходимых компонентов добавляют дистиллированную воду до необходимого объема, перемешивают, стерилизуют фильтрацией в реактор для культивирования клеток.
Формула изобретения
Питательная среда для суспензионного культивирования клеток млекопитающих, содержащая натрий хлористый, калий хлористый, магний сернокислый, натрий фосфорнокислый двузамещенный, калий фосфорнокислый однозамещенный, кальций хлористый, натрий двууглекислый, L-аргинин, L-глутамин, L-тирозин, L-триптофан, L-цистин, пантотенат кальция, пиридоксаль HCl, тиамин, мезо-инозит, никотинамид, рибофлавин, фолиевую кислоту, глюкозу, ферментативный гидролизат мышечных белков, ферментативный гидролизат лактальбумина, сыворотку крупного рогатого скота, амфотерицин, бензилпенициллина натриевую соль, канамицина сульфат и дистиллированную воду, при следующем содержании компонентов, г/л:
QB4A – Регистрация лицензионного договора на использование изобретения
Лицензиар(ы): Открытое акционерное общество “Институт биотехнологий ветеринарной медицины”
Вид лицензии*: НИЛ
Лицензиат(ы): Федеральное государственное унитарное предприятие “Щелковский биокомбинат”
Договор № РД0033858 зарегистрирован 17.03.2008
Извещение опубликовано: 27.04.2008 БИ: 12/2008
* ИЛ – исключительная лицензия НИЛ – неисключительная лицензия
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||