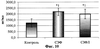Патент на изобретение №2300384
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ, ИММУНОМОДУЛИРУЮЩЕЙ И РАНОЗАЖИВЛЯЮЩЕЙ АКТИВНОСТЬЮ
(57) Реферат:
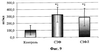
Изобретение относится к медицине, в частности к фармации и биотехнологии, и может быть использовано для получения лекарственных средств с противовоспалительным, иммуномодулирующим и ранозаживляющим свойствами и касается нового биологически активного вещества, содержащего комплекс гуморальных факторов аллогенных диплоидных фибробластов (АДФ), и полученное механической дезагрегацией донорской ткани, добавлением питательной среды, культивированием во влажной атмосфере с 5% CO2 и отделением супернатанта. Изобретение обеспечивает уменьшение ограничения в применении и удешевление в получении. 2 табл., 10 ил. мононуклеарами периферической крови здоровых доноров; – на фиг.6 – влияние супернатантов АДФ на ЛПС-стимулированную продукцию ФНО- – на фиг.7 – влияние супернатантов АДФ на спонтанную продукцию ИЛ-1 – на фиг.8 – влияние супернатантов АДФ на ЛПС-стимулированную продукцию ИЛ-1 – на фиг.9 – влияние супернатантов АДФ на спонтанную продукцию раИЛ-1 мононуклеарами периферической крови здоровых доноров; – на фиг.10 – влияние супернатантов АДФ на ЛПС-стимулированную продукцию раИЛ-1 мононуклеарами периферической крови здоровых доноров. На всех фигурах и во всех таблицах: *1 – р<0,05 по сравнению с контролем. Для статобработки использовали дисперсионный анализ и критерий Ньюмена-Кейлса. Способ осуществляется следующим образом. Перевиваемые линии АДФ получали оригинальным бесферментативным методом, отличающимся от общепринятого отказом от использования протеолитических ферментов (трипсин, коллагеназа, террилитин и др.). Кусочки тканей (абортный материал, кусочки дермы, костный мозг, легких) подвергали механической дезагрегации до фрагментов размером 0,1-0,2 мм3, добавляли питательную среду 199, дополненную 10% сыворотки крови крупного рогатого скота, – для эмбриональных и фетальных тканей, или питательную среду RPMI 1640, дополненную 20% сыворотки эмбрионов коров, – для постнатального материала. Фрагменты тканей ресуспендировали в указанной среде, вносили в культуральные пластиковые флаконы и культивировали во влажной атмосфере с 5% СО2. В течение 1-3 суток происходила миграция фибробластов из тканевых фрагментов и прикрепление к дну культуральных флаконов. После этого фрагменты тканей со средой из флаконов удаляли, а к прикрепленным клетками добавляли свежую среду, соответствующую степени зрелости их источника. После формирования на дне культуральных флаконов монослоя АДФ отработанную питательную среду удаляли, к клеткам добавляли бессывороточную среду 199 и вновь культивировали в течение 24 ч в стандартных условиях. Через сутки кондиционированную АДФ среду сливали и проверяли в последующих экспериментах на биологическую активность, а клеточный монослой пересевали на новые флаконы со сменой среды и контролем бактериологической чистоты и кариотипа клеток. Предлагаемый способ бесферментативного получения культур клеток позволяет обеспечить минимальное повреждение клеток и снизить экономические затраты на начальном этапе. Биологическая активность вещества иллюстрирована в нижеприведенных экспериментах. Пример 1. Влияние супернатантов АДФ на функциональную активность Нф периферической крови здоровых доноров in vitro. В качестве супернатантов использовали кондиционированную в течение 24 ч эмбриональными (СЭФ) или зрелыми легочными (СЗФЛ) фибробластами среду 199. МНК и нейтрофилы (Нф) получали из венозной крови здоровых добровольцев общепринятым методом выделения на двойном градиенте плотности фиколл-гипак 1,077 и 1,114. После отмывки Нф ресуспендировали в бессывороточной среде 199 и вносили в лунки 96-луночного планшета в конечной концентрации 2×105/лунку. К МНК добавляли суточный СЭФ и СЗФЛ в конечной концентрации 25%, в контрольные лунки добавляли аналогичный объем бессывороточной среды 199. Клетки инкубировали в течение 2 ч в термостате при +37°С, по окончании инкубации трижды отмывали от неприкрепившихся клеток подогретым до +37°С фосфатно-солевым буфером. Дальнейшие эксперименты проводили по методикам, описанным Р.М.Хаитовым и соавт. (Экологическая иммунология / Р.М.Хаитов, Б.В.Пинегин, Х.И.Истамов. – М.: ВНИРО, 1995. – 219 с.). Показатели активности нейтрофилов представлены в табл. 1 и на фиг.1-4. Пример 2. Влияние супернатантов АДФ на продукцию ФНО- После отмывки МНК ресуспендировали в полной питательной среде RPMI-1640 с добавлением 5% эмбриональной телячьей сыворотки и вносили в лунки 24-луночного планшета в конечной концентрации 1×106/лунку. К МНК добавляли суточный СЭФ и СЗФЛ в конечной концентрации 25%, в контрольные лунки добавляли аналогичный объем бессывороточной среды 199. В часть лунок вносили ЛПС в концентрации 10 мкг/лунку. Клетки инкубировали в течение суток в СО2-инкубаторе и по окончании инкубации оценивали концентрацию ФНО Пример 3. Влияние супернатантов АДФ на продукцию рецепторного антагониста ИЛ-1 (раИЛ-1) МНК периферической крови здоровых доноров in vitro. Общая схема опытов идентична описанной для исследования продукции ФНО- Таким образом, супернатанты АДФ in vitro оказывали противовоспалительное влияние, выражавшееся в подавлении продукции провоспалительных цитокинов аллогенными мононуклеарными клетками в условиях стимуляции липополисахаридом, подавление адгезионной способности аллогенных нейтрофилов. При этом отмечается стимуляция продукции раИЛ-1 мононуклеарами, особенно в условиях индукции липополисахаридом, и повышение активности факторов бактерицидности нейтрофилов. Пример 4. Влияние супернатантов АДФ на сроки эпителизации экспериментальной ожоговой раны (ЭОР) у крыс. Под эфирным наркозом 10 крысам линии Вистар раскаленным до 200°С электродом площадью 1 см2 путем контактного воздействия в течение 2 с наносили 3 экспериментальных ожоговых раны (ЭОР) на область спины. На каждую из ран накладывали стерильную салфетку, пропитанную раствором 0,05% фурацилина (контроль), СЭФ или СЗФЛ, которые фиксировали лейкопластырем. На шею крысы фиксировали пластиковый воротник и каждую крысу помещали в отдельную клетку для исключения самостоятельного и взаимного повреждения наклеек. Под эфирным наркозом ежедневно в течение 21 дня производили перевязку со сменой салфеток с супернатантами АДФ и раствором антисептика. При формировании струпа на ране во время перевязки его тангенциально иссекали. За указанный период отмечена полная эпителизация ЭОР, леченных СЭФ, – у 8 крыс, леченных СЗФЛ – у 7 крыс, леченных раствором фурацилина – у 2 крыс.
Формула изобретения
Вещество, обладающее противовоспалительной, иммуномодулирующей и ранозаживляющей активностью, характеризующееся тем, что содержит супернатант культуры аллогенных диплоидных фибробластов (АДФ), включающий комплекс гуморальных факторов, продуцируемых АДФ, и полученное механической дезагрегацией донорской ткани, добавлением питательной среды, культивированием во влажной атмосфере с 5% CO2 и отделением супернатанта.
РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 01.02.2007
Извещение опубликовано: 10.04.2009 БИ: 10/2009
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 мононуклеарами периферической крови здоровых доноров;
мононуклеарами периферической крови здоровых доноров; мононуклеарами периферической крови здоровых доноров;
мононуклеарами периферической крови здоровых доноров;