Патент на изобретение №2298553
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 2-(3′,5′-ДИАМИНО-1′,2′,4′-ТРИАЗОЛ-1′-ИЛ)-4-R1-5-R2-1,3-ТИАЗОЛОВ
(57) Реферат:
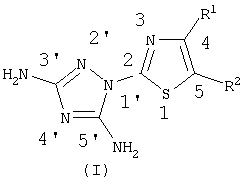
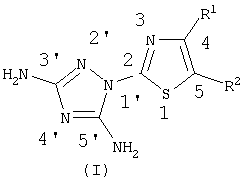
Изобретение относится к усовершенствованному способу получения 2-(3′,5′-диамино-1′,2′,4′-триазол-1’ил)-4-R1-5-R2-1,3-тиазолов общей формулы (I), которые могут использоваться для синтеза лекарственных или биологически активных веществ
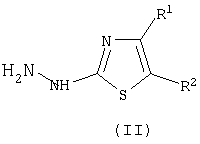
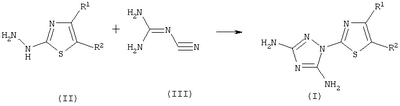
где R1 представляет собой Н, прямой или разветвленный C1-С4 алкил, или СООС1-С4-алкил, или фенил, необязательно замещенный одним или несколькими заместителями, выбранными из галогена, R2 представляет собой Н, прямой или разветвленный C1-C4 алкил или СООС1-С4-алкил, в котором к водному раствору гидрохлорида 4-R1-5-R2-2-гидразино-1,3-тиазола формулы (II),
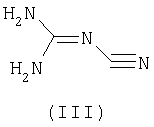
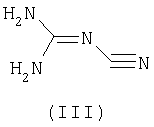
где R1 и R2 имеют указанные значения, прибавляют N-цианогуанидин (III)
при мольном соотношении (II):(III)=1,10-1,20:1,00 и полученную смесь нагревают при температуре 80-95°С и выдерживают при этой температуре с последующими ее нейтрализацией, отфильтровыванием и перекристаллизацией. Способ позволяет получать 2-(3′,5′-диамино-1′,2′,4′-триазол-1′-ил)-4-R1-5-R2-1,3-тиазолы из дешевого и доступного сырья без применения сложных технологических операций.
(56) (продолжение): CLASS=”b560m”студентов и аспирантов ЮРГТУ. – Новочеркасск: Набла, 2003, с.146-147. КОСОВ А.Е. и др. Синтез и свойства 1-тиазолил-3,5-диамино-1,2,4-триазолов. Студенческая научная весна – 2004. Материалы 53 научно-технической конференции студентов и аспирантов ЮРГТУ. – Новочеркасск: НПО «ТЕМП», 2004, с.152-154.
Изобретение относится к области получения органических веществ и может быть использовано в производстве лекарственных и биологически активных веществ. Задачей изобретения является разработка способа получения 2-(3′,5′-диамино-1′,2′,4′-триазол-1′-ил)-4-R1-5-R2-1,3-тиазолов из доступного сырья, позволяющий повысить выход целевых продуктов. Поставленная задача достигается в данном способе получения, заключающемся во взаимодействии гидрохлорида 4-R1-5-R2-2-гидразино-1,3-тиазола (II) с N-цианогуанидином (III) в водном растворе при мольном соотношении (II):(III)=1,10-1,20:1,00 и температуре 80-95°С и выдерживают при этой температуре, с последующими ее нейтрализацией, отфильтровыванием и перекристаллизацией. Мольное соотношение (II):(III)=1,10-1,20:1,00 является оптимальным. Изменение мольного соотношения приводит либо к образованию побочных продуктов и снижению чистоты целевых продуктов, либо к перерасходу реагентов, что экономически нецелесообразно. Температурный интервал 80-95°С также является оптимальным. При температурах ниже 80°С скорость реакции снижается, поэтому необходимо увеличивать время синтеза, что экономически нецелесообразно. При температурах выше 95°С наблюдается сильное осмоление реакционной массы, вследствие чего выход целевого продукта уменьшается. Способ осуществляется следующим образом. К водному раствору гидрохлорида общей формулы (II) прибавляют N-цианогуанидин (III) при мольном соотношении (II):(III)=1,10-1,20:1,00. Реакционную смесь выдерживают при температуре 80-95°С 1 час, нейтрализуют водным раствором ацетата натрия, выпавший осадок целевого продукта (I) отфильтровывают и перекристаллизовывают. Пример 1 К раствору 8.1 г (0.0342 моль) гидрохлорида 2-гидразино-4-метил-5-карбэтокси-1,3-тиазола в 100 мл воды прибавляют 2.4 г (0.0285 моль) N-цианогуанидина и нагревают при температуре 80-95°С в течение 1.0 ч. Затем при охлаждении реакционную смесь нейтрализуют водным раствором ацетата натрия, выпавший осадок отфильтровывают. Получают 4.6 г (60%) 2-(3′,5′-диамино-1′,2′,4′-триазол-1′-ил)-4-метил-5-карбэтокси-13-тиазола. Тпл=223-224°С (АсОН/EtOH). Спектр ЯМР 1H, Найдено (%): С 40.29, N 31.32, S 11.95 C9H12N6SO2 Вычислено (%):С 40.00, N 32.05, S 12.03 Пример 2 К раствору 5.4 г (0.0228 моль) гидрохлорида 2-гидразино-4-метил-5-карбэтокси-1,3-тиазола в 100 мл воды прибавляют 2.4 г (0.0285 моль) N-цианогуанидина и нагревают при температуре 80-95°С в течение 1.0 ч. Затем при охлаждении реакционную смесь нейтрализуют водным раствором ацетата натрия, выпавший осадок отфильтровывают. Получают 1.8 г (35%) 2-(3′,5′-диамино-1′,2′,4′-триазол-1′-ил)-4-метил-5-карбэтокси-1,3-тиазола. Тпл=220-222°С (АсОН/EtOH). Пример 3 К раствору 3.9 г (0.01641 моль) гидрохлорида 2-гидразино-4-метил-5-карбэтокси-1,3-тиазола в 100 мл воды прибавляют 1.2 г (0.01427 моль) N-цианогуанидина и нагревают при температуре 50-60°С в течение 1.0 ч. Затем при охлаждении реакционную смесь нейтрализуют водным раствором ацетата натрия, выпавший осадок отфильтровывают. Получают 0.6 г (15%) 2-(3′,5′-диамино-1′,2′,4′-триазол-1′-ил)-4-метил-5-карбэтокси-1,3-тиазола. Тпл=222-223°С (АсОН/EtOH). Пример 4 К раствору 3.9 г (0.01641 моль) гидрохлорида 2-гидразино-4-метил-5-карбэтокси-1,3-тиазола в 100 мл воды прибавляют 1.2 г (0.01427 моль) N-цианогуанидина и кипятят в течение 1.0 ч. Затем при охлаждении реакционную смесь нейтрализуют водным раствором ацетата натрия, выпавший осадок отфильтровывают. Получают 1.5 г (40%) 2-(3′,5′ -диамино-1′,2′,4′-триазол-1′-ил)-4-метил-5-карбэтокси-1,3-тиазола. Тпл=223-224°С (АсОН/EtOH). Пример 5 К раствору 7.7 г (0.0342 моль) гидрохлорида 2-гидразино-4-фенил-1,3-тиазола в 100 мл воды прибавляют 2.4 г (0.0285 моль) N-цианогуанидина и нагревают при температуре 80-95°С в течение 1.0 ч. После охлаждения реакционную смесь нейтрализуют водным раствором ацетата натрия, выпавший осадок отфильтровывают, промывают водой и кристаллизуют. Выход 2-(3′,5′-диамино-1′,2′,4′-триазол-1′-ил)-4-фенил-1,3-тиазола составляет 1.4 г (20%). Тпл=218.5-219°С(СН3CN). Спектр ЯМР 1H Найдено (%): С 51.15, N 32.54, S 12.41 C11H10N6S Вычислено (%): С 51.71, N 32.50, S 12.00 Пример 6 К раствору 9.0 г (0.0342 моль) гидрохлорида 2-гидразино-4-(n-хлорфенил)-1,3-тиазола в 100 мл воды прибавляют 2.4 г (0.0285 моль) N-цианогуанидина и нагревают при температуре 80-95°С в течение 1.0 ч. После охлаждения реакционную смесь нейтрализуют водным раствором ацетата натрия, выпавший осадок отфильтровывают, промывают водой и кристаллизуют. Выход 2-(3′,5′-диамино-1′,2′,4′-триазол-1′-ил)-4-(n-хлорфенил)-1,3-тиазола составляет 4.4 г (53%). Тпл=255-256°С (АсОН/EtOH). Спектр ЯМР 1H Найдено (%): С 45.13, N 28.71, S 10.95 С11Н9N6SCl Вычислено (%): С 46.15, N 28.79, S 12.06 Пример 7 К раствору 1.0 г (0.0060 моль) гидрохлорида 2-гидразино-4-метил-1,3-тиазола в 20 мл воды прибавляют 0.4 г (0.0050 моль) N-цианогуанидина и реакционную смесь выдерживают в течение 1.0 ч при температуре 80-95°С. После охлаждения смесь нейтрализуют водным раствором ацетата натрия, выпавший осадок 2-(3′,5′-диамино-1′,2′,4′-триазол-1′-ил)-4-метил-1,3-тиазола отфильтровывают и кристаллизуют. Выход 0.25 г (25%). Тпл=250.5-251°С (СН3CN). Спектр ЯМР 1H Найдено (%): С 36.72, N 42.83, S 16.34 C6H8N6S Вычислено (%): С 36.04, N 43.03, S 16.30 Пример 8 К раствору 8.4 г (0.0342 моль) гидрохлорида 2-гидразино-4-(n-фторфенил)-1,3-тиазола в 100 мл воды прибавляют 2.4 г (0.0285 моль) N-цианогуанидина и нагревают при температуре 90-95°С в течение 1.0 ч. После охлаждения реакционную смесь нейтрализуют водным раствором ацетата натрия, выпавший осадок отфильтровывают, промывают водой и кристаллизуют. Выход 2-(3′,5′-диамино-1′,2′,4′-триазол-1′-ил)-4-(n-фторфенил)-1,3-тиазола составляет 3.93 г (50%). Тпл=241-243°С (EtOH). Спектр ЯМР 1H Найдено (%): С 48.00, Н 3.30, N 30.21 C11H9N6FS Вычислено (%): С 47.82, Н 3.28, N 30.42 Пример 9 К раствору 1.1 г (0.006 моль) гидрохлорида 2-гидразино-4,5-диметил-1,3-тиазола в 20 мл воды прибавляют 0.42 г (0.005 моль) N-цианогуанидина и реакционную смесь выдерживают в течение 1.0 ч при температуре 90-95°С. После охлаждения смесь нейтрализуют водным раствором ацетата натрия, выпавший осадок 2-(3′,5′-диамино-1′,2′,4′-триазол-1′-ил)-4,5-диметил-1,3-тиазола отфильтровывают и кристаллизуют.Выход 0.37 г (35%). Тпл=238.5-241°С (СН3CN). Спектр ЯМР 1H Найдено (%): С 40.12, Н 4.80, N 39.69 C7H10N6S Вычислено (%): С 39.99, Н 4,79, N 39.97 Пример 10 К раствору 1.34 г (0.006 моль) гидрохлорида 2-гидразино-4-метил-5-карбометокси-1,3-тиазола в 20 мл воды прибавляют 0.42 г (0.005 моль) N-цианогуанидина и реакционную смесь выдерживают в течение 1.5 ч при температуре 90-95°С. После охлаждения смесь нейтрализуют водным раствором ацетата натрия, выпавший осадок 2-(3′,5′-диамино-1′,2′,4′-триазол-1′-ил)-4-метил-5-карбометокси-1,3-тиазола отфильтровывают и кристаллизуют. Выход 0.69 г (54%). Тпл=210-213°С (EtOH). Спектр ЯМР 1Н, Найдено (%): N 33.12 C8H10N6O2S Вычислено (%):N 33.05
Формула изобретения
Способ получения 2-(3′,5′-диамино-1′,2′,4′-триазол-1′-ил)-4-R1-5-R2-1,3-тиазолов общей формулы (I)
где R1 представляет собой Н, прямой или разветвленный C1-C4 алкил, или СООС1-С4-алкил, или фенил, необязательно замещенный одним или несколькими заместителями, выбранными из галогена, R2 представляет собой Н, прямой или разветвленный C1-C4 алкил, или СООС1-С4-алкил, отличающийся тем, что к водному раствору гидрохлорида 4-R1-5-R2-2-гидразино-1,3-тиазола формулы (II),
где R1 и R2 имеют указанные значения, прибавляют N-цианогуанидин (III)
при мольном соотношении (II):(III)=1,10-1,20:1,00 и полученную смесь нагревают при температуре 80-95°С и выдерживают при этой температуре, с последующими ее нейтрализацией, отфильтровыванием и перекристаллизацией.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 19.11.2007
Извещение опубликовано: 20.05.2009 БИ: 14/2009
|
||||||||||||||||||||||||||

 , м.д. (DMSO-d6) 1.31-1.36 т (3Н, СН3),
, м.д. (DMSO-d6) 1.31-1.36 т (3Н, СН3),