Патент на изобретение №2298408
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СОСТАВ ДЛЯ ЛЕЧЕНИЯ КАТАРАКТЫ
(57) Реферат:
Изобретение относится к области медицины. Состав содержит водный экстракт прополиса 1:5, растворенного в нем 50% полифлерного цветочного меда и 2% нативного маточного молочка. Изобретение позволяет добиться стабилизации и определенного регресса помутнений хрусталика, снизить активность перекисного окисления липидов хрусталика, увеличить содержание восстановленной формы глутатиона, предотвратить окисление восстановленных белковых тиоловых групп, позитивно влияет на активность глутатион-зависимых ферментов антиоксидантной защиты хрусталика. Изобретение обеспечивает стабилизацию и регресс формирующейся катаракты. 5 табл.
(56) (продолжение): CLASS=”b560m”antioxidants on selenite-induced cataract formation and oxidative stress-related parameters in rats. Toxicology. 1999 Dec 6; 139 (3); 219-32. PMID: 10647922 (реферат), [он-лайн] [03.07.2006.] найдено из БД PubMed.
Изобретение относится к медицине, а именно к фармакотерапии глазных болезней, и может быть использовано для консервативного лечения катаракты. В этиопатогенезе катаракты одним из ведущих моментов является патологическая активация свободнорадикального окисления липидов мембран и других биополимеров хрусталика [1]. В обеспечении прозрачности хрусталика большую роль играет восстановленная форма глутатиона, поддерживая белковые тиоловые группы в восстановленном состоянии [2]. Для консервативного лечения катаракты используются капли “Офтан Катахром”. Препарат оказывает антиоксидантное действие, улучшает метаболизм и трофику тканей глаза. По данным ряда исследований, препарат не обладает высоким антикатарактальным действием, а эффективен для тканей, расположенных впереди хрусталика [3, 4, 5]. Состав препарата: цитохром С – 675 мкг, аденозин – 2 мг, никотинамид – 20 мг, натрия сукцинат – 1 мг, бензалкония хлорид – 40 мкг в 1 мл готового препарата. Продукты пчеловодства – маточное молочко, мед, прополис – обладают высокой антиоксидантной и мембраностабилизирующей активностью, стимулирующим эффектом на обменные процессы тканей организма, имеют в своем составе широкий спектр биологически активных соединений, не токсичны, синергичны живому организму [6]. Имеются данные об увеличении биологического эффекта и стабильности биологических свойств указанных продуктов пчеловодства при совместном применении. В частности, используются комплексные препараты меда, маточного молочка и прополиса (“Апиток”, “Апитонус”, “Тополек”, “Апитоник”) для стимуляции обменных процессов, увеличения неспецифической сопротивляемости, расширения адаптивных возможностей организма, в комплексной терапии заболеваний, связанных с увеличением активности свободнорадикальных процессов окисления биополимеров [6, 7]. В офтальмологической практике местно используется лекарственный препарат маточного молочка “Колгель” (2% водный раствор) для улучшения репаративных процессов эпителия роговицы [7, 8]. Водный экстракт прополиса 1:5 применялся в эксперименте при гнойной язве и химическом ожоге роговицы, при этом нормализацию активности протеолитических ферментов в ткани роговицы авторами была связана с мембраностабилизирующей активностью [9]. Информации о влиянии на метаболизм хрусталика этих препаратов и возможном антикатарактальном эффекте нет. Имеются данные о положительном эффекте местного применения 50% водного раствора меда при возрастной катаракте на начальных стадиях [10]. В литературе есть указание на положительные результаты системного применения маточного молочка в сочетании с медом при катаракте [11]. Однако эти исследования имеют эмпирическую основу, отсутствует биохимическое объяснение полученных позитивных результатов. Состав нативного маточного молочка: ацетилхолин, свободный холин, эстрадиол, прогестерон, тестостерон, энтомологические гормоны (проторактотропные, гормоны линьки, товенильные гормоны), инсулиноподобные пептиды, лизоцим, витамины (B1, В2, РР, пантотеновая кислота, В6, B12, фолиевая кислота, биотин), органические кислоты (10-окси-транс-дельта-деценовая кислота, 9-окси-дельта-деценовая, 2-кето-децендикарбоновая, 9-кето-2-децендикарбоновая, 10-оксидекановая, параоксибензойная, лауриновая, адипиновая, янтарная, азелаиновая, пальмитиновая, стеариновая, олеиновая, линолевая, липоевая и ряд других), углеводы (глюкоза, фруктоза, рибоза, сахароза, мальтоза, изомальтоза, трегалоза, неотрегалоза, тураноза, гентиобиноза), минеральные вещества (калий, натрий, кальций, магний, фосфор, марганец, медь, цинк) [8, 12]. Состав цветочного меда: углеводы (фруктоза, глюкоза, незначительное количество олигосахаров), органические кислоты (яблочная, молочная, глюконовая, янтарная, винная, лимонная, щавелевая, муравьиная, уксусная, масляная), аминокислоты (пролин, фенилаланин, тирозин, аспарагиновая, глутаминовая), ферменты (диастаза, инвертаза, каталаза, пероксидаза, о-дифенолоксидаза, глюкозооксидаза), витамины (В2, РР, С, В6, К, Е), минеральные вещества и микроэлементы (медь, железо, марганец, кальций, калий, натрий, магний, цинк, кобальт и другие), литтиды и свободные жирные кислоты (пальмитиновая, стеариновая, олеиновая, лауриновая, арахидоновая, триацилглицериды), липоиды (стеролы, фосфолипиды), гидрооксиметилфурфурол, флавоноиды [6, 8]. Состав водного экстракта прополиса 1:5: флавоноиды, деценовые кислоты, фенольные соединения (кофейная, n-кумаровая, феруловая кислоты; скополетин, эскулетин, умбеллифон), терпены, сапонины, экдистероиды [9]. Цель изобретения. Разработка местного глазного лекарственного препарата биологического происхождения с высокими антиоксидантными свойствами, применение которого в эксперименте вызовет стабилизацию и регресс формирующейся катаракты. Сущность изобретения состоит в том, что для лечения катаракты в эксперименте применен состав “апикомпозиция”, содержащий водный экстракт прополиса 1:5, 50% раствор полифлерного цветочного меда и 2% раствор нативного маточного молочка, и в виде инстилляций в конъюнктивальную полость глаза 4 раза в день. Предполагаемый результат. Получение достоверно значимого антикатарактального и антиоксидантного (для ткани хрусталика) эффектов при применении заявляемого препарата на лабораторной модели катаракты. Заявляемый препарат готовился путем приготовления 200 мл водного экстракта прополиса 1:5 [13], растворения в полученном экстракте 100 г полифлерного цветочного меда свежего урожая. Конечный раствор для инстилляций готовился ежедневно путем растворения 100 мг нативного маточного в 5,0 мл раствора меда в экстракте прополиса. Между закапываниями препарат хранился в холодильнике при +2°С, непосредственно перед инсталляцией препарат нагревался до комнатной температуры. Сравнительное исследование антиоксидантной и антикатарактальной эффективности заявляемого состав проведено на 42 кроликах-самцах средним весом 2 кг, породы “Шиншилла”. В каждой группе лечения (и группа без лечения) – по 12 животных, по 3 кролика (6 глаз) на каждый срок биохимических исследований. Группа интактных – 6 животных (12 глаз). У всех животных (кроме интактных) была вызвана катаракта путем химической инициации свободнорадикального окисления биополимеров тканей глаза [14]. Контрольные методы лечения: placebo, “Офтан Катахром”. Длительность эксперимента – 56 суток. Схема лечения: 3-кратные ежедневные инстилляции 2 капель препарата в конъюнктивальную полость каждого глаза. Динамику процесса формирования катаракты и эффективность проводимого лечения оценивали экспериментально-клиническими методами: бокового освещения, проходящего света и биомикроскопии. Для изучения активности свободнорадикального окисления липидов определяли содержание малонового диальдегида; для оценки состояния антиоксидантной защиты хрусталика определяли количество восстановленного глутатиона, суммарную емкость антиоксидантной защиты ткани хрусталика (по продолжительности лаг-фазы накопления малонового диальдегида в инкубируемом в присутствии кислорода гомогенате хрусталика), активность глутатионпероксидазы, глутатионредуктазы и глутатион-SH-трансферазы. Так же определяли количество восстановленных тиоловых белковых групп. Выведение животных из опыта для проведения биохимических исследований хрусталиков осуществляли на 14, 28, 42 и 56 сутки от момента введения индуктора катарактогенеза. У животных всех групп начальные катарактальные изменения хрусталиков появились к 3-7 суткам в коре и при отсутствии медикаментозного лечения имели тенденцию к неуклонному прогрессу, за исключением 1 случая стабилизации к 42 суткам. К 56 суткам у животных, не получавших лечения, наблюдались сливные очаги помутнения корковых отделов хрусталика. Лечение препаратами начинали со времени появления начальных катарактальных изменений хрусталиков у всех животных (с 7 суток от введения индуктора катарактогенеза). Эффект заявляемого состава. Терапия препаратом маточного молочка оказалась более эффективной по проценту стабилизации и регресса помутнений уже к 28 суткам (табл.1).
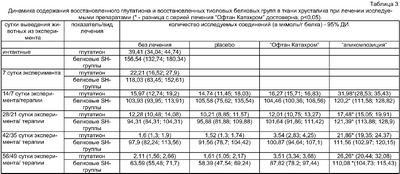
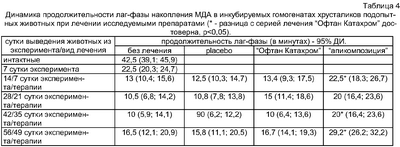
Лечение заявляемым составом, в сравнении с контрольными методами лечения, достоверно значимо (р<0,05) снизило активность свободнорадикального окисления липидов хрусталика на 14, 28 и 42 сутки; предотвратило окисление белковых восстановленных тиоловых групп на 14, 28 и 56 сутки; увеличило содержание восстановленного глутатиона на 14, 28, 42 и 56 сутки; более существенно предотвратило уменьшение продолжительности лаг-фазы накопления малонового диальдегида в гомогенатах хрусталиков на 14, 28 и 56 сутки. Применение состава “апикомпозиция” сместило пик активности глутатион-пероксидазы с 7-х на 14-е сутки, предотвратило значительное истощение (на 28 сутки) и способствовало увеличению активности фермента на 42 и 56 сутки; предотвратило значительное снижение активности глутатион-редуктазы во все сроки наблюдения; несколько увеличило активность глутатион-SH-трансферазы на 14, 28, 42 и 56 сутки. В цифровом выражении результаты представлены в таблицах 2, 3, 4 и 5.
Источники информации 2. Э.В.Мальцев. Хрусталик. М.: Медицина, 1988. 3. Справочник Видаль. Лекарственные препараты в России: Справочник. Изд. 9-е. М.: АстраФармСервис, 2003. 6. Т.В.Вахонина, Пчелиная аптека. СПб.: Лениздат, 1992 – прототип. 7. В.Г.Макарова, Н.И.Кривцов, В.И.Лебедев, Д.Г.Узбекова, Е.Н.Якушева, К.В.Савилов. Основы апитерапии: учебное пособие. Рязань: ГОУ ВПО РГМУ, 2004. 8. А.А.Комаров. Да ужалит вас пчела! Тула: Коммунар. 1991. 12. B.H.Крылов, С.С.Сокольский. Маточное молочко пчел. Свойства, получение, применение: научно-справочное издание. Краснодар: Агропромполиграфист, 2000. Формула изобретения
Состав для лечения катаракты на основе полифлерного цветочного меда, отличающийся тем, что он дополнительно содержит водный экстракт прополиса 1:5, 2%-ного нативного маточного молочка, а содержание полифлерного цветочного меда составляет 50% раствора.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 06.03.2007
Извещение опубликовано: 10.04.2009 БИ: 10/2009
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||