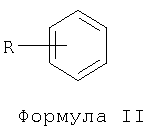Патент на изобретение №2297998
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 4-ФЕНИЛМАСЛЯНОЙ КИСЛОТЫ И ЕЕ СОЛЕЙ (ВАРИАНТЫ)
(57) Реферат:
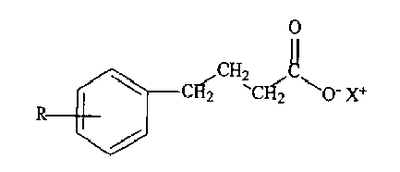
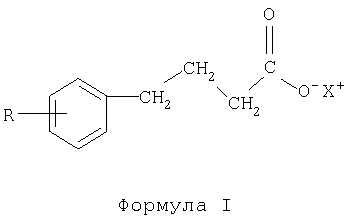
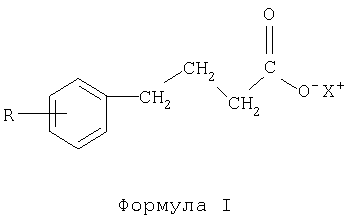
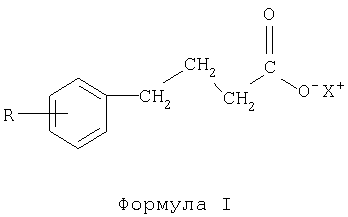
Изобретение относится к получению фармацевтически активных соединений, в частности производных фенилмасляной кислоты формулы I
где R выбран из группы: водород, галоген, С1-С4 алкил, алкенил, алкинил, С3-С6 циклоалкил, С1-С4 алкокси, алкенокси, алкинокси; и Х представляет собой водород, катион щелочного металла, аммоний или замещенный аммоний. Способ осуществляют путем взаимодействия замещенного бензола с бутиролактоном в присутствии хлорида алюминия, с последующей нейтрализацией основанием или осаждением соединения добавлением кислоты. В качестве катализатора используют кислоту Льюиса, предпочтительно хлорид алюминия, хлорид цинка, хлорид железа, хлорид олова, трибромид бора, трифторид бора или серную кислоту. Технический результат – упрощение способа с высоким выходом конечного продукта. 2 н. и 17 з.п. ф-лы.
Предпосылки изобретения Данное изобретение относится к новому способу синтеза соединений формулы I.
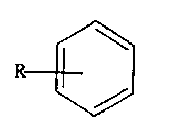
Особенно предпочтительными объектами по настоящему изобретению являются фенилмасляная кислота и ее фармацевтически приемлемые производные. Фенилбутират натрия широко использовался при лечении расстройств орнитинового цикла (цикла образования мочевины) (Batshaw et al., Brusilow et al. (Ped. Research), Brusilow et al. (New Eng. J. Med.), Finkelstein et al., Maestri et al., Redonnet-Vernhet et al., Rowe et al.). Производные фенилбутирата также демонстрируют многообещающие фармацевтические свойства при лечении серповидно-клеточной анемии (Collins et al., Dover et al. (New Eng. J. Med.), Dover et al. (Blood)), кистозного фиброза (Bradbury et al., Loffing et al.), СПИДа (Roberts et al.), и некоторых видов рака (Carducci et al., Darmanun et al., Englehard et al., Gorospe et al.). Ранее производные фенилбутирата получали путем реакции Арндта-Айстерта (Arndt-Eistert), используя диазометан с оксидом серебра и тиосульфат натрия (J. Chem. Soc., 1997-99 (1938)). Альтернативно, тианафтен-2-уксусную кислоту и тианафтен-3-уксусную кислоту использовали для получения Был бы удобен такой путь синтеза фенилбутирата и его производных, который не был бы усложнен ограничениями, предъявляемыми к синтезу, то есть необходимостью строгого исключения влаги из диазометана и реактива Гриньяра, и который давал бы более высокий выход продукта, чем описанные выше реакции. Сущность изобретения Одним аспектом настоящего изобретения является способ получения соединения формулы I: Формула I где R независимо выбран из водорода, галогена, C1-C4 алкила, алкенила, алкинила, C3-C6 циклоалкила, C1-C4 алкокси, алкенокси, алкинокси; и X представляет собой водород, катион щелочного металла, аммоний или замещенный аммоний. В соответствии с одним вариантом воплощения изобретения способ включает следующие стадии, a) взаимодействие соединения формулы II;
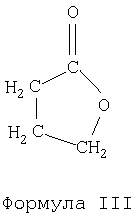
Формула II где R определен выше, с соединением формулы III;
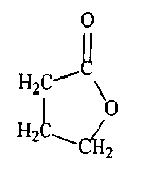
Формула III, и b) взаимодействие полученного соединения с соединением формулы IV; Xb-Zc Формула IV где X определен выше, и Z представляет собой гидрокси, сульфат, фосфат, бикарбонат, карбонат или алкокси, и b и c независимо равны 1-5. Особенно подходящее соединение формулы IV представляет собой гидроксид натрия. В соответствии с одним аспектом изобретения взаимодействие соединения формулы I с соединением формулы II проводят в присутствии катализатора. Особенно подходящими катализаторами являются кислоты Льюиса, включая, но не ограничиваясь ими, хлорид алюминия, хлорид цинка, хлорид железа, хлорид олова, трибромид бора, трифторид бора или серную кислоту. Конкретным аспектом настоящего изобретения является способ получения 4-фенилмасляной кислоты путем взаимодействия бензола с бутиролактоном. Подробное описание изобретения Для специалиста в данной области на основании следующего описания и иллюстративных примерах будет понятно, определит, что настоящее изобретение представляет собой способ синтеза соединений формулы I: Формула I где R независимо выбран из водорода, галогена, C1-C4 алкила, алкенила, алкинила, C3-C6 циклоалкила, C1-C4 алкокси, алкенокси, алкинокси; и X представляет собой водород, катион щелочного металла, аммоний или замещенный аммоний. Следует, конечно, принимать во внимание, что при разработке любого подобного конкретного варианта воплощения, могут быть осуществлены многочисленные реализации конкретных решений для достижения конкретных задач разработки, отвечающие системным и деловым ограничивающим условиям, которые будут изменяться от одной реализации к другой. Более того, следует учитывать, что такие усилия по разработке могут быть сложными и трудоемкими, но, тем не менее, являются рутинным делом для специалиста в данной области, располагающего преимуществами данного описания. Способ по настоящему изобретению включает взаимодействие соединения формулы II
Формула II с соединением формулы III.
Формула III Особенно предпочтительным соединением формулы II является бензол. В соответствии с одним из вариантов воплощения по настоящему изобретению, взаимодействие проводят в растворителе. В соответствии с альтернативным вариантом воплощения, соединение формулы II, само по себе, является растворителем для реакции. Катализатор может использоваться для облегчения взаимодействия соединения формулы II с соединением формулы III. Одним из предпочтительных классов катализаторов являются кислоты Льюиса. Примерами особенно предпочтительных катализаторов являются хлорид алюминия, хлорид цинка, хлорид железа, хлорид олова, трибромид бора, трифторид бора и серная кислота. В соответствии с одним из вариантов воплощения изобретения, катализатор добавляют к смеси соединения формулы II и соответствующего растворителя или к чистому соединению формулы II, если не используется растворитель. Эту смесь выдерживают, предпочтительно при перемешивании, при температуре в интервале между около -80°C и точкой кипения растворителя при давлении окружающей среды. Предпочтительно, смесь выдерживают при температуре между 0°C и точкой кипения растворителя. Перед добавлением соединения формулы III к смеси смесь соединения формулы II и катализатора может перемешиваться в течение промежутка времени от нескольких секунд до нескольких дней. Предпочтительно, перед добавлением соединения формулы III смесь соединения формулы II и катализатор перемешивают в течение промежутка времени от около 1 минуты до около 30 минут. Соединение формулы III может быть добавлено к смеси соединения формулы II и катализатора в виде чистого реагента, или может быть добавлено в виде раствора в соответствующем растворителе. Соединение формулы III добавляют по каплям, небольшими аликвотными частями или в виде большой порции. После завершения добавления соединения формулы III, реакционную смесь выдерживают, предпочтительно при перемешивании, при температуре в интервале между около -80°C и точкой кипения растворителя при давлении окружающей среды. Предпочтительно, температуру смеси поддерживают в интервале между 0°C и точкой кипения растворителя. Реакционная смесь может выдерживаться в этих условиях в течение времени, равного от нескольких секунд до около 24 часов. Предпочтительно, реакционную смесь выдерживают в течение от около 10 минут до около 180 минут, более предпочтительно, от около 60 минут до около 120 минут. Реакционная смесь может быть погашена добавлением гасящего агента. Подходящие гасящие агенты представлены формулой IV: Xb-Zc Формула IV где X определен выше, и Z представляет собой гидрокси, сульфат, фосфат, бикарбонат, карбонат или алкокси, и b и c независимо равны 1-5. Гасящий агент может быть добавлен в чистом виде или в виде раствора в соответствующем растворителе. Особенно предпочтительным гасящим агентом является раствор основания. Предпочтительным основанием является гидроксид натрия. Другим предпочтительным гасящим агентом является смесь раствора водного основания и льда. Погашенный раствор может выдерживаться при температуре от около 0 до около 50°C в течение промежутка времени, равного от нескольких минут до 10 часов, предпочтительно, от около 1 часа до около 3 часов. Значение pH раствора может поддерживаться равным от около 6,5 до около 10, предпочтительно от около 9 до около 9,5. Значение pH раствора может далее быть увеличено путем добавления основания. Погашенный раствор может быть очищен фильтрованием для удаления любых частиц, которые могут присутствовать. Погашенный раствор может быть дополнительно очищен путем контактирования с органическим растворителем для экстракции оставшихся исходных продуктов, побочных продуктов и примесей. Примеры подходящих растворителей для экстракции включают хлороформ, дихлорметан, трихлорметан, тетрахлорид углерода и диэтиловый эфир. Продукт может быть осажден из водного раствора путем добавления кислоты. Продукт может быть восстановлен путем фильтрации, или экстрагирован соответствующим органическим растворителем. Если продукт экстрагируют органическим растворителем, он может быть выделен при выпаривании растворителя. Следующие примеры включены для демонстрации предпочтительных вариантов воплощения изобретения. Специалистам в данной области следует учитывать, что методики, описанные в следующих примерах, представляют методики, описанные заявителем с целью хорошего практического осуществления изобретения, и, таким образом, могут рассматриваться как предпочтительные способы при практическом осуществлении. Тем не менее, специалисту в данной области в свете настоящего изобретения понятно, что может быть предпринято множество модификаций в конкретных описанных вариантах воплощения с получением тех же или аналогичных результатов без отхода от духа и объема изобретения. Пример 1 К бензолу (400 г) добавляли порошкообразный хлорид алюминия (200 г) и перемешивали в течение 10 минут при 50°C. Небольшими порциями добавляли бутиролактон (86 г). Поддерживали температуру в интервале между 50 и 60°C в течение 90 минут и затем при перемешивании реакционную смесь добавляли к смеси льда и 5% гидроксида натрия. Температуру поддерживали ниже 35°C, и значение pH поддерживали в интервале между 9 и 9,5 в течение 2 часов. Смесь фильтровали в вакууме. Фенилмасляную кислоту осаждали из водной фракции путем добавления льда и соляной кислоты. Сырую (93,7%-94,3%) 4-фенилмасляную кислоту выделяли путем вакуумной фильтрации. Сырую 4-фенилмасляную кислоту очищали вакуумной дистилляцией (120-125°C, 1 мм ртутного столба). Кислоту растворяли в 5% гидроксиде натрия и взбалтывали. Кислоту растворяли в 5% гидроксиде натрия и взбалтывали с тетрахлоридом углерода в течение 15 минут. Тетрахлорид углерода удаляли и раствор 4-фенилмасляной кислоты перемешивали с ацетоном, метанолом и небольшим количеством активированного угля в течение 15 минут при комнатной температуре. Смесь фильтровали и подкисляли путем добавления HCl. Кристаллы 4-фенилмасляной кислоты (выход 81,15%) выделяли и сушили лиофилизацией. Анализ ВЭЖХ показал 99,87%-ную чистоту конечного продукта. Все описанные и заявленные здесь способы могут быть спланированы и выполнены без лишних экспериментов в свете настоящего описания. Хотя композиции и способы данного изобретения были описаны в виде предпочтительных вариантов воплощения, специалистам в данной области будет понятно, что в способах и на стадиях или в последовательностях стадий описанного здесь способа могут быть использованы вариации без отхода от сущности, духа и объема изобретения. Более конкретно, специалисту будет понятно, что некоторые реагенты, как химически, так и физиологически родственные, могут быть заменены описанными здесь реагентами с получением одинаковых или аналогичных результатов. Все такие аналогичные замены и модификации, очевидные для специалиста в данной области, охватываются духом, объемом и сущностью изобретения, что определено в прилагаемой формуле изобретения. Ссылки Следующие ссылки, в объеме, который предусматривает иллюстративные, методические или другие детали, дополняющие изложенное здесь, конкретно включены в настоящее описание в качестве ссылки. Carducci M. A., Nelson J., Chan-Tack K., Ayyagari S. R., Sweatt W., Campbell P., Nelson W., Simons J. Phenylbutyrate Induces Apoptosis in Human Prostate Cancer Therapy and is More Potent than Phenylacetate. Podium Presentation, American Urological Association, Las Vegas, NV. April, 1995. Clinical Cancer Research 2: 379-387. 1996. Darmanun D., Welch S., Rini A., et al Phenylbutyrate-induced Glutamine Depletion in Humans: Effect on Leucine Metabolism. Am J Physiol 274(5 Pt 1): E801-7. May 1998. Englehard H., Homer R. J., Duncan H., Rozental J. Inhibitory Effects of Phenylbutyrate on the Proliferation, Morphology, Migration and Invasiveness of Malignant Glioma Cells. J. Neuro-Oncology. 37:97-108. 1998. Roberts J, McGregor W. G. Inhibition of Mouse Retroviral Disease by Bioactive Glutaminase-asparaginase J. Gen. Virol. 72: 299-305. 1991. Bradbury N. A., Focus on “Sodium 4-phenylbutyrate Downregulates Hsc70: Implications for Intracellular Trafficking of DF508-CFTR.” Am J Physiol Cell Physiol 278(2):C257-8. February 2000. Loffing J., Moyer B. D., Reynolds D., Stanton B. A., PBA Increases CFTR Expression but at High Doses Inhibits C1(-) Secretion in Calu-3 Airway Epithelial Cells. Am J. Physiol 277(4 Pt 1):L700-8. October 1999. Collins A. F., Pearson H. A., Giardina P., McDonagh K T., Brusilow S W., Dover G. J. Oral Sodium Фенилбутират Therapy in Homozygous b Thalassemia: A Clinical Trial. Blood. 85: 43-49. 1995. Dover D., Brusilow S., Samid D. Increased Fetal Hemoglobin in Patients Receiving Sodium 4-Фенилбутират. New Eng. J. Med. 327:569-570, October 1, 1992. Dover G. J., Brusilow, S., Charache S., Induction of Fetal Hemoglobin Production in Subjects with Sickle Cell Anemia by Oral Sodium Фенилбутират. Blood. 184(1):339-43. July 1994. Brusilow S. Phenylacetylglutamine May Replace Urea as a Vehicle for Waste Nitrogen Excretion. Ped. Research. 29(2):147-150. 1991. Brusilow S., Danney M., Waber L., Batshaw M., et al. Treatment of Episodic Hyperammonemia in Children with Inborn Errors of Urea Synthesis. New Eng. J. Med. 310:1630-34. June 1984. Finkelstein J. E., Hauser E. R., Leonard C. O., Brusilow S. W. Late-onset Ornithine Transcarbamylase Deficiency in Male Patients. J Ped. 117(6):897-902. 1990. Maestri N., Hauser E., Bartholomew D., Brusilow S. Prospective Treatment of Urea Cycle Disorders. J Ped. 119(6):923-928. 1991. Redonnet-Vernhet I., Rouanet F., Pedespan J M, Hocke, C., Parrot F., A Successful Pregnancy in a Heterozygote for OTC Deficiency Treated with Sodium Фенилбутират. Neurology. 54(4):1008. Feb 2000. Rowe P., Newman S., Brusilow S. Natural History of Symptomatic Partial Omithine Transcarbamylase Deficiency. New Eng. J. Med. 314:541-547. 1986.
Формула изобретения
1. Способ получения соединения формулы I
где R независимо выбран из водорода, галогена, С1-С4 алкила, алкенила, алкинила, С3-С6 циклоалкила, С1-С4 алкокси, алкенокси, алкинокси; Х представляет собой водород, катион щелочного металла, аммоний или замещенный аммоний, который включает; а) взаимодействие соединения формулы II
где R определен выше, с соединением формулы III
где взаимодействие соединения формулы II с соединением формулы III проводят в присутствии катализатора; и b) гашение реакционной смеси со стадии а) путем добавления водного раствора основания; и c) выделение соединения формулы I или осаждение соединения формулы I путем добавления к реакционной смеси кислоты. 2. Способ по п.1, где основание представляет собой гидроксид натрия. 3. Способ по п.1, где все R представляют собой водород. 4. Способ по п.1, где катализатор представляет собой кислоту Льюиса. 5. Способ по п.4, где катализатор представляет собой хлорид алюминия, хлорид цинка, хлорид железа, хлорид олова, трибромид бора, трифторид бора или серную кислоту. 6. Способ по п.5, где катализатор представляет собой хлорид алюминия. 7. Способ по п.6, где смесь, содержащую соединение формулы II и хлорид алюминия, перемешивают в течение около 10 мин при температуре между около 40 и около 60°С с последующим добавлением соединения формулы III. 8. Способ по п.7, где соединение формулы III перемешивают со смесью, содержащей соединение формулы II и хлорид алюминия, в течение около 90 мин при температуре между около 50 и около 60°С с последующим добавлением гидроксида натрия. 9. Способ получения 4-фенилмасляной кислоты включающий a) взаимодействие бензола с бутиролактоном; b) взаимодействие полученной смеси с водным раствором основания и c) выделение 4-фенилмасляной кислоты или осаждение 4-фенилмасляной кислоты путем добавления к реакционной смеси кислоты, 10. Способ по п.9, где взаимодействие бензола с бутиролактоном происходит в присутствии катализатора. 11. Способ по п.10, где катализатор представляет собой кислоту Льюиса. 12. Способ по п.11, где катализатор представляет собой хлорид алюминия, хлорид цинка, хлорид железа, хлорид олова, трибромид бора, трифторид бора или серную кислоту. 13. Способ по п.12, где катализатор добавляют в бензол перед взаимодействием с бутиролактоном с получением смеси бензола и катализатора. 14. Способ по п.13, где смесь бензола и катализатора перемешивают в течение от 1 до около 15 мин перед взаимодействием с бутиролактоном. 15. Способ по п.14, где смесь бензола и катализатора перемешивают при температуре между около 50 и около 60°С перед добавлением бутиролактона. 16. Способ по п.13, где бутиролактон добавляют к смеси бензола и катализатора с получением реакционной смеси, содержащей бензол, катализатор и бутиролактон. 17. Способ по п.16, где реакционную смесь, содержащую бензол, катализатор и бутиролактон, перемешивают в течение от 30 до около 120 мин. 18. Способ по п.17, где температуру реакционной смеси, содержащей бензол, катализатор и бутиролактон, поддерживают между 50 и около 60°C. 19. Способ по п.1, дополнительно включающий следующие стадии: с1) фильтрование раствора со стадии b) для удаления твердых продуктов из водного раствора, с2) контактирование раствора со стадии с1) с органическим растворителем с получением органической фазы и водной фазы, с3) отделение водной фазы от органической фазы, с4) добавление кислоты в водную фазу для снижения значения рН водной фазы в количестве, достаточном для осаждения продукта из водной фазы, и с5) выделение продукта из водной фазы.
|
||||||||||||||||||||||||||

 -фенилмасляной кислоты (J. Am. Chem. Soc., 70, 3768 (1948)). Реактив Гриньяра, бензилмагнийхлорид также использовали в синтезе фенилмасляной кислоты с выходом 16,1% (J. Am. Chem. Soc., 71, 2807-2808 (1949)).
-фенилмасляной кислоты (J. Am. Chem. Soc., 70, 3768 (1948)). Реактив Гриньяра, бензилмагнийхлорид также использовали в синтезе фенилмасляной кислоты с выходом 16,1% (J. Am. Chem. Soc., 71, 2807-2808 (1949)).