Патент на изобретение №2296749
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ТРАНС-ПИНЕНИЛСУЛЬФИДОВ
(57) Реферат:
Изобретение относится к химии серосодержащих органических соединений, а именно к новому способу получения транс-пиненилсульфидов общей формулы
где R: -СН2СН3; -СН(СН3)2; -(СН2)7СН3; -СН2СООН; -СН2СООСН3. Способ заключается в том, что синтез транс-пиненилсульфидов ведут реакцией цис-вербенола с избытком соответствующего тиола в присутствии каталитических количеств хлористого цинка в среде хлористого метилена при 20-25°С. Реакция идет в одну стадию, выход продуктов составляет 65-76%. Транс-пиненилсульфиды содержат реакционно-способные фрагменты (сульфидную группу и двойную связь) и могут использоваться для синтеза новых соединений с потенциальной биологической активностью.
Изобретение относится к химии серосодержащих органических соединений, конкретно к способу получения транс-пиненилсульфидов общей формулы
где R: -CH2CH3; -CH(CH3)2; -(CH2)7CH3; -CH2COOH; -CH2COOCH3. Транс-пиненилсульфиды содержат реакционно-способные фрагменты (сульфидную группу и двойную связь) и могут использоваться для синтеза новых соединений с потенциальной биологической активностью. Известен способ получения 4 Изобретение касается транс-пиненилсульфидов как потенциальных биологически активных веществ с радикалами сульфидной группы: -СН2СН3; -СН(СН3)2; -(СН2)7СН3; -СН2СООН; -СН2СООСН3. Цель – создание способа получения новых веществ класса транс-пиненилсульфидов. Цель достигается взаимодействием цис-вербенола с соответствующими тиолами, взятыми в молярном соотношении 1:3, и проведением процесса в присутствии каталитических количеств хлористого цинка в среде хлористого метилена при 20-25°С. Недостатком вышеуказанных известных способов получения терпенсульфидов является осуществление процесса в течение длительного времени (12-50 часов) и при повышенной температуре (75-140°С). Синтез транс-пиненилсульфидов ведут реакцией цис-вербенола с избытком соответствующего тиола в присутствии каталитических количеств хлористого цинка в среде хлористого метилена при 20-25°С в течение 2-3 часов. Выход, %; брутто-формула:
Пример 1. Получение транс-(пинен-2(3)-ил-4)тиоэтан. К 6,5 ммоль цис-вербенола. при комнатной температуре и перемешивании добавили 22 ммоль тиола СН3СН2SH в 20 мл СН2Cl2 и 0,2 г ZnCl2. Через 2 часа к реакционной смеси прилили 200 мл воды, экстрагировали хлористым метиленом, сушили MgSO4. После удаления растворителя продукт очищали с помощью колоночной хроматографии на силикагеле (гексан). Получено 0,9 г продукта транс-(пинен-2(3)-ил-4)тиоэтана (выход 70,64%). Спектр ПМР (300 МГц, CDCl3, Масс-спектр, m/z (Iотн., %): 196 (M+, 5), 167 (22), 135 (15), 119 (40), 107 (18), 103 (28), 93 (100), 79 (13), 69 (67), 53 (18). Пример 2. Получение транс-(пинен-2(3)-ил-4)тио(2-метил)пропан. К 6,5 ммоль цис-вербенола при комнатной температуре и перемешивании добавили 22 ммоль тиола (СН3)2CHSH в 20 мл СН2Cl2 и 0,2 г ZnCl2. Через 3 часа к реакционной смеси прилили 200 мл воды, экстрагировали хлористым метиленом, сушили MgSO4. После удаления растворителя продукт очищали с помощью колоночной хроматографии на силикагеле (гексан). Получено 0,88 г продукта транс-(пинен-2(3)-ил-4)тио(2-метил)пропана (выход 65,00%). Спектр ПМР (300 МГц, CDCl3, Масс-спектр, m/z (Iотн., %): 210 (М+, 98), 195 (20), 167 (30), 134 (17), 93 (60). Пример 3. Получение транс-(пинен-2(3)-ил-4)тиооктан К 6,5 ммоль цис-вербенола при комнатной температуре и перемешивании добавили 22 ммоль тиола CH3-(CH2)7SH в 20 мл СН2Cl2 и 0,2 г ZnCl2. Через 3 часа к реакционной смеси прилили 200 мл воды, экстрагировали хлористым метиленом, сушили MgSO4. После удаления растворителя продукт очищали с помощью колоночной хроматографии на силикагеле (гексан). Получено 1,20 г продукта транс-(пинен-2(3)-ил-4)тиооктана (выход 65,90%). Спектр ПМР (300 МГц, CDCl3, Спектр ЯМР 13С (75.43 МГц, CDCl3): 150 (С-2), 116 (С-3), 49 (С-5), 48 (С-1), 46 (С-4), 33 (С-6), 32 (С-7), 30 (С-11-17), 27 (С-10), 23, 21 (С-8,9). Масс-спектр, m/z (Iотн., %): 280 (М+, 2), 200 (10), 187 (12), 167 (14), 135 (16), 119 (40), 105 (12), 93 (100), 77 (13), 69 (64), 55 (12). Пример 4. Получение транс-(пинен-2(3)-ил-4)тиоуксусная кислота К 6,5 ммоль цис-вербенола при комнатной температуре и перемешивании добавили 22 ммоль тиола HSCH2COOH в 20 мл СН2Cl2 и 0,2 г ZnCl2. Через 3 часа к реакционной смеси прилили 200 мл воды, экстрагировали хлористым метиленом, сушили MgSO4. После удаления растворителя продукт очищали с помощью колоночной хроматографии на силикагеле (гексан). Получено 1,0 г продукта транс-(пинен-2(3)-ил-4)тиоуксусная кислоты (выход 68,00%). Спектр ПМР (300 МГц, CDCl3, Спектр ЯМР 13С (75.43 МГц, CDCl3): 177 (С=0), 147 (С-2), 117 (С-3), 49 (SCH2), 48 (С-5), 47 (С-1), 46 (С-4), 33 (С-6), 29 (С-7), 27 (С-10), 23, 21 (С-8, 9). Масс-спектр, m/z (Iотн., %): 226 (М+, 13), 203 (26), 167 (28), 134 (72), 93 (89), 43 (90). Пример 5. Получение метилового эфира транс-(пинен-2(3)-ил-4)тиоуксусной кислоты К 6,5 ммоль цис-вербенола при комнатной температуре и перемешивании добавили 22 ммоль тиола CH3COOCH2SH в 20 мл СН2Cl2. Реакция не идет. Параллельно к 6,5 ммоль цис-вербенола при комнатной температуре и перемешивании добавили 22 ммоль тиола СН3СООСН2SH в 20 мл CH2Cl2 и 0,2 г ZnCl2. Через 3 часа к реакционной смеси прилили 200 мл воды, экстрагировали хлористым метиленом, сушили MgSO4. После удаления растворителя продукт очищали с помощью колоночной хроматографии на силикагеле (гексан). Получено 1,2 г продукта метилового эфира транс-(пинен-2(3)-ил-4) тиоуксусной кислоты (выход 76,00%). Спектр ПМР (300 МГц, CDCl3, Спектр ЯМР 13С (75.43 МГц, CDCl3): 170 (С=O), 150 (С-2), 118 (С-3), 53 (SCH2), 48 (С-5), 47,5 (С-1), 46 (С-4), 33 (С-6), 29 (С-7), 27 (С-10), 23,21 (С-8,9). Масс-спектр, m/z (Iотн., %): 240 (M+, 1), 167 (20), 147 (22), 134 (50), 119 (70), 105 (25), 93 (100), 77 (55), 69 (68), 43 (98), 27 (31). При использовании предлагаемого способа обеспечивается получение транс-пиненилсульфидов с удовлетворительными выходами (65-76%), образование в каждом случае только одного изомера, простота технологии способа: способ осуществляется в одну стадию, достигается надежная воспроизводимость результатов. Кроме того, целевые соединения легко выделяются в аналитически чистом виде, доступными являются исходные соединения: цис-вербенол – вещество, получаемое из вербенона, производимого из Источники информации 1. A.C. 1498760, СССР. Способ получения 4 Формула изобретения
Способ получения транс-пиненилсульфидов общей формулы
где R – -СН2СН3; -СН(СН3)2; -(СН2)7СН3; -СН2СООН; -СН2СООСН3, отличающийся тем, что синтез ведут реакцией цис-вербенола с избытком соответствующего тиола в присутствии каталитических количеств хлористого цинка в среде хлористого метилена при 20-25°С.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 19.08.2007
Извещение опубликовано: 10.03.2009 БИ: 07/2009
|
||||||||||||||||||||||||||

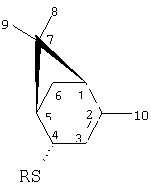
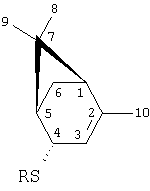
 -алкилтиокаран-3
-алкилтиокаран-3 -олов (A.C. 1498760, СССР. Способ получения 4
-олов (A.C. 1498760, СССР. Способ получения 4 , м.д., J/Гц): 0,88 с, 1.31 с (6Н, Н-8,9), 1.20 м (1Н, Н
, м.д., J/Гц): 0,88 с, 1.31 с (6Н, Н-8,9), 1.20 м (1Н, Н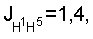
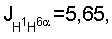
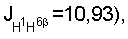 2.28 м (1Н, Н-5), 2.35 дд, 2,38 дд (1Н, Н
2.28 м (1Н, Н-5), 2.35 дд, 2,38 дд (1Н, Н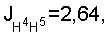
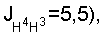 5.22 м (1H, H-3, J=1.5).
5.22 м (1H, H-3, J=1.5).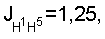
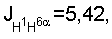
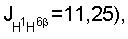 2.16 м (1H, Н-5), 2.24 дд, 2,27 дд (1Н, Н
2.16 м (1H, Н-5), 2.24 дд, 2,27 дд (1Н, Н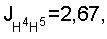
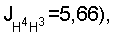 5.21 м (1H, Н-3, J-1.5).
5.21 м (1H, Н-3, J-1.5).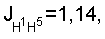
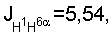
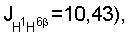 2,13 м (1H, H-5), 2.18 д, 2.21 д (1Н, Н
2,13 м (1H, H-5), 2.18 д, 2.21 д (1Н, Н