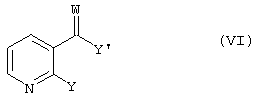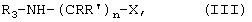Патент на изобретение №2296124
|
||||||||||||||||||||||||||
(54) ПРОИЗВОДНЫЕ 2-АМИНОНИКОТИНАМИДА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ VEGF-РЕЦЕПТОРА ТИРОЗИНКИНАЗЫ
(57) Реферат:
Изобретение относится к производным 2-аминоникотинамида формулы (I), к способу их получения, к фармацевтической композиции на их основе, ингибирующей активность эндотелиального фактора роста сосудов (VEGF) рецепторной тирозинкиназы, и к соответствующему способу ингибирования активности VEGF-рецепторной тирозинкиназы. Предполагается, что данная активность позволит оказывать лечебное воздействие при пролиферативных заболеваниях, связанных с ангиогенезом: к лечению опухолей, ретинопатии или возрастной дегенерации желтого пятна.
4 н. и 5 з.п. ф-лы.
Изобретение относится к применению производных 2-аминоникотинамида, отдельно или в сочетании с одним или более других фармацевтически активных соединений, для получения фармацевтической композиции для использования в терапии заболевания, чувствительного к ингибированию активности VEGF-рецепторной тирозинкиназы, прежде всего опухолевого заболевания, ретинопатии или возрастной дегенерации желтого пятна; к способу лечения такого заболевания у млекопитающих, прежде всего человека; к новым производным 2-аминоникотинамида и способам их получения. Известен ряд заболеваний, связанных с нарушением ангиогенеза, например заболевания, вызванные неоваскуляризацией глаз, такие как ретинопатии (включая диабетическую ретинопатию), возрастная дегенерация желтого пятна, псориаз, гемангиобластома, гемангиома, эндометриоз и, прежде всего, опухолевые заболевания, например так называемые солидные опухоли и жидкие опухоли (такие, как лейкоз). Согласно последним данным центральное место в системе регуляции роста и дифференциации сосудистой системы и ее компонентов во время эмбрионального развития и нормального роста при разнообразных патологических аномалиях и заболеваниях занимает ангиогенный фактор, известный, как «эндотелиальный фактор роста сосудов» (VGEF, первоначально называвшийся «фактор проницаемости сосудов», VPF), вместе с его клеточными рецепторами (см. обзор Breier G. и др.. Trends in Cell Biology, 6, 454-456 (1996), и другие документы, цитированные в описании заявки). VEGF является димерным, связанным дисульфидными связями гликопротеином с ММ 46 кДа, продуцируемым линиями нормальных и опухолевых клеток. Он является специфичным митогеном эндотелиальных клеток, обладает ангиогенной активностью в системах тестирования in vivo (например, на роговице кролика), обладает хемотаксическими свойствами в отношении эндотелиальных клеток и моноцитов и индуцирует образование эндотелиальными клетками активаторов плазминогена, которые затем принимают участие в протеолитической деградации межклеточного матрикса при образовании капилляров. Известен ряд изоформ VEGF, которые обладают аналогичной биологической активностью, но отличаются по типу секретирующих их клеток и гепарин-связывающей активностью. Кроме того, известны другие члены семейства VEGF, такие как “плацентарный фактор роста” (PLGF) и VEGF-С. Рецепторы VEGF являются трансмембранными рецепторными тирозинкиназами. Они характеризуются наличием внеклеточного домена, содержащего семь иммуноглобулин подобных доменов, и внутриклеточного домена, обладающего тирозинкиназной активностью. Известны различные типы рецептора VEGF, например VEGFR-1, VEGFR-2 и VEGFR-3. Для многих видов опухолей человека, прежде всего глиом и карцином, характерен высокий уровень экспрессии VEGF и его рецепторов. Это привело к предположению, что VEGF, высвобождаемый опухолевыми клетками, может стимулировать рост кровеносных капилляров и пролиферацию опухолевого эндотелия по механизму паракринной регуляции и, таким образом, за счет улучшенного притока крови, ускорять рост опухоли. Усиление экспрессии VEGF может объяснить появление отека мозга у пациентов с глиомой. Прямое доказательство роли VEGF как фактора опухолевого ангиогенеза in vivo получено в работах по ингибированию экспрессии или активности VEGF. Это достигается благодаря использованию антител, ингибирующих активность VEGF, мутантов, доминантно-негативных по VEGFR-2, которые ингибируют передачу сигнала, или антисмысловых VEGF-PHK. Все подходы приводят к уменьшению роста клеточных линий глиомы или других линий опухолевых клеток в экспериментах in vivo в результате подавления опухолевого ангиогенеза. Ангиогенез считается безусловной предпосылкой таких опухолей, которые в росте превышают максимальный диаметр, равный приблизительно 1-2 мм, поскольку до этого предельного размера кислород и питательные вещества могут поступать в опухолевые клетки за счет диффузии. Таким образом, каждая опухоль, независимо от ее происхождения и причины, после достижения определенных размеров зависит от ангиогенеза, необходимого для ее дальнейшего роста. При воздействии ингибиторов ангиогенеза на опухоли большое значение имеют три основных механизма: 1) ингибирование роста сосудов, прежде всего капилляров, в направлении бессосудистых покоящихся опухолей, что предотвращает общий рост опухоли благодаря равновесию между апоптозом и пролиферацией, 2) предотвращение миграции опухолевых клеток благодаря отсутствию кровотока в направлении опухоли и обратно, и 3) ингибирование пролиферации эндотелиальных клеток и, таким образом, исключение паракринного ростстимулирующего действия на окружающую ткань эндотелиальных клеток, обычно прилегающих к сосудам. Неожиданно было установлено, что производные никотинамида формулы I, описанной ниже, являются новым классом соединений, которые обладают полезными фармакологическими свойствами и ингибируют, например, активность VEGF-рецепторной тирозинкиназы, рост опухолей и VEGF-зависимую клеточную пролиферацию, а также прочие выше- и нижеописанные заболевания. Соединения формулы I обеспечивают неожиданный новый терапевтический подход, например, прежде всего, к лечению заболеваний, при терапии которых, а также при профилактике которых, ингибирование ангиогенеза и/или VEGF-рецепторной тирозинкиназы оказывает лечебное действие. Изобретение относится к применению соединения формулы I
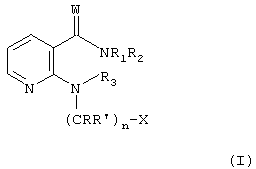
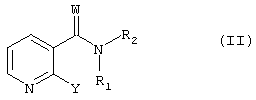
где n равно от 1 до 6 включительно; W означает О или S; R1 и R3 независимо друг от друга каждый означает водород, (низш.)алкил или (низш.)ацил; R2 означает группу циклоалкил, группу арил или моно- или бициклическую группу гетероарил, содержащую один или более атомов азота в цикле и 0, 1 или 2 гетероатома, независимо друг от друга выбранные из группы, включающей кислород и серу, причем группы в каждом случае являются незамещенными или моно- или полизамещенными; R и R’ независимо друг от друга каждый означает водород или (низш.)алкил; Х означает группу арил или моно- или бициклическую группу гетероарил, содержащую один или более атомов азота в цикле и 0, 1 или 2 гетероатома, независимо друг от друга выбранные из группы, включающей кислород и серу, причем группы в каждом случае являются незамещенными или моно- или полизамещенными; и его N-оксида или возможного таутомера, или фармацевтически приемлемой соли такого соединения для получения фармацевтической композиции для применения в терапии заболевания, которое является чувствительным к ингибированию активности VEGF-рецепторной тирозинкиназы. Если не указано иное, общие термины, используемые выше и ниже по тексту, предпочтительно имеют следующие значения. Приставка «низш.» означает радикал, содержащий от 1 до максимум 7 включительно, прежде всего до максимум 4 включительно, атомов углерода, причем упомянутые радикалы являются линейными или разветвленными с одним или несколькими разветвлениями. Если для обозначения соединений, солей и т.п. используется множественное число, следует полагать, что оно также означает одно соединение, соль и т.п. Любые асимметричные атомы углерода (например, в соединении формулы I, где R или R’ означает (низш.)алкил) могут быть представлены в (R)-, (S)- или (R,S)-конфигурации, предпочтительно в (R)- или (S)-конфигурации. Таким образом, соединения могут быть представлены в виде смесей изомеров или в виде чистых изомеров, предпочтительно в виде диастереомеров, не содержащих энантиомеров. Кроме того, изобретение относится к возможным таутомерам соединений формулы I. Х предпочтительно означает пиридил или фенил, наиболее предпочтительно 3- или 4-пиридил. В предпочтительном варианте осуществления изобретения Х является замещенным группой (низш.)алкокси. В другом преимущественно предпочтительном варианте изобретения Х означает подструктуру X’
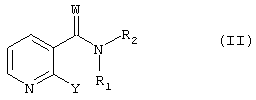
где Rx означает водород или (низш.)алкил. R2 предпочтительно означает фенил, моно- или дизамещенный группой ряда (низш.)алкил, (низш.)алкинил, галоген, предпочтительно фтор и трифторметил; или циклоалкил, предпочтительно циклогексил, замещенный (низш.)алкилом, предпочтительно трет-бутилом. R3 предпочтительно означает водород. W предпочтительно означает О. Целое число n предпочтительно означает 1 или 2, более предпочтительно 1. (Низш.)алкил предпочтительно означает алкил, содержащий от включительно 1 до включительно 7, предпочтительно от включительно 1 до включительно 5, атомов углерода и который является линейным или разветвленным; предпочтительно (низш.)алкил означает пентил, такой как н-пентил, бутил, такой как н-бутил, втор-бутил, изобутил, трет-бутил, пропил, такой как н-пропил или изопропил, этил или метил. Предпочтительно (низш.)алкил означает метил, пропил или трет-бутил. (Низш.)ацил предпочтительно означает формил или ацетил. “Арил” означает ароматический радикал, связанный с молекулой химической связью через углеродный атом ароматического кольца. В предпочтительном варианте осуществления изобретения арил означает ароматический радикал, содержащий от 6 до 14 атомов углерода, прежде всего фенил, нафтил, тетрагидронафтил, флуоренил или фенантренил, причем указанный радикал является незамещенным или замещенным одним или более, предпочтительно вплоть до трех, прежде всего одним или двумя заместителями, прежде всего, выбранными из ряда амино, моно- или дизамещенный амино, галоген, (низш.)алкил, замещенный алкил, (низш.)алкенил, (низш.)алкинил, (низш.)алканоил, гидрокси, простой или сложный эфир гидроксигруппы, нитро, циано, карбокси, этерифицированный карбокси, алканоил, бензоил, карбамоил, N-моно- или N,N-дизамещенный карбамоил, амидино, гуанидино, уреидо, меркапто, сульфо, (низш.)алкилтио, фенил, фенокси, фенилтио, фенил(низш.)алкилтио, алкилфенилтио, (низш.)алкилсульфинил, фенилсульфинил, фенил(низш.)алкилсульфинил, алкилфенилсульфинил, (низш.)алкансульфонил, фенилсульфонил, фенил(низш.)алкилсульфонил, алкилфенилсульфонил, галоген(низш.)алкилмеркапто, галоген(низш.)алкилсульфонил, такой как, прежде всего, трифторметансульфонил, дигидроксибора(-В(ОН)2), гетероциклил и (низш.)алкилендиокси, связанный с соседними атомами углерода в цикле, такой как метилендиокси. Более предпочтительно арил означает фенил или нафтил, который в каждом случае является незамещенным или независимо замещенным одним или двумя заместителями, выбранными из группы, включающей галоген, прежде всего фтор, хлор или бром; гидрокси; гидрокси, этерифицированный (низш.)алкилом, например метилом, или галоген(низш.)алкилом, например трифторметилом; (низш.)алкил, например метил или пропил; (низш.)алкенил, такой как 1-пропинил; этерифицированная карбоксигруппа, прежде всего (низш.)алкоксикарбонил, например метоксикарбонил, н-пропоксикарбонил или изопропоксикарбонил; N-монозамещенный карбамоил, например карбамоил, монозамещенный (низш.)алкилом, например метилом, н-пропилом или изопропилом; замещенный алкил, прежде всего (низш.)алкил, например метил или этил, замещенный (низш.)алкоксикарбонилом, например метоксикарбонилом или этоксикарбонилом; и галоген(низш.)алкил, наиболее предпочтительно трифторметил. В качестве арила в форме фенила, который является замещенным группой (низш.)алкилендиокси, связанной с двумя соседними атомами углерода, такой как метилендиокси, предпочтителен 3,4-метилендиоксифенил. Группа циклоалкил предпочтительно означает циклопентил, циклогексил или циклогептил, причем группа циклоалкил может быть незамещенной или замещенной одним или более, прежде всего, одним или двумя заместителями, выбранными из группы, указанной выше, как заместители арила, наиболее предпочтительно (низш.)алкилом, таким как метил, (низш.)алкокси, таким как метокси или этокси, или группой гидрокси. Замещенный алкил означает алкил, имеющий значения, указанные в предыдущем абзаце, прежде всего (низш.)алкил, предпочтительно метил; и который может содержать один или более, прежде всего вплоть до 3, заместителей, главным образом, из группы, выбранной из ряда галоген, прежде всего фтор, амино, N-(низш.)алкиламино, N,N-ди(низш.)алкиламино, N-(низш.)алканоиламино, гидрокси, циано, карбокси, (низш.)алкоксикарбонил и фенил(низш.)алкоксикарбонил. Прежде всего, предпочтителен трифторметил. Моно- или дизамещенный амино означает, прежде всего, аминогруппу, замещенную одним или двумя радикалами, независимо друг от друга выбранными из ряда (низш.)алкил, такой как метил; гидрокси(низш.)алкил, такой как 2-гидроксиэтил; фенил(низш.)алкил; (низш.)алканоил, такой как ацетил; бензоил; замещенный бензоил, в котором радикал фенил, прежде всего, является замещенным одним или более, предпочтительно одним или двумя заместителями, выбранными из ряда нитро, амино, галоген, N-(низш.)алкиламино, N,N-ди(низш.)алкиламино, гидрокси, циано, карбокси, (низш.)алкоксикарбонил, (низш.)алканоил и карбамоил; и фенил(низш.)алкоксикарбонил, в котором фенильный радикал является незамещенным или, прежде всего, замещенным одним или более, предпочтительно одним или двумя заместителями, выбранными из ряда нитро, амино, галоген, N-(низш.)алкиламино N,N-ди(низш.)алкиламино, гидрокси, циано, карбокси, (низш.)алкоксикарбонил, (низш.)алканоил и карбамоил; и предпочтительно означает N-(низш.)алкиламино, такой как N-метиламино, гидрокси(низш.)алкиламино, такой как 2-гидроксиэтиламино, фенил(низш.)алкиламино, такой как бензиламино, N,N-ди(низш.)алкиламино, N-фенил(низш.)алкил-N-(низш.)алкиламино, N,N-ди(низш.)алкилфениламино, (низш.)алканоиламино, такой как ацетиламино, или заместитель, выбранный из группы, включающей бензоиламино и фенил(низш.)алкоксикарбониламино, в котором фенильный радикал в каждом случае является незамещенным или, прежде всего, замещенным, группой нитро или амино, или, кроме того, группой галоген, амино, N-(низш.)алкиламино, N,N-ди(низш.)алкиламино, гидрокси, циано, карбокси, (низш.)алкоксикарбонил, (низш.)алканоил, карбамоил или аминокарбониламино. Галоген означает, прежде всего, фтор, хлор, бром или иод, прежде всего фтор, хлор или бром. Этерифицированный гидрокси (сложноэфирная группа) означает, прежде всего, С8-С20 алкилокси, такой, как н-децилокси, (низш.)алкокси (предпочтительно), такой как метокси, этокси, изопропилокси или н-пентилокси, фенил(низш.)алкокси, такой как бензилокси, или, кроме того, фенилокси, или в другом варианте, или в дополнение к указанной выше группе С8-С20 алкилокси, такой как н-децилокси, галоген(низш.)алкокси, такой как трифторметилокси или 1,1,2,2-тетрафторэтокси. Этерифицированный гидрокси (группа простого эфира) означает, прежде всего, (низш.)алканоилокси, бензоилокси, (низш.)алкоксикарбонилокси, такой как трет-бутоксикарбонилокси, или фенил(низш)алкоксикарбонилокси, такой как бензилоксикарбонилокси. Этерифицированный карбокси означает, прежде всего, (низш.)алкоксикарбонил, такой как трет-бутоксикарбонил, изопропоксикарбонил, метоксикарбонил или этоксикарбонил, фенил(низш.)алкоксикарбонил или фенилоксикарбонил. Алканоил главным образом означает алкилкарбонил, прежде всего (низш.)алканоил, например ацетил. N-моно- или N,N-дизамещенный карбамоил означает, прежде всего, концевой атом азота, замещенный одним или двумя заместителями, независимо выбранными из ряда (низш.)алкил, фенил(низш.)алкил и гидрокси(низш.)алкил. Алкилфенилтио означает, прежде всего, (низш.)алкилфенилтио. Алкилфенилсульфонил означает, прежде всего, (низш.)алкилфенилсульфонил. Алкилфенилсульфинил означает, прежде всего, (низш.)алкилфенилсульфинил. Моно- или бициклическая гетероарильная группа, содержащая один или более атомов азота в цикле и 0, 1 или 2 гетероатома, независимо друг от друга выбранные из группы, включающей кислород и серу, причем группы в каждом случае являются незамещенными или моно- или полизамещенными, означает гетероциклический остаток, который является ненасыщенным в цикле, связывающем гетероарильный радикал с остатком молекулы формулы I, и предпочтительно означает цикл, где по меньшей мере в связывающем цикле, и кроме того, необязательно в любом конденсированном цикле, один или более, предпочтительно от 1 до 4, наиболее предпочтительно 1 или 2, атома углерода, каждый заменен гетероатомом, выбранным из группы, включающей азот, кислород и серу; где связывающий цикл предпочтительно содержит от 5 до 12, более предпочтительно от 5 до 7, атомов в цикле; и может быть незамещенной или замещенной одним или более, предпочтительно одним или двумя заместителями, выбранными из группы, указанной выше в качестве заместителей у группы арил, наиболее предпочтительно (низш.)алкилом, таким как метил, (низш.)алкокси, таким как метокси или этокси, или гидрокси; предпочтительно моно- или бициклическую гетероарильную группу выбирают из ряда 2Н-пирролил, пирролил, имидазолил, бензимидазолил, пиразолил, индазолил, пуринил, пиридил, пиразинил, пиримидинил, пиридазинил, 4Н-хинолизинил, изохинолил, хинолил, фталазинил, нафтиридинил, хиноксалил, хиназолинил, хинолинил, птеридинил, индолизинил, 2Н-индолил, индолил, изоиндолил, оксазолил, изоксазолил, тиазолил, изотиазолил, триазолил, тетразолил, фуразанил и бенз[d]пиразол. Более предпочтительно моно- или бициклическую гетероарильную группу выбирают из группы, включающей пирролил, бензимидазолил, такой как 1-бензимидазолил, индазолил, прежде всего 5-индазолил, пиридил, прежде всего 2-, 3- или 4-пиридил, изохинолинил, прежде всего 3-изохинолинил, хинолинил, прежде всего 4-хинолинил, индолил, прежде всего 3-индолил, тиазолил или бенз[d] пиразол. В одном предпочтительном варианте осуществления изобретения радикал пиридил является замещенным группой гидрокси в орто положении к атому азота и, следовательно, существует по меньшей мере частично в форме соответствующего таутомера, который означает пиридин-(1Н)-2-он. Гетероциклил предпочтительно означает пяти- или шестичленную гетероциклическую систему с 1 или 2 гетроатомами, выбранными из группы, включающей азот, кислород и серу, причем система может быть ненасыщенной или полностью или частично насыщенной и является незамещенной или замещенной, прежде всего, (низш.)алкилом, таким как метил; предпочтителен радикал, выбранный из ряда 2-метилпиримидин-4-ил, оксазол-5-ил, 2-метил-1,3-диоксолан-2-ил, 1H-пиразол-3-ил и 1-метилпиразол-3-ил. Соли, прежде всего, означают фармацевтически приемлемые соли соединений формулы I. Такие соли образуются, например, в виде кислотно-аддитивных солей, предпочтительно, при взаимодействии соединений формулы I, имеющих основной атом азота, с органическими или неорганическими кислотами, прежде всего, в виде фармацевтически приемлемых солей. Соответствующими неорганическими кислотами являются, например, галогенсодержащие кислоты, такие как, хлористоводородная кислота, серная кислота или фосфорная кислота. Приемлемые органические кислоты включают, например, карбоновые, фосфоновые, сульфоновые или сульфаминовые кислоты, например уксусную кислоту, пропионовую кислоту, октановую кислоту, декановую кислоту, додекановую кислоту, гликолевую кислоту, молочную кислоту, фумаровую кислоту, янтарную кислоту, адипиновую кислоту, пимелиновую кислоту, пробковую кислоту, азелаиновую кислоту, яблочную кислоту, винную кислоту, лимонную кислоту, аминокислоты, такие как глутаминовую кислоту или аспарагиновую кислоту, малеиновую кислоту, гидроксималеиновую кислоту, метилмалеиновую кислоту, циклогексанкарбоновую кислоту, адамантанкарбоновую кислоту, бензойную кислоту, салициловую кислоту, 4-аминосалициловую кислоту, фталевую кислоту, фенилуксусную кислоту, миндальную кислоту, коричную кислоту, метан- или этансульфоновую кислоту, 2-гидроксиэтансульфоновую кислоту, этан-1,2-дисульфоновую кислоту, бензолсульфоновую кислоту, 2-нафталинсульфоновую кислоту, 1,5-нафталиндисульфоновую кислоту, 2-, 3- или 4-метилбензолсульфоновую кислоту, метилсерную кислоту, этилсерную кислоту, додецилсерную кислоту, N-циклогексилсульфаминовую кислоту, N-метил-, N-этил или N-пропилсульфаминовую кислоту, или другие органически протонные кислоты, такие как аскорбиновую кислоту. При наличии в молекуле отрицательно заряженных групп, таких как карбокси или сульфо, соединения могут образовывать соли с основаниями, например соли металлов или аммониевые соли, такие как соли щелочных или щелочноземельных металлов, например соли натрия, калия, магния или кальция, или аммониевые соли с аммиаком или соответствующими органическими аминами, такими как четвертичные моноамины, например триэтиламином или три(2-гидроксиэтил)амином, или гетероциклическими основаниями, например N-этилпиперидином или N,N’-диметилпиперазином. Если в молекуле присутствуют основная и кислотная группа, то соединение формулы I может также образовывать внутренние соли. С целью выделения или очистки возможно также использование фармацевтически неприемлемых солей, например пикратов или перхлоратов. Для терапевтического применения используются только фармацевтически приемлемые соли или свободные соединения (которые применимы в форме лекарственных препаратов), и, следовательно, эти соли и соединения являются предпочтительными. Ввиду близкого сходства между новыми соединениями в свободной форме и в форме их солей, включая те соли, которые могут быть использованы в качестве промежуточных соединений, например, при очистке или идентификации новых соединений, любые ссылки на свободные соединения выше и далее по тексту следует воспринимать как относящиеся также к соответствующим солям, как соответствующие и целесообразные. Соединения формулы I и их N-оксиды обладают ценными фармакологическими свойствами, как описано выше и далее по тексту. Эффективность соединений по изобретению в качестве ингибиторов активности VEGF-рецепторной тирозинкиназы может быть продемонстрирована следующим образом. Определение ингибирующей активности соединений в отношении VEGF-рецепторной тирозинкиназы. Анализ проводят с использованием VEGF-рецепторной тирозинкиназы Flt-1. Ниже дается подробное описание методики. 30 мкл раствора киназы (10 нг домена киназы Flt-1, см. статью Shibuya и др., Oncogen, 5, 519-524 (1990)) в буферном растворе, содержащем 20 мМ трис Противоопухолевое действие соединений по изобретению может быть продемонстрировано in vivo по следующей методике. Активность in vivo на модели голых ксенотрансплантантных мышей. Самок голых мышей линии BALB/c (8-12 недель, фирма Novartis Animal Farm, Sisseln, Швейцария) содержат в стерильных условиях при обеспечении водой и кормом по потребности. Опухоли индуцируют либо подкожной инъекцией мышам опухолевых клеток (например, клеточной линии DU 145 карциномы простаты (АТСС № НТВ 81; см. Cancer Res., 37, 4049-4058 (1978)) или имплантацией фрагментов опухоли (приблизительно 25 мг) подкожно в левый бок мыши с использованием игл троакаров №13 при анестезии препаратом Forene (фирма Abbott, Швейцария). Анализируемое соединение начинают вводить в тот момент, когда опухоль достигает в среднем объема 100 мм3. Рост опухоли измеряют два или три раза в неделю и через 24 ч после последней обработки, определяя размер вдоль двух перпендикулярных осей. Объемы опухолей рассчитывают, как описано в литературе (см. статью Evans и др., Brit. J. Cancer, 45, 466-468 (1982)). Эффективность противоопухолевого действия определяют как частное от деления среднего увеличения объема опухоли у животных, получавших анализируемое соединение, на среднее увеличение объема опухоли в контрольной группе животных (не получавших анализируемое соединение) и после умножения на 100 представляют как Т/С%. Регрессию опухоли (в %) представляют как частное от деления минимального среднего объема опухоли на средний объем опухоли в начале обработки препаратом. Анализируемое соединение вводят ежедневно желудочным зондом. В другом варианте аналогичным образом могут быть также использованы другие клеточные линии, например: клеточная линия MCF-7 аденокарциномы молочной железы (АТСС №НТВ 22; см. также J. Natl. Cancer Inst. (Bethesda), 51, 1409-1416 (1973)); клеточная линия MDA-МВ 468 аденокарциномы молочной железы MCF-7 (АТСС №НТВ 132; см. также In Vitro, 14, 911-915 (1978)); клеточная линия MDA-МВ 231 аденокарциномы молочной железы (АТСС №НТВ 26; см. также J. Natl. Cancer Inst. (Bethesda), 53, 661-674 (1974)); клеточная линия Colo 205 карциномы толстой кишки (АТСС № CCL 222; см. также Cancer Res., 38, 1345-1355 (1978)); клеточная линия НСТ 116 карциномы толстой кишки (АТСС № CCL 247; см. также Cancer Res., 41, 1751-1756 (1981)); клеточная линия DU 145 карциномы простаты (АТСС № НТВ 81; см. также Cancer Res., 37, 4049-4058 (1978)); и клеточная линия PC-3 карциномы простаты (АТСС № CRL 1435; см. также Cancer Res., 40, 524-534 (1980)). Ингибирование аутофосфорилирования KDR-рецептора, индуцированное VEGF, может быть подтверждено еще одним экспериментом на клетках in vitro. Трансфектные клетки СНО, постоянно экспрессирующие рецептор VEGF человека (KDR), в полной культуральной среде (содержащей 10% ФБС) вносят в 6-луночные планшеты и инкубируют при 37°С в присутствии 5% CO2 до достижения 80% конфлюентности. Затем анализируемые соединения растворяют в культуральной среде (не содержащей ФБС, но содержащей 0,1% бычьего сывороточного альбумина, БСА) и добавляют к клеткам. Контроль включает среду, не содержащую анализируемых соединений. Затем инкубируют при 37°С в течение 2 ч и добавляют рекомбинантный VEGF, причем конечная концентрация VEGF составляет 20 нг/мл. Инкубируют при 37°С в течение еще пяти мин, после чего клетки дважды промывают охлажденным на ледяной бане фосфатно-солевым буфером (ФСБ) и сразу лизируют, добавляя в лунки по 100 мкл лизирующего буферного раствора. Затем лизаты центрифугируют, удаляя клеточные ядра, и определяют концентрацию белка в супернатантах с использованием набора реактивов для определения белка фирмы BioRad. Лизаты могут быть использованы непосредственно после приготовления или при необходимости их можно хранить при -20°С. Измерение фосфорилирования KDR-рецептора проводят с использованием иммуноферментного анализа (ИФА) по следующей методике. Моноклональные антитела к KDR (например, Mab 14985.12.14, полученные H.Towbin) иммобилизуют на черных планшетах для проведения ИФА (OptiPlate Соединение формулы I или его N-оксид в различной степени также ингибируют другие тирозинкиназы, принимающие участие в передаче сигнала, которые опосредованы трофическими факторами, например, Abl киназы, киназы из семейства Src, прежде всего c-Src киназы, Lck и Fyn; кроме того, киназы семейства EGF, например с-еrbВ2 киназы (HER-2), с-еrbВ3 киназы, с-еrbВ4 киназы; рецепторную киназу инсулин-подобного ростового фактора (IGF-1 киназа), прежде всего членов семейства PDGF-рецепторной тирозинкиназы, таких как PDGF-рецепторная киназа, CSF-1-рецепторную киназа, Kit-рецепторная киназа и VEGF- рецепторная киназа; а также серин/треонин киназы, каждая из которых принимает участие в регуляции роста и трансформации клеток млекопитающих, включая клетки человека. Ингибирование с-еrbВ2 тирозинкиназы (HER-2) может быть определено, например, аналогично тому, как измеряют ингибирование EGF-R протеинкиназы (см. статью House и др., Europ. J. Biochem., 140, 363-367 (1984)). еrbВ2 Киназа может быть выделена, а ее активность может быть определена с использованием известных методов (см. статью Т.Akiyama и др. Science, 232, 1644 (1986)). По результатам этих испытаний соединение формулы I по настоящему изобретению оказывает лечебное действие, прежде всего, при нарушениях, зависимых от протеинкиназы, прежде всего, при пролиферативных заболеваниях. Аналгетическая активность соединений формулы I может быть показана на следующей модели восприятия боли. В этой модели, гипералгезию, вызванную интрапланарной инъекцией дрожжей, измеряют при воздействии механического давления на конечность до тех пор, пока животное не подаст голос или не извлечет лапу из прижимной колодки. Эта модель чувствительна к ингибиторам СОХ, причем в качестве положительного контроля используют диклофенак в дозе 3 мг/кг. Методика проведения испытаний приведена ниже. За два ч до инъекции определяют рабочее давление, необходимое для того, чтобы заставить самцов крыс Sprague Dawley (весом приблизительно 180 г, поставляемых фирмой Iffa Credo, Франция) подать голос или извлечь лапу, затем проводят интрапланарную инъекцию 100 мкл 20%-ной суспензии дрожжей в воде в заднюю лапу. Через 2 ч (время отсчета 0 ч) крысам дают анализируемое соединение перорально (в дозе 3, 10 или 30 мг/кг), диклофенак (3 мг/кг) или носитель (физиологический раствор) и испытание давлением повторяют через 1 и 2 ч после дозировки. При этом определяют давление, необходимое для подачи голоса или извлечения лапы с использованием стандартного прибора фирмы Ugo Basile (Италия), и сравнивают с результатами, полученными на животных, получавших носитель. По результатам этих испытаний соединение формулы I неожиданно оказалось пригодными для снижения боли. Соединения формулы I или их N-оксиды по изобретению также оказывают лечебное действие, прежде всего, при нарушениях, зависимых от протеинкиназы, прежде всего, при пролиферативных заболеваниях. Благодаря ингибирующей активности в отношении VEGF-рецепторной тирозинкиназы соединения формулы I, прежде всего, ингибируют рост кровеносных сосудов и, таким образом, например, эффективны против ряда заболеваний, связанных с нарушением ангиогенеза, прежде всего, заболеваний, вызванных неоваскуляризацией глаз, прежде всего ретинопатий, таких как диабетическая ретинопатия или возрастная дегенерация желтого пятна, псориаз, гемангиобластома, такая как гемангиома, пролиферативные нарушения мезангиальных клеток, такие как хронические и острые заболевания почек, например диабетическая нефропатия, злокачественный нефросклероз, синдромы тромботической микроангиопатии или отторжение трансплантата, или, прежде всего, воспалительного заболевания почек, такого как гломерулонефрит, прежде всего мезангиопролиферативный гломерулонефрит, гемолитико-уремический синдром, диабетическая нефропатия, гипертенсивный нефросклероз, атерома (атеросклеротическая бляшка), артериальный рестеноз, аутоиммунные заболевания, диабеты, эндометриозы, хроническая астма, и, прежде всего, опухолевые заболевания (солидные опухоли, а также лейкозы и другие, так называемые «жидкие опухоли», прежде всего, связанные с экспрессией c-kit, KDR, flt-1 или Flt-3), такие как, прежде всего, рак молочной железы, рак толстой кишки, рак легких (прежде всего, мелкоклеточный рак легких), рак простаты или саркома Капоши. Соединение формулы I (или его N-окид) ингибирует рост опухолей и, прежде всего, пригодно для профилактики метастазирования опухолей и роста микрометастаз. Соединение формулы I можно вводить отдельно или в сочетании с одним или более других терапевтических агентов, возможна сочетанная терапия, т.е. введение фиксированных комбинаций, или введение соединения по изобретению и одного или более других терапевтических агентов попеременно или независимо друг от друга, или одновременное введение фиксированных комбинаций и одного или более других терапевтических агентов. Соединение формулы I можно вводить отдельно или дополнительно, прежде всего, при терапии опухолей в сочетании с химиотерапией, радиотерапией, иммунотерапией, хирургическим вмешательством или при сочетании указанных подходов. Долговременная терапия в равной степени возможна в виде адьювантной терапии в сочетании с другими вышеописанными стратегиями лечения. Другими возможными видами лечения являются поддержание статуса пациента после регрессии опухоли или даже химиопрофилактической терапии, например, в случае пациентов с повышенным риском. Терапевтические агенты для возможной комбинации представляют собой, прежде всего, одно или более соединений, обладающих цитостатическим или токсическим действием, например, это может быть химиотерапевтический агент или несколько агентов, выбранных из группы, включающей ингибитор биосинтеза полиамина, ингибитор протеинкиназы, прежде всего серин/треонин протеинкиназы, такой как протеинкиназа С, или тирозинпротеинкиназы, такой как рецепторная протеинкиназа эпидермального фактора роста, цитокин, отрицательный регулятор роста, такой как TGF- Соединение по изобретению предназначено не только для оказания помощи человеку (профилактики или лечения), но и для лечения других теплокровных животных, например коммерческих животных, например грызунов, таких как мыши, кролики или крысы, или морские свинки. Такое соединение может быть также использовано в качестве стандартного образца в вышеописанных аналитических системах для сравнения с другими соединениями. В общем случае изобретение относится также к применению соединения формулы I или его N-оксида для ингибирования активности VEGF-рецепторной тирозинкиназы, in vitro или in vivo. Соединение формулы I или его N-оксид могут быть также использованы для диагностических целей, например для изучения опухолей, которые были получены от «хозяина» в виде теплокровного животного, прежде всего человека, и были имплантированы в организм мыши для анализа на увеличение роста после введения такого соединения с целью изучения чувствительности опухоли к упомянутому соединению и, таким образом, для поиска и разработки возможных методов лечения опухолевых заболеваний в организме хозяина. Что касается групп предпочтительных соединений формулы I и их N-оксидов, упомянутых в данном описании, то в них для замены более общих значений на более специфические или, прежде всего, на значения, определенные как предпочтительные, целесообразно использовать значения заместителей из вышеописанных общих определений. Более подробно, изобретение относится к применению соединения формулы I, где n равно от 1 до 6 включительно; W означает О или S; R1 и R3 независимо друг от друга каждый означает водород, (низш.)алкил или (низш.)ацил; R2 означает группу циклоалкил, группу арил или моно- или бициклическую группу гетероарил, содержащую один или более атомов азота в цикле и 0, 1 или 2 гетероатома, независимо друг от друга выбранные из группы, включающей кислород и серу, причем группы в каждом случае являются незамещенными или могут иметь вплоть до трех заместителей, выбранных из ряда амино, моно- или дизамещенный амино, галоген, (низш.)алкил, замещенный алкил, (низш.)алкенил, (низш.)алкинил, (низш.)алканоил, гидрокси, простой или сложный эфир гидроксигруппы, нитро, циано, карбокси, этерифицированный карбокси, алканоил, бензоил, карбамоил, N-моно- или N,N-дизамещенный карбамоил, амидино, гуанидино, уреидо, меркапто, сульфо, (низш.)алкилтио, фенил, фенокси, фенилтио, фенил(низш.)алкилтио, алкилфенилтио, (низш.)алкилсульфинил, фенилсульфинил, фенил(низш.)алкилсульфинил, алкилфенилсульфинил, (низш.)алкансульфонил, фенилсульфонил, фенил(низш.)алкилсульфонил, алкилфенилсульфонил, галоген(низш.)алкилмеркапто, галоген(низш.)алкилсульфонил, дигидроксибора(-В(ОН)2), гетероциклил и (низш.)алкилендиокси, связанный с соседними атомами углерода в цикле; R и R’ независимо друг от друга каждый означает водород или (низш.)алкил; Х означает группу арил или моно- или бициклическую группу гетероарил, содержащую один или более атомов азота в цикле и 0, 1 или 2 гетероатома, независимо друг от друга выбранные из группы, включающей кислород и серу, причем группы в каждом случае являются незамещенными или могут содержать вплоть до трех заместителей, выбранных из ряда амино, моно- или дизамещенный амино, галоген, (низш.)алкил, замещенный алкил, (низш.)алкенил, (низш.)алкинил, (низш.)алканоил, гидрокси, простой или сложный эфир гидроксигруппы, нитро, циано, карбокси, этерифицированный карбокси, алканоил, бензоил, карбамоил, N-моно- или N,N-дизамещенный карбамоил, амидино, гуанидино, уреидо, меркапто, сульфо, (низш.)алкилтио, фенил, фенокси, фенилтио, фенил(низш.)алкилтио, алкилфенилтио, (низш.)алкилсульфинил, фенилсульфинил, фенил(низш.)алкилсульфинил, алкилфенилсульфинил, (низш.)алкансульфонил, фенилсульфонил, фенил(низш.)алкилсульфонил, алкилфенилсульфонил, галоген(низш.)алкилмеркапто, галоген(низш.)алкилсульфонил, дигидроксибора(-В(ОН)2), гетероциклил и (низш.)алкилендиокси, связанный с соседними атомами углерода в цикле; или его N-оксида или возможного таутомера; или фармацевтически приемлемой соли такого соединения для получения фармацевтической композиции для терапии заболевания, чувствительного к ингибированию активности VEGF-рецепторной тирозинкиназы. Более предпочтительно, изобретение относится к применению соединения формулы I, где n равно от 1 до 3 включительно; W означает О или S; R1 и R3 независимо друг от друга каждый означает водород, (низш.)алкил или (низш.)ацил; R2 означает циклогексил, фенил, индазолил, тиазолил, бензо[d]тиазолил, бензо[d]пиразолил или изохинолинил, который в каждом случае является незамещенным или моно- или дизамещенным (низш.)алкилом, (низш.)алкенилом или (низш.)алкинилом; и где каждый радикал R2 может быть незамещенным или моно- или полизамещенным галогеном; R и R’ независимо друг от друга каждый означает водород или (низш.)алкил; Х означает фенил, пиридил, пиримидил или хинолил, который в каждом случае является незамещенным или моно- или полизамещенным группой оксо, гидрокси, (низш.)алкил или (низш.)алкокси; или его N-оксида или возможного таутомера; или фармацевтически приемлемой соли такого соединения для получения фармацевтической композиции для терапии заболевания, чувствительного к ингибированию активности VEGF-рецепторной тирозинкиназы. Один предпочтительный вариант осуществления изобретения относится к соединению формулы I, где n равно 1 или 2; W означает О; R1 и R3 означают водород; R2 означает циклогексил, фенил, индазолил, тиазолил или изохинолинил, который в каждом случае является незамещенным или моно- или дизамещенным (низш.)алкилом или (низш.)алкинилом; и где каждый радикал R2 может быть незамещенным или моно- или полизамещенным галогеном; R и R’ независимо друг от друга каждый означает водород или (низш.)алкил; Х означает фенил, пиридил, пиримидил или хинолил, который в каждом случае является незамещенным или моно- или полизамещенным группой оксо, гидрокси, (низш.)алкил или (низш.)алкокси; или к его N-оксиду или возможному таутомеру; или к фармацевтически приемлемой соли такого соединения, которое применяют для получения фармацевтической композиции для терапии заболевания, чувствительного к ингибированию активности VEGF-рецепторной тирозинкиназы. Прежде всего, изобретение относится к применению соединения формулы I или его N-оксида или возможного таутомера или фармацевтически приемлемой соли такого соединения для получения фармацевтической композиции для терапии заболевания, чувствительного к ингибированию активности VEGF-рецепторной тирозинкиназы, причем заболевание означает онкологическое заболевание. В другом предпочтительном варианте изобретение относится к применению соединения формулы I или его N-оксида или возможного таутомера или фармацевтически приемлемой соли такого соединения для получения фармацевтической композиции для терапии заболевания, чувствительного к ингибированию активности VEGF-рецепторной тирозинкиназы, причем заболевание означает ретинопатию или возрастную дегенерацию желтого пятна. Кроме того, изобретение относится к способу лечения заболевания, чувствительного к ингибированию активности VEGF-рецепторной тирозинкиназы, который включает введение соединения формулы I или его N-оксида или фармацевтически приемлемой соли, где радикалы и символы имеют значения, указанные выше, в количестве, эффективном в отношении вышеупомянутого заболевания, теплокровному животному, нуждающемуся в таком лечении. Кроме того, изобретение относится к соединениям формулы I, где n равно от 1 до 6 включительно; W означает О или S; R1 и R3 независимо друг от друга каждый означает водород, (низш.)алкил или (низш.)ацил; R2 означает группу циклоалкил, группу арил или моно- или бициклическую группу гетероарил, содержащую один или более атомов азота в цикле и 0, 1 или 2 гетероатома, независимо друг от друга выбранные из группы, включающей кислород и серу, причем группы в каждом случае являются незамещенными или моно- или полизамещенными; R и R’ независимо друг от друга каждый означает водород или (низш.)алкил, Х означает группу арил или моно- или бициклическую группу гетероарил, содержащую один или более атомов азота в цикле и 0, 1 или 2 гетероатома, независимо друг от друга выбранные из группы, включающей кислород и серу, причем группы в каждом случае являются незамещенными или моно- или полизамещенными; и к их N-оксидам или возможным таутомерам; и к фармацевтически приемлемым солям таких соединений, за исключением соединений формулы I, где n равно 1, W означает O, R1, R3, R, R’ означают водород, Х означает фенил, a R2 означает 3-трифторметилфенил или 2-метоксифенил. Более предпочтительно, изобретение относится к соединениям формулы I, где n равно от 1 до 6 включительно; W означает О или S; R1 и R3 независимо друг от друга каждый означает водород, (низш.)алкил или (низш.)ацил; R2 означает группу циклоалкил, группу арил или моно- или бициклическую группу гетероарил, содержащую один или более атомов азота в цикле и 0, 1 или 2 гетероатома, независимо друг от друга выбранные из группы, включающей кислород и серу, причем группы в каждом случае являются незамещенными или могут иметь вплоть до трех заместителей, выбранных из ряда амино, моно- или дизамещенный амино, галоген, (низш.)алкил, замещенный алкил, (низш.)алкенил, (низш.)алкинил, (низш.)алканоил, гидрокси, простой или сложный эфир гидроксигруппы, нитро, циано, карбокси, этерифицированный карбокси, алканоил, бензоил, карбамоил, N-моно- или N,N-дизамещенный карбамоил, амидино, гуанидино, уреидо, меркапто, сульфо, (низш.)алкилтио, фенил, фенокси, фенилтио, фенил(низш.)алкилтио, алкилфенилтио, (низш.)алкилсульфинил, фенилсульфинил, фенил(низш.)алкилсульфинил, алкилфенилсульфинил, (низш.)алкансульфонил, фенилсульфонил, фенил(низш.)алкилсульфонил, алкилфенилсульфонил, галоген(низш.)алкилмеркапто, галоген(низш.)алкилсульфонил, дигидроксибора(-В(ОН)2), гетероциклил и (низш.)алкилендиокси, связанный с соседними атомами углерода в цикле; R и R’ независимо друг от друга каждый означает водород или (низш.)алкил; Х означает группу арил или моно- или бициклическую группу гетероарил, содержащую один или более атомов азота в цикле и 0, 1 или 2 гетероатома, независимо друг от друга выбранные из группы, включающей кислород и серу, причем группы в каждом случае являются незамещенными или могут содержать вплоть до трех заместителей, выбранных из ряда амино, моно- или дизамещенный амино, галоген, (низш.)алкил, замещенный алкил, (низш.)алкенил, (низш.)алкинил, (низш.)алканоил, гидрокси, простой или сложный эфир гидроксигруппы, нитро, циано, карбокси, этерифицированный карбокси, алканоил, бензоил, карбамоил, N-моно- или N,N-дизамещенный карбамоил, амидино, гуанидино, уреидо, меркапто, сульфо, (низш.)алкилтио, фенил, фенокси, фенилтио, фенил(низш.)алкилтио, алкилфенилтио, (низш.)алкилсульфинил, фенилсульфинил, фенил(низш.)алкилсульфинил, алкилфенилсульфинил, (низш.)алкансульфонил, фенилсульфонил, фенил(низш.)алкилсульфонил, алкилфенилсульфонил, галоген(низш.)алкилмеркапто, галоген(низш.)алкилсульфонил, дигидроксибора(-В(ОН)2), гетероциклил и (низш.)алкилендиокси, связанный с соседними атомами углерода в цикле; или их N-оксидам или возможным таутомерам; или фармацевтически приемлемым солям таких соединений, за исключением соединений формулы I, где n равно 1, W означает О, R1, R3, R, R’ означают водород, Х означает фенил, a R2 означает 3-трифторметилфенил или 2-метоксифенил. Предпочтительными являются соединения формулы I, где n равно от 1 до 3 включительно; W означает О или S; R1 и R3 независимо друг от друга каждый означает водород, (низш.)алкил или (низш.)ацил; R2 означает циклогексил, фенил, индазолил, тиазолил, бензо[d]тиазолил, бензо[d]пиразолил или изохинолинил, который в каждом случае является незамещенным или моно- или дизамещенным (низш.)алкилом, (низш.)алкенилом или (низш.)алкинилом; и где каждый радикал R2 может быть незамещенным или моно- или полизамещенным галогеном; R и R’ независимо друг от друга каждый означает водород или (низш.)алкил; Х означает фенил, пиридил, пиримидил или хинолил, который в каждом случае является незамещенным или моно- или полизамещенным группой оксо, гидрокси, (низш.)алкил или (низш.)алкокси; или их N-оксиды или возможные таутомеры; или фармацевтически приемлемые соли таких соединений, за исключением соединений формулы I, где n равно 1, W означает О, R1, R3, R, R’ означают водород, Х означает фенил, a R2 означает 3-трифторметилфенил или 2-метоксифенил. Прежде всего, предпочтительными являются соединения формулы I, где n равно 1 или 2; W означает О; R1 и R3 означают водород; R2 означает циклогексил, фенил, индазолил, тиазолил или изохинолинил, который в каждом случае является незамещенным или моно- или дизамещенным (низш.)алкилом или (низш.)алкинилом; и где каждый радикал R2 может быть незамещенным или моно- или полизамещенным галогеном; R и R’ независимо друг от друга каждый означает водород или (низш.)алкил; Х означает фенил, пиридил, пиримидил или хинолил, который в каждом случае является незамещенным или моно- или полизамещенным группой оксо, гидрокси, (низш.)алкил или (низш.)алкокси; или их N-оксиды или возможные таутомеры; или фармацевтически приемлемые соли таких соединений, за исключением соединений формулы I, где n равно 1, R, R’ означают водород, Х означает фенил, a R2 означает 3-трифторметилфенил или 2-метоксифенил. В вышеуказанном определении R2 формулировка “где каждый радикал R2 может быть незамещенным или моно- или полизамещенным галогеном” означает радикал R2, в котором заместители (низш.)алкил, (низш.)алкенил или (низш.)алкинил в составе упомянутых групп (циклогексил, фенил, имидазолил и т.д.) в свою очередь необязательно являются замещенными галогеном. Таким образом, определение включает наряду с прочими радикалы R2, подобные трифторметилфенилу или бис(трифторметил)фенилу. Наиболее предпочтительно соединение, выбранное из группы соединений, включающей: 2-[2-(4-пиридил)этил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(2-метил-4-пиридил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(6-метокси-3-пиридил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-[3,4-бис(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-[5-фтор-3-трифторметилфенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(транс-4-трет-бутилциклогексан)-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(4-н-пропилфенил)-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(4-н-бутилфенил)-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(4-н-пентилфенил)-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-[4-(1-пропинил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(5-индазолил)-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(3-изохинолинил)-3-пиридинкарбоксамид, 2-[(пиридин-6(1Н)-он-3-ил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид и их фармацевтически приемлемые соли. Кроме того, наиболее предпочтительными являются соединения, выбранные из группы соединений, включающей гидрохлорид 2-(фенилметиламино)-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамида, 2-[(4-пиридил)метиламино]-N-[2-фтор-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метиламино]-N-[4-бром-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метиламино]-N-[2-метил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метиламино]-N-[2-метил-5-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метиламино]-N-(цис-4-трет-бутилциклогексил)-3-пиридинкарбоксамид, 2-[(6-метоксипирид-3-ил)метиламино]-N-[4-бром-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(6-метоксипирид-3-ил)метиламино]-N-[2-фтор-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(6-метоксипирид-3-ил)метиламино]-N-[2-метил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(1-оксидо-4-пиридил)метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[3-[N-метилкарбоксамидо)фенил]метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(1-метилпиридин-2(1Н)-он-5-ил)метиламино]-N-[3-(трифторметил)-фенил]-3-пиридинкарбоксамид, 2-[(6-метоксипирид-3-ил)метиламино]-N-[4-пропинил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метиламино]-N-[4-пропинил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-пропинил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(3-гидроксифенил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-бром-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[2-фтор-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[2-метил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-пропил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(6-метоксипирид-3-ил)метиламино]-N-[4-пропил-3-(трифторметил)-фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-[4-(н-пропил)-3-(трифторметил)-фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(5-тиазолил)-3-пиридинкарбоксамид, 2-[(4-гидроксифенил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(бензо[d]пиразол-5-ил)-3-пиридинкарбоксамид, 2-[(6-метокси-3-пиридил)метил]амино-N-(3-изохинолинил)-3-пиридинкарбоксамид, 2-[(6-метокси-3-пиридил)метил]амино-N-(бензо[d]пиразол-5-ил)-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-(3-изохинолинил)-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-(бензо[d]пиразол-5-ил)-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-(цис-4-трет-бутилциклогексил)-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-(транс-4-трет-бутилциклогексил)-3-пиридинкарбоксамид, 2-[(1-оксидо-4-пиридил)метиламино]-N-[4-пропил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-этил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[3,4-бис(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(1-метилпиридин-2(1Н)-он-5-ил)метиламино]-N-[3,4-бис(трифторметил)фенил]-3-пиридинкарбоксамид и их фармацевтически приемлемые соли. Соединение по изобретению может быть получено способами, которые, хотя до настоящего времени не были использованы для получения новых соединений по настоящему изобретению, по существу известны; прежде всего, такой способ характеризуется тем, что для синтеза соединения формулы I, где R1, R2, R3, R, R’, X, W и n имеют значения, указанные для соединения формулы I, производное пиридина формулы II
где W, R1 и R2 имеют значения, указанные для соединения формулы I, a Y означает уходящую группу, такую как галоген, предпочтительно хлор, взаимодействует с амином формулы III
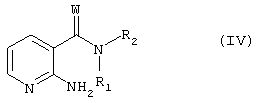
где n, R, R’, R3 и Х имеют значения, указанные для соединения формулы I, необязательно в присутствии основания и соответствующего катализатора, такого как соединение меди(I), необязательно в присутствии инертного растворителя; причем вышеуказанные исходные соединения II и III могут также присутствовать с защищенными функциональными группами, если это необходимо, и/или в форме солей при условии, что такая солеобразующая группа в соединении присутствует и возможна реакция в солевой форме; причем любые защитные группы в защищенном соединении формулы I удаляют; и, если это необходимо, полученное соединение формулы I превращают в другое соединение формулы I или его N-оксид, свободное соединение формулы I превращают в соль, полученную соль соединения формулы I превращают в свободное соединение или другую соль, и/или смесь изомеров соединения формулы I разделяют на индивидуальные изомеры. В другом варианте соединение по изобретению, где R’, присоединенный к атому углерода, связанному с атомом азота в мостиковой группе, означает водород, может быть получено способом, в котором аминопиридин формулы IV
где R1 и R2 имеют значения, указанные для соединения формулы I, взаимодействует с карбонилсодержащим соединением формулы V
где X, n, R и R’ имеют значения, указанные для соединения формулы I, в присутствии восстанавливающего агента. Карбонилсодержащее соединение формулы V может также присутствовать в форме реакционно-способного производного, однако предпочтительны свободный альдегид или кетон. Реакционно-способными производными соединений формулы V являются, например, соответствующие аддукты с бисульфитом, или, прежде всего, полуацетали, ацетали, полукетали или кетали соединений формулы V со спиртами, например (низш.)алканолами; или тиоцетали или тиокетали соединений формулы V с меркаптанами, например (низш.)алкилсульфидами. Восстановительное алкилирование предпочтительно проводят гидрированием в присутствии катализатора, прежде всего катализатора на основе благородного металла, такого как платина или, прежде всего, палладия, который предпочтительно связан с материалом носителя, таким как уголь, или катализатора на основе тяжелого металла, такого как никель Ренея, при нормальном давлении или при давлении от 0,1 до 10 МПа (мегапаскалей), или восстановлением с использованием комплексных гидридов, таких как боргидриды, прежде всего цианборгидриды щелочного металла, например цианборгидрида натрия, в присутствии соответствующей кислоты, предпочтительно относительно слабых кислот, таких как (низш.)алканкарбоновые кислоты, прежде всего уксусная кислота, или сульфоновой кислоты, такой как пара-толуолсульфокислота; в обычных растворителях, например спиртах, таких как метанол или этанол, или простых эфирах, например циклических эфирах, таких как тетрагидрофуран, в присутствии или в отсутствии воды. Подробное описание способа Если не указано иное, ниже в подробном описании способа R1, R2, R3, R, R’, X, W и n имеют значения, указанные для соединений формулы I. Взаимодействие соединений формулы II и III предпочтительно проводят в полярном растворителе, например в спиртах, например этаноле, изопропаноле, бутаноле, 3-этил-3-пентаноле, в диметилацетамиде, диметилформамиде или N-метилпирролидоне, и предпочтительно в атмосфере инертного газа, например в атмосфере азота или аргона. Основание, которое используют в реакции, может быть выбрано из обычных оснований, таких как карбонат калия, карбонат цезия, или органическое основание, такое как третичный амин, такой как этилдиизопропиламин, или ароматический амин, такой как пиридин, или реакцию проводят в присутствии избытка реагента формулы III. Удовлетворительные результаты получают при использовании карбоната калия. Реакцию проводят в присутствии катализатора на основе иона меди или солей никеля. В качестве катализатора предпочтительны оксид меди(I) или иодид меди(II). Время реакции предпочтительно составляет от 0,5 ч до 24 ч, например 120 мин, температура реакции составляет от комнатной температуры до температуры кипения растворителя. Если в качестве растворителя используют диметилформамид, температура реакции предпочтительно находится в диапазоне от 80°С до температуры кипения растворителя. Защитные группы Если в соединениях формул II, III и/или IV следует или необходимо защитить одну или более других функциональных групп, например, карбокси, гидрокси, амино или меркапто, не принимающих участия в реакции, то при этом используют такие группы, которые обычно применяются в синтезе пептидов, а также цефалоспоринов и пенициллинов, производных нуклеиновых кислот и сахаров. Защитные группы могут уже присутствовать в предшественниках и должны защищать соответствующие функциональные группы от нежелательных побочных реакций, таких как ацилирование, образование простых и сложных эфиров, окисление, сольволиз и аналогичные реакции. Для защитных групп характерно, что их можно легко удалить, т.е. без нежелательных побочных реакций, обычно сольвользом, восстановлением, фотолизом, а также с использованием ферментов, например, в условиях, аналогичных физиологическим условиям, причем характерно, что эти группы отсутствуют в конечных продуктах. Для специалиста очевидно, или он может легко определить, какие защитные группы являются приемлемыми в выше- и нижеупомянутых реакциях. Защита таких функциональных групп такими защитными группами, сами защитные группы и реакции их удаления описаны, например, в ряде монографий, таких как J.F.W.McOmie, “Protective Groups in Organic Chemistry”, Plenum Press, London and New York (1973), Т.W.Greene, “Protective Groups in Organic Synthesis”, Wiley, New York (1981), “The Peptides”; Volume 3 (изд. E.Gross and J.Meienhofer), Academic Press, London and New York (1981), “Methoden der organischen Chemie” (Methods of organic chemistry), Houben Weyl, 4th edition. Volume 15/I, Georg Thieme Verlag, Stuttgart (1974), H.-D.Jakubke and H.Jescheit, “Aminosäuren, Peptide, Proteine” (Amino acids, peptides, proteins), Verlag Chemie, Weinheim, Deerfield Beach, and Basel (1982), и Jochen Lehmann, “Chemie der Kohlenhydrate: Monosaccharide und Derivate” (Chemistry of carbohydrates: monosaccharides and derivatives), Georg Thieme Verlag, Stuttgart (1974). В одном из предпочтительных вариантов осуществления изобретения из соединения формулы I, включающего радикал 2-метоксипиридил, получают соединение формулы I, включающее радикал 2-гидроксипиридил, обработкой триметилсилилиодидом в течение приблизительно от 20 ч до 35 ч при температуре от 45°С до 70°С в соответствующем растворителе, т.е. галогенированном алкане, например, в хлороформе, необязательно с последующей обработкой метанолом. Дополнительные стадии способа На дополнительных стадиях способа, если это необходимо, функциональные группы исходных соединений, не принимающие участие в реакции, могут присутствовать в незащищенной форме или могут быть защищены, например, одной или более группами, описанными выше в качестве «защитных групп». Затем защитные группы полностью или частично удаляют одним из нижеописанных способов. Соли соединения формулы I с солеобразующей группой могут быть получены известным способом. Таким образом, кислотно-аддитивные соли соединений формулы I могут быть получены взаимодействием с кислотой или с соответствующим анионообменным реагентом. Соль с двумя молекулами кислоты (например, дигалогенид соединения формулы I) также может быть превращена в соль с одной молекулой кислоты (например, в моногалогенид); эту стадию можно осуществить нагреванием расплава, или, например, нагреванием твердого вещества в высоком вакууме при повышенной температуре, например при температуре от 130°С до 170°С, при этом из молекулы соединения формулы I удаляется одна молекула кислоты. Соли обычно могут быть превращены в свободные соединения, например, обработкой соответствующими основными агентами, например карбонатами щелочных металлов, гидрокарбонатами щелочных металлов или гидроксидами щелочных металлов, обычно карбонатом калия или гидроксидом натрия. Стереоизомерные смеси, например смеси диастереомеров, могут быть разделены на соответствующие изомеры известным способом с использованием обычных методов разделения. Например, диастереомерные смеси могут быть разделены на индивидуальные диастереомеры с использованием фракционной кристаллизации, хроматографии, распределения в растворителях и т.п. Подобное разделение можно проводить на уровне исходного соединения или конечного соединения формулы I. Энантиомеры могут быть разделены с использованием диастереомерных солей, например, образованием соли с энантиомерно-чистой хиральной кислотой, или хроматографией, например, ЖХВР, с использованием хроматографических сорбентов с хиральными лигандами. Соединение формулы I, где W означает О, может быть превращено в соответствующее соединение, где W означает S, например, с использованием соответствующего соединения серы, например, по реакции с реагентом Лавессона (2,4-бис-(4-метоксифенил)-2,4-дитиооксо-1,2,3,4-дитиафосфетан) в галогенированном углеводороде, таком как дихлорметан, или в апротонном растворителе, таком как толуол или ксилол, при температуре от приблизительно 30°С до температуры кипения растворителя. Соединение формулы I, где R1 означает водород, может быть превращено в соответствующее соединение, где R1 означает (низш.)алкил, по реакции, например, с диазо(низш.)алкилом, прежде всего, диазометаном, в инертном растворителе, предпочтительно в присутствии катализатора на основе благородного металла, прежде всего, в дисперсной форме, например меди, или соли благородного металла, например хлорида меди(I) или сульфата меди(II). Кроме того, возможна реакция с (низш.)алкилгалогенидами, или (низш.)алканами, содержащими другие уходящие группы, например, (низш.)алкильными спиртами, этерифицированными сильной органической сульфоновой кислотой, такой как (низш.)алкансульфоновая кислота (необязательно замещенной галогеном, таким как фтор), ароматической сульфоновой кислотой, например незамещенной или замещенной бензолсульфоновой кислотой, в которой заместители предпочтительно выбраны из ряда (низш.)алкил, например метил, галоген, например бром, и/или нитро, например этерифицированная метаном сульфоновая кислота, например триметансульфоновая кислота или пара-толуолсульфоновая кислота. Алкилирование проводят, прежде всего, в водном растворе и/или в присутствии полярных растворителей, обычно спиртов, например метанола, этанола, изопропанола или этиленгликоля, простых эфиров, обычно диоксана, амидов, обычно диметилформамида, или фенолов, обычно фенола, а также в отсутствии воды, в неполярных растворителях, обычно в бензоле и толуоле, или в эмульсиях вода/бензол, и, если возможно, в присутствии кислотных или основных катализаторов, например щелочей, обычно раствора гидроксида натрия, или в присутствии твердофазных катализаторов, обычно оксида алюминия, с привитым гидразином, в простых эфирах, например диэтиловом эфире, обычно при температуре от приблизительно 0°С до температуры кипения реакционной смеси, предпочтительно от 20°С до температуры кипения (растворителя), при необходимости при повышенном давлении, например, в запаянной ампуле, возможно также при температуре выше температуры кипения (растворителя), и/или в атмосфере инертного газа, обычно азота или аргона. Следует подчеркнуть, что реакции, аналогичные описанным в данном разделе, могут быть также проведены с соответствующими промежуточными соединениями. Общие условия осуществления способа Все нижеописанные стадии способа могут быть проведены в известных условиях, предпочтительно упомянутых выше, в отсутствии или обычно в присутствии растворителей или разбавителей, предпочтительно инертных к используемым реагентам и растворяющих их, в отсутствие или в присутствии катализаторов, конденсирующих агентов и нейтрализующих агентов, например ионообменников, обычно катионообменников, например, в Н+ – форме, в зависимости от типа реакции и/или реагентов, при пониженной, нормальной или повышенной температуре, например в диапазоне от -100°С до приблизительно 190°С, предпочтительно от приблизительно -80°С до приблизительно 150°С, например от -80°С до -60°С, при комнатной температуре, от -20°С до 40°С, или при температуре кипения растворителя, при атмосферном давлении или в закрытом сосуде, если возможно под давлением, и/или в инертной атмосфере, например в атмосфере аргона или азота. Все исходные и промежуточные соединения, содержащие солеобразующие группы, могут присутствовать в виде солей. Соли могут также присутствовать во время реакций, в которые вступают такие соединения, при условии, что наличие солевой формы не препятствует прохождению реакции. На всех стадиях синтеза, образующиеся смеси изомеров могут быть разделены на отдельные изомеры, например диастереомеры или энантиомеры, или на любую смесь изомеров, например рацематы или смеси диастереомеров, обычно, как описано в разделе «Дополнительные стадии способа». В некоторых случаях, обычно при гидрировании, можно проводить стереоселективные реакции, которые обеспечивают, например, более простое выделение индивидуальных изомеров. Если в описании способа не указано иное, растворители, из которых выбирают приемлемые для проведения упомянутых реакций, включают, например, воду, сложные эфиры, обычно (низш.)алкил(низш.)алканоаты, например этилацетат, простые эфиры, обычно алифатические эфиры, например диэтиловый эфир, или циклические эфиры, например тетрагидрофуран, жидкие ароматические углеводороды, обычно бензол или толуол, спирты, обычно метанол, этанол или 1- или 2-пропанол, нитрилы, обычно ацетонитрил, галогенированные углеводороды, обычно дихлорметан, амиды кислот, обычно диметилформамид, основания, обычно гетероциклические азотистые основания, например пиридин, карбоновые кислоты, обычно (низш.)алканкарбоновые кислоты, например уксусная кислота, ангидриды карбоновых кислот, обычно ангидриды (низш.)алканкарбоновых кислот, например уксусный ангидрид, циклические, линейные или разветвленные углеводороды, обычно циклогексан, гексан или изопентан, или смеси указанных растворителей, например водные растворы. Такие смеси растворителей могут быть также использованы в способе (по изобретению), например, при хроматографии или распределении. Изобретение относится также к таким формам способа, в которых синтез начинают с соединения, полученного на любой другой стадии в качестве промежуточного соединения, проводят стадии, не достигшие цели, или прерывают способ на любой из стадий, или получают исходный материал в условиях реакции, или используют упомянутый исходный материал в форме реакционно-способного производного или соли, или получают соединение способом по изобретению и перерабатывают упомянутое соединение in situ. В предпочтительном варианте изобретения синтез начинают с таких исходных материалов, которые позволяют получать соединения, описанные выше, как предпочтительные, прежде всего, предпочтительные, наиболее предпочтительные и/или самые предпочтительные. В предпочтительном варианте изобретения соединение формулы I получают по способам и стадиям способа, описанным в примерах или аналогичным им. Соединения формулы I, включая их соли, также могут быть получены в форме гидратов, или их кристаллы могут включать, например, растворитель, использованный для кристаллизации (в виде сольвата). Фармацевтические препараты, способы их получения и применения. Настоящее изобретение относится также к способу лечения опухолевого заболевания, которое чувствительно к ингибированию активности VEGF-рецепторной тирозинкиназы, который включает введение соединения формулы I или его N-оксида или фармацевтически приемлемой соли, где радикалы и символы имеют значения, указанные для формулы I, в количестве, эффективном в отношении упомянутого заболевания, теплокровному животному, нуждающемуся в таком лечении. В другом варианте изобретение относится к способу лечения ретинопатии или возрастной дегенерации желтого пятна, который включает введение соединения формулы I или его N-оксида или фармацевтически приемлемой соли, где радикалы и символы имеют значения, указанные для формулы I, в количестве, эффективном в отношении упомянутого заболевания, теплокровному животному, нуждающемуся в таком лечении. Настоящее изобретение относится также к фармацевтическим композициям, включающим соединение формулы I или его N-оксид в качестве активного ингредиента, которые могут быть использованы, прежде всего, при лечении заболеваний, упомянутых в начале описания заявки. Прежде всего, предпочтительны композиции для энтерального введения, такого как назальное, трансбуккальное, ректальное или, прежде всего, пероральное введение, и для парентерального введения, такого как внутривенное, внутримышечное или подкожное введение, теплокровным животным, прежде всего человеку. Композиции включают активный ингредиент, отдельно или, предпочтительно, в смеси с фармацевтически приемлемым носителем. Дозировка активного ингредиента зависит от заболевания, подлежащего лечению, от вида животного, его возраста, веса и состояния, индивидуальных фармакокинетических данных и способа введения. Настоящее изобретение относится, прежде всего, к фармацевтическим композициям, включающим соединение формулы I, таутомер, N-оксид или фармацевтически приемлемую соль, или его гидрат, или сольват и по меньшей мере один фармацевтически приемлемый носитель. Изобретение относится также к фармацевтическим композициям для применения в способе профилактики или, прежде всего, терапевтического лечения организма человека или животного, к способу их получения (прежде всего, в форме композиций для лечения опухолей) и к способу лечения онкологических заболеваний, прежде всего, упомянутых выше по тексту. Изобретение относится также к способам получения и применению соединений формулы I или их N-оксидов в способе получения фармацевтических препаратов, которые включают соединения формулы I или их N-оксиды в качестве активного компонента (активного ингредиента). В предпочтительном варианте изобретения фармацевтический препарат является пригодным для введения теплокровному животному, прежде всего человеку или коммерческим млекопитающим, страдающим от болезни, чувствительной к ингибированию ангиогенеза или VEGF-рецепторной тирозинкиназы, например псориаза или, прежде всего, онкологического заболевания, и включает количество соединения формулы I или его N-оксида, эффективного в отношении ингибирования ангиогенеза или VEGF-рецепторной тирозинкиназы, или его фармацевтически приемлемой соли, если в нем содержатся солеобразующие группы, и по меньшей мере один фармацевтически приемлемый носитель. Аналогичным образом предпочтительна фармацевтическая композиция для профилактики или, прежде всего, для терапевтического лечения онкологических и других пролиферативных заболеваний теплокровного животного, прежде всего человека или коммерческого млекопитающего, нуждающегося в таком лечении, прежде всего, страдающего от такого заболевания, включающая в качестве активного ингредиента новое соединение формулы I или его N-оксид в количестве, которое активно в профилактическом или, прежде всего, терапевтическом отношении, в случае упомянутых заболеваний. Фармацевтические композиции включают от приблизительно 1% до приблизительно 95% активного ингредиента, причем в предпочтительном варианте изобретения формы для однократного введения включают от приблизительно 20% до приблизительно 90% активного ингредиента, а формы для неоднократного применения в предпочтительном варианте изобретения включают от приблизительно 5% до приблизительно 20% активного ингредиента. Формами, содержащими стандартные дозы, являются, например, таблетки с покрытием и без покрытия, ампулы, флаконы, суппозитории или капсулы. Другими дозировочными формами являются, например, мази, кремы, пасты, пены, настойки, губные помады, капли, спреи, дисперсии и т.п. Примером являются капсулы, содержащие от приблизительно 0,05 г до приблизительно 1,0 г активного ингредиента. Фармацевтические композиции по настоящему изобретению получают известными способами, например, с использованием обычных способов смешивания, гранулирования, покрытия, растворения или лиофилизации. Предпочтительно использовать активный ингредиент в растворе, а также в виде суспензий или дисперсий, прежде всего, в виде изотонических водных растворов, дисперсий или суспензий, которые, например, в случае лиофильно высушенных композиций, включающих активный ингредиент отдельно или в смеси с носителем, например маннитом, могут быть приготовлены непосредственно перед употреблением. Фармацевтические композиции могут быть стерильными и/или могут включать эксципиенты, например консерванты, стабилизаторы, смачивающие агенты и/или эмульгаторы, солюбилизирующие агенты, соли для регуляции осмотического давления и/или буферные вещества, и могут быть приготовлены известными способами, например обычным растворением и лиофилизацией. Упомянутые растворы или суспензии могут включать загустители, обычно натриевую соль карбоксиметилцеллюлозы, карбоксиметилцеллюлозу, декстран, поливинилпирролидон или желатин, или также солюбилизирующие агенты, например твин 80 (моноолеат полиоксиэтилен(20)сорбита, торговая марка фирмы ICI Americans, США). Суспензии в масле включают в качестве масляного компонента растительные, синтетические или полусинтетические масла, используемые для инъекций. В связи с этим следует упомянуть эфиры жидких жирных кислот, которые содержат в качестве кислотной компоненты длинноцепочечные жирные кислоты, имеющие от 8 до 22, прежде всего от 12 до 22, атомов углерода, например лауриновую кислоту, тридециловую кислоту, миристиновую кислоту, пентадециловую кислоту, пальмитиновую кислоту, маргариновую кислоту, стеариновую кислоту, арахидоновую кислоту, бегеновую кислоту, или соответствующие ненасыщенные кислоты, например олеиновую кислоту, элаидиновую кислоту, эруковую кислоту, брассидиновую кислоту или линолевую кислоту, при необходимости с добавлением антиоксидантов, например витамина Е, “Labrafil М 1944 CS” (ненасыщенные полигликозилированные глицериды, полученные алкоголизом персикового масла и включающие глицериды и сложный эфир полиэтиленгликоля, фирма Gattefosse, Франция), “Labrasol” (насыщенные полигликозилированные глицериды, полученные алкоголизом ТСМ и включающие глицериды и сложный эфир полиэтиленгликоля, фирма Gattefosse, Франция), и/или “Miglyol 812” (триглицериды насыщенных жирных кислот с длиной цепи от C8 до C12, фирма Hulls AG, Германия), но, прежде всего, растительные масла, такие как хлопковое масло, миндальное масло, оливковое масло, касторовое масло, кунжутное масло, соевое масло и, более предпочтительно, арахисовое масло. Инъекционные препараты обычно готовят в стерильных условиях, например, разливают по ампулам или флаконам и запечатывают. Фармацевтические композиции для перорального применения могут быть получены смешиванием активного ингредиента с одним или более твердым носителем, необязательно гранулированием полученной смеси и переработкой смеси или гранул, если желательно или необходимо при включении дополнительных эксципиентов, в таблетки или ядра таблеток. Приемлемыми носителями являются, прежде всего, наполнители, такие как сахара, например лактоза, сахароза, маннит или сорбит, препараты целлюлозы и/или фосфаты кальция, например трикальцийфосфат или гидрофосфат кальция, а также связующие агенты, такие как крахмалы, например кукурузный, пшеничный, рисовый или картофельный крахмал, метилцеллюлоза, гидроксипропилметилцеллюлоза, натриевая соль карбоксиметилцеллюлозы и/или поливинилпирролидон, и/или, необязательно, дезинтеграторы, такие как вышеупомянутые крахмалы, а также карбоксиметилкрахмал, сшитый поливинилпирролидон, альгиновая кислота и ее соли, такие как альгинат натрия. Дополнительными эксципиентами являются, прежде всего, жидкие кондиционеры и замасливатели, такие как кремневая кислота, тальк, стеариновая кислота или ее соли, такие как стеарат магния или кальция, и/или полиэтиленгликоль или его производные. Ядра таблеток могут быть покрыты необязательно энтеросолюбильным покрытием с использованием, наряду с прочими материалами концентрированных растворов, сахара, который может включать аравийскую камедь, тальк, поливинилпирролидон, полиэтиленгликоль и/или диоксид титана, или растворов для покрытия в соответствующих органических растворителях или смесях растворителей, или для получения энтеросолюбильных покрытий растворов соответствующих препаратов целлюлозы, таких как фталат ацетилцеллюлозы или фталат гидроксипропилметилцеллюлозы. В таблетки или покрытия таблеток могут быть добавлены красители или пигменты, например, с целью идентификации или определения различных доз активного ингредиента. Фармацевтические композиции для перорального применения также включают твердые капсулы, содержащие желатин, а также мягкие, герметичные капсулы, содержащие желатин и пластификатор, такой как глицерин или сорбит. Твердые капсулы могут содержать активный ингредиент в форме гранул, например, в смеси с наполнителями, такими как кукурузный крахмал, связующими агентами, и/или замасливателями, такими как тальк или стеарат магния, и необязательно стабилизаторами. В мягких капсулах активный ингредиент предпочтительно растворен или суспендирован в жидких эксципиентах, таких как нелетучие масла, парафиновые масла или жидкие полиэтиленгликоли или эфиры жирных кислот или этилен- или пропиленгликоль, к которым могут быть добавлены стабилизаторы и ПАВы, например, типа эфира жирной кислоты с полиоксиэтиленсорбитом. Фармацевтические композиции, пригодные для ректального применения, представляют собой, например, суппозитории, которые содержат смесь активного ингредиента с основой суппозитория. Пригодными основами суппозитория являются, например, природные или синтетические триглицериды, парафиновые углеводороды, полиэтиленгликоли или высшие алканолы. Для парентерального введения, прежде всего, приемлемы водные растворы активного ингредиента в водорастворимой форме, например, водорастворимой соли, или инъекционные суспензии в воде, которые содержат загустители, например натриевую соль карбоксиметилцеллюлозы, сорбит и/или декстран, и, если необходимо, стабилизаторы. Активный ингредиент, необязательно вместе с эксципиентами, может присутствовать также в форме лиофильно высушенного препарата, и может быть приготовлен в виде раствора добавлением соответствующих растворителей непосредственно перед парентеральным введением. Растворы, используемые, например, для парентерального введения, могут быть также использованы в качестве растворов для вливания. Предпочтительными консервантами являются, например, антиоксиданты, такие как аскорбиновая кислота, или бактерицидные средства, такие как сорбиновая или бензойная кислота. Изобретение также относится к способу или методу лечения одного из вышеуказанных патологических состояний, прежде всего, заболевания, чувствительного к ингибированию VEGF-рецепторной тирозинкиназы или к ингибированию ангиогенеза, прежде всего, соответствующего онкологического заболевания или также псориаза. Соединения формулы I или их N-оксиды могут быть введены как таковые или, прежде всего, в форме фармацевтических композиций, с профилактическими или терапевтическими целями, предпочтительно в количестве, эффективном в отношении упомянутых заболеваний, теплокровному животному, например человеку, нуждающемуся в таком лечении. Для пациента массой 70 кг суточная доза составляет от приблизительно 0,05 г до приблизительно 5 г, предпочтительно от приблизительно 0,25 г до приблизительно 1,5 г соединения по настоящему изобретению. Прежде всего, настоящее изобретение относится также к применению соединения формулы I, или его N-оксида, или его фармацевтически приемлемой соли, прежде всего, соединения формулы I, упомянутого как предпочтительное, или его фармацевтически приемлемой соли, как такового или в форме фармацевтического препарата в смеси по меньшей мере с одним фармацевтически приемлемым носителем, для терапевтического, а также профилактического лечения одного или более вышеуказанных заболеваний, предпочтительно заболевания, чувствительного к ингибированию VEGF-рецепторной тирозинкиназы, или ангиогенеза, прежде всего, соответствующего онкологического заболевания или также псориаза, более предпочтительно, если упомянутое заболевание чувствительно к ингибированию VEGF-рецепторной тирозинкиназы или ангиогенеза. Предпочтительные дозировки, состав(ы) и получение фармацевтических препаратов (лекарственных средств), которые следует использовать в каждом случае, описаны выше. Исходные материалы Объектом изобретения являются также новые исходные материалы и/или промежуточные соединения, а также способы их получения. В предпочтительном варианте изобретения используют такие исходные материалы и выбирают такие условия проведения реакций, которые обеспечивают получение предпочтительных соединений. Исходные материалы формул II и III известны, являются коммерческими препаратами или могут быть синтезированы аналогично или по методам, известными в данной области техники. Например, производное пиридина формулы II может быть получено по реакции соединения формулы VI
где W имеет значения, указанные для формулы I, Y означает галоген, предпочтительно хлор, а Y’ означает уходящую группу, например алкилтио, азид или предпочтительно галоген, например хлор, с соединением формулы VII
где радикалы R1 и R2 имеют значения, указанные для формулы I. В процессе проведения реакции температуру предпочтительно строго контролируют охлаждением или разбавлением реакционной смеси и поддерживают в диапазоне от 0°С до комнатной температуры. Необязательно в раствор добавляют водный раствор щелочи, чтобы нейтрализовать протонированную уходящую группу, например, HCl. Например, реакцию проводят добавлением амина формулы VII в инертном растворителе, таком как этилацетат, этанол, диметилформамид или тетрагидрофуран, к водному раствору щелочи, например водному раствору гидроксида натрия, гидроксида калия, гидрокарбоната натрия или карбоната калия, необязательно содержащему каталитические количества 4-(диметиламино)пиридина, а затем добавлением по каплям к щелочному раствору амина VII соединения формулы VI в этом же или ином инертном растворителе. Все остальные исходные материалы известны, могут быть получены известными способами или являются коммерческими препаратами; прежде всего, они могут быть получены способами, описанными в примерах. При получении исходных материалов имеющиеся функциональные группы, которые не должны принимать участие в реакции, если это необходимо, должны быть защищены. Предпочтительные защитные группы, способы их введения и удаления описаны в разделе «Защитные группы» или в примерах. Изобретение иллюстрируется следующими примерами, не ограничивающими его объем. Если не указано иное, реакции проводят при комнатной температуре. А. Получение промежуточных соединений Промежуточное соединение 1а 2-Хлор-N-(3-фторметилфенил)-3-пиридинкарбоксамид Раствор 3-аминобензотрифторида (фирма Fluka, Buchs, Швейцария; 2,5 мл, 2,90 г, 18 ммолей) в этилацетате (40 мл) добавляли при комнатной температуре к перемешиваемому водному раствору гидроксида натрия (40 мл 1 М раствора). Полученный перемешиваемый раствор обрабатывали по каплям в течение 30 мин раствором 2-хлорникотиноилхлорида (фирма Lancaster Synthesis, Ланкашир, Англия; 3,52 г, 20 ммолей) в сухом этилацетате (25 мл) и полученную смесь перемешивали при температуре окружающей среды в течение 2 ч. Затем смесь экстрагировали этилацетатом (3×100 мл) и объединенные экстракты последовательно промывали водой (2×100 мл), хлористоводородной кислотой (2×100 мл 2 М раствора), водой (2×100 мл), насыщенным водным раствором гидрокарбоната натрия (2×100 мл), насыщенным водным раствором хлорида натрия (1×100 мл), сушили (Na2SO4), фильтровали и растворитель выпаривали при пониженном давлении, при этом получали неочищенный продукт, который очищали перекристаллизацией из этилацетата/гексана с получением указанного в заголовке соединения в виде бесцветного кристаллического твердого вещества, tпл.117-118°С. Следующие соединения получали аналогично тому, как описано выше, с использованием соответствующего амина (фирма Fluka или Aldrich, Buchs, Швейцария, или фирма, указанная в скобках). Промежуточное соединение 1б, 2-хлор-N-(4-бром-3-трифторметилфенил)-3-пиридинкарбоксамид, tпл. 173-174°С, получали с использованием 4-бром-3-трифторметиланилина. Промежуточное соединение 1в, 2-хлор-N-[3,4-бис(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 167-169°С, получали с использованием 3,4-бис(трифторметил)анилина (фирма Fluorochem, Дербишир, Англия). Промежуточное соединение 1г, 2-хлор-N-(3-фтор-5-трифторметилфенил)-3-пиридинкарбоксамид, получали с использованием 3-фтор-5-(трифторметил)анилина (фирма Fluorochem, Дербишир, Англия). Промежуточное соединение 1д, 2-хлор-N-(транс-4-трет-бутилциклогексил)-3-пиридинкарбоксамид, tпл. 135-136°C, получали с использованием транс-4-трет-бутилциклогексиламина (фирма Lancaster Synthesis, Ланкашир, Англия). Промежуточное соединение 1е, 2-хлор-N-(цис-4-трет-бутилциклогексил)-3-пиридинкарбоксамид, tпл. 171-173°С, получали с использованием цис-4-трет-бутилциклогексиламина (фирма Lancaster Synthesis, Ланкашир, Англия). Промежуточное соединение 1ж, 2-хлор-N-(4-пропилфенил)-3-пиридинкарбоксамид, tпл. 107-110°С, получали с использованием 4-н-пропиланилина. Промежуточное соединение 1з, 2-хлор-N-(4-бутилфенил)-3-пиридинкарбоксамид, tпл. 96-98°С, получали с использованием 4-н-бутиланилина. Промежуточное соединение 1и, 2-хлор-N-(4-пентилфенил)-3-пиридинкарбоксамид, tпл. 94-96°C, получали с использованием 4-н-пентиланилина. Промежуточное соединение 1к, 2-хлор-N-(5-индазолил)-3-пиридинкарбоксамид, tпл. 233-255°С, получали с использованием 5-аминоиндазола. Промежуточное соединение 1л, 2-хлор-N-(3-изохинолинил)-3-пиридинкарбоксамид, tпл. 180°С, получали с использованием 3-аминоизохинолина (фирма Maybridge Chemical Co. Ltd., Англия). Промежуточное соединение 1м, 2-хлор-N-(4-фтор-3-трифторметилфенил)-3-пиридинкарбоксамид, tпл. 140-141°С, получали с использованием 4-фтор-3-(трифторметил)анилина. Промежуточное соединение 1н, 2-хлор-N-[4-(1,1-диметилэтил)фенил]-3-пиридинкарбоксамид, tпл. 74-76°С, получали с использованием 4-трет-бутиланилина. Промежуточное соединение 1о, 2-хлор-N-[3-(1,1-диметилэтил)фенил]-3-пиридинкарбоксамид, получали с использованием 3-трет-бутиланилина (фирма Maybridge Chemical Co. Ltd., Англия). Промежуточное соединение 1п, 2-хлор-N-(2-фтор-3-трифторметилфенил)-3-пиридинкарбоксамид, tпл. 104-105°С, получали с использованием 2-фтор-3-трифторметиланилина. Промежуточное соединение 1р, 2-хлор-N-(2-метил-3-трифторметилфенил)-3-пиридинкарбоксамид, tпл. 142-143°С, получали с использованием 2-метил-3-трифторметиланилина (фирма Fluorochem, Дербишир, Англия). Промежуточное соединение 1с, 2-хлор-N-(2-метил-5-трифторметилфенил)-3-пиридинкарбоксамид, tпл. 182-183°С, получали с использованием 2-метил-5-трифторметиланилина (фирма Fluorochem, Дербишир, Англия). Промежуточное соединение 2 2-Хлор-N-[4-(1-пропинил)фенил]-3-пиридинкарбоксамид Через перемешиваемый раствор 4-броманилина (0,86 г, 5,0 ммолей) в сухом толуоле (50 мл) продували аргон в течение 10 мин. Затем добавляли трибутил-1-пропинилстаннан (2,5 г, 6,0 ммолей) и тетракис(трифенилфосфин)палладий(0) (0,15 г) и полученную смесь нагревали при 100°С в атмосфере аргона в течение 10 ч. Затем смесь охлаждали, фильтровали и упаривали при пониженном давлении, при этом получали неочищенный 4-(1-пропинил)бензоламин в виде масла. Масло растворяли в этилацетате (15 мл) и добавляли к перемешиваемому водному раствору гидроксида натрия (12 мл 1 М раствора) при комнатной температуре. Полученный перемешиваемый раствор обрабатывали по каплям в течение 30 мин раствором 2-хлорникотиноилхлорида (фирма Lancaster Synthesis, Ланкашир, Англия; 1,06 г, 6 ммолей) в сухом этилацетате (20 мл) и полученную смесь перемешивали в течение 2 ч при температуре окружающей среды. Затем смесь экстрагировали этилацетатом (3×50 мл) и объединенные экстракты последовательно промывали водой (2×40 мл), насыщенным водным раствором гидрокарбоната натрия (2×40 мл), насыщенным водным раствором хлорида натрия (1×40 мл), сушили (Na2SO4), фильтровали и растворитель выпаривали при пониженном давлении, при этом получали неочищенный продукт, который очищали хроматографией на колонке с силикагелем при элюировании раствором этилацетата (50%) в гексане и перекристаллизовывали из эфира/гексана с получением указанного в заголовке соединения в виде кристаллического твердого вещества бежевого цвета, tпл. 136-138°С. Б. Примеры Пример 1 2-[[2-(4-Пиридил)этил]амино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид 4-Пиридинэтанамин (фирма Maybridge Chemical Co., Корнуэл, Англия; 0,31 г, 2,5 ммоля) добавляли к перемешиваемой смеси 2-хлор-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамида (промежуточное соединение 1а, 0,90 г, 3 ммоля), порошкообразного карбоната калия (0,35 г, 2,5 ммоля) и иодида меди(I) (0,48 г, 2,5 ммоля) в диметилформамиде (10 мл). Полученную смесь продували аргоном и затем нагревали при 100°С в атмосфере аргона в течение 2 часов. Затем смесь охлаждали, обрабатывали водой (100 мл) и экстрагировали этилацетатом (3×80 мл). Объединенные экстракты промывали водным раствором аммиака (2×50 мл 10%-ного раствора), сушили (Na2SO4), фильтровали и растворитель выпаривали при пониженном давлении, при этом получали неочищенный продукт, который очищали хроматографией на колонке с силикагелем при элюировании этилацетатом и перекристаллизовывали из этилацетата/гексана с получением указанного в заголовке соединения в виде бесцветного кристаллического твердого вещества, tпл. 128-138°С. Пример 2 2-[(4-Пиридил)метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид Смесь промежуточного соединения 1а (6,00 г, 20 ммолей) и 4-пиридинметанамина (30 мл) перемешивали при 150°С в течение 16 ч в атмосфере аргона. Охлажденную смесь разбавляли этилацетатом (100 мл) и экстрагировали насыщенным водным раствором гидрокарбоната натрия (100 мл), водой (4×50 мл) и насыщенным водным раствором хлорида натрия (50 мл). Раствор этилацетата сушили (Na2SO4), фильтровали и растворитель выпаривали при пониженном давлении, при этом получали неочищенный продукт, который очищали хроматографией на колонке с силикагелем при элюировании этилацетатом и перекристаллизовывали из 2-пропанола/диизопропилового эфира с получением указанного в заголовке соединения в виде бесцветного кристаллического твердого вещества, tпл. 152-153°С. Соединения, описанные в примерах 3-16, получали аналогично тому, как описано в примерах 1 и 2, с использованием соответствующих аминов и необязательно с использованием других известных методов (например, деметилирование с использованием триметилсилилиодида). Пример 3 2-[(2-Метил-4-пиридил)метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 144-142°С. Пример 4 (а) 2-[(6-Метоксипирид-3-ил)метиламино]-N-[3-(трифторметил)-фенил]-3-пиридинкарбоксамид, tпл. 89-90°С. (б) Дигидрохлорид 2-[(6-метоксипирид-3-ил)метиламино]-N-[3-(трифторметил)-фенил]-3-пиридинкарбоксамида, tпл. 85°C. Пример 5 2-[(3-Метоксифенил)метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид. Пример 6 2-[(4-Пиридил)метиламино]-N-[3,4-бис(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 194-196°С. Пример 7 2-[(4-Пиридил)метиламино]-N-[3-фтор-5-(трифторметил)-фенил]-3-пиридинкарбоксамид, tпл. 195-196°С. Пример 8 2-[(4-Пиридил)метиламино]-N-(транс-4-трет-бутилциклогексил)-3-пиридинкарбоксамид, tпл. 165-167°С. Пример 9 2-[(4-Пиридил)метиламино]-N-[4-(н-пропил)фенил]-3-пиридинкарбоксамид, tпл. 147-149°С. Пример 10 2-[(4-Пиридил)метиламино]-N-[4-(н-бутил)фенил]-3-пиридинкарбоксамид, tпл. 107-108°С. Пример 11 2-[(4-Пиридил)метиламино]-N-[4-(н-пентил)фенил]-3-пиридинкарбоксамид, tпл. 106-107°С. Пример 12 2-[(4-Пиридил)метиламино]-N-[4-(1-пропинил)фенил]-3-пиридинкарбоксамид, tпл. 216-221°С. Пример 13 2-[(4-Пиридил)метиламино]-N-(5-индазолил)-3-пиридинкарбоксамид, tпл. 225-230°С. Пример 14 2-[(4-Пиридил)метиламино]-N-(3-изохинолинил)-3-пиридинкарбоксамид, tпл. 191-195°С. Пример 15 Гидрохлорид 2-(фенилметиламино)-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамида, tпл. 203-207°С. Пример 16 2-[(4-Пиридил)метиламино]-N-[4-фтор-3-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 172-173°С. Пример 17 2-[(4-Пиридил)метиламино]-N-[4-(трет-бутил)фенил]-3-пиридинкарбоксамид, tпл. 186-187°С. Пример 18 2-[(4-Пиридил)метиламино]-N-[4-((трет-бутилэтил)фенил]-3-пиридинкарбоксамид, tпл. 162-163°С. Пример 19 2-[(4-Пиридил)метиламино]-N-[2-фтор-3-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 137-140°С. Пример 20 2-[(4-Пиридил)метиламино]-N-[4-бром-3-(трифторметил)-фенил]-3-пиридинкарбоксамид, tпл. 164-165°С. Пример 21 2-[(4-Пиридил)метиламино]-N-[2-метил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 146-147°С. Пример 22 2-[(4-Пиридил)метиламино]-N-[2-метил-5-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 155-156°С. Пример 23 2-[(4-Пиридил)метиламино]-N-(цис-4-трет-бутилциклогексил)-3-пиридинкарбоксамид, tпл. 103-106°С. Пример 24 2-[(6-Метоксипирид-3-ил)метиламино]-N-[4-бром-3-(трифторметил)-фенил]-3-пиридинкарбоксамид, tпл. 124-125°С. Пример 25 2-[(6-Метоксипирид-3-ил)метиламино]-N-[2-фтор-3-(трифторметил)- фенил]-3-пиридинкарбоксамид, tпл. 107-108°С. Пример 26 2-[(6-Метоксипирид-3-ил)метиламино]-N-[2-метил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 144-146°С. Пример 27 2-[(1-Оксо-4-пиридил)метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 169-171°С. Пример 28 2-[3-(N-Метилкарбоксамидо)фенил]метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид. Смесь 2-амино-N-(3-трифторметилфенил)-3-пиридинкарбоксамида (0,56 г, 2,0 ммоля), 3-формил-N-метилбензамида (0,50 г, 2,4 ммоля) и уксусной кислоты (0,5 мл) в метаноле (50 мл) перемешивали при 25°С в атмосфере аргона в течение 12 ч. Затем порциями в течение 30 мин добавляли цианборгидрид натрия (0,40 г 90%-ного раствора, 5,75 ммоля), смесь перемешивали в течение 8 ч, разбавляли дихлорметаном (100 мл) и обрабатывали насыщенным водным раствором гидрокарбоната натрия (50 мл). Затем смесь перемешивали еще в течение 5 мин и фильтровали, при этом получали неочищенный продукт, который очищали кристаллизацией из изопропанола с получением указанного в заголовке соединения в виде бесцветного кристаллического твердого вещества, tпл. 208-210°С. Пример 29 2-[(1-Метилпиридин-2(1Н)-он-5-ил)метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид 2-[(6-Метоксипирид-3-ил)метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид нагревали при 140°С в течение 18 ч, при этом получали неочищенный продукт, который очищали хроматографией на колонке с силикагелем при элюировании раствором этанола (10%-ным) в дихлорметане и перекристаллизовывали из этилацетата с получением указанного в заголовке соединения в виде кристаллического твердого вещества бежевого цвета, tпл. 224-225°С. Пример 30 2-[(6-Метоксипирид-3-ил)метиламино]-N-[4-пропинил-3-(трифторметил)фенил]-3-пиридинкарбоксамид Перемешиваемый раствор 2-[(6-метоксипирид-3-ил)метиламино]-N-[4-бром-3-(трифторметил)фенил]-3-пиридинкарбоксамида (см. пример 24, 0,96 г, 2,0 ммоля) в сухом толуоле (50 мл) продували аргоном при 40°С в течение 20 мин. Затем добавляли трибутил-1-пропинилстаннан (1,0 г, 2,4 ммоля) и тетракис(трифенилфосфин)палладий(0) (60 мг) и полученную смесь нагревали при 100°С в атмосфере аргона в течение 30 ч. Смесь охлаждали, обрабатывали водным раствором гидроксида натрия (20 мл 0,1 М раствора), продували воздухом в течение 2 ч и полученную смесь разбавляли этилацетатом (200 мл). Органическую фазу последовательно промывали водой (2×40 мл), насыщенным водным раствором хлорида натрия (1×40 мл), сушили (Na2SO4), фильтровали и растворитель выпаривали при пониженном давлении, при этом получали неочищенный продукт, который очищали хроматографией на колонке с силикагелем при элюировании раствором этилацетата (50%-ным) в гексане и перекристаллизовывали из эфира/гексана с получением указанного в заголовке соединения в виде кристаллического твердого вещества светло-желтого цвета, tпл. 109-111°C. Соединения, описанные в примерах 31-32, получали аналогично тому, как описано в примере 30, с использованием соответствующего арилбромида. Пример 31 2-[(4-Пиридил)метиламино]-N-[4-пропинил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 213-217°С, получали с использованием 2-[(4-пиридил)метиламино]-N-[4-бром-3-(трифторметил)фенил]-3-пиридинкарбоксамида (см. пример 20). Пример 32 2-[(Пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-пропинил-3-трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 211-218°С, получали с использованием 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-бром-3-(трифторметил)фенил]-3-пиридинкарбоксамида(см. пример 35). Пример 33 2-[(Пиридин-2(1Н)-он-5-ил)метил]амино-N-[3-трифторметил)фенил]-3-пиридинкарбоксамид. Смесь 2-[(6-метоксипирид-3-ил)метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамида (см. пример 4; 1,4 г, 3,5 ммоля) и триметисилилиодида (фирма Fluka, Buchs, Швейцария; 1,4 мл, 10,3 ммоля) в хлороформе (30 мл) перемешивали при 60°С в течение 10 мин. Охлажденную смесь обрабатывали метанолом (2 мл) и перемешивали при комнатной температуре в течение 10 мин. Растворитель выпаривали при пониженном давлении, остаток обрабатывали водным раствором аммиака (100 мл 10%-ного раствора) и экстрагировали этилацетатом (3×100 мл). Объединенные экстракты промывали насыщенным раствором хлорида натрия (50 мл), сушили (Na2SO4), фильтровали и растворитель упаривали при пониженном давлении, при этом получали неочищенный продукт, который очищали перекристаллизацией из горячего этилацетата с получением указанного в заголовке соединения в виде бесцветного кристаллического твердого вещества, tпл. 200-202°C. Соединения, описанные в примерах 34-38, получали аналогично тому, как описано в примере 33, с использованием соответствующего метоксипиридина. Пример 34 2-[(3-Гидроксифенил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 143-146°С, получали с использованием 2-[(3-метоксифенил)метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамида (см. пример 5). Пример 35 2-[(Пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-бром-3-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 202-205°C, получали с использованием 2-[(6-метоксипирид-3-ил)метиламино]-N-[4-бром-3-(трифторметил)фенил]-3-пиридинкарбоксамида (см. пример 24). Пример 36 2-[(Пиридин-2(1Н)-он-5-ил)метил]амино-N-[2-фтор-3-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 219-222°C, получали с использованием 2-[(6-метоксипирид-3-ил)метиламино]-N-[2-фтор-3-(трифторметил)фенил]-3-пиридинкарбоксамида (см. пример 25). Пример 37 2-[(Пиридин-2(1Н)-он-5-ил)метил]амино-N-[2-метил-3-трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 196-201°С, получали с использованием 2-[(6-метоксипирид-3-ил)метиламино]-N-[2-метил-3-(трифторметил)фенил]-3-пиридинкарбоксамида (см. пример 26). Пример 38 2-[(Пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-пропил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 220-224°С, получали с использованием 2-[(6-метоксипирид-3-ил)метиламино]-N-[4-пропил-3-(трифторметил)фенил]-3-пиридинкарбоксамида(см. пример 39). Пример 39 2-[(6-Метоксипирид-3-ил)метиламино]-N-[4-пропил-3-(трифторметил)фенил]-3-пиридинкарбоксамид. Раствор 2-[(6-метоксипирид-3-ил)метиламино]-N-[4-пропинил-3-(трифторметил)-фенил]-3-пиридинкарбоксамида (см. пример 30; 1,87 г, 4,25 ммоля) в метаноле (100 мл) гидрировали при атмосферном давлении в присутствии катализатора платина на угле (5%Pt/C) (0,4 г) при 22°С. Рассчитанное количество водорода поглощалось в течение 13 ч. Затем смесь фильтровали, растворитель выпаривали при пониженном давлении, при этом получали неочищенный продукт, который очищали перекристаллизацией из дихлорметана/гексана с получением указанного в заголовке соединения в виде бесцветного кристаллического твердого соединения, tпл. 51-61°С. Пример 40 2-[(4-Пиридил)метил]амино-N-[4-(н-пропил)-3-(трифторметил)фенил]-3-пиридинкарбоксамид, tпл. 147-149°С, получали аналогично тому, как описано в примере 39, с использованием 2-[(4-пиридил)метиламино]-N-[4-пропинил-3-(трифторметил)фенил]-3-пиридинкарбоксамида (см. пример 31). Пример 41 Следующие соединения могут быть получены аналогично тому, как описано выше. Пример 41а 2-[(4-Пиридил)метил]амино-N-(5-тиазолил)-3-пиридинкарбоксамид. Пример 41б 2-[(4-Гидроксифенил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид. Пример 41в 2-(4-Пиридил)метил]амино-N-(бензо[d]пиразол-5-ил)-3-пиридинкарбоксамид. Пример 41г 2-[(6-Метокси-3-пиридил)метил]амино-N-(3-изохинолинил)-3-пиридинкарбоксамид. Пример 41д 2-[(6-Метокси-3-пиридил)метил]амино-N-(бензо[d]пиразол-5-ил)-3-пиридинкарбоксамид. Пример 41е 2-[(Пиридин-2(1Н)-он-5-ил)метил]амино-N-(3-изохинолинил)-3-пиридинкарбоксамид. Пример 41ж 2-[(Пиридин-2(1Н)-он-5-ил)метил]амино-N-(бензо[d]пиразол-5-ил)-3-пиридинкарбоксамид. Пример 41з 2-[(Пиридин-2(1Н)-он-5-ил)метил]амино-N-(цис-4-трет-бутилциклогексил)-3-пиридинкарбоксамид. Пример 41и 2-[(Пиридин-2(1Н)-он-5-ил)метил]амино-N-(транс-4-трет-бутилциклогексил)-3-пиридинкарбоксамид. Пример 41к 2-[(1-Оксидо-4-пиридил)метиламино]-N-[4-пропил-3-(трифторметил)-фенил]-3-пиридинкарбоксамид. Пример 41л 2-[(Пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-этил-3-(трифторметил)фенил]-3-пиридинкарбоксамид. Пример 41м 2-[(Пиридин-2(1Н)-он-5-ил)метил]амино-N-[3,4-бис(трифторметил)фенил]-3-пиридинкарбоксамид. Пример 41н 2-[(1-Метилпиридин-2(1Н)-он-5-ил)метиламино]-N-[3,4-бис(трифторметил)фенил]-3-пиридинкарбоксамид. Пример 42 Мягкие капсулы 5000 мягких желатиновых капсул, каждая из которых включает в качестве активного ингредиента 0,05 г одного из соединений формулы I, упомянутых в предыдущих примерах, получали следующим образом: Состав
Методика получения: порошкообразный активный компонент суспендировали в лаурогликоле (лаурат пропиленгликоля, фирма Gattefosse S.A., Saint Priest, Франция) и измельчали с помощью влажного пульверизатора с получением частиц размером от 1 до 3 мкм. Затем полученной смесью порциями по 0,419 г заполняли мягкие капсулы из желатина с использованием устройства для наполнения капсул.
Формула изобретения
1. Способ ингибирования активности эндотелиального фактора роста сосудов (VEGF) рецепторной тирозинкиназы, включающий введение соединения формулы I
где n равно от 1 до 6 включительно; W означает О; R1 и R3 независимо друг от друга каждый означает водород, C1-C7алкил или C1-C7ацил; R2 означает группу циклоалкил, незамещенный, моно- или полизамещенный арил, незамещенный, моно- или полизамещенный моно- или бициклический гетероарил, содержащий один или два атома азота; R и R’ независимо друг от друга каждый означает водород или C1-C7алкил; Х означает группу циклоалкил, незамещенный, моно- или полизамещенный арил, полизамещенный, незамещенный, моно- или полизамещенный моно- или бициклический гетероарил, содержащий один или два атома азота, или фармацевтически приемлемой соли такого соединения, в количестве, эффективном для ингибирования VEGF-рецепторной тирозинкиназы 2. Соединение формулы I
где n равно от 1 до 6 включительно; W означает О; R1 и R3 независимо друг от друга каждый означает водород, C1-C7алкил или C1-C7ацил; R2 означает группу циклоалкил, незамещенный, моно- или полизамещенный арил, незамещенный, моно- или полизамещенный моно- или бициклический гетероарил, содержащий один или два атома азота; R и R’ независимо друг от друга каждый означает водород или C1-C7алкил; Х означает группу циклоалкил, незамещенный, моно- или полизамещенный арил, незамещенный, моно- или полизамещенный моно- или бициклический гетероарил, содержащий один или два атома азота; или фармацевтически приемлемая соль такого соединения, за исключением соединений формулы I, где n равно 1, W означает О, R1, R3, R, R’ означают водород, Х означает фенил, а R2 означает 3-трифторметилфенил или 2-метоксифенил или 2-хлор-3-пиридил, или Х означает 4-метоксифенил, a R2 означает 2-хлор-3-пиридил, или Х означает 4-пиридил, a R2 означает 4-[3-(3-пиридил)-5-трифторметилпиразол-1-ил]фенил, и соединения формулы I, где n равно 1, W означает О, R3, R, R’ означают водород, R1 означает метил, R2 означает 2-хлор-3-пиридил, а Х означает фенил. 3. Соединение формулы I по п.2, где n равно от 1 до 6 включительно; W означает О; R1 и R3 независимо друг от друга каждый означает водород, C1-C7алкил или C1-C7ацил; R2 означает группу циклоалкил, группу арил или моно- или бициклическую группу гетероарил, содержащую один или два атома азота, причем две последние группы в каждом случае являются незамещенными или могут иметь вплоть до трех заместителей, выбранных из ряда амино, моно- или дизамещенный амино, галоген, C1-C7алкил, замещенный алкил, C1-C7алкенил, C1-C7алкинил, C1-C7алканоил, гидрокси, простой или сложный эфир гидроксигруппы, нитро, циано, карбокси, этерифицированный карбокси, алканоил, бензоил, карбамоил, N-моно- или N,N-дизамещенный карбамоил, амидино, гуанидино, уреидо, меркапто, сульфо, C1-C7алкилтио, фенил, фенокси, фенилтио, фенил C1-C7алкилтио, алкилфенилтио, C1-C7алкилсульфинил, фенилсульфинил, фенил C1-C7алкилсульфинил, алкилфенилсульфинил, C1-C7алкансульфонил, фенилсульфонил, фенил C1-C7алкилсульфонил, алкилфенилсульфонил, галоген C1-C7алкилмеркапто, галогенС1-C7алкилсульфонил, дигидроксибора(-В(ОН)2), гетероциклил и C1-C7алкилендиокси, связанный с соседними атомами углерода в цикле; R и R’ независимо друг от друга каждый означает водород или C1-C7алкил; Х означает группу арил или моно- или бициклическую группу гетероарил, содержащую один или два атома азота, где термин «моно- или бициклическая гетероарильная группа» включает, не ограничиваясь перечисленным, радикал (1Н)2-он-пиридинил, причем группы в каждом случае являются незамещенными или могут содержать вплоть до трех заместителей, выбранных из ряда амино, моно- или дизамещенный амино, галоген, C1-C7алкил, замещенный алкил, C1-C7алкенил, C1-C7алкинил, C1-C7алканоил, гидрокси, простой или сложный эфир гидроксигруппы, нитро, циано, карбокси, этерифицированный карбокси, алканоил, бензоил, карбамоил, N-моно- или N,N-дизамещенный карбамоил, амидино, гуанидино, уреидо, меркапто, сульфо, C1-C7алкилтио, фенил, фенокси, фенилтио, фенил C1-C7алкилтио, алкилфенилтио, C1-C7алкилсульфинил, фенилсульфинил, фенил C1-C7алкилсульфинил, алкилфенилсульфинил, C1-C7алкансульфонил, фенилсульфонил, фенил C1-C7алкилсульфонил, алкилфенилсульфонил, галоген C1-C7алкилмеркапто, галоген C1-C7алкилсульфонил, дигидроксибора(-В(ОН)2), гетероциклил и C1-C7алкилендиокси, связанный с соседними атомами углерода в цикле; или фармацевтически приемлемая соль такого соединения, за исключением соединений формулы I, где n равно 1, W означает О, R1, R3, R, R’ означают водород, Х означает фенил, a R2 означает 3-трифторметилфенил, 2-метоксифенил или 2-хлор-3-пиридил, или Х означает 4-пиридил, a R2 означает фенил, замещенный в положении 4 незамещенной или замещенной группой 1-пиразолил, и соединения формулы I, где n равно 1, W означает О, R3, R, R’ означают водород, R1 означает метил, R2 означает 2-хлор-3-пиридил, а Х означает фенил. 4. Соединение формулы I по п.2, где n равно от 1 до 3 включительно; W означает О; R1 и R3 независимо друг от друга каждый означает водород, C1-C7алкил или C1-C7ацил; R2 означает циклогексил, фенил, индазолил, тиазолил, бензо[d]тиазолил, бензо[d]пиразолил или изохинолинил, который в каждом случае является незамещенным или моно- или дизамещенным C1-C7алкилом, C1-C7алкенилом или C1-C7алкинилом; где каждый радикал R2 может быть незамещенным или моно- или полизамещенным галогеном; R и R’ независимо друг от друга каждый означает водород или C1-C7алкил; Х означает фенил, пиридил, пиримидил или хинолил, который в каждом случае является незамещенным или моно- или полизамещенным группой оксо, гидрокси, C1-C7алкил, C1-C7алкокси или N- C1-C7алкилкарбамоил; или фармацевтически приемлемая соль такого соединения, за исключением соединений формулы I, где n равно 1, W означает О, R1, R3, R, R’ означают водород, Х означает фенил, a R2 означает 3-трифторметилфенил или 2-метоксифенил. 5. Соединение формулы I по п.2, где n равно 1 или 2; W означает О; R1 и R3 означают водород; R2 означает циклогексил, фенил, индазолил, тиазолил или изохинолинил, который в каждом случае является незамещенным или моно- или дизамещенным C1-C7алкилом или C1-C7алкинилом; где каждый радикал R2 может быть незамещенным или моно- или полизамещенным галогеном; R и R’ независимо друг от друга каждый означает водород или C1-C7алкил; Х означает фенил, пиридил, пиримидил или хинолил, который в каждом случае является незамещенным или моно- или полизамещенным группой оксо, гидрокси, C1-C7алкил, C1-C7алкокси или C1-C7алкилкарбамоил; или фармацевтически приемлемая соль такого соединения, за исключением соединений формулы I, где n равно 1, R, R’ означают водород, Х означает фенил, a R2 означает 3-трифторметилфенил или 2-метоксифенил. 6. Соединение формулы I по п.2, выбранное из группы соединений, включающей 2-[2-(4-пиридил)этил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(2-метил-4-пиридил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(6-метокси-3-пиридил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-[3,4-бис(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-[5-фтор-3-трифторметилфенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(транс-4-трет-бутилциклогексан)-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(4-н-пропилфенил)-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(4-н-бутилфенил)-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(4-н-пентилфенил)-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-[4-(1-пропинил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(5-индазолил)-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(3-изохинолинил)-3-пиридинкарбоксамид, 2-[(пиридин-6(1Н)-он-3-ил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид и их фармацевтически приемлемые соли. 7. Соединение формулы I по п.2, выбранное из группы соединений, включающей гидрохлорид 2-(фенилметиламино)-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамида, 2-[(4-пиридил)метиламино]-N-[2-фтор-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метиламино]-N-[4-бром-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метиламино]-N-[2-метил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метиламино]-N-[2-метил-5-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метиламино]-N-(цис-4-трет-бутилциклогексил)-3-пиридинкарбоксамид, 2-[(6-метоксипирид-3-ил)метиламино]-N-[4-бром-3-(трифторметил)-фенил]-3-пиридинкарбоксамид, 2-[(6-метоксипирид-3-ил)метиламино]-N-[2-фтор-3-(трифторметил)-фенил]-3-пиридинкарбоксамид, 2-[(6-метоксипирид-3-ил)метиламино]-N-[2-метил-3-(трифторметил)-фенил]-3-пиридинкарбоксамид, 2-[(1-оксидо-4-пиридил)метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[3-(N-метилкарбоксамидо)фенил]метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(1-метилпиридин-2(1Н)-он-5-ил)метиламино]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(6-метоксипирид-3-ил)метиламино]-N-[4-пропинил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метиламино]-N-[4-пропинил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-пропинил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-]-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(3-гидроксифенил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-бром-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[2-фтор-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-]-N-[2-метил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-пропил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(6-метоксипирид-3-ил)метиламино]-N-[4-пропил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-[4-(н-пропил)-3-(трифторметил)-фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(5-тиазолил)-3-пиридинкарбоксамид, 2-[(4-гидроксифенил)метил]амино-N-[3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(4-пиридил)метил]амино-N-(бензо[d]пиразол-5-ил)-3-пиридинкарбоксамид, 2-[(6-метокси-3-пиридил)метил]амино-N-(3-изохинолинил)-3-пиридинкарбоксамид, 2-[(6-метокси-3-пиридил)метил]амино-N-(бензо[d]пиразол-5-ил)-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-(3-изохинолинил)-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-(бензо[d]пиразол-5-ил)-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-(цис-4-трет-бутилциклогексил)-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-(транс-4-трет-бутилциклогексил)-3-пиридинкарбоксамид, 2-[(1-оксидо-4-пиридил)метиламино]-N-[4-пропил-3-(трифторметил)-фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[4-этил-3-(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(пиридин-2(1Н)-он-5-ил)метил]амино-N-[3,4-бис(трифторметил)фенил]-3-пиридинкарбоксамид, 2-[(1-метилпиридин-2(1Н)-он-5-ил)метиламино]-N-[3,4-бис(трифторметил)фенил]-3-пиридинкарбоксамид и их фармацевтически приемлемые соли. 8. Фармацевтическая композиция, ингибирующая активность эндотелиального фактора роста сосудов – рецепторной тирозинкиназы, включающая соединение формулы I по любому из пп.2-7 или его фармацевтически приемлемую соль в эффективном для ингибирования количестве, и по меньшей мере один фармацевтически приемлемый носитель. 9. Способ получения соединения формулы I по п.2 или его N-оксида, или фармацевтически приемлемой соли, который характеризуется тем, что производное пиридина формулы II
где W, R1 и R2 имеют значения, указанные для соединения формулы I, a Y означает галоген, взаимодействует с амином формулы III
где n, R, R’, R3 и Х имеют значения, указанные для соединения формулы I, в присутствии основания и соединения меди(I), необязательно в присутствии инертного растворителя; где вышеупомянутые исходные соединения II и III при необходимости могут также присутствовать с защищенными функциональными группами и/или в форме солей, при условии, что такая солеобразующая группа в соединении присутствует и реакция в солевой форме возможна; любые защитные группы в защищенном производном соединения формулы I удаляют; и, если необходимо, полученное соединение формулы I превращают в другое соединение формулы I или в соль, полученную соль соединения формулы I превращают в свободное соединение или другую соль.
|
||||||||||||||||||||||||||

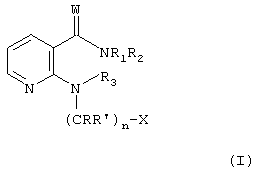
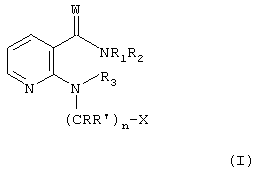
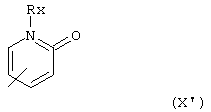
 HCl, рН 7,5, 3 мМ дихлорид марганца (MnCl2), 3 мМ хлорид магния (MgCl2), 10 мкМ ванадат натрия, 0,25 мг/мл полиэтиленгликоль (PEG) 20000, 1 мМ дитиотреит и 3 мкг/мкл поли(глу, тир) 4:1 (фирма Sigma, Buchs, Швейцария), 8 мкМ [33P]АТФ (0,2 мкКи), 1% диметилсульфоксид, и от 0 до 100 мкМ анализируемого соединения, инкубируют при комнатной температуре в течение 10 мин, после чего реакцию останавливают добавлением 10 мкл 0,25 М раствора этилендиаминтетраацетата (ЭДТА) с рН 7. Затем многоканальной пипеткой-дозатором (фирма Lab Systems, США) отбирают аликвотные части объемом 20 мкл, которые через микротитрационный фильтр Gibco-BRL наносят на поливинилдифторидную мембрану Immobilon P (фирма Millipor, США) и подключают к вакуумной линии. После полного удаления жидкости мембрану четырежды последовательно промывают в бане, содержащей 0,5% раствор фосфорной кислоты (Н3PO4), и однократно промывают этанолом, инкубируя в каждом случае при встряхивании в течение 10 мин, а затем помещают в счетчик импульсов TopCount Manifold (фирма Hewlett Packard) и после добавления 10 мкл сцинтилляционной жидкости Microscint (для счета
HCl, рН 7,5, 3 мМ дихлорид марганца (MnCl2), 3 мМ хлорид магния (MgCl2), 10 мкМ ванадат натрия, 0,25 мг/мл полиэтиленгликоль (PEG) 20000, 1 мМ дитиотреит и 3 мкг/мкл поли(глу, тир) 4:1 (фирма Sigma, Buchs, Швейцария), 8 мкМ [33P]АТФ (0,2 мкКи), 1% диметилсульфоксид, и от 0 до 100 мкМ анализируемого соединения, инкубируют при комнатной температуре в течение 10 мин, после чего реакцию останавливают добавлением 10 мкл 0,25 М раствора этилендиаминтетраацетата (ЭДТА) с рН 7. Затем многоканальной пипеткой-дозатором (фирма Lab Systems, США) отбирают аликвотные части объемом 20 мкл, которые через микротитрационный фильтр Gibco-BRL наносят на поливинилдифторидную мембрану Immobilon P (фирма Millipor, США) и подключают к вакуумной линии. После полного удаления жидкости мембрану четырежды последовательно промывают в бане, содержащей 0,5% раствор фосфорной кислоты (Н3PO4), и однократно промывают этанолом, инкубируя в каждом случае при встряхивании в течение 10 мин, а затем помещают в счетчик импульсов TopCount Manifold (фирма Hewlett Packard) и после добавления 10 мкл сцинтилляционной жидкости Microscint (для счета  -импульсов) измеряют радиоактивность. Значения IC50 рассчитывают с использованием линейного регрессионного анализа в виде процента ингибирования каждым соединением при трех концентрациях (как правило, 0,01, 0,1 и 1 мкмоль). IC50 соединений формулы I имеют значения в диапазоне от 1 до 1000 нМ, предпочтительно в диапазоне от 1 до 100 нМ.
-импульсов) измеряют радиоактивность. Значения IC50 рассчитывают с использованием линейного регрессионного анализа в виде процента ингибирования каждым соединением при трех концентрациях (как правило, 0,01, 0,1 и 1 мкмоль). IC50 соединений формулы I имеют значения в диапазоне от 1 до 1000 нМ, предпочтительно в диапазоне от 1 до 100 нМ. HTRF-96, фирма Packard). Затем планшеты промывают и свободные связывающие белки участки насыщают 1% раствором БСА в ФБС. Затем в этих планшетах инкубируют клеточные лизаты (20 мкг белка в лунку) при 4°С в течение ночи в смеси с антителами к фосфотирозину, коньюгированными с щелочной фосфатазой (PY20:AP, производства Transduction Laboratories). Планшеты снова промывают, а затем связывание антифосфотирозиновых антител с иммобилизованным фосфорилированным рецептором определяют визуально с использованием люминесцентного АР субстрата (CDP-Star, готового к применению, в смеси с Emerald II; фирма Tropix). Люминесценцию измеряют в сцинтиляционном счетчике для микропланшетов (Packard Top Count). Разность между сигналом положительного контроля (стимулированного VEGF) и сигналом отрицательного контроля (не стимулированного VEGF) соответствует фосфорилированию (=100%) KDR-рецептора, индуцированному VEGF. Активность анализируемых соединений рассчитывают как процент ингибирования фосфорилирования KDR-рецептора, индуцированного VEGF, при этом концентрацию соединения, при которой наблюдается ингибирование, равное половине от максимума, определяют как ED50 (эффективная доза, вызывающая 50%-ное ингибирование). Соединения формулы I предпочтительно имеют значения ED50 в диапазоне от 0,25 нМ до 1000 нМ, предпочтительно от 0,25 нМ до 250 нМ.
HTRF-96, фирма Packard). Затем планшеты промывают и свободные связывающие белки участки насыщают 1% раствором БСА в ФБС. Затем в этих планшетах инкубируют клеточные лизаты (20 мкг белка в лунку) при 4°С в течение ночи в смеси с антителами к фосфотирозину, коньюгированными с щелочной фосфатазой (PY20:AP, производства Transduction Laboratories). Планшеты снова промывают, а затем связывание антифосфотирозиновых антител с иммобилизованным фосфорилированным рецептором определяют визуально с использованием люминесцентного АР субстрата (CDP-Star, готового к применению, в смеси с Emerald II; фирма Tropix). Люминесценцию измеряют в сцинтиляционном счетчике для микропланшетов (Packard Top Count). Разность между сигналом положительного контроля (стимулированного VEGF) и сигналом отрицательного контроля (не стимулированного VEGF) соответствует фосфорилированию (=100%) KDR-рецептора, индуцированному VEGF. Активность анализируемых соединений рассчитывают как процент ингибирования фосфорилирования KDR-рецептора, индуцированного VEGF, при этом концентрацию соединения, при которой наблюдается ингибирование, равное половине от максимума, определяют как ED50 (эффективная доза, вызывающая 50%-ное ингибирование). Соединения формулы I предпочтительно имеют значения ED50 в диапазоне от 0,25 нМ до 1000 нМ, предпочтительно от 0,25 нМ до 250 нМ.