|
|
(21), (22) Заявка: 2004116216/15, 28.05.2004
(24) Дата начала отсчета срока действия патента:
28.05.2004
(43) Дата публикации заявки: 10.11.2005
(46) Опубликовано: 20.03.2007
(56) Список документов, цитированных в отчете о
поиске:
АНДРЕЕВ Б.М. и др., Разделение стабильных изотопов физико-химическими методами, Москва, Энергоатомиздат, 1982, сс.44-49, 68-69, 75-79. RU 2031085 C1, 20.03.1995. RU 2060861 C1, 27.05.1996. RU 2091335 C1, 27.09.1997. RU 2091336 C1, 27.09.1997. RU 2098452 C1, 10.12.1997. RU 2101982 C1, 20.01.1998. RU 2125817 C1, 10.02.1999. RU 2139062 C1, 10.10.1999. RU 2182562 C2, 20.05.2001.
Адрес для переписки:
125222, Москва, ул. Генерала Белобородова, 27, кв. 78, Н.Д.Тепловой
|
(72) Автор(ы):
Соловьев Сергей Павлович (RU)
(73) Патентообладатель(и):
Соловьев Сергей Павлович (RU)
|
(54) СПОСОБ И УСТАНОВКА ДЛЯ ПРОИЗВОДСТВА ЛЕГКОЙ ВОДЫ
(57) Реферат:
Изобретение может быть использовано при проведении технологических процессов, получении лекарственных, парфюмерно-косметических средств и питьевой воды. Установка включает ректификационную колонну с контактным устройством для увеличения поверхности для взаимодействия пар-жидкость, узел приготовления водяного пара из исходной воды с концентрацией 1H2 16O, равной C1, узел подачи водяного пара в ректификационную колонну, узел конденсации водяного пара с концентрацией 1Н2 16O, равной C2, в конденсаторе, установленном в верхней части ректификационной колонны, причем C2>C1. Способ по изобретению предусматривает накопление части конденсата в виде конденсированной легкой воды. Ректификационная колонна представляет собой узел взаимодействия пар-жидкость между нисходящим потоком жидкости и восходящим потоком пара на поверхности расположенного внутри контактного устройства, при направлении основного потока жидкости и основного потока пара вдоль оси колонны. Давление пара в ректификационной колонне 0,05-0,6 бар, выход конденсированной легкой воды – 0,001-0,25 от общего объема водяного пара, прошедшего через ректификационную колонну. Контактное устройство может быть выполнено в виде тарелок, структурированной или рандомизированной насадки. Изобретение позволяет получить в промышленных масштабах легкую воду с содержанием 1Н2 16O не менее 997,13 г/кг и суммарным содержанием 1Н2 17O, 1Н2 18O, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O не более 2,87 г/кг от общего количества H2O. 2 н. и 8 з.п. ф-лы, 1 ил., 2 табл.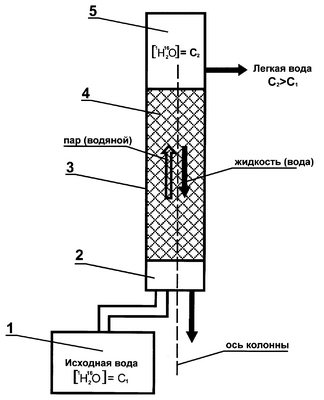
Изобретение относится к способу и устройству для очистки воды от примесей в виде молекул воды, содержащих в своем составе тяжелые изотопы водорода и кислорода, а более конкретно – к способу и установке для получения легкой, особо чистой воды с повышенным содержанием в ней доли молекул 1Н2 16О.
Вода с точки зрения химии является веществом, состоящим из молекул Н2О. В природе совершенно чистой воды не существует. Природная вода всегда в той или иной мере содержит механические, химические и биологические примеси.
На сегодняшний день проблема очистки воды для ее использования в различных отраслях промышленности стоит очень остро.
В зависимости от предполагаемого применения вода подвергается разным способам очистки. Фильтрация, дистилляция, использование эффекта обратного осмоса позволяют получать воду с необходимой степенью чистоты: дистиллированную, деионизированную, при этом стерильную или нестерильную, апирогенную и т.д. и т.п. Количество механических, химических, биологических примесей может быть снижено до весьма низких уровней, например, при использовании методов с применением процесса осмоса. Однако традиционные способы очистки не изменяют изотопный состав молекул Н2О, в результате чего остаются молекулы воды, содержащие тяжелые изотопы водорода и кислорода, в среднем в природной воде суммарно по весу до 2,97 г/кг (расчеты приведены далее).
Общеизвестно, что молекула воды Н2О состоит из двух химических элементов – водорода Н и кислорода О. В свою очередь каждый элемент представляет собой совокупность нескольких изотопов [1].
В дальнейшем в тексте:
– понятие «водород» (буквенное обозначение: H) подразумевает под собой химический элемент как совокупность всех возможных изотопов водорода;
– понятие «кислород» (буквенное обозначение: O) подразумевает под собой химический элемент как совокупность всех возможных изотопов кислорода;
– понятие «вода» подразумевает под собой любую реальную воду, в том числе природную или полученную промышленным способом, представляющую собой смесь Н2О и большого числа различных веществ в виде механических примесей, растворенных газов, солей, биологических примесей и т.д., подлежащих или не подлежащих удалению в зависимости от дальнейшего применения воды;
– буквенное обозначение Н2О подразумевает под собой совокупность всех возможных изотопных разновидностей молекул воды, образованных изотопами химических элементов – водорода H и кислорода O;
Водород в природе представлен стабильными нерадиоактивными изотопами:
– протием (буквенное обозначение 1Н);
– дейтерием (буквенное обозначение 2H, историческое обозначение D, далее по тексту используются буквенные обозначения D, либо равнозначное 2Н).
Кислород, в свою очередь, представлен тремя стабильными нерадиоактивными изотопами:
– кислородом-16 (буквенное обозначение 16О);
– кислородом-17 (буквенное обозначение 17О);
– кислородом-18 (буквенное обозначение 18О).
Данное изобретение касается только вышеперечисленных стабильных нерадиоактивных изотопов.
Стабильные изотопы водорода со стабильными изотопами кислорода образуют 9 изотопных разновидностей молекул воды, а именно: 1Н2 16О, 1Н2 17О, 1H2 18O, 1HD16О, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O. В количественном отношении основная масса воды природных источников представлена молекулами 1Н2 16О, состоящими из легких изотопов 1Н и 16О. Количество молекул воды, содержащих тяжелые изотопы: D, 17O, 18O, зависит от концентрации указанных изотопов, которая в природной воде колеблется в пределах, зафиксированных в основных стандартах изотопного состава гидросферы SMOW и SLAP.
Объем запасов воды в различных резервуарах гидросферы Земли равен примерно 1834 млн м3. Из них доля вод Мирового океана составляет 1370 млн м3, речных и озерных вод – 0,231 млн м3, ледниковых вод – 24 млн м3 и т.д. [2].
Поскольку основная часть воды на Земле сосредоточена в Мировом океане и океаническая вода весьма стабильна по изотопному составу, количественное содержание тяжелых изотопов D и 18O в ней принято в качестве международного стандарта SMOW (стандарт среднеокеанической воды).
Для стандарта SMOW отношение содержания в воде дейтерия к протию составляет D/H=155,76×10-6, а отношение содержания изотопов кислорода составляет 18О/16О=2005,20×10-6 [3].
Концентрация изотопов D, 17О, 18О в воде может выражаться либо в долях, либо в атомных процентах (ат. % или 0/00), либо в единицах ppm (part per million – часть на миллион) [2, 4]. Сумма концентраций протия и D, равно как и сумма концентраций трех изотопов кислорода, равна 100 ат.% или миллиону (в единицах ppm).
По международному стандарту SMOW абсолютное содержание дейтерия и кислорода-18 в океанической воде составляет:
DSMOW/1HSMOW=(155,76±0,05)×10-6, или 155,76 ppm
18OSMOW/16OSMOW=(2005,20±0,45)×10-6, или 2005 ppm [3].
Именно эти значения в стандарте SMOW приняты за точку отсчета. Существуют относительные единицы, выражающие содержание дейтерия и кислорода-18 в молекулах воды, приравненные к нулю и обозначаемые для дейтерия как  D=00/00 (или 155,76 ppm), для кислорода-18 D=00/00 (или 155,76 ppm), для кислорода-18  18O=00/00 (или 2005,2 ppm). 18O=00/00 (или 2005,2 ppm).
В образцах проб воды с содержанием изотопных разновидностей молекул Н2О отличающимся от SMOW, величины  D и D и  18O выражаются в 0/00 в виде относительного отклонения от нулевого значения в большую (со знаком +) или меньшую (со знаком -) сторону. 18O выражаются в 0/00 в виде относительного отклонения от нулевого значения в большую (со знаком +) или меньшую (со знаком -) сторону.
Для расчета единиц  D и D и  18O используется следующая формула [5]: 18O используется следующая формула [5]:
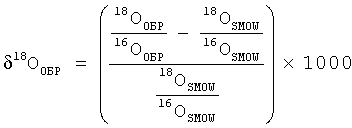
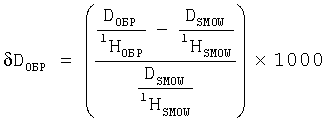
В результате проведения математических преобразований и подстановок значений вышеуказанных величин получаем следующую формулу для пересчета концентрации из относительных величин  D и D и  18O в единицы ppm: 18O в единицы ppm:
(D) ppm=155,76 ( D/1000+1) D/1000+1)
(18О) ppm=2005,2 ( 18O/1000+1), 18O/1000+1),
где (D) ppm и (О) ppm содержание соответственно D и 18О, выраженное в ppm.
Наименьшие концентрации дейтерия и кислорода-18, обнаруженные в природной воде, описываются международным стандартом SLAP (стандарт легких антарктических осадков). Концентрация дейтерия по SLAP составляет D/H=89×10-6 (89 ppm или  D=-4280/00). Концентрация кислорода-18 по SLAP составляет 18O/16O=1894×10-6 (1894 ppm или D=-4280/00). Концентрация кислорода-18 по SLAP составляет 18O/16O=1894×10-6 (1894 ppm или  18O=-55,50/00) [3]. 18O=-55,50/00) [3].
Изменение концентрации кислорода-17 в природных водах в связи с его физико-химическими свойствами достаточно жестко связано с изменением концентрации кислорода-18. По данным разных авторов соотношение концентраций 18О/17О находится в пределах от 4,9 до 5,5 [6, 7]. Таким образом, концентрация кислорода-17 в природных водах по SMOW составляет 390 ppm (0,039 ат.%), а по SLAP может снижаться до 368 ppm (0,0368 ат.%) [2, 3, 6].
Вышеприведенные стандартные значения концентраций тяжелых изотопов дают возможность подсчитать процентное и, в конечном итоге, весовое количество изотопных разновидностей молекул в воде из природных источников в рамках стандартов SMOW и SLAP.
В воде между молекулами Н2О происходит интенсивный изотопный обмен атомами водорода (протием и дейтерием). При этом устанавливается термодинамическое равновесие между изотопными разновидностями молекул воды, содержащими дейтерий. В результате этого процесса наибольшую в количественном отношении долю молекул воды, содержащих дейтерий, составляют молекулы 1HD16О. В водах, близких по изотопному составу к природным, количественная доля молекул D2 16O, D2 17O, D2 18O, HD17O, HD18O мала и составляет в сумме менее 0,0009 г/кг. В дальнейших расчетах доля этих молекул присоединяется к доле 1HD16О.
В результате перераспределения атомов дейтерия между молекулами воды величина 1HD16O/1H16O удваивается по сравнению с величиной D/1H.
Например, для SMOW при соотношении концентрации D/1H=155,76×10-6 соотношение концентраций 1HD16О/1H2 16O удваивается и составляет 311,52×10-6.
Таким образом, в природных водах в 1000000 молекул Н2О в среднем содержится 997284 молекулы 1Н2 16O, 311 молекул 1HD16O, 390 молекул 1H2 17O и около 2005 молекул 1Н2 18О. Массовая доля и соответствующее ей весовое количество изотопных разновидностей молекул Н2O в природной воде, соответствующей стандарту SMOW, приведено в таблице 1. Аналогичные показатели для природной воды, соответствующей стандарту SLAP, приведены в таблице 2.
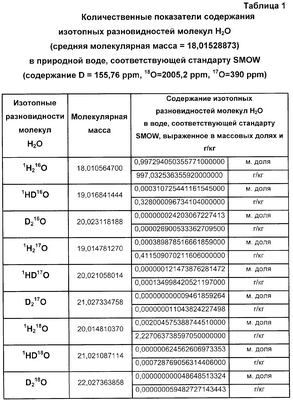 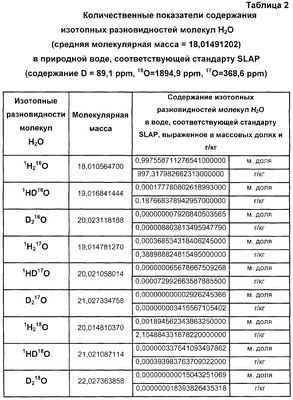
При расчете молекулярных масс изотопных разновидностей молекул воды использовались следующие значения атомных масс в международных углеродных единицах:
масса 1Н равна 1.007825035,
масса D равна 2,014101779,
масса 16О равна 15,99491463,
масса 17О равна 16,9991312,
масса 18О равна 17,9991603 [9].
Как видно из результатов, представленных в таблицах, в совокупности в природной воде весовая концентрация молекул 1H2 17O, 1Н2 18O, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17О, D2 18O, может составлять до 2,97 г/кг, что является значимой величиной, сопоставимой с содержанием в природной воде других характерных компонентов. Например, общая минерализация питьевой воды может составлять от 1 до 5 г/кг. Такой переход от условных атомарных единиц к весовым показателям количества изотопных разновидностей молекул Н2О позволяет оценить чистоту и однородность воды по изотопному составу.
В соответствии с приведенными данными можно условно определить понятия изотопно-легких и изотопно-тяжелых вод.
К изотопно-легким относят природную воду, в которой содержание молекул, включающих в себя тяжелые изотопы, приближается к стандарту SLAP. Также к этой категории относятся искусственно полученные воды с пониженной концентрацией дейтерия, но с природным изотопным составом кислорода в Н2О. Такими водами являются «Талая вода», «Реликтовая вода» и ряд других [9-14]. Автором патентов [13, 14] для воды, из которой определенным методом удаляется дейтерий, предлагается собственное название DDW (Deuterium Depleted Water – вода, обедненная по дейтерию) [4].
Традиционно в литературе в отношении изотопно-тяжелых вод употребляется несколько терминов.
Тяжелой водой называется вода с повышенным содержанием дейтерия и природным изотопным составом кислорода.
Тяжелокислородной водой называется вода с повышенным содержанием кислорода-18 и природным изотопным составом водорода.
Тяжелокислородной по кислороду-17 водой называется вода с повышенным содержанием кислорода-17 и природным изотопным составом водорода.
Таким образом, изотопно-тяжелой, в целом, может считаться вода с увеличенным содержанием, как минимум, одной из разновидностей молекул: 1H2 17О, 1H2 18O, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O, и соответственно уменьшенным содержанием молекул 1Н2 16О, а изотопно-легкой – вода с уменьшенным содержанием, как минимум, одной из разновидностей молекул: 1H2 17O, 1H2 18O, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O, и соответственно увеличенным содержанием молекул 1H2 16О. При этом увеличение или уменьшение количества молекул 1Н2 16O, а также молекул, содержащих тяжелые изотопы, может быть не только абсолютным (выше или ниже стандартных показателей SMOW и SLAP), но и относительным – по отношению к этому показателю, характерному для питьевой воды в конкретном регионе проживания человека.
Молекула 1H2 16О является наиболее легкой из совокупности изотопных разновидностей молекул воды. Поэтому вода с существенно увеличенной долей 1Н2 16О характеризуется меньшим молекулярным весом, обладает меньшей плотностью и является наиболее легкой в категории изотопно-легких вод. Такая вода в заявленном изобретении терминологически определяется как легкая очищенная или легкая особо чистая вода.
Физические, химические и биологические свойства изотопно-тяжелых вод (тяжелой по D, тяжелой по кислороду 17O и кислороду 18O) существенно отличаются друг от друга и от свойств природной воды. Например, изменяются температуры кипения и замерзания, плотность скорость химических и биохимических реакций [2, 9, 10, 11]. Это позволяет рассматривать вышеперечисленные тяжелые изотопные модификации Н2О как различные самостоятельные вещества, которые по отношению к воде 1Н2 16О являются примесями.
Реакция биосистем при воздействии на них Н2О, может изменяться в зависимости от количественных и качественных изменений изотопного состава Н2О. Применение воды с повышенной концентрацией тяжелых изотопов, в частности дейтерия, вызывает выраженные токсические эффекты на уровне организма, ограничивая возможность ее использования в лечебно-профилактических целях [12]. В то же время на разных объектах зарегистрирована положительная биологическая активность вод, полученных с помощью различных технологических процессов, относящихся к категории изотопно-легких, со сниженной в той или иной мере по сравнению с исходной концентрацией дейтерия [4, 13-21]. То есть количественные и качественные показатели изотопного состава воды существенным образом отражаются на ее эффективности при использовании воды в качестве растворителя или ингредиента. Поэтому очевидна необходимость в зависимости от целей применения регулирования изотопного состава воды, употребляемой человеком для технологических процессов, питья, в составе лекарственных, косметических, гигиенических, парфюмерных средств и т.д. Наличие примесей в виде изотопно-тяжелой воды, уменьшая долю 1H2 16O, изменяет некоторые характеристики и, следовательно, качество воды, так как первичным активным действующим началом является именно вода с молекулярным составом 1Н2 16O, т.е. собственно «вода по определению» в химическом, физическом и биологическом смыслах. В природных водах количественное соотношение изотопных разновидностей молекул Н2О зависит от географического положения региона, климатических условий, осадков, сезона года [3]. Океаническая вода, которая составляет основную массу воды на Земле, содержит меньшее количество 1Н2 16O по сравнению с основными запасами пресных вод. Для пресноводных источников этот показатель колеблется, но в целом имеет тенденцию к увеличению по сравнению с океанической водой. Однако природные источники воды с наибольшим содержанием 1Н2 16O (антарктические и высокогорные ледники), находятся в местах малонаселенных или практически незаселенных человеком.
Хотя изотопный состав атмосферной влаги поверхностных и подземных вод континентов колеблется в довольно широких пределах, эти колебания, однако, подчиняются определенным закономерностям [3]. Например, при уменьшении концентрации дейтерия в атмосферных осадках содержание кислорода-17 и кислорода-18 также снижается. Это обусловлено физико-химическими процессами испарения-конденсации воды, протекающими в природе. Корреляционная зависимость между  D и D и  18О для природной воды, построенная на основании большого количества опытных данных, впервые была установлена Крейгом [5] и уравнение регрессии 18О для природной воды, построенная на основании большого количества опытных данных, впервые была установлена Крейгом [5] и уравнение регрессии  D=8 D=8 18O+10%o носит его имя. 18O+10%o носит его имя.
Поэтому предпочтительнее, чтобы увеличение содержания 1Н2 16О в воде при ее промышленном производстве происходило за счет удаления молекул, содержащих не только дейтерий, но и тяжелые изотопы кислорода (17О и 18О).
Уровень техники по вопросам производства изотопно-легкой воды представлен рядом патентов, однако все они касаются способов и установок, позволяющих снизить в воде в той или иной мере только количество тяжелых изотопов водорода, в основном дейтерия, при сохранении исходного изотопного состава кислорода в Н2О.
Так, описаны способ и установки для получения «талой» и «реликтовой» воды с пониженным содержанием тяжелых изотопов дейтерия и трития [13-15]. Сущность предлагаемого способа состоит в том, что он включает операции охлаждения воды и последующего оттаивания замороженной воды [13]. Однако степень снижения количества дейтерия при этом весьма невелика. Существует установка, позволяющая методом электролиза достигать довольно значительного обеднения воды изотопами дейтерия в условиях отсутствия гравитации с целью использования такой воды в обитаемых космических объектах [16]. Но производительность такой установки крайне мала.
Наиболее близким техническим решением к объектам наших изобретений является патент RU 2125817 [17].
Согласно этому патенту воду с пониженным содержанием дейтерия получают методами дистилляции и/или стандартного электролиза. Из описания следует, что дистилляция происходит путем кипячения дистиллированной воды в перегонной колонке на 30-50 тарелок при давлении 50-60 мбар с флегмовым числом 12-13 и 10-кратным кубовым остатком. При использовании таких параметров концентрация дейтерия в первых фракциях составляет 20-30 ppm. Увеличивая число тарелок, можно еще снизить содержание дейтерия в воде до 1-10 ppm. В этом же патенте [17] предлагается способ производства D-обедненной воды с использованием электролиза. При этом концентрация D в полученной таким образом воде составляет 30-40 ppm. Далее предлагается смешивать приготовленную такими способами воду с обычной водой до получения содержания дейтерия между 111 и 135 ppm. To есть основной задачей является снижение в получаемой воде только содержания тяжелого изотопа водорода – дейтерия.
Хотя снижение содержания дейтерия в воде и приводит к некоторому увеличению доли 1Н2 16O в H2O, тем не менее обеднение воды только по дейтерию ограничивает возможность дальнейшего увеличения в ней содержания 1Н2 16О. Как показали наши расчеты, максимально возможное содержание 1Н2 16О в DDW, как и в любой воде, из которой удаляются только тяжелые изотопы водорода, составляет не более 997,36 г/кг (при минимальном остаточном содержании дейтерия 0,01 ppm), что находится в пределах, близких к природному уровню по стандарту SLAP.
Таким образом, предложенные способы и установки не дают возможности, тем более в промышленном масштабе, существенным образом увеличить долю 1Н2 16О в исходной воде. Существенное возрастание доли 1H2 16O в Н2О возможно лишь при удалении всех разновидностей тяжелых изотопов D, 17О, 18О, точнее при удалении максимального числа молекул, содержащих вышеназванные изотопы: 1Н2 16О, 1Н2 17О, 1Н2 18О, 1HD16О, 1HD17О, 1HD18O, D2 16O, D2 17О, D2 18O.
Задачей настоящего изобретения является создание способа и установки для производства воды с повышенным содержанием 1H2 16O в промышленном масштабе. Исходной водой для производства воды с повышенным содержанием 1Н2 16О может служить натуральная природная вода, водопроводная вода, вода любой степени очистки (дистиллированная, деионизированная и т.д.).
Решение поставленной задачи достигается за счет разработки способа получения легкой воды, предусматривающего ректификацию исходной воды с помощью ректификационной колонны, содержащей контактное устройство, увеличивающее площадь поверхности для взаимодействия пар-жидкость, при этом содержание 1Н2 16О в легкой воде составляет не менее 997,13 г/кг от общего количества Н2О, а суммарное содержание 1Н2 17О, 1Н2 18О, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O в легкой воде составляет не более 2,87 г/кг от общего количества Н2О, при этом ректификация включает в себя следующие этапы:
– приготовление водяного пара из исходной воды с концентрацией 1Н2 16О, равной C1;
– подача водяного пара в ректификационную колонну;
– взаимодействие пар-жидкость между нисходящим потоком жидкости и восходящим потоком пара на поверхности контактного устройства внутри ректификационной колонны, путем противотока жидкости и пара при направлении основного потока жидкости и основного потока пара вдоль оси колонны;
– конденсация водяного пара с концентрацией 1Н2 16О, равной С2, в конденсаторе, установленном в верхней части ректификационной колонны, и накопление части конденсата в виде конденсированной легкой воды, при этом С2>C1;
предпочтительно, чтобы давление пара в ректификационной колонне составляло от 0,05 до 0,6 бар;
предпочтительно, чтобы выход сконденсированной легкой воды составлял от 0,001 до 0,25 от общего объема водяного пара, прошедшего через ректификационную колонну.
Контактное устройство может быть представлено в виде тарелок.
Предпочтительнее, чтобы контактное устройство представляло собой структурированную или рандомизированную насадку.
Предпочтительнее, чтобы содержание 1Н2 16О в полученной легкой воде составляло не менее 997,36 г/кг от общего количества Н2О, а суммарное содержание 1Н2 17О, 1Н2 18О, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O в легкой воде составляло не более 2,64 г/кг от общего количества Н2О.
Более предпочтительно, чтобы содержание 1Н2 16О в легкой воде составляло не менее 997,51 г/кг от общего количества Н2О, а суммарное содержание 1Н2 17О, 1Н2 18О, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O в легкой воде составляло не более 2,49 г/кг от общего количества Н2О.
Поставленная задача также решается за счет создания установки для получения легкой воды, включающей в себя ректификационную колонну, которая содержит контактное устройство для увеличения поверхности для взаимодействия пар-жидкость, при этом содержание 1Н2 16О в легкой воде составляет не менее 997,13 г/кг от общего количества Н2О, а суммарное содержание 1H2 17O, 1Н2 18О, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O в легкой воде составляет не более 2,87 г/кг от общего количества Н2О, при этом установка включает в себя:
– узел приготовления водяного пара из исходной воды с концентрацией 1Н2 16О, равной C1;
– узел подачи водяного пара в ректификационную колонну;
– ректификационную колонну, представляющую собой узел взаимодействия пар-жидкость между нисходящим потоком жидкости и восходящим потоком пара на поверхности контактного устройства внутри ректификационной колонны путем противотока жидкости и пара при направлении основного потока жидкости и основного потока пара вдоль оси колонны;
– узел конденсации водяного пара с концентрацией 1Н2 16О, равной С2, в конденсаторе, установленном в верхней части ректификационной колонны, и накопление части конденсата в виде конденсированной легкой воды, при этом С2>С1;
предпочтительно, чтобы давление пара в ректификационной колонне составляло от 0,05 до 0,6 бар;
предпочтительно, чтобы выход сконденсированной легкой воды составлял от 0,001 до 0,25 от общего объема водяного пара, прошедшего через ректификационную колонну.
Контактное устройство может быть представлено в виде тарелок.
Предпочтительнее, чтобы контактное устройство представляло собой структурированную или рандомизированную насадку.
Предпочтительнее, чтобы содержание 1Н2 16О в полученной легкой воде составляло не менее 997,36 г/кг от общего количества Н2О, а суммарное содержание 1H2 17O, 1H2 18O, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O в легкой воде составляло не более 2,64 г/кг от общего количества H2O.
Более предпочтительно, чтобы содержание 1Н2 16О в легкой воде составляло не менее 997,51 г/кг от общего количества Н2О, а суммарное содержание 1Н2 17О, 1Н2 18О, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O в легкой воде составляло не более 2,49 г/кг от общего количества Н2О.
Иллюстративным примером материала насадки является медь, никель, нержавеющая сталь или сплавы.
Процесс ректификации исходной воды с целью получения воды с повышенным содержанием 1Н2 16О иллюстрируется фиг.1, где схематично изображена установка, состоящая из узла приготовления водяного пара из исходной воды с концентрацией 1Н2 16О, равной С1 (1), узла подачи водяного пара в ректификационную колонну (2), узла взаимодействия пар-жидкость, представляющего собой ректификационную колонну (3) с контактным устройством внутри нее (4), узла конденсации водяного пара с концентрацией 1Н2 16О, равной С2 (5), где С2>С1; стрелками показаны направления потоков восходящего пара и нисходящей жидкости.
Варьируя количество ступеней разделения в колонне, рабочее давление, а также отношение отбора части конденсата в виде воды с повышенным содержанием 1Н2 16О к потоку жидкости в ректификационной колонне, получаем заданную степень обогащения воды ее наиболее легкой составляющей 1Н2 16О. Степень обогащения зависит от конкретной цели применения легкой воды.
Техническим результатом настоящего изобретения является создание эффективного способа и установки для промышленного производства легкой особо чистой воды с повышенным содержанием 1Н2 16О. Способ и установка для производства легкой воды, предложенные в патенте, позволяют промышленным путем достигать весьма значительной степени удаления из исходной воды совокупности молекул, содержащих тяжелые изотопы водорода и кислорода: 1Н2 17О, 1Н2 18О, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O и, следовательно, значительного увеличения содержания Н2 16О. В результате этого получается новый продукт – легкая особо чистая вода с высокой степенью однородности по изотопному составу. Работ по созданию целенаправленной технологии получения воды с увеличенным содержанием доли 1H2 16O в патентной и периодической литературе не обнаружено.
Процесс производства легкой очищенной воды с повышенным содержанием 1Н2 16О с применением способа и установки, заявленных в изобретении, продемонстрирован в примере. Пример приведен только для иллюстрации эффективности и возможностей данного изобретения, ни в коей мере не ограничивая области его применения.
Пример 1 Процесс производства легкой особо чистой воды с повышенным содержанием 1Н2 16О с применением способа и установки, заявленных в изобретении.
Исходная дистиллированная вода с содержанием 1Н2 16О, равным 997,0927 г/кг (концентрация С1), поступает в отдельную емкость для приготовления водяного пара (1, фиг.1). Пар вырабатывается с помощью тепло-электронагревательных элементов общей мощности 12 кВт. Полученный водяной пар направляется в ректификационную колонну через специальный узел подачи и распределения водяного пара (2, фиг.1), примыкающий к основанию ректификационной колонны. Отсюда водяной пар поступает непосредственно в ректификационную колонну, представляющую собой узел взаимодействия между восходящим потоком пара и нисходящим потоком жидкости (3, фиг.1). Процесс происходит путем противотока жидкости и пара при направлении основного потока жидкости и основного потока пара вдоль оси колонны. Колонна представляет собой полый цилиндр, выполненный из нержавеющей стали 02Х12Т, толщина стенки 2 мм, высотой 6000 мм, диаметром 100 мм. Внутреннее пространство колонны засыпным способом заполнено рандомизированной насадкой (4, фиг.1) для увеличения поверхности взаимодействия между восходящим потоком пара и нисходящим потоком жидкости в ректификационной колонне.
Насадка представляет собой 3-миллиметровые спирально-призматические элементы, выполненные из нержавеющей проволоки диаметром 0,2 мм. Удельная поверхность насадки составляет 2550 м2/м3, доля свободного объема 0,84 м2/м3, масса единицы объема 1100 кг/м3.
Процесс обогащения водяного пара наиболее легкими молекулами происходит в ректификационной колонне на поверхности контактного устройства (насадки) при температуре 60°С и давлении 0,2 бар. Полученный водяной пар с повышенным содержанием 1Н2 16О в объеме 16 л/час конденсируется в узле конденсации (5, фиг.1), расположенном в верхней части ректификационной колонны. Выход сконденсированной легкой воды составляет 0,025 часть от общего объема водяного пара, прошедшего через ректификационную колонну, и равен 0,4 л/час. Готовый продукт – легкая вода с повышенным содержанием 1Н2 16О, равным 997.65 г/кг (концентрация С2; при этом С2>C1).
Источники информации
1. Глинка. Общая химия. М.: «Химия», 1975 г., стр.102.
2. Андреев Б.М., Зельвенский Я.Д., Катальников С.Г. Тяжелые изотопы водорода в ядерной технике. Москва: ИздАТ, 2000 г., с.186.
3. Ферронский В.И., Поляков В.А. Изотопия гидросферы. М.: Наука, 1983 г., стр.47., стр.10, 47, 46, 10.
4. Somlyai G. «Let’s Defeat Cancer!». Akademiai Kiado, Budapest, 2001.
5. Creig H. «Standard for reporting concentration of deuterium and oxygen-18 in natural water». Science, 1961, vol.133, p.1833-1834.
6. Шатенштейн А.И. Варшавский Я.М. и соавт. Изотопный анализ воды. Москва: Издательство Академии Наук, 1954 г., стр.15.
7. ACOS Bulletin, №21, October 1979, стр.14.
8. Куликов И.С. Изотопы и свойства элементов. Справочник. Москва: Металлургия, 1990.
9. Кульский Л.А., Гороновский И.Т., Когановский А.М., Шевченко М.А. Справочник по свойствам, методам анализа и очистке воды. Киев: Наукова думка, 1980.
10. Лобышев В.И., Калиниченко Л.П. Изотопные эффекты D2O в биологических системах. Москва: Наука, 1978 г.
11. Лобышев В.И. Механизмы термодинамических и кинетических изотопных эффектов D2O в биологических системах Автореф. докт. диссертации. Москва, – 1987 (биофак МГУ).
12. Kushner D.J., Baker F., Dunstall T.G. Can. J. Physiol. Pharmacol. 1999, Feb.77(2): 79-88.
13. Патент RU 2031085. Способ получения биологически активной питьевой воды и установка вин-6 для его осуществления. Варнавский И.И. и др.
14. Патент RU 2091335. Установка ВИН-7 “Надiя” для получения целебной питьевой воды с пониженным содержанием дейтерия и трития “Реликтовая вода”. Варнавский И.Н. и др.
15. Патент RU 2091336. “Способ получения целебной питьевой воды с пониженным содержанием дейтерия и трития “Реликтовая вода”. Варнавский И.Н. и др.
16. Патент RU 2182562. Способ получения биологически активной питьевой воды с пониженным содержанием дейтерия устройство для ее получения. Государственный научный центр Российской Федерации Институт медико-биологических проблем, Синяк Ю.Е.
17. Патент RU 2125817. Пищевой продукт для профилактики развития заболеваний и способ производства пищевых продуктов, пригодных для профилактики развития опухолевых заболеваний. Шомяи Г. (Hu).
18. Патент RU 2139062. Гигиенические и косметические препараты для профилактики и лечения заболеваний кожи. Шомяи Г. (Hu).
19. Синяк Ю.Е., Левинских М.А., Гайдадымов В.Б., и др. Организм и окружающая среда: жизнеобеспечение и защита человека в экстремальных условиях (материалы Российской конференции) Москва, 26-29 сентября 2000 г., стр.90-92.
20. Синяк Ю.Е., Гурьева Т.С., Гайдадымов В.Б., и др. Космическая биология и авиакосмическая медицина. (Тезисы док. 11 конференции), Москва, Россия, 22-26 июня, 1998 г., стр.201-202.
21. Родимов Б.Н. Действие снеговой воды на живые организмы. «Сельскохозяйственное производство Сибири и Дальнего Востока». Омск 4, 1965 г., стр.56-57.
Формула изобретения
1. Способ получения легкой воды, предусматривающий ректификацию содержащей исходной воды с помощью ректификационной колонны, содержащей контактное устройство, увеличивающее площадь поверхности для взаимодействия пар-жидкость, при этом содержание 1Н2 16О в легкой воде составляет не менее 997,13 г/кг от общего количества H2O, а суммарное содержание 1H2 17O, 1H2 18O, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O в легкой воде составляет не более 2,87 г/кг от общего количества Н2O, при этом ректификация включает в себя следующие этапы:
приготовление водяного пара из исходной воды с концентрацией 1Н2 16O, равной С1;
подачу водяного пара в ректификационную колонну;
взаимодействие пар-жидкость между нисходящим потоком жидкости и восходящим потоком пара на поверхности контактного устройства внутри ректификационной колонны путем противотока жидкости и пара при направлении основного потока жидкости и основного потока пара вдоль оси колонны;
конденсацию водяного пара с концентрацией 1Н2 16O, равной С2, в конденсаторе, установленном в верхней части ректификационной колонны, и накопление части конденсата в виде конденсированной легкой воды, при этом С2>С1;
при этом давление пара в ректификационной колонне составляет от 0,05 до 0,6 бар и выход конденсированной легкой воды составляет от 0,001 до 0,25 общего объема водяного пара, прошедшего через ректификационную колонну.
2. Способ по п.1, отличающийся тем, что контактное устройство представлено в виде тарелок.
3. Способ по п.1, отличающийся тем, что контактное устройство представлено в виде структурированной или рандомизированной насадки.
4. Способ по п.1, отличающийся тем, что содержание 1Н2 16O в легкой воде составляет не менее 997,36 г/кг от общего количества Н2О, а суммарное содержание 1Н2 17О, 1Н2 18О, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O в легкой воде составляет не более 2,64 г/кг от общего количества Н2О.
5. Способ по п.1, отличающийся тем, что содержание 1Н2 16О в легкой воде составляет не менее 997,51 г/кг от общего количества Н2О, а суммарное содержание 1Н2 17O, 1Н2 18О, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O в легкой воде составляет не более 2,49 г/кг от общего количества Н2О.
6. Установка для получения легкой воды, включающая ректификационную колонну, которая содержит контактное устройство для увеличения поверхности для взаимодействия пар-жидкость, при этом содержание 1H2 16О в легкой воде составляет не менее 997,13 г/кг от общего количества Н2О, а суммарное содержание 1H2 17O, 1Н2 18О, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O в легкой воде составляет не более 2,87 г/кг от общего количества Н2О,
при этом установка включает в себя
узел приготовления водяного пара из исходной воды с концентрацией 1Н2 16О, равной C1;
узел подачи водяного пара в ректификационную колонну;
ректификационную колонну, представляющую собой узел взаимодействия пар-жидкость между нисходящим потоком жидкости и восходящим потоком пара на поверхности контактного устройства внутри ректификационной колонны путем противотока жидкости и пара при направлении основного потока жидкости и основного потока пара вдоль оси колонны;
узел конденсации водяного пара с концентрацией 1H2 16O, равной С2, в конденсаторе, установленном в верхней части ректификационной колонны, и накопление части конденсата в виде конденсированной легкой воды, при этом C2>C1;
при этом давление пара в ректификационной колонне составляет от 0,05 до 0,6 бар и выход конденсированной легкой воды составляет от 0,001 до 0,25 общего объема водяного пара, прошедшего через ректификационную колонну.
7. Установка по п.6, отличающаяся тем, что контактное устройство представлено в виде тарелок.
8. Установка по п.6, отличающаяся тем, что контактное устройство представлено структурированной или рандомизированной насадкой.
9. Установка по п.6, отличающаяся тем, что содержание 1Н2 16О в легкой воде составляет не менее 997,36 г/кг от общего количества Н2О, а суммарное содержание 1H2 17O, 1Н2 18О, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O в легкой воде составляет не более 2,64 г/кг от общего количества Н2О.
10. Установка по п.6, отличающаяся тем, что содержание 1Н2 16О в легкой воде составляет не менее 997,51 г/кг от общего количества Н2О, а суммарное содержание 1H2 17O, 1H2 18O, 1HD16O, 1HD17O, 1HD18O, D2 16O, D2 17O, D2 18O в легкой воде составляет не более 2,49 г/кг от общего количества Н2О.
РИСУНКИ
PC4A – Регистрация договора об уступке патента СССР или патента Российской Федерации на изобретение
Прежний патентообладатель:
Соловьев Сергей Павлович
(73) Патентообладатель:
Вудфорд Ассошиэйтс Лимитэд (GB)
Договор № РД0039734 зарегистрирован 18.08.2008
Извещение опубликовано: 27.09.2008 БИ: 27/2008
|
|