|
|
(21), (22) Заявка: 2005120250/04, 29.06.2005
(24) Дата начала отсчета срока действия патента:
29.06.2005
(46) Опубликовано: 10.03.2007
(56) Список документов, цитированных в отчете о
поиске:
УЛОМСКИЙ Е.Н. и др. Восстановление нитропроизводных азоло[5,1-e][1,2,4]-триазинов. Химия гетероциклических соединений. (5), 1992, с.674-677. УЛОМСКИЙ Е.Н. и др. Нитроазины. Химия гетероциклических соединений. (11), 1987, с.1543-1550. РУСИНОВ В.Л. и др. Нитроазины. Журнал органической химии. 32(5), 1996, с.770-776. УЛОМСКИЙ Е.Н. и др. Нитроазины.
Адрес для переписки:
620002, г.Екатеринбург, ул. Мира, 19, УГТУ-УПИ, центр интеллектуальной собственности, Т.В. Маркс
|
(72) Автор(ы):
Чупахин Олег Николаевич (RU),
Русинов Владимир Леонидович (RU),
Уломский Евгений Нарциссович (RU),
Чарушин Валерий Николаевич (RU),
Петров Александр Юрьевич (RU),
Киселев Олег Иванович (RU)
(73) Патентообладатель(и):
Государственное образовательное учреждение высшего профессионального образования Уральский государственный технический университет-УПИ (RU),
Общество с ограниченной ответственностью Научно-техническое предприятие “Лиганд” (RU)
|
(54) НАТРИЕВАЯ СОЛЬ 2-МЕТИЛТИО-6-НИТРО-1,2-4-ТРИАЗОЛО[5,1-C]-1,2,4-ТРИАЗИН-7(4H)-ОНА, ДИГИДРАТ, ОБЛАДАЮЩАЯ ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ
(57) Реферат:
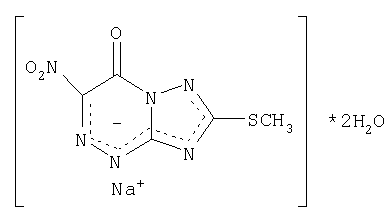
Изобретение относится к области биологически активных соединений, касается разработки нового вещества – натриевой соли 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата и предназначено для лечения и профилактики заболеваний, вызываемых патогенными для человека и животных вирусами и имеющего формулу:
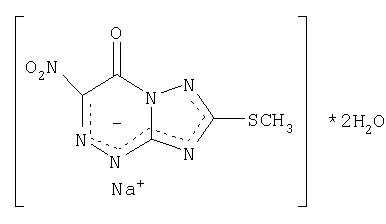
Описываемое соединение защищает от инфекций, вызываемых вирусами лихорадки долины Рифт. Особенно ценно, что соединение активно при лечебной схеме применения. Оно активно в отношении вируса ЗЭЛ, парагриппа, респираторно-синцитиального вируса, вируса болезни Ауески, инфекционного ляринготрахеита птиц, вируса гриппа птиц, всего более 10 РНК и ДНК содержащих вирусов. 6 табл., 2 ил.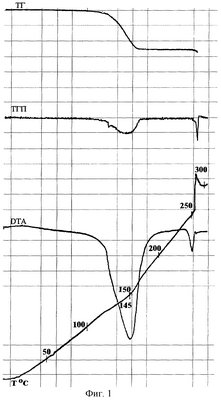
(56) (продолжение):
CLASS=”b560m”Химия гетероциклических соединений. (11), 1987, с.1543-1550. РУСИНОВ В.Л. и др. Нитроазины. Химия гетероциклических соединений. (11) (305), 1992, с.1555-1559. SU 1210416 А, 27.12.1999.
1. Область техники, к которой относится изобретение.
Изобретение относится к области биологически активных соединений и касается натриевой соли 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрата, обладающей противовирусным действием, предназначенной для лечения и профилактики инфекционных заболеваний вирусной природы человека и животных. Изобретение может быть использовано в лечебных учреждениях, научно-исследовательских лабораториях, а также в животноводстве и птицеводстве.
Актуальность проблемы противовирусной терапии, в особенности в условиях быстрой мутации вирусов, выявления новых возбудителей опасных и медленных вирусных инфекций, вызывает постоянную потребность в новых средствах, которые бы обладали высокой активностью, продолжительным действием и низкой токсичностью.
2. Предшествующий уровень техники.
В ряду конденсированных азолоазинов имеются данные о противовирусном действии 6-нитро-4,7-дигидро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7-онов в отношении вируса болезни Ауески (ВБА) [Русинов В.Л., Уломский Е.Н., Чупахин О.Н. и др. Химико-фармацевтический журнал. 1990, № 96, с.41-44]. Известно также противовирусное действие 4-алкилтио-5,7-дигидро-7-оксо-1,2,4-триазоло[4,3-с1]-1,2,4-триазинов [Cristesku С., Derivati de 5-oxo-5,6-dihidro-s-triazolo(4,3-d)-as-triazina si procedeu pentru prepararea lor. Пат. СРР, кл. 12(C 07 d 55/10), № 56269, 13.03. 1974], а также – противоопухолевое действие имидазо[2,1-с]-1,2,3,5-тетразинов [Yongfeng W., Stevens M.F.G. Antitumor Imidazotetrasines. 35. New Synthetic Routesto to the Antitumor Drug Temozolomide. J. Org. Chem. 1997, vol. 62, №21, p.7288-7294]. В качестве прототипа наиболее подходящим является соединение – натриевая соль 6-нитро-4,7-дигидро-1,2,4-триазоло[5.1-с]-1,2,4-триазин-7-она – проявившее противовирусное действие в отношении в отношении ВБА [Русинов В.Л., Уломский Е.Н., Чупахин О.Н. и др. Химико-фармацевтический журнал. 1990, № 96, с.41-44].
3. Раскрытие изобретения.
Техническим результатом предлагаемого изобретение является нахождение нового химического соединения, обладающего широким спектром противовирусного действия, эффективного в отношении РНК и ДНК содержащих вирусов.
Указанный технический результат достигается тем, что согласно изобретению, предложено новое соединение – натриевая соль 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрат, обладающее противовирусной активностью и имеющее формулу 1
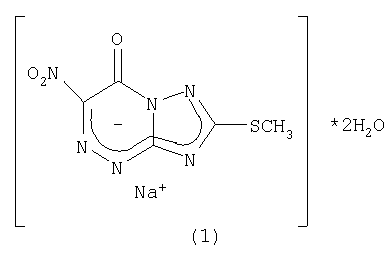
Натриевую соль 2-метилтио-6-нитро-1,2,4-триазоло [5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрата (1) получают конденсацией соли диазония (3), получаемой диазотированием 3-амино-5-метилтио-1,2,4-триазола (2), с этилнитроацетатом в щелочной среде.
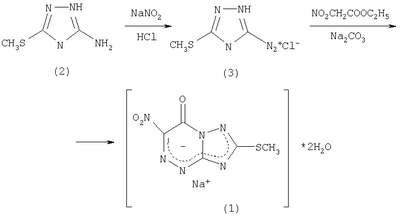
Заявляемое соединение представляет собой желтое кристаллическое высокоплавкое, растворимое в воде, метаноле, ацетоне, диметилформамиде, диметилсульфоксиде, малорастворимое в метаноле, нерастворимое в бензоле, хлороформе и большинстве апротонных растворителей.
Данные элементного анализа и ЯМР-спектроскопии полностью соответствуют приписываемому строению. Присутствие в заявляемом соединении двух молекул воды подтверждается данными дериватографии (фиг.1, 2).
Фиг.1. Термограмма натриевой соли 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с] -1,2,4-триазин-7(4Н)-она, дигидрата.
Фиг.2. Убыль массы натриевой соли 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрата при нагревании.
Для отрыва воды из натриевой соли 2-метилтио-6-нитро-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрата вещество необходимо длительное время нагревать при 150°С в вакууме над P2O5. Безводный препарат на воздухе моментально поглощает влагу и при обычных условиях и за 2-3 ч полностью превращается в дигидрат.
Пример 1. Синтез натриевой соли 2-метилтио-6-нитро-1,2,4-триазоло [5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрата (1)
К охлажденному до 0°С раствору 13 г (0,1 моль) 5-амино-3-метилтио-1,2,4-триазола в 16 мл азотной кислоты (d=1,4) и 100 мл воды добавляют раствор 8 г нитрита натрия в 50 мл воды в течение 15 мин, выдерживают 10 мин и вносят порциями охлажденную смесь 11 мл (0,1 моль) этилнитроацетата в 150 мл 2 М растворе карбоната натрия. Перемешивают 2 часа при 0-5°С, образовавшийся осадок отфильтровывают, последовательно кристаллизуют из 20%-ной уксусной кислоты, воды и сушат на воздухе. Выход: 21,2 г (74%).
Натриевая соль 2-метилтио-6-нитро-1,2,4-триазоло [5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрат имеет следующие физико-химические характеристики: ТПЛ>300°С; 1H ЯМР спектр в ДМСО-d6  , м.д.: 2,52 (3Н, с, SCH3), 4,76 (4Н, уш.с., 2 Н2O). Найдено: С – 20.83, Н – 2.62, N – 29.21, S – 11.54%. Брутто-формула – C5H7N6NaO5S. Вычислено: С – 20.98, Н – 2.47, N – 29.36, S – 11.20%. , м.д.: 2,52 (3Н, с, SCH3), 4,76 (4Н, уш.с., 2 Н2O). Найдено: С – 20.83, Н – 2.62, N – 29.21, S – 11.54%. Брутто-формула – C5H7N6NaO5S. Вычислено: С – 20.98, Н – 2.47, N – 29.36, S – 11.20%.
Пример 2. Изучение противовирусного действия в отношении вируса венесуэльского энцефаломиелита лошадей (ВЭЛ) и Синдбис
Противовирусную активность и цитотоксическое действие заявляемого соединения изучали микрометодом в 96-луночных микропанелях в перевиваемой культуре клеток Vero в отношении вирусов ВЭЛ штамм 230 и Синдбис штамм EgA2-339, относящихся к роду альфавирусов. Множественность инфекции вирусов (м.и.) была 0,01 ТЦД50. Опыт учитывали через 72 часа до наступления 100% цитопатического эффекта (ЦПЭ) в лунках контроля вируса. ЦПЭ определяли по 4-крестовой схеме; 4+-100% деструкции клеточного монослоя, 3+-75%, 2+-26% деструкции (табл.1, 2).
Антивирусную активность изучали по снижению инфекционного титра (И.Т.) вируса ВЭЛ-230 и вируса Синдбис в культуре клеток Vero через 24 часа после заражения при инфицирующей дозе вируса 0.01 БОЕ/клетку. Результаты приведены в табл.2. Заявляемое соединение в концентрации 200, 12,5 мкг/мл снижало И.Т. вируса ВЭЛ-230 на 4,0, 1,9 IgБОЕ/мл соответственно, а И.Т. вируса Синдбис на 3,9, 1,8 lg БОЕ/мл соответственно. Соединение-прототип в концентрации 125, 6,25 мкг/мл снижало И.Р. вируса Синдбис на 3,0, 1,0 lg БОЕ/мл соответственно, а И.Т. вируса ВЭЛ-230 на 3,3, 1,5 lg БОЕ/мл соответственно. Ремантадин в концентрации 50, 25 мкт/мл снижал И.Т. вируса ВЭЛ-230 на 2,0, 1,4 lg БОЕ/мл соответственно. ХТИ (химиотерапевтический индекс) соединений: описываемого – 20, прототипа – 12, ремантадина – 2.
Пример 3. Изучение антивирусной активности в отношении вируса западного энцефаломиелита лошадей (ЗЭЛ)
Заявляемое соединение вводили беспородным мышам массой 10-12 г перорально по 2-м схемам: 1 – профилактическая – за 24 часа, через 2, 24, 48, 72, 96 часов после инфицирования 10 ЛД50 вируса, II схема – лечебная – вирус вводили через 2, 24, 48, 72, 96 часов после заражения той же инфицирующей дозой вируса.
Разовая доза соединений 50 мг/кг массы, соответствовала 1/32 ЛД50 для этих соединений. Курсовая доза обоих соединений составляла 300-250 мг/кг массы в зависимости от применяемой схемы. Инфицирующая доза вируса ЗЭЛ 10 ЛД50 в объеме 0,1 мл внутримышечно. Способ применения соединений пероральный. Как видно из таблицы 3, при лечебно-профилактической схеме введения (I) описываемого соединения защита составила 65%, средняя продолжительность жизни животных удлинена на 10 суток (табл.3). Процент защиты при применении лечебной схемы составил 60%, а средняя продолжительность жизни увеличилась на 5,9 суток. Соединение-прототип оказалось неэффективно в отношении ЗЭЛ.
Пример 4. Изучение противовирусного действия в отношении вирусов лихорадки долины Рифт (ЛДР)
Заявляемое соединение вводили беспородным белым мышам массой 6-8 г перорально по 2-схемам: 1 схема – лечебно-прфилактическая (за 24 часа и через 1, 2, 3, 6, 7, 8, 9, 10 суток после заражения той же инфицирующей дозой вируса). Разовая доза соединений 50 мг/кг массы, что соответствует 1/32 ЛД50 этих соединений. Курсовая доза обоих соединений составляла 500-450 мг/кг массы в зависимости от применяемой схемы. Инфицирующую дозу вируса 10 ЛД50 в объеме 0,2 мл вводили подкожно. Как видно из таблицы 4, при лечебно-профилактической схеме введения заявляемого соединения защита составила 90%, средняя продолжительность жизни леченных животных увеличилась на 12,2 суток. Процент защиты при применении лечебной схемы был несколько выше и равнялся 80%, а средняя продолжительность жизни увеличилась на 13,4 суток (табл.4).
Пример 5. Изучение противовирусной активности в отношении вируса парагриппа и респираторно-синцитиального вируса
Изучение противовирусной активности в отношении данных вирусов проводили в опытах на культуре ткани с использованием вируса парагриппа 3 типа (штамм НА-1) и респираторно-синцитиального вируса (штамм Лонг).
В каждый опыт включали 2 группы:
1) пробирки с культурой ткани, в которые вводили испытуемое соединение;
2) пробирки с культурой ткани, в которые вместо испытуемого соединения вводили питательную среду.
Установлено, что ингибиция вируса парагриппа наблюдалась при использовании дозы препарата 500 мкг/мл, тогда как для ингибирования респираторно-синцитиального вируса достаточной была концентрация 60 мкг/мл (табл.5).
Пример 6. Изучение противовирусного действия в отношении вируса болезни Ауески, гриппа птиц и инфекционного ляринготрахеита птиц
Испытания проводили с вирусом гриппа птиц (ВГП) и инфекционного ляринготрахеита птиц (ИЛТ) на 10-дневных куриных эмбрионах (КЭ) и вирусом болезни Ауески (ВБА) на культуре клеток куриных фибробластов (КФ).
При определении вирусстатического (ингибирующего) действия КЭ инфицировали вирусом ИЛТ в дозе 50-100 БОЕ50, а культуру клеток КФ-ВБА в дозе ТЦД50 (тканевых цитопатических доз). Через 1-1,5 часа после заражения КЭ и КФ вносили испытуемое соединение в дозах 50, 100, 250 мкг/КЭ и инкубировали в термостате при 37,5°С КЭ в течение 120 часов до 100% образования бляшек на хориоаллантоисной оболочке (ХАО), а КФ – до четкого цитопатического действия в контроле. На каждую дозу изучаемого соединения брали по 10 КЭ или 4 флакона с КФ эксперименты проводили в 3-х повторностях.
Вирусстатическое действие определяли по разнице титров вируса в опыте и в контроле в КФ и по подавлению бляшкообразования в опыте и контроле с КЭ. Ингибирующее действие выражено в ТЦД50 в КФ и в % подавления бляшек с КЭ. Контролем служили КЭ и КФ, зараженные вирусом, а также интактные КЭ и КФ.
При изучении вирулицидного действия (инактивирующего) заявляемое соединение смешивали с материалом, содержащим ВГП, и инкубировали при 37,5°С в течение 24 часов, после чего титровали на КЭ параллельно с контролем. Контролем служил вирусосодержащий материал, к которое вместо заявляемого соединения добавляли физраствор (плацебо) и интактные КЭВ. Вирулицидное действие определяли по разнице титров в опыте и контроле и выражали в ЭЛД50 (эмбриональных летальных доз).
Установлено, что в опытах на КЭ с вирусом ИЛТ заявляемое соединение в дозе 500 мкг/КЭ подавляло развитие бляшек ХАО на 30% при 100%-ном образовании в контроле. В опытах на КЭ с ВБА заявляемое соединение в дозе 100 мкг/мл подавляло репродукцию вируса на 2,75, а в дозе 50 мкг/мл – 1,5 ТЦД50. В опытах на КЭ с ВГП заявляемое соединение в дозе 500 мкг/мл и при экспозиции 24 часа интактировало ВГП на 3,6 ЭЛД50.
Пример 7. Определение токсичности заявляемого соединения
Определение токсичности проводили на беспородных белых мышах массой 7-8 г в диапазоне концентрации 50-200 мг/кг (табл.6). Из табл.7 видно, что ЛД50 натриевой соли 2-метилтио-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7-она, дигидрата составляет 1400 мг/кг.
Изучение противовирусного действия заявляемого соединения (натриевой соли 2-метилтио-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрата) и сопоставление его с прототипом – натриевой солью 1,2,4-триазоло[5,1-с]-1,2,4-триазин-7-она и используемым в медицинской практике препаратом “ремантадин” показало следующее.
1. В отношении вирусов ВЭЛ и Синдбис заявляемое соединение значительно превосходит ремантадин. В опытах на лабораторных животных заявляемое соединение обладает более сильным защитным эффектом, чем прототип.
2. Заявляемое соединение обладает более широким спектром противовирусного действия, чем прототип. Натриевая соль 2-метилтио-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрат защищает животных от инфекций, вызываемых вирусами лихорадки долины Рифт. Особенно ценно, что соединение активно при лечебной схеме применения.
Заявляемое соединение, в отличие от соединения-прототипа и ремантадина, активно в отношении вируса ЗЭЛ, парагриппа, респираторно-синцитиального вируса, вируса болезни Ауески, инфекционного ляринготрахеита птиц, вируса гриппа птиц.
Таким образом натриевая соль 2-метилтио-1,2,4-триазоло[5,1-с]-1,2,4-триазин-7(4Н)-она, дигидрат обладает более выраженным, чем прототип и рематадин противовирусным действием. Заявляемое соединение имеет более широкий спектр биологической активности, чем соединение-прототип и используемый в медицинской практике препарат ремантадин.
Таблица 1
Противовирусная активность заявляемого соединения, прототипа и ремантадина в отношении вирусов ВЭЛ и Синдбис |
| соединение |
МПК, мкг/мл |
ВЭЛ-230 |
Синдбис |
| ЭД50, мкг/мл |
ХТИ |
ЭД50; мкг/мл |
ХТИ |
Р |
| Заявляемое |
200 |
10,0 |
20 |
10,0 |
20 |
0,01 |
| прототип |
125 |
10,0 |
12 |
10,0 |
12 |
0,01 |
| ремантадин |
50 |
25 |
2 |
25 |
2 |
0,01 |
МПК – максимально переносимая концентрация; ЭД50 – минимальная концентрация, задерживающая развитие цитопатического эффета (ЦПЭ) на 50%;
ХТИ – химиотерапевтический индекс (МПК/ ЭД50); Р – уровень достоверности. |
Таблица 2
Противовирусная активность заявляемого соединения, прототипа и ремантадина в отношении вирусов ВЭЛ и Синдбис |
| соединение |
МПК, мкг/мл |
концентрация, мкг/мл |
ВЭЛ-230 |
Синдбис |
| титр вируса, lg БОЕ/мл |
сниж. титра, lg БОЕ/мл |
ХТИ |
титр вируса, lg БОЕ/мл |
сниж. титра, lg БОЕ/мл |
ХТИ |
Р |
| |
|
200 |
5,5 |
4,0±0,06 |
|
6,0 |
3,9±0,14 |
|
0,01 |
| заявляемое |
200 |
12,5 |
7,6 |
1,9±0,08 |
16 |
7,9 |
1,8±0,11 |
16 |
0,01 |
| |
|
0 |
9,3 |
|
|
9,5 |
|
|
|
| |
|
50 |
6,0 |
3,3±0,16 |
|
5,2 |
3,0±0,14 |
|
0,01 |
| прототип |
125 |
5,12 |
7,8 |
1,5±0,06 |
12 |
8,0 |
1,0±0,08 |
12 |
0,01 |
| |
|
0 |
9,3 |
|
|
9,5 |
|
|
|
| |
|
50 |
7,3 |
2,0±0,11 |
|
7,5 |
2,0±0,08 |
|
0,01 |
| ремантадин |
50 |
25 |
7,9 |
1,4±0,16 |
2 |
8,0 |
1,5±0,14 |
2 |
0,01 |
| |
|
0 |
9,3 |
|
|
9,5 |
|
|
|
| МПК – максимально переносимая концентрация; ХТИ – химиотерапевтический индекс (МПК/ЭД50); Р – уровень достоверности. |
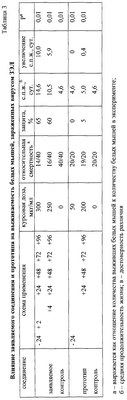 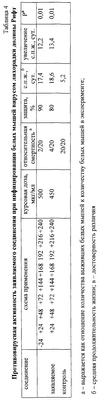
Таблица 5
Противовирусная активность заявляемого соединения в отношении вирусов парагриппа и респираторно-синцитиального |
| вирус |
доза соединения, мкг/мл |
доза вируса, ТЦД50 |
опыт |
контроль |
| всего пробирок |
из них содержащих вирус |
индекс защиты, % |
всего пробирок |
из них содержащих вирус |
| парагрипп |
500 |
1-10 |
20 |
4 |
60 |
20 |
19 |
| |
|
10-100 |
20 |
16 |
15 |
20 |
13 |
| респираторно- |
60 |
1-10 |
10 |
3 |
55 |
10 |
10 |
| синтициальный |
|
10-100 |
10 |
10 |
10 |
10 |
10 |
Таблица 6
Определение ЛД50 заявляемого соединения при пероральном введении его белым мышам массой 7-8 г |
| концентрация препарата, мг/кг |
50 |
100 |
200 |
400 |
800 |
1400 |
2000 |
| относительная смертность а |
0/6 |
0/6 |
0/6 |
0/6 |
0/6 |
3/6 |
4/6 |
| а – выражается как отношение количества павших белых мышей к количеству белых мышей в эксперименте. |
Формула изобретения
Натриевая соль 2-метилтио-6-нитро-1,2,4-триазоло[5,1-c]-1,2,4-триазин-7(4Н)-она, дигидрат, обладающая противовирусной активностью и имеющая формулу
РИСУНКИ
PC4A – Регистрация договора об уступке патента СССР или патента Российской Федерации на изобретение
Прежний патентообладатель:
Государственное образовательное учреждение высшего профессионального образования “Уральский государственный технический университет-УПИ”,
Общество с ограниченной ответственностью Научно-технологическое предприятие “Лиганд”
(73) Патентообладатель:
Общество с ограниченной ответственностью Научно-технологическое предприятие “Лиганд”
Договор № РД0028028 зарегистрирован 22.10.2007
Извещение опубликовано: 10.12.2007 БИ: 34/2007
QB4A – Регистрация лицензионного договора на использование изобретения
Лицензиар(ы): Общество с ограниченной ответственностью “Научно-технологическое предприятие “Лиганд”
Вид лицензии*: ИЛ
Лицензиат(ы): Общество с ограниченной ответственностью “Завод Медсинтез”
Договор № РД0061614 зарегистрирован 11.03.2010
Извещение опубликовано: 20.04.2010 БИ: 11/2010
* ИЛ – исключительная лицензия НИЛ – неисключительная лицензия
|
|