Патент на изобретение №2293729
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ИНГИБИТОРЫ МЕТАЛЛОПРОТЕИНАЗ, ИХ ПРИМЕНЕНИЕ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ
(57) Реферат:
Описывается соединение формулы I где Х представляет собой NR1; Y1 и Y2 представляют собой О; Z выбран из SO2N(R6), N(R7)SO2; m равно 1 или 2; А выбран из прямой связи, (С1-6)алкила; R1 представляет собой Н; R2 и R3, каждый независимо, выбран из Н, алкила, арила, алкиларила, арилалкила; каждый R4 независимо выбран из Н, (С1-3)алкила; R6 выбран из Н, алкила, арила, гетероарила, алкиларила, алкилгетероарила, арилалкила, гетероарилалкила; R2 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R3 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R4 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов; R5 представляет собой моноциклическую, бициклическую или трициклическую группу, содержащую одну или две кольцевые структуры, каждая из которых содержит вплоть до 7 кольцевых атомов, независимо выбранные из циклоалкила, арила, гетероциклоалкила или гетероарила, возможно замещенные; когда R5 представляет собой бициклическую группу, каждая кольцевая структура соединена со следующей кольцевой структурой через прямую связь, через -O-, через (С1-6)алкил или конденсирована с этой следующей кольцевой структурой; R7 выбран из (С1-6)алкила. Описывается также соединение формулы II, фармацевтические композиции и применение соединения формулы I или формулы II в изготовлении лекарства для применения в лечении заболевания или состояния, опосредованного одним или более чем одним ферментом, представляющим собой металлопротеиназу. Представленные соединения полезны в качестве ингибиторов металлопротеиназ, особенно в качестве ингибиторов ММР12. 5 н. и 15 з.п. ф-лы, 3 табл.
Настоящее изобретение относится к соединениям, полезным при ингибировании металлопротеиназ и, в частности, к фармацевтическим композициям, содержащим эти соединения, а также к их применению. Соединения по данному изобретению являются ингибиторами одного или более чем одного фермента, представляющего собой металлопротеиназу. Металлопротеиназы представляют собой надсемейство протеиназ (ферментов), число которых в последние годы резко возросло. По структурным и функциональным соображениям эти ферменты разделены на семейства и подсемейства, как описано в N.М.Hooper (1994) FEBS Letters 354: 1-6. Примерами металлопротеиназ являются матриксные металлопротеиназы (MMPs), такие как коллагеназы (ММР1, ММР8, ММР13), желатиназы (ММР2, ММР9), стромелизины (ММРЗ, ММР10, ММР11), матрилизин (ММР7), металлоэластаза (ММР12), энамелизин (ММР19), МТ-ММР (ММР14, ММР15, ММР16, ММР17); репролизин или адамализин или семейство MDC, которое включает в себя секретазы и шеддазы, такие как TNF-конвертирующие ферменты (ADAM10 и ТАСЕ); семейство астацинов, которое включает в себя такие ферменты, как протеиназа процессинга проколлагена (РСР), а также другие металлопротеиназы, такие как аггриканаза, семейство эндотелин-конвертирующих ферментов и семейство ангиотензин-конвертирующих ферментов. Считается, что металлопротеиназы имеют важное значение при многих физиологических болезненных процессах, в которые вовлечено ремоделирование тканей, такое как развитие эмбриона, костеобразование и маточное ремоделирование во время менструации. В основе этого лежит способность металлопротеиназ расщеплять целый ряд матриксных субстратов, таких как коллаген, протеогликан и фибронектин. Считается также, что металлопротеиназы играют важную роль в процессинге, или секреции, биологически значимых клеточных медиаторов, таких как фактор некроза опухоли (TNF), и в посттрансляционном протеолитическом процессинге, или шеддинге, биологически значимых мембранных белков, таких как IgE рецептор CD23 низкой аффинности (более полный перечень смотри в N.М.Hooper et al., (1997) Biochem. J. 321: 265-279). Металлопротеиназы связаны со многими заболеваниями или состояниями. Ингибирование активности одной или более чем одной металлопротеиназы может принести большую пользу при этих заболеваниях или состояниях, например при различных воспалительных и аллергических заболеваниях, таких как воспаление сустава (особенно ревматоидный артрит, остеоартрит и подагра), воспаление желудочно-кишечного тракта (особенно воспалительное кишечное заболевание, неспецифический язвенный колит и гастрит), воспаление кожи (особенно псориаз, экзема, дерматит); при метастазировании или инвазии опухоли; при заболевании, связанном с неконтролируемым разрушением внеклеточного матрикса, таком как остеоартрит; при заболевании, связанном с резорбцией кости (таком как остеопороз и болезнь Педжета); при заболеваниях, связанных с аберрантным ангиогенезом; при усиленном ремоделировании коллагена, связанном с диабетом, заболеванием периодонта (таким как гингивит), изъязвлением роговицы, изъязвлением кожи, послеоперационными состояниями (такими как кишечный анастомоз) и заживлением кожных ран; при заболеваниях, связанных с демиелинизацией центральной и периферической нервных систем (таких как рассеянный склероз); при болезни Альцгеймера; при ремоделировании внеклеточного матрикса, которое наблюдается при сердечно-сосудистых заболеваниях, таких как рестеноз и атеросклероз; при астме; при рините и при хронических обструктивных болезнях легких (ХОБЛ). ММР12, известная также как макрофагальная эластаза или металлоэластаза, первоначально была клонирована в мыши исследователями Shapiro et al. [1992, Journal of Biological Chemistry 267:4664] и в человеке той же группой исследователей в 1995 году. ММР12 преимущественно экспрессируется в активированных макрофагах, и было показано, что она секретируется из альвеолярных макрофагов курящих людей [Shapiro et al., 1993, Journal of Biological Chemistry 268:23824], а также в пенистых клетках в атеросклеротических повреждениях [Matsumoto et al., 1998, Am J Pathol 153:109]. Мышиная модель ХОБЛ основана на провокации мышей сигаретным дымом в течение шести месяцев, две сигареты в сутки шесть суток в неделю. После такой обработки у мышей дикого типа развивалась легочная эмфизема. Когда в данной модели тестировали мышей, нокаутированных по ММР12, у них не развивалась значительная эмфизема, что четко указывает на то, что ММР12 является ключевым ферментом в патогенезе ХОБЛ. Роль ММР, таких как ММР 12, при ХОБЛ (эмфиземе и бронхите) обсуждалась в Anderson and Shinagawa, 1999, Current Opinion in Anti-inflammatory and Immunomodulatory Investigational Drugs 1(1):29-38. Недавно было обнаружено, что курение усиливает инфильтрацию макрофагов и экспрессию ММР12 макрофагального происхождения в бляшках Кангавари сонной артерии человека [Matetzky S., Fishbein МС et al., Circulation 102(18). 36-39 Suppl. S, Oct 31, 2000]. ММР13, или коллагеназа 3, первоначально была клонирована из библиотеки кДНК, полученной из опухоли молочной железы [J. M. P. Freije et al. (1994) Journal of Biological Chemistry 269 (24): 16766-16773]. ПЦР-РНК анализ РНК из различных тканей показал, что экспрессия ММР13 ограничивается карциномами молочной железы, так как она не была обнаружена в фиброаденомах молочной железы, в нормальной или покоящейся молочной железе, в плаценте, печени, яичнике, матке, простате или околоушной железе, или в клеточных линиях рака молочной железы (T47-D, MCF-7 и ZR75-1). После этого наблюдения ММР13 была обнаружена в трансформированных эпидермальных кератиноцитах [N. Johansson et al. (1997) Cell Growth Differ. 8(2):243-250], плоскоклеточных карциномах [N. Johansson et al. (1997) Am. J. Pathol. 151(2):499-508] и эпидермальных опухолях [К.Airola et al. (1997) J. Invest. Dermatol. 109(2):225-231]. Эти результаты говорят о том, что ММР13 секретируется трансформированными эпителиальными клетками и может быть вовлечена в разрушение внеклеточного матрикса и во взаимодействие клетка-матрикс, связанное с метастазированием, в частности, как это было обнаружено при инвазивных повреждениях раковой опухолью молочной железы и при злокачественном эпителиальном росте при онкогенезе кожи. Из недавно опубликованных данных вытекает, что ММР13 играет роль в обновлении других соединительных тканей. Например, была выдвинута гипотеза, согласующаяся с субстратной специфичностью ММР13 и предпочтительным разрушением коллагена типа II [Р. G. Mitchell et at. (1996) J. Clin. Invest. 97(3):761-768; V.Knauper et al., (1996) The Biochemical Journal 271:1544-1550], о том, что ММР13 выполняет определенную роль в процессе первичного окостенения и скелетного ремоделирования [М. Stahle-Backdahl et al. (1997) Lab. Invest. 76(5):717-728; N. Johansson et al. (1997) Dev. Dyn. 208(3):387-397], в деструктивных заболеваниях суставов, таких как ревматоидный артрит и остеоартрит [D. Wernicke et al. (1996) J. Pheumatol. 23:590-595; P.G.Mitchell et al., (1996) J.Clin. Invest. 97(3):761-768; О.Lindy et al., (1997) Arthritis Rheum 40(8):1391-1399], и при асептическом ослаблении заменителей тазобедренного сустава [S.Imai et al. (1998) J. Bone Joint Surg. Br. 80(4):701-710]. MMP13 также вовлечена в хронический периодонтит взрослых, так как она локализуется в эпителии хронически воспаленной слизистой оболочки ткани десен человека [V.J.Uitto et al. (1998) Am.J.Pathol. 152(6):1489-1499], и в ремоделирование коллагенового матрикса в застарелых ранах [М. Vaalamo et al. (1997) J.Invest. Dermatol. 109(1):96-101]. ММР9 (желатиназа В; коллагеназа типа IV 92 кДа; желатиназа 92 кДа) представляет собой секретируемый белок, который впервые был очищен, а затем клонирован и секвенирован в 1989 году [S.М.Wilhelm et at. (1989) J.Biol. Chem. 264(29):17213-17221; опечатки опубликованы в J.Biol. Chem. (1990) 265(36):22570]. Недавно опубликованный обзор по ММР9 [Т.Н.Vu & Z. Werb (1998) (In: Matrix Metalloproteases, 1998. Edited by W.C.Parks & R.P.Mecnam. pp 115-148. Academic Press. ISBN 0-12-545090-7] является отличным источником подробной информации и ссылок по этой протеазе. Из указанного обзора Т.Н. Vu & Z. Werb (1998) вытекает следующее. Экспрессия ММР9 в норме ограничена несколькими типами клеток, в том числе трофобластами, остеокластами, нейтрофилами и макрофагами. Однако ее экспрессия может быть индуцирована в этих клетках и в клетках других типов несколькими медиаторами, включая воздействие на эти клетки факторов роста или цитокинов. Они представляют собой те самые медиаторы, которые, как правило, вовлечены в инициирование воспалительной реакции. Как и другие секретируемые ММР, ММР9 высвобождается в виде неактивного профермента (Pro-), который впоследствии расщепляется с образованием ферментативно активного фермента. Протеазы, необходимые для этой активации in vivo, неизвестны. Баланс активной ММР9 в сравнении с неактивным ферментом дополнительно регулируется in vivo взаимодействием с природным белком TIMP-1 (тканевый ингибитор металлопротеаз-1). TIMP-1 связывается с С-концевым участком ММР9, что приводит к ингибированию каталитического домена ММР9. Сочетание баланса индуцированной экспрессии РгоММР9, расщепления Pro- до активной ММР9 и присутствия TIMP-1 определяет количество каталитически активной ММР9, присутствующей в сайте локализации. Протеолитически активная ММР9 атакует субстраты, которые включают в себя желатин, эластин и природные коллагены типа IV и типа V; она не обладает активностью против нативного коллагена типа I, протеогликанов или ламининов. Возрастает масса сведений о роли ММР9 в различных физиологических и патологических процессах. Физиологические роли включают в себя инвазию эмбриональных трофобластов через эпителий матки на ранних стадиях эмбриональной имплантации, определенное участие в росте и развитии костей и миграцию воспалительных клеток из сосудистой сети в ткани. Высвобождение ММР9, измеренное с применением иммуноферментного анализа, было значительно более высоким в жидкостях и в AM супернатантах от не подвергавшихся лечению астматиков по сравнению с другими популяциями [Am.J.Resp. Cell & Mol. Biol., Nov 1997, 17(5):583-591]. Повышенную экспрессию ММР9 наблюдали также при некоторых других патологических состояниях, и эти наблюдения свидетельствуют о том, что ММР9 вовлечена в такие болезненные процессы, как ХОБЛ, артрит, метастазирование опухолей, болезнь Альцгеймера, рассеянный склероз и перфорация бляшек при атеросклерозе, приводящая к острым коронарным состояниям, таким как инфаркт миокарда. ММР8 (коллагеназа-2, нейтрофильная коллагеназа) представляет собой фермент 53 кД семейства матриксных металлопротеаз, которые преимущественно экспрессируются в нейтрофилах. Последние исследования указывают на то, что ММР-8 экспрессируется также в других клетках, таких как остеоартритные хондроциты [Shlopov et al., 1997, Arthritis Rheum, 40:2065]. ММР, продуцируемые нейтрофилами, могут вызывать ремоделирование тканей. Следовательно, блокирование ММР-8 может оказывать положительный эффект при фиброзных заболеваниях, например, легкого, и при дегенеративных заболеваниях, подобных эмфиземе легких. Обнаружена также положительная регуляция ММР-8 при остеоартрите, указывающая на то, что блокирование ММР8 также может быть полезным при этом заболевании. ММР3 (стромелизин-1) представляет собой фермент 53 кД семейства матриксных металлопротеаз. Активность ММР-3 была продемонстрирована в фибробластах, выделенных из воспаленной десны [Uitto V.J. et al., 1981, J.Periodontal Res., 16:417-424], и было показано, что уровни фермента коррелируют с тяжестью заболевания десны [Overall С.М. et al., 1987, J.Periodontal Res., 22:81-88]. ММР-3 продуцируется также базальными кератиноцитами при различных хронических язвах [Saarialho-Kere U.К. et al., 1994, J. Clin. invest. 94:79-88]. мРНК и белок ММР-3 были обнаружены в базальных кератиноцитах рядом с краем раны, но дистально от него, где, вероятно, имеются сайты пролиферирующего эпидермиса. Таким образом, ММР-3 может препятствовать заживлению эпидермиса. Несколько исследователей продемонстрировали стойкое повышение ММР3 в синовиальных жидкостях пациентов с ревматоидным и остеоартритом по сравнению с контролями [Walakovits L.A. et al., 1992, Arthritis Rheum., 35:35-42, Zafarullah M. et al., 1993, J. Rheumatol. 20:693-697]. Эти исследования дают основание полагать, что ингибитор ММР-3 будет лечить заболевания, в которые вовлечено разрушение внеклеточного матрикса, приводящее к воспалению вследствие инфильтрации лимфоцитов или к потере структурной целостности, необходимой для функционирования органа. Известно множество ингибиторов металлопротеиназ (см., например, обзор по ингибиторам ММР Beckett R. P. and Whittaker M., 1998, Exp. Opin. Ther. Patents, 8(3):259-282). Разные классы соединений могут иметь разные степени эффективности и избирательности в отношении ингибирования различных металлопротеиназ. Whittaker M. et al. [1999, Chemical Reviews 99(9):2735-2776] рассматривают целый ряд известных соединений-ингибиторов ММР. Они утверждают, что эффективному ингибитору ММР необходима связывающая цинк группа (ZBG) (функциональная группа, способная хелатировать ион цинка(II) в активном сайте), по меньшей мере одна функциональная группа, которая обеспечивает взаимодействие водородной связи с основной цепью фермента, и одна или более чем одна боковая цепь, которая подвергается эффективным Ван-дер-Ваальсовым взаимодействиям с подсайтами фермента. В известных ингибиторах ММР связывающие цинк группы включают карбоновокислотные группы, гидроксамовокислотные группы, сульфгидрильные или меркаптогруппы и т.д. Например, Whittaker M. et al. обсуждают следующие ингибиторы ММР.
Приведенное выше соединение вошло в стадию клинической разработки. Оно имеет меркаптоацильную связывающую цинк группу, триметилгидантоинилэтильную группу в положении Р1 и лейцинил-трет-бутилглициниловую основную цепь.
Приведенное выше соединение имеет меркаптоацильную связывающую цинк группу и имидную группу в положении Р1.
Приведенное выше соединение разработано для лечения артрита. Оно имеет непептидную сукцинилгидроксаматную связывающую цинк группу и триметилгидантоинилэтильную группу в положении Р1.
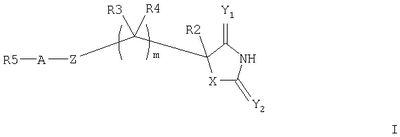
Приведенное выше соединение представляет собой фталимидопроизводное, которое ингибирует коллагеназы. Оно имеет непептидную сукцинилгидроксаматную связывающую цинк группу и циклическую имидную группу в положении Р1. Whittaker M. et al. также обсуждают другие ингибиторы ММР, имеющие Р1 циклическую имидогруппу и различные связывающие цинк группы (сукцинилгидроксаматную, карбоновокислотную, тиоловую группу, группу на основе фосфора). Приведенные выше соединения представляются хорошими ингибиторами ММР8 и ММР9 (международные заявки WO 9858925, WO 9858915). Они имеют пиримидин-2,3,4-трионовую связывающую цинк группу. Указанные ниже соединения не известны как ингибиторы ММР: Lora-Tamayo M. et al. (1968, An. Quim 64(6): 591-606) описывают синтез указанных ниже соединений как потенциальных противораковых агентов: В патентах Чехии №№151744 (19731119) и 152617 (1974022) описаны синтез и противосудорожная активность следующих соединений: R=4-NO2, 4-ОМе, 2-NO2. В патенте США №3529019 (19700915) описаны указанные ниже соединения, используемые в качестве промежуточных соединений: В международной заявке WO 00/09103 описаны соединения, полезные для лечения расстройства зрения, в том числе следующие (соединения 81 и 83, таблица А, с.47): Теперь авторы изобретения открыли новый класс соединений, которые действуют как ингибиторы металлопротеиназ и представляют особый интерес при ингибировании ММР, таких как ММР12. Эти соединения являются ингибиторами металлопротеиназ, имеющими связывающую металл группу, которой нет в известных ингибиторах металлопротеиназ. В частности, авторы изобретения открыли соединения, которые являются эффективными ингибиторами ММР12 и обладают желательными профилями активности. Соединения по данному изобретению обладают благоприятными эффективностью, избирательностью и/или фармакокинетическими свойствами. Соединения по данному изобретению, представляющие собой ингибиторы металлопротеиназ, содержат связывающую металл группу и одну или более чем одну функциональную группу или боковую цепь, отличаются тем, что связывающая металл группа имеет формулу (k)
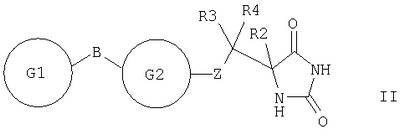
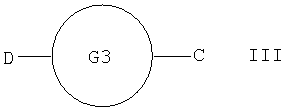
где Х выбран из NR1, О, S; Y1 и Y2 независимо выбраны из О, S; R1 выбран из Н, алкила, галогеноалкила; любые алкильные группы, упомянутые выше, могут быть прямоцепочечными или разветвленными; любая алкильная группа, упомянутая выше, предпочтительно представляет собой (С1-7)алкил и наиболее предпочтительно (С1-6) алкил. Соединение, представляющее собой ингибитор металлопротеиназ, является соединением, которое ингибирует активность фермента, представляющего собой металлопротеиназу (например ММР). В качестве неограничивающего примера соединение-ингибитор может показывать IC50 in vitro в диапазоне 0,1-10000 наномоль, предпочтительно 0,1-1000 наномоль. Связывающая металл группа представляет собой функциональную группу, способную связывать ион металла в активном сайте фермента. Например, связывающая металл группа будет представлять собой связывающую цинк группу в ингибиторах ММР, связывающую ион цинка(II) в активном сайте. Связывающая металл группа формулы (k) основана на пятичленной кольцевой структуре и предпочтительно представляет собой гидантоиновую группу, наиболее предпочтительно 5-замещенный 1-Н,3-Н-имидазолидин-2,4-дион. Таким образом, в первом аспекте изобретения предложены соединения формулы I где X выбран из NR1, О, S; Y1 и Y2 независимо выбраны из О, S; Z выбран из SO2N(R6), N(R7)SO2, N(R7)SO2N(R6); m равно 1 или 2; А выбран из прямой связи, (С1-6)алкила, (С1-6)галогеноалкила или (С1-6)гетероалкила, содержащего гетерогруппу, выбранную из N, О, S, SO, SO2, или содержащего две гетерогруппы, выбранные из N, О, S, SO, SO2 и разделенные по меньшей мере двумя атомами углерода; R1 выбран из H, (С1-3)алкила, галогеноалкила; R2 и R3, каждый независимо, выбран из H, галогена (предпочтительно фтора), алкила, гетероалкила, циклоалкила, гетероциклоалкила, арила, гетероарила, алкиларила, алкилгетероарила, гетероалкиларила, гетероалкилгетероарила, арилалкила, арилгетероалкила, гетероарилалкила, гетероарилгетероалкила, ариларила, арилгетероарила, гетероариларила, гетероарилгетероарила, циклоалкилалкила, гетероциклоалкилалкила; каждый R4 независимо выбран из H, галогена (предпочтительно фтора), (С1-3)алкила или галогеноалкила; R6 выбран из H, алкила, гетероалкила, гетероциклоалкила, арила, гетероарила, алкиларила, алкилгетероарила, гетероалкиларила, гетероалкилгетероарила, арилалкила, арилгетероалкила, гетероарилалкила, гетероарилгетероалкила, ариларила, арилгетероарила, гетероариларила, гетероарилгетероарила; каждый из радикалов R2, R3 и R6 независимо возможно может быть замещен одной или более (предпочтительно одной) группой, выбранной из алкила, гетероалкила, арила, гетероарила, галогено, галогеноалкила, гидрокси, алкокси, галогеноалкокси, тиола, алкилтиола, арилтиола, алкилсульфона, галогеноалкилсульфона, арилсульфона, аминосульфона, N-алкиламиносульфона, N,N-диалкиламиносульфона, ариламиносульфона, амино, N-алкиламино, N,N-диалкиламино, амидо, N-алкиламидо, N,N-диалкиламидо, циано, сульфонамино, алкилсульфонамино, арилсульфонамино, амидино, N-аминосульфонамидино, гуанидино, N-цианогуанидино, тиогуанидино, 2-нитро-этен-1,1-диамина, карбокси, алкилкарбокси, нитро; R2 и R3 возможно могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R2 и R4 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R2 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R3 и R4 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R3 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R4 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов; R5 представляет собой моноциклическую, бициклическую или трициклическую группу, содержащую одну, две или три кольцевые структуры, каждая из которых содержит вплоть до 7 кольцевых атомов, независимо выбранных из циклоалкила, арила, гетероциклоалкила или гетероарила, причем каждая кольцевая структура независимо возможно замещена одним или более чем одним заместителем, независимо выбранным из галогена, гидрокси, алкила, алкокси, галогеноалкокси, амино, N-алкиламино, N,N-диалкиламино, алкилсульфонамино, алкилкарбоксиамино, циано, нитро, тиола, алкилтиола, алкилсульфонила, галогеноалкилсульфонила, алкиламиносульфонила, карбоксилата, алкилкарбоксилата, аминокарбокси, N-алкиламинокарбокси, N,N-диалкиламинокарбокси, где любой алкильный радикал в пределах любого заместителя сам возможно может быть замещен одной или более чем одной группой, выбранной из галогена, гидрокси, алкокси, галогеноалкокси, амино, N-алкиламино, N,N-диалкиламино, N-алкилсульфонамино, N-алкилкарбоксиамино, циано, нитро, тиола, алкилтиола, алкилсульфонила, N-алкиламиносульфонила, карбоксилата, алкилкарбокси, аминокарбокси, N-алкиламинокарбокси, N,N-диалкиламинокарбокси; когда R5 представляет собой бициклическую или трициклическую группу, каждая кольцевая структура соединена со следующей кольцевой структурой через прямую связь, через -О-, через (С1-6)алкил, через (С1-6)галогеноалкил, через (С1-6)гетероалкил, через (С1-6)алкенил, через (С1-6)алкинил, через сульфон или конденсирована с этой следующей кольцевой структурой; R7 выбран из (С1-6)алкила, (С3-7)циклоалкила, (С2-6)гетероалкила, (С2-6) циклогетероалкила; любая гетероалкильная группа, упомянутая выше, представляет собой замещенный гетероатомом алкил, содержащий одну или более чем одну гетерогруппу, независимо выбранную из N, О, S, SO, SO2 (причем гетерогруппа представляет собой гетероатом или группу атомов); любая гетероциклоалкильная или гетероарильная группа, упомянутая выше, содержит одну или более чем одну гетерогруппу, независимо выбранную из N, О, S, SO, SO2; любая алкильная, алкенильная или алкинильная группа, упомянутая выше, может быть прямоцепочечной или разветвленной; если не указано иное, любая алкильная группа, упомянутая выше, предпочтительно представляет собой (С1-7)алкил и наиболее предпочтительно (С1-6)алкил; при условии, что когда Х представляет собой NR1, R1 представляет собой Н, Y1 представляет собой О, Y2 представляет собой О, Z представляет собой SO2N(R6), R6 представляет собой Н, R2 представляет собой Н, m равно 1, R3 представляет собой Н, R4 представляет собой Н и А представляет собой прямую связь, тогда R5 не представляет собой фенил, пара-нитрофенил, пара-этоксифенил или мета-метилфенил; когда Х представляет собой S или NR1 и R1 представляет собой Н, Y1 представляет собой О, Y2 представляет собой О, Z представляет собой SO2N(R6), R6 представляет собой алкил, R2 представляет собой Н, m равно 1, один из R3 и R4 представляет собой Н, а другой представляет собой алкил, R3 и R6 или R4 и R6 соединены с образованием 5-членного кольца и А представляет собой прямую связь, тогда R5 не представляет собой фенил. Предпочтительными соединениями формулы I являются те, к которым применимо одно или более чем одно из указанного ниже: Х представляет собой NR1; Z представляет собой SO2N(R6), особенно когда атом S группы Z присоединен к группе А в соединении формулы I; по меньшей мере один из Y1 и Y2 представляет собой О, особенно предпочтительно и Y1, и Y2 представляет собой О; m равно 1; R1 представляет собой Н, (С1-3)алкил, (С1-3)галогеноалкил, особенно предпочтительно R1 представляет собой Н; R2 представляет собой Н, алкил, гидроксиалкил, аминоалкил, циклоалкилалкил, алкилциклоалкил, арилалкил, алкиларил, гетероалкил, гетероциклоалкилалкил, алкилгетероциклоалкил, гетероарилалкил, гетероалкиларил, особенно предпочтительно R2 представляет собой алкил, аминоалкил или гетероарилалкил; R3 и/или R4 представляют собой Н; R3 и/или R4 представляют собой метил; R3 и R4 образуют 5- или 6-членное кольцо (предпочтительно 5-членное кольцо) или R3 и R6 образуют 5- или 6-членное кольцо (предпочтительно 5-членное кольцо), или R4 и R6 образуют 5- или 6-членное кольцо (предпочтительно 5-членное кольцо); особенно предпочтительно R3 и R6 образуют 5- или 6-членное кольцо, наиболее предпочтительно 5-членное кольцо; R2 и R3 образуют 5-членное кольцо или R2 и R6 образуют 5-членное кольцо; R5 содержит возможно замещенные арильные или гетероарильные 5-или 6-членные кольца в количестве одного, двух или трех; R5 представляет собой бициклическую или трициклическую группу, содержащую две или три возможно замещенные кольцевые структуры; R3 и R6 образуют 5- или 6-членное кольцо (предпочтительно 5-членное кольцо), или R4 и R6 образуют 5- или 6-членное кольцо (предпочтительно 5-членное кольцо), и R5 представляет собой бициклическую или трициклическую группу, содержащую две или три возможно замещенные кольцевые структуры. Особенно предпочтительными соединениями формулы I являются те, где R5 представляет собой бициклическую или трициклическую группу, содержащую две или три возможно замещенные кольцевые структуры. Например, конкретными соединениями формулы I являются те, где Y1 представляет собой О, Y2 представляет собой О, Х представляет собой NR1, R1 представляет собой Н, R2 представляет собой Н, m равно 1, R3 представляет собой Н, R4 представляет собой Н, Z представляет собой SO2N(R6), R6 представляет собой Н, (С1-4)алкил, метилбензил или метилпиридил, А представляет собой прямую связь и R5 представляет собой бициклическую или трициклическую группу, содержащую две или три возможно замещенные кольцевые структуры. Некоторые такие соединения описаны в примерах 1 и 2. Другими конкретными соединениями формулы I являются те, где Y1 представляет собой О, Y2 представляет собой О, Х представляет собой NR1, R1 представляет собой Н, R2 представляет собой Н, метил или бензил, m равно 1, R3 представляет собой Н или метил, R4 представляет собой Н, Z представляет собой SO2N(R6), R6 представляет собой Н, А представляет собой прямую связь и R5 представляет собой бициклическую или трициклическую группу, содержащую две или три возможно замещенные кольцевые структуры. Некоторые из таких соединений описаны в примере 3. Далее, согласно изобретению предложены соединения формулы II где каждый из G1 и G2 представляет собой моноциклическую кольцевую структуру, каждая из которых содержит вплоть до 7 кольцевых атомов, независимо выбранную из циклоалкила, арила, гетероциклоалкила или гетероарила, причем каждая кольцевая структура независимо возможно замещена одним или двумя заместителями, независимо выбранными из галогена, гидрокси, галогеноалкокси, амино, N-алкиламино, N,N-диалкиламино, циано, нитро, алкила, алкокси, алкилсульфона, галогеноалкилсульфона, алкилкарбамата, алкиламида, где любой алкильный радикал в пределах любого заместителя сам может быть возможно замещен одной или более чем одной группой, выбранной из галогена, гидрокси, амино, N-алкиламино, N,N-диалкиламино, циано, нитро, алкокси, галогеноалкокси; Z представляет собой SO2N(R6); В выбран из прямой связи, О, (С1-6)алкила, (С1-6)гетероалкила; R2 выбран из Н, (С1-6)алкила, галогеноалкила, гидроксиалкила, алкоксиалкила, аминоалкила, (N-алкиламино)алкила, (N,N-диалкиламино)алкила, амидоалкила, тиоалкила или R2 представляет собой группу формулы III
С и D независимо выбраны из прямой связи, Н, (С1-6)алкила, (С1-6)галогеноалкила или (С1-6)гетероалкила, содержащего один или два гетероатома, выбранных из N, О или S, так что, когда присутствуют два гетероатома, они разделены по меньшей мере двумя атомами углерода; G3 представляет собой моноциклическую кольцевую структуру, содержащую вплоть до 7 кольцевых атомов, независимо выбранную из циклоалкила, арила, гетероциклоалкила или гетероарила, возможно замещенную одним или двумя заместителями, независимо выбранными из галогена, гидрокси, амино, N-алкиламино, N,N-диалкиламино, циано, нитро, алкила, алкокси, алкилсульфона, галогеноалкилсульфона или алкила, замещенного одной или более чем одной группой, выбранной из галогена, гидрокси, амино, N-алкиламино, N,N-диалкиламино, циано, нитро, алкокси, галогеноалкокси; R2 возможно замещен галогено, галогеноалкилом, гидрокси, алкокси, галогеноалкокси, амино, аминоалкилом, N-алкиламино, N,N-диалкиламино, (N-алкиламино)алкилом, (N,N-диалкиламино)алкилом, алкилсульфоном, аминосульфоном, N-алкиламиносульфоном, N,N-диалкиламиносульфоном, амидо, N-алкиламидо, N,N-диалкиламидо, циано, сульфонамино, алкилсульфонамино, амидино, N-аминосульфонамидино, гуанидино, N-цианогуанидино, тиогуанидино, 2-нитрогуанидино, 2-нитроэтен-1,1-диамино, карбокси, алкилкарбокси; R3 и R4 независимо выбраны из Н или (С1-3)алкила; R6 выбран из Н, (С1-3)алкиламино или R6 представляет собой (С1-3) алкил, возможно замещенный арилом, гетероарилом, гетероциклоалкилом; R2 и R3 возможно могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R2 и R4 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R2 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов; либо R3 и R4 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов; либо R3 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов; либо R4 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов; любая гетероалкильная группа, упомянутая выше, представляет собой замещенный гетероатомом алкил, содержащий одну или более чем одну гетерогруппу, независимо выбранную из N, О, S, SO, SO2 (причем гетерогруппа представляет собой гетероатом или группу атомов); любая гетероциклоалкильная или гетероарильная группа, упомянутая выше, содержит одну или более чем одну гетерогруппу, независимо выбранную из N, О, S,SO, SO2; любая алкильная, алкенильная или алкинильная группа, упомянутая выше, может быть прямоцепочечной или разветвленной; если не указано иное, любая алкильная группа, упомянутая выше, предпочтительно представляет собой (С1-7)алкил и наиболее предпочтительно (С1-6)алкил. Предпочтительными соединениями формулы II являются те, к которым применимо одно или более чем одно из указанного ниже: Z представляет собой SO2N(R6) и атом S группы Z присоединен к кольцу G2; В представляет собой прямую связь или О; R2 не является возможно замещенным, или R2 выбран из Н, (С1-6)алкила, арил-(С1-6)алкила или гетероарил-(С1-6)алкила, возможно замещенных галогено, галогеноалкилом, гидрокси, алкокси, галогеноалкокси, амино, аминоалкилом, N-алкиламино, N,N-диалкиламино, (N-алкиламино)алкилом, (N,N-диалкиламино)алкилом, алкилсульфоном, аминосульфоном, N-алкиламиносульфоном, N,N-диалкиламиносульфоном, амидо, N-алкиламидо, N,N-диалкиламидо, циано, сульфонамино, алкилсульфонамино, амидино, N-аминосульфонамидино, гуанидино, N-цианогуанидино, тиогуанидино, 2-нитрогуанидино, 2-нитроэтен-1,1-диамино, карбокси, алкилкарбокси; каждый из R3 и R4 представляет собой Н; R6 представляет собой Н, бензил или метиленпиридин; G1 и G2, каждый, выбраны из арила или гетероарила; R3 и R4 образуют 5- или 6-членное кольцо (предпочтительно 5-членное кольцо), или R3 и R6 образуют 5- или 6-членное кольцо (предпочтительно 5-членное кольцо), или R4 и R6 образуют 5- или 6-членное кольцо (предпочтительно 5-членное кольцо); особенно предпочтительно R3 и R6 образуют 5- или 6-членное кольцо, наиболее предпочтительно 5-членное кольцо; R2 и R3 образуют 5-членное кольцо или R2 и R6 образуют 5-членное кольцо. Особенно предпочтительными соединениями формулы II являются те, где Z представляет собой SO2N(R6) и атом S группы Z присоединен к кольцу G2. Например, конкретные соединения по изобретению включают соединения формулы II, где (а) В представляет собой прямую связь или О; Z представляет собой SO2N(R6) и R2 выбран из Н, (С1-6)алкила, арил-(С1-6)алкила или гетероарил-(С1-6)алкила, возможно замещенных галогено, галогеноалкилом, гидрокси, алкокси, галогеноалкокси, амино, аминоалкилом, N-алкиламино, N,N-диалкиламино, (N-алкиламино)алкилом, (N,N-диалкиламино)алкилом, алкилсульфонилом, аминосульфонилом, N-алкиламиносульфонилом, N,N-диалкиламиносульфонилом, амидо, N-алкиламидо, N,N-диалкиламидо, циано, сульфонамино, алкилсульфонамино, амидино, N-аминосульфонамидино, гуанидино, N-цианогуанидино, тиогуанидино, 2-нитрогуанидино, 2-нитроэтен-1,1-диамино, карбокси, алкилкарбокси; каждый из R3 и R4 представляет собой Н и R6 представляет собой Н, бензил или метиленпиридин, или (б) Z представляет собой SO2N(R6) и R3 представляет собой Н, и R4 представляет собой Н (соединения формулы II’), где R2 не является возможно замещенным; предпочтительно G1 и G2, каждый, выбраны из арила или гетероарила Подходящие значения для R2 включают указанные ниже: Подходящие значения для R5 включают указанные ниже: X’=связь, О, СН2, CHF, CF2; R=F, Cl, Br, CF3, CF3О, CH3О, ОН, CF3CH2, Должно быть понятно, что конкретные заместители и количество заместителей в соединениях по изобретению выбраны таким образом, чтобы избежать стерически нежелательных комбинаций. Каждое проиллюстрированное примером соединение представляет собой конкретный и независимый аспект изобретения. Если в соединениях по изобретению имеются оптически активные центры, авторы изобретения раскрывают все индивидуальные оптически активные формы и их комбинации как индивидуальные конкретные воплощения изобретения, также как и их соответствующие рацематы. Рацематы могут быть разделены на индивидуальные оптически активные формы с использованием известных методик (см. Advanced Organic Chemistry: 3rd Edition: author J March, p 104-107), включая, например, образование диастереомерных производных, имеющих подходящие оптически активные вспомогательные группы, с последующим разделением, а затем отщеплением этих вспомогательных групп. Должно быть понятно, что соединения по изобретению могут содержать один или более чем один асимметрически замещенный атом углерода. Наличие одного или более чем одного из таких асимметрических центров (хиральных центров) в соединении формулы I способно давать стереоизомеры, и в каждом случае следует иметь в виду, что изобретение распространяется на все такие стереоизомеры, включая энантиомеры и диастереомеры, а также их смеси, включая их рацемические смеси. В тех случаях, когда существуют таутомеры соединений по изобретению, авторы изобретения раскрывают все индивидуальные таутомерные формы и их комбинации как индивидуальные конкретные воплощения изобретения. Как упомянуто выше, соединения по изобретению являются ингибиторами металлопротеиназ, в частности они являются ингибиторами ММР12. Каждое из перечисленных выше показаний для соединений формулы I представляет собой независимое и конкретное воплощение изобретения. Некоторые соединения по изобретению имеют особенно применимые в качестве ингибиторов ММР13 и/или ММР9, и/или ММР8, и/или ММР3. Соединения по изобретению проявляют благоприятный профиль селективности. Хотя авторы изобретения не желают быть связанными теоретическими соображениями, они считают, что соединения по изобретению проявляют селективное ингибирование в отношении любого из перечисленных выше показаний по сравнению с любой ингибиторной активностью в отношении ММР1, в качестве неограничивающего примера они могут проявлять 100-1000-кратную селективность по сравнению с ингибиторной активностью в отношении ММР1. Соединения по изобретению могут быть предоставлены в виде фармацевтически приемлемых солей. Эти соли включают соли присоединения кислот, такие как гидрохлорид, гидробромид, цитрат и малеат, и соли, образованные с фосфорной кислотой и серной кислотой. В другом аспекте подходящими солями являются соли оснований, такие как соль щелочного металла, например натрия или калия, соль щелочноземельного металла, например кальция или магния, или соль органического амина, например триэтиламина. Они также могут быть предоставлены в виде in vivo гидролизуемых эфиров. Эти эфиры представляют собой фармацевтически приемлемые эфиры, которые гидролизуются в организме человека, давая родоначальное соединение. Такие эфиры можно идентифицировать путем введения, например, внутривенно испытуемому животному тестируемого соединения и последующего исследования жидкостей организма этого испытуемомого животного. Подходящие in vivo гидролизуемые эфиры для карбокси включают метоксиметил и для гидрокси включают формил и ацетил, особенно ацетил. Для того чтобы использовать соединение по изобретению, представляющее собой ингибитор металлопротеиназ (соединение формулы I или II), или его фармацевтически приемлемую соль или in vivo гидролизуемый эфир для терапевтического лечения (включая профилактическое лечение) млекопитающих, включая людей, обычно его готовят в соответствии со стандартной фармацевтической практикой в виде фармацевтической композиции. Следовательно, в другом аспекте настоящего изобретения предложена фармацевтическая композиция, которая содержит соединение по изобретению (соединение формулы I или II) или его фармацевтически приемлемую соль, или in vivo гидролизуемый эфир и фармацевтически приемлемый носитель. Фармацевтические композиции по изобретению можно вводить стандартным способом при заболевании или состоянии, которое требуется лечить, например пероральным, местным, парентеральным, трансбуккальным, интраназальным, вагинальным или ректальным путем введения или ингаляцией. Для этих целей соединения по данному изобретению могут быть приготовлены известными в данной области техники способами в форме, например, таблеток, капсул, водных или масляных растворов, суспензий, эмульсий, кремов, мазей, гелей, назальных спреев, суппозиториев, тонко измельченных порошков или аэрозолей для ингаляции, а для парентерального применения (включая внутривенное, внутримышечное или инфузию) в форме стерильных водных или масляных растворов или суспензий или стерильных эмульсий. В дополнение к соединению по настоящему изобретению фармацевтическая композиция по данному изобретению может также содержать один или более чем один фармакологический агент, полезный при лечении одного или более чем одного заболевания или состояния, описанного здесь выше, либо ее можно совместно вводить (одновременно или последовательно) с одним или более чем одним таким фармакологическим агентом. Фармацевтические композиции по изобретению обычно будут вводить людям так, чтобы суточная доза составляла, например, от 0,5 до 75 мг/кг массы тела (и предпочтительно от 0,5 до 30 мг/кг массы тела). Эту суточную дозу можно давать в разделенных дозах, как необходимо, причем точное количество получаемого соединения и путь введения зависят от массы, возраста и пола пациента, которого лечат, и от конкретного заболевания или состояния, которое лечат, в соответствии с известными в данной области принципами. Типичные стандартные лекарственные формы будут содержать примерно от 1 до 500 мг соединения по данному изобретению. Таким образом, в следующем аспекте предложено соединение формулы I или его фармацевтически приемлемая соль, или in vivo гидролизуемый эфир для применения в способе терапевтического лечения человеческого или животного организма или для применения в качестве терапевтического агента. Авторы изобретения раскрывают применение в лечении заболевания или состояния, опосредованного одним или более чем одним ферментом, представляющим собой металлопротеиназу. В частности, авторы изобретения раскрывают применение в лечении заболевания или состояния, опосредованного ММР12 и/или ММР13, и/или ММР9, и/или ММР8, и/или ММР3, особенно применение в лечении заболевания или состояния, опосредованного ММР12 или ММР9, главным образом применение в лечении заболевания или состояния, опосредованного ММР12. В частности, предложено соединение формулы II или его фармацевтически приемлемая соль, или in vivo гидролизуемый эфир для применения в способе терапевтического лечения человеческого или животного организма или для применения в качестве терапевтического агента (такого как применение в лечении заболевания или состояния, опосредованного ММР12 и/или ММР13, и/или ММР9, и/или ММР8, и/или ММР3, особенно ММР12 или ММР9, главным образом ММР12). В следующем аспекте изобретения предложен способ лечения опосредованного металлопротеиназами заболевания или состояния, при котором теплокровному животному вводят терапевтически эффективное количество соединения формулы I или его фармацевтически приемлемой соли или in vivo гидролизуемого эфира. Авторы изобретения также раскрывают применение соединения формулы I или его фармацевтически приемлемой соли или in vivo гидролизуемого предшественника в изготовлении лекарства для применения в лечении заболевания или состояния, опосредованного одним или более чем одним ферментом, представляющим собой металлопротеиназу. Например, предложен способ лечения опосредованного металлопротеиназами заболевания или состояния, при котором теплокровному животному вводят терапевтически эффективное количество соединения формулы II (или его фармацевтически приемлемой соли, или in vivo гидролизуемого эфира). Предложено также применение соединения формулы II (или его фармацевтически приемлемой соли, или in vivo гидролизуемого предшественника) в изготовлении лекарства для применения в лечении заболевания или состояния, опосредованного одним или более чем одним ферментом, представляющим собой металлопротеиназу. Заболевания или состояния, опосредованные металлопротеиназами, включают астму, ринит, хронические обструктивные болезни легких (ХОБЛ), артрит (такой как ревматоидный артрит и остеоартрит), атеросклероз и рестеноз, рак, инвазию и метастазирование, заболевания, в которые вовлечено разрушение тканей, ослабление заменителей тазобедренного сустава, заболевание периодонта, фиброзное заболевание, инфаркт и сердечное заболевание, фиброз печени и почки, эндометриоз, заболевания, связанные с истощением внеклеточного матрикса, сердечную недостаточность, аневризмы аорты, заболевания ЦНС, такие как болезнь Альцгеймера и рассеянный склероз (PC), гематологические расстройства. Получение соединений по изобретению В другом аспекте настоящего изобретения предложен способ получения соединения формулы I или II или его фармацевтически приемлемой соли или in vivo гидролизуемого эфира, как описано ниже в (а)-(в). Понятно, что многие релевантные исходные вещества имеются в продаже, или доступны иным путем, или их можно синтезировать известными способами, или найти в научной литературе. (а) Соединения формулы I, в которой Y1 и Y2 каждый представляет собой О, Z представляет собой SO2N(R6), А представляет собой прямую связь, Х представляет собой NR1, R1 представляет собой Н, R2 представляет собой Н, m равно 1, R3 представляет собой Н, R4 представляет собой Н, a R5 и R6 являются такими, как определено в формуле I, могут быть получены согласно схеме 1. Когда R6 представляет собой Н, производное N1-BOC-D-диаминопропионовой кислоты формулы IV подвергают взаимодействию с подходящим сульфонилхлоридом формулы V в основной среде с образованием сульфонамидов формулы VI. Удаление защиты в кислой среде, взаимодействие с цианатом калия до соответствующей мочевины и, наконец, циклизация в кислой среде приводят к получению соединения формулы I. Когда R6 представляет собой алкил, такой как метил, этил, пропил, изопропил и н-бутил, N2-алкил-N1-ВОС-D-диаминопропионовую кислоту формулы IV получают согласно Andruszkiewics, R.: Pol. J.Chem., 62, 257 (1988). Когда R6 представляет собой возможно замещенный бензил, метилбензил, метилпиридил, метилгетероарил, N2-замещенную аминокислоту формулы IV получают согласно Helv. Chim. Acta, 46, 327 (1963). Схема 1 Реакцию IV-VI предпочтительно проводят в подходящем растворителе, возможно в присутствии основания, в течение 1-24 ч при температуре от температуры окружающей среды до температуры дефлегмации. Предпочтительно растворители, такие как пиридин, диметилформамид, тетрагидрофуран, ацетонитрил или дихлорметан, используют с основаниями, такими как триэтиламин, N-метилморфолин, пиридин или карбонаты щелочных металлов, при температуре окружающей среды в течение времени реакции 2-16 ч или до окончания реакции, которое определяют хроматографическим или спектроскопическим способом. Реакции сульфонилхлоридов формулы V с различными вторичными аминами описаны ранее в литературе, и варианты условий будут очевидны специалистам в данной области техники. Многие соединения формулы V имеются в продаже, либо их синтез описан в литературе. Конкретные производные формулы VI могут быть получены способами, известными специалистам в данной области техники. (б) Соединения формулы I, в которой Y1 и Y2 каждый представляет собой О, Z представляет собой SO2N(R6), R6 представляет собой Н, А представляет собой прямую связь, Х представляет собой NR1, R1 представляет собой Н, m равно 1, a R2, R3, R4 и R5 являются такими, как определено в формуле I, могут быть получены согласно схеме 1. Соединения, в которых R2 представляет собой Н, R3 представляет собой Н и R4 представляет собой алкил или арил, могут быть получены из соответствующих BOC-N-защищенных- Соединения, в которых R2 представляет собой алкил или арил, R3 представляет собой Н и R4 представляет собой алкил или арил, могут быть получены из соответствующего ВОС-N-защищенного- Схема 2 Соединения формулы VII подвергают взаимодействию с цианидом щелочного металла и карбонатом аммония (реакция Штрекера) с получением соответствующих гидантоинов формулы VIIa. Диастереоизомеры возможно могут быть разделены после любой из трех остальных стадий синтеза: карбаматы формулы VIIa и сульфонамидные соединения формулы II – хроматографией на силикагеле, после удаления защиты промежуточного аминосоединения кристаллизацией. Промежуточные аминосоединения возможно используют для прямого связывания с сульфонилхлоридами формулы V, как это описано в сульфонилировании (а) выше, в основной среде с образованием соединений формулы I. Реакцию от VII до VIIa предпочтительно проводят в закрытом стальном сосуде в водном спиртовом растворителе при 90-130°С в течение 3-16 часов или до окончания реакции, которое определяют хроматографическим или спектроскопическим способом. Обработка 1-4-кратным избытком цианидных солей, предпочтительно 1-2 эквивалентами, и 2-6-кратным избытком карбоната аммония, предпочтительно 4-6 эквивалентами, приводит к получению гидантоинов формулы VIIa. Последующее удаление защиты и сульфонилирование, как показано на схеме 1, приводят к получению соединения формулы I. Аминоальдегиды или кетоны формулы VII и их защищенные производные имеются в продаже. Известны и другие способы получения (в) Соединения формулы I, в которой Y1 и Y2 каждый представляет собой О, Х представляет собой NR1 (R1=H), Z=N(R7)SO2, m=1, R4=H, a R2, R3, R5 и R7 являются такими, как определено в формуле I, могут быть получены путем взаимодействия соединения формулы VIII, в которой R2, R3, R5, R7 и А являются такими, как описано в формуле I, с сульфонилхлоридами формулы IX в полярных апротонных растворителях, таких как ТГФ или ДМФ, в присутствии оснований, таких как карбонаты щелочных металлов, или третичные алкиламины, или полимерные амины. Амины формулы VIII широко известны в литературе и доступны из многочисленных коммерческих источников. Конкретные новые варианты соединений формулы VIII могут быть получены способами, известными специалистам в данной области техники. Сульфонилхлориды формулы IX могут быть получены окислением хлором сульфидов и дисульфидов формулы X, где R8 представляет собой такую группу как водород, изопропил, бензил или сульфид, так что формула Х включает в себя симметричный дисульфид. Сульфиды формулы Х могут быть получены из цистеина или цистина (R2, R3=H) и их эфиров последовательной обработкой цианатом щелочного металла и сильными кислотами, например цианатом калия и соляной кислотой. Альтернативно сульфиды формулы Х можно получить, подвернув кетоны формулы XI воздействию условий, которые описаны в превращении VII в VIIa в (а) выше. Соединения по изобретению можно оценить, например, в следующих анализах. Анализы выделенного фермента Семейство матриксных металлопротеиназ, включая, например. ММР12, ММР13 Каталитический домен рекомбинантной человеческой ММР12 можно экспрессировать и очистить, как описано в Parkar A.A. et al. (2000), Protein Expression and Purification, 20: 152. Этот очищенный фермент можно использовать для мониторинга ингибиторов активности следующим образом: ММР12 (конечная концентрация 50 нг/мл) инкубируют в течение 30 минут при КТ (комнатной температуре) в аналитическом буфере (0,1 М Трис-HCl, рН 7,3, содержащий 0,1 М NaCl, 20 мМ CaCl2, 0,040 мМ ZnCl и 0,05% (мас./об.) Brij 35), используя синтетический субстрат Mac-Pro-Cha-Gly-Nva-His-Ala-Dpa-NH2, в присутствии или в отсутствие ингибиторов. Активность определяют путем измерения флуоресценции при Рекомбинантную человеческую ргоММР13 можно экспрессировать и очистить, как описано Knauper et al. [V.Knauper et al. (1996), The Biochemical Journal 271: 1544-1550 (1996)]. Этот очищенный фермент можно использовать для мониторинга ингибиторов активности следующим образом: очищенную proMMP13 активируют, используя 1 мМ аминофенилмеркуровую кислоту (АРМА, amino phenyl mercuric acid), 20 часов при 21°С; активированную ММР13 (11,25 нг на анализ) инкубируют в течение 4-5 часов при 35°С в аналитическом буфере (0,1 М Трис-HCl, рН 7,5, содержащий 0,1 М NaCl, 20 мМ CaCl2, 0,02 мМ ZnCl и 0,05% (мас./об.) Brij 35), используя синтетический субстрат 7-(метоксикумарин-4-ил)ацетил. Pro. Leu.Gly.Leu. N-3-(2,4-динитрофенил)-L-2,3-диаминопропионил.Ala.Arg.NH2, в присутствии или в отсутствие ингибиторов. Активность определяют путем измерения флуоресценции при Аналогичный протокол можно использовать для других экспрессированных и очищенных proMMP, используя условия субстратов и буферов, оптимальные для конкретной ММР, например, как описано в С.Graham Knight et al. (1992) FEBS Lett. 296 (3): 263-266. Семейство адамализинов, включая, например, TNF-конвертазу Способность соединений ингибировать фермент proTNF Этот выделенный пептид подвергали взаимодействию с 4-(N-малеимидо)флуоресцеином в ДМФ, содержащем диизопропилэтиламин, продукт очищали с помощью ВЭЖХ с обращенной фазой и, наконец, выделяли из водной уксусной кислоты лиофилизацией. Характеристики продукта определяли с помощью MALDI-TOF MS (времяпролетного масс-спектрометра с лазерной ионизацией путем десорбции из матрицы) и аминокислотного анализа. Природные субстраты Активность соединений по изобретению как ингибиторов разрушения аггрекана можно проанализировать с использованием методов, основанных, например, на сведениях Е.С.Arner et al., (1998) Osteoarthritis and Cartilage 6: 214-228; (1999) Journal of Biological Chemistry, 274 (10), 6594-6601, и антителах, описанных там. Эффективность соединений действовать в качестве ингибиторов против коллагеназ может быть определена, как описано Т.Cawston and A. Barrett (1979) Anal. Biochem. 99: 340-345. Ингибирование активности металлопротеиназ в основанном на клетках/тканях тесте на способность агента ингибировать мембранные шеддазы, такие как TNF-конвертаза Способность соединений по данному изобретению ингибировать клеточный процессинг продуцирования TNF Тест на способность агента ингибировать клеточную инвазию Способность соединений по данному изобретению ингибировать миграцию клеток в анализе на инвазию можно определить, как описано в А.Albini et al. (1987) Cancer Research 47: 3239-3245. Тест на способность агента ингибировать активность TNF-шеддазы цельной крови Способность соединений по данному изобретению ингибировать продуцирование TNF Тест на способность агента ингибировать разрушение хряща in vitro Способность соединений по данному изобретению ингибировать разрушение аггреканового или коллагенового компонентов хряща можно оценить, по существу, как описано в К.М.Bottomley et al. (1997) Biochem. J. 323: 483-488. Фармакодинамический тест Для оценки свойств клиренса и биодоступности соединений по данному изобретению применяют ex vivo фармакодинамический тест, в котором используют вышеописанные анализы синтетического субстрата или, альтернативно, ВЭЖХ или масс-спектрометрический анализ. Этот тест является общим тестом, который можно использовать для оценки скорости клиренса соединений у различных видов. Животным (например, крысам, мартышкам) внутривенно или перорально вводят дозы растворимого препарата соединения (такого как 20% мас./об. ДМСО, 60% мас./об. PEG400) и в последующие моменты времени (например 5, 15, 30, 60, 120, 240, 480, 720, 1220 минут) из подходящего сосуда забирают образцы крови в 10 ед. гепарина. Плазматические фракции получают, осуществляя центрифугирование, и плазматические белки осаждают ацетонитрилом (конечная концентрация 80% мас./об.). После 30 мин при -20°С плазматические белки осаждают центрифугированием, а надосадочную фракцию выпаривают до сухости, используя скоростной вакуумный насос Savant. Осадок перерастворяют в аналитическом буфере, после чего анализируют на содержание соединения, используя анализ синтетического субстрата. Кратко, для оцениваемого соединения строят кривую концентрация соединения – ответ. Серийные разведения перерастворенных плазматических экстрактов оценивают на активность и количество соединения, присутствующего в исходном образце плазмы, вычисляют, используя кривую концентрация-ответ с учетом коэффициента разведения суммарной плазмы. Оценка in vivo Тест на способность действовать в качестве анти-TMF-агента Способность соединений по данному изобретению действовать в качестве ингибиторов TNF Специализированная компьютерная программа анализирует данные и вычисляет для каждого соединения/дозы: Тест на активность в качестве противоартритного агента Активность соединения как противоартритного агента тестируют на индуцированном коллагеном артрите (CIA, collagen-induced arthritis), как определено в D.Е.Trentham et al. (1977) J.Exp. Med. 146: 857. В данной модели растворимый в кислоте нативный коллаген типа II вызывает полиартрит у крыс при введении в неполном адъюванте Фрейнда. Подобные условия можно использовать для индуцирования артрита у мышей и приматов. Тест на активность в качестве противоракового агента Активность соединения в качестве противоракового агента можно оценить в сущности, как описано в I.J.Fidler (1978) Methods in Cancer Research 15: 399-439, используя, например, клеточную линию В16 (описана в В.Hibner et al., Abstract 283 p75 10th NCI-EORTC Symposium, Amsterdam June 16-19 (1998). Тест на активность в качестве противоэмфиземного агента Активность соединения в качестве противоэмфиземного агента можно оценить в сущности, как описано в Hautamaki et al. (1997) Science 277: 2002. Изобретение далее иллюстрируется, но не ограничивается, следующими примерами. Общие методы анализа. Спектры 1H-ЯМР записывали на приборах либо VarianUnity Inova 400 МГц, либо Varian Mercury-VX 300 МГц. В качестве внутренних стандартов использовали центральный пик растворителя хлороформ-d ( ПРИМЕР 1 N-{[(4S)-2,5-Диоксоимидазолидинил]метил}-4-(4-фторфенокси)бензолсульфонамид и N-{[(4S)-2,5-диоксоимидазолидинил]метил}[1,1′-бифенил]-4-сульфонамид К перемешиваемому раствору N-альфа-ВОС-(S)-диаминопропионовой кислоты (100 мг, 0,5 ммоль) в 2,5 мл воды, содержащему 0,04 г (0,55 ммоль) карбоната натрия, добавляли раствор сульфонилхлорида (0,5 ммоль) в 2,5 мл диоксана. Этот раствор перемешивали в течение ночи при комнатной температуре, распределяли между этилацетатом (10 мл) и примерно 20% лимонной кислотой (10 мл), водную фазу три раза экстрагировали этилацетатом, органический экстракт промывали рассолом, высушивали, упаривали, и остаток обрабатывали 4 н. HCl в диоксане. Эту смесь перемешивали в течение 20 мин, упаривали и высушивали в вакууме в течение 4 ч при 40°С. Затем остаток гасили 3 мл водного раствора карбоната натрия (0,08 г, 0,85 ммоль) и добавляли 0,9 г (1,1 ммоль) цианата калия, эту смесь перемешивали в течение 4 ч при 100°С. После этого периода добавляли 1 мл концентрированной HCl, перемешивали в течение 1 ч при той же температуре, а затем оставляли стоять при комнатной температуре в течение ночи. Кристаллы отфильтровывали, промывали дистиллированной водой и высушивали в вакууме (если необходимо, перекристаллизовывали из этанола). N-{[(4S)-2,5-Диоксоимидазолидинил]метил}-4-(4-фторфенокси)бензолсульфонамид MC: m/z=380,1. N-{[(4S)-2,5-Диоксоимидазолидинил]метил}[1,1′-бифенил]-4-сульфонамид MC: m/z=346,1. 1Н ЯМР (ДМСО): 3.00 m (1,5 Н), 3.10 m (0,6 H), (CH2), 4.10 m (1H, СН), 7.5 m (3H), 7.70 d (2H), 7.4 s (4H). ПРИМЕР 2 Были получены соединения формулы I, где Y1 представляет собой О, Y2 представляет собой О, Х представляет собой NR1, R1 представляет собой Н, R2 представляет собой Н, m равно 1, R3 представляет собой Н, R4 представляет собой Н, Z представляет собой SO2N(R6), R6 представляет собой Н, (С1-4)алкил, метилбензил или метилпиридил, А представляет собой прямую связь и R5 варьирует. Синтезы проводили параллельно на 20-луночном планшете, проводя операции вручную. Аминокислоту (20 мкМ) растворяли в 5 мл воды, содержащей 6,36 мг (60 мкМ) карбоната натрия. В каждую лунку пипеткой добавляли по 0,5 мл этого раствора, затем добавляли по 0,5 мл раствора диоксана, содержащего 20 мкМ соответствующего сульфонилхлорида. Реакционную смесь встряхивали в течение 18 ч при комнатной температуре, разбавляли 2 мл метанола и обрабатывали 20 мг катионообменной смолы Lewatite S100 (кислотная форма) в каждой лунке в течение 5 мин. Затем все реакционные смеси фильтровали, упаривали в вакууме и остаток обрабатывали 1 мл 4 н. HCl в диоксане в течение 30 мин, упаривали в вакууме и добавляли 0,5 мл 0,5 М раствора цианата калия и нагревали до 100°С в течение 3 ч. Затем после охлаждения до комнатной температуры в каждую лунку добавляли по 10 мг Lewatite S100 (кислотная форма), а затем добавляли по 2 мл метанола, упаривали в вакууме и обрабатывали трифторуксусной кислотой при 80°С в течение 2 ч. После упаривания остаток очищали флэш-хроматографией на диоксиде кремния, используя градиент этилацетата-метанола (вплоть до 10% МеОН). Мониторинг степени очистки и молекулярной массы проводили с помощью ВЭЖХ-МС. Выходы 0,5-1 мг на каждую лунку. (2,5-Диоксоимидазолидин-4-илметил)амид 5-(2-метилтиазол-5-ил)тиофен-2-сульфоновой кислоты
ЖХ-МС (ХИАД) M++H+=373,4 (m/z). 3-(4-Хлорфенокси)-N-(2,5-диоксоимидазолидин-4-илметил)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=396,8 (m/z). 4-(4-Хлорфенокси)-N-(2,5-диоксоимидазолидин-4-илметил)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=396,8 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-(4-метоксифенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=392,6 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-3-(4-метоксифенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++Н+=392,6 (m/z). (2,5-Диоксоимидазолидин-4-илметил)амид 5-(5-трифторметил-Н-пиразол-3-ил)тиофен-2-сульфоновой кислоты.
ЖХ-МС (ХИАД) M++Н+=410,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-толилоксибензолсульфонамид
ЖХ-МС (ХИАД) M++H+=376,4 (m/z). 3-(3,4-Дихлорфенокси)-N-(диоксоимидазолидин-4-илметил)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=430,6 (m/z). 4-(3,4-Дихлорфенокси)-N-(2,5-диоксоимидазолидин-4-илметил)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=430,6 (m/z). (2,5-Диоксоимидазолидин-4-илметил)амид 4′-фторбифинил-4-сульфоновой кислоты
ЖХ-МС (ХИАД) M++H+=364,4 (m/z). (2,5-Диоксоимидазолидин-4-илметил)амид 5-пиридин-2-илтиофен-2-сульфоновой кислоты
ЖХ-МС (ХИАД) M++H+=353,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-(2-метоксифенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=392,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-3-(2-трифторметилфенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=430,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-3-(4-трифторметилфенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=430,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-(4-трифторметилфенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=430,4 (m/z). 4′-Трифторметилбифенил-4-сульфоновой кислоты (2,5-диоксоимилазолидин-4-илметил)амид
ЖХ-МС (ХИАД) M++H+=414,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-о-толилоксибензолсульфонамид
ЖХ-МС (ХИАД) M++H+=376,4 (m/z). 4-(3,5-Дихлорфенокси)-N-(2,5-диоксоимидазолидин-4-илметил)бензолсульфонамид
ЖХ-МС (ХИАД) М++Н+=431,3 (m/z). 4-(2-Хлорфенокси)-N-(диоксоимидазолидин-4-илметил)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=396,8 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-п-толилоксибензолсульфонамид
ЖХ-МС (ХИАД) M++H+=376,4 (m/z). 4-(4-Цианофенокси)-N-(2,5-диоксоимидазолидин-4-илметил)бензолсульфонамид
ЖХ-МС (ХИАД) М++H+=387,4 (m/z). 4-(4-Цианофенокси)-N-(2,5-диоксо-имидазолидин-4-илметил)-N-метилбензолсульфонамид
ЖХ-МС (ХИАД) M++Н+=401,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-метил-4-(4-трифторметилфенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=444,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-этил-4-(4-трифторметилфенокси)бензолсульфонамид
ЖХ-МС (ХИАД) М++H+=458,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-изопропил-4-(4-трифторметилфенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=472,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-изобутил-4-(4-трифторметилфенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=486,5 (m/z). N-Бензил-N-(2,5-диоксоимидазолидин-4-илметил)-4-(4-трифторметилфенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=520,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-пиридин-3-илметил-4-(4-трифторметилфенокси)бензол
ЖХ-МС (ХИАД) M++H+=521,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-(4-фторфенокси)-N-метилбензолсульфонамид
ЖХ-МС (ХИАД) M++H+=394,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-этил-4-(4-фторфенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=408,4 (m/z). N-Бензил-N-(2,5-диоксоимидазолидин-4-илметил)-4-(4-фторфенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=470,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-(4-фторфенокси)-N-пиридин-3-илметилбензолсульфонамид
ЖХ-МС (ХИАД) M++H+=471,5 (m/z). 4-(4-Хлорфенокси)-N-(2,5-диоксоимидазолидин-4-илметил)-N-метилбензолсульфонамид
ЖХ-МС (ХИАД) M++H+=410,5 (m/z). 4-(4-Хлорфенокси)-N-(2,5-диоксоимидазолидин-4-илметил)-N-этилбензолсульфонамид
ЖХ-МС (ХИАД) M++H+=424,88 (m/z). 4-(4-Хлорфенокси)-N-(2,5-диоксоимидазолидин-4-илметил)-N-изопропилбензолсульфонамид
ЖХ-МС (ХИАД) M++H+=424,88 (m/z). N-Бензил-4-(4-хлорфенокси)-N-(2,5-диоксоимидазолидин-4-илметил)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=486,9 (m/z). 4-(4-Хлорфенокси)-N-(2,5-диоксоимидазолидин-4-илметил)-N-пиридин-3-илметилбензолсульфонамид
ЖХ-МС (ХИАД) M++Н+=487,9 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-метил-4-п-толилоксибензолсульфонамид
ЖХ-МС (ХИАД) M++H+=390,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-этил-4-п-толилоксибензолсульфонамид
ЖХ-МС (ХИАД) M++H+=404,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-изопропил-4-п-толилоксибензолсульфонамид
ЖХ-МС (ХИАД) M++H+=418,5 (m/z). N-Бензил-N-(2,5-диоксоимидазолидин-4-илметил)-4-п-толилоксибензолсульфонамид
ЖХ-МС (ХИАД) M++H+=466,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-пиридин-3-илметил-4-п-толилоксибензолсульфонамид
ЖХ-МС (ХИАД) M++H+=467,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-(4-метоксифенокси)-N-метилбензолсульфонамид
ЖХ-МС (ХИАД) M++H+=406,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-этил-4-(4-метоксифенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=420,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-изопропил-4-(4-метоксифенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=433,5 (m/z). N-Бензил-N-(2,5-диоксоимидазолидин-4-илметил)-4-(4-метоксифенокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=482,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-(4-метоксифенокси)-N-пиридин-3-илметилбензолсульфонамид
ЖХ-МС (ХИАД) M++H+=483,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-(пиридин-4-илокси) бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=363,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-метил-4-(пиридин-4-илокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=377,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-этил-4-(пиридин-4-илокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=363,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-(пиридин-4-илокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=363,5 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-(пиридин-2-илокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=376,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-этил-4-(пиридин-2-илокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=391,4 (m/z). 4-(5-Хлорпиридин-2-илокси)-N-(2,5-диоксоимидазолидин-4-илметил)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=397,8 (m/z). 4-(5-Хлорпиридин-2-илокси)-N-(2,5-диоксоимидазолидин-4-илметил)-N-метилбензолсульфонамид
ЖХ-МС (ХИАД) M++H+=410,8 (m/z). 4-(5-Хлорпиридин-2-илокси)-N-(2,5-диоксоимидазолидин-4-илметил)-N-этилбензолсульфонамид
ЖХ-МС (ХИАД) M++H+=425,8 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-N-этил-4-(5-фторпиримидин-2-илокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=409,8 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-(5-фторпиримидин-2-илокси)-N-метилбензолсульфонамид
ЖХ-МС (ХИАД) M++H+=396,4 (m/z). N-(2,5-Диоксоимидазолидин-4-илметил)-4-(5-фторпиримидин-2-илокси)бензолсульфонамид
ЖХ-МС (ХИАД) M++H+=382,4 (m/z). ПРИМЕР 3 Соединения получали согласно схеме 2, как показано выше в описании. (а) Получение исходных веществ (альдегидов или кетонов) Альдегиды были получены по методике, описанной Fehrentz JA and Castro В, Synthesis, 676 (1983). Кетоны были получены по методике, описанной Nahm S., Weinreb S. M.: Tetrahedron Lett, 22, 3815 (1981). (б) Получение промежуточных гидантоинов Альдегид или кетон (5 ммоль) растворяли в 50% водном этаноле (10 мл) и добавляли 0,55 г (10 ммоль) цианида натрия и 2,7 г (25 ммоль) карбоната аммония, эту смесь нагревали в запаянной трубке до 80°С в течение 6 ч. Затем ее охлаждали, рН доводили до 4 и упаривали ее в вакууме. Остаток распределяли между водой (10 мл) и этилацетатом и водную фазу 3 раза реэкстрагировали этилацетатом, затем упаривали и диастереомеры разделяли хроматографией на диоксиде кремния (градиент ТВМЕ (трет-бутилметиловый эфир)-метанол 0-10% МеОН). Получили следующие гидантоины. трет-Бутиловый эфир R-1-(2,5-диоксоимидазолидин-4-S-ил)этилкарбаминовой кислоты
ЖХ-МС (ХИАД): М++H+=244,4, М+-56 (изобутилен) 188,6, М+-ВОС=144,4 (основной пик). 1Н-ЯМР (CDCl3, млн-1): 1.23 d (3Н), 1.45 s (9,1 Н), 4.36 m (1,1 Н), 5.30 bs (1,1 Н), 10,1 bs (1,31-1). R-1-(4-Метил-2,5-диоксоимидазолидин-4-8-ил)этилкарбаминовая кислота
ЖХ-МС (ХИАД): [М++Н+]=258,3, M+-56 (-изобутилен) 202,3, М+-ВОС=158,3 (основной пик). 1Н-ЯМР (CDCl3, млн-1): 1.22 d (3Н), 1.44 s (9,2 Н), 1.58 s (3,1 Н), 3.95 m (0,9 H),5.5 bs (1,5H),7,9 bs (0,8H). трет-Бутиловый эфир R-1-(4-метил-2,5-диоксоимидазолин-4-R-ил)этилкарбаминовой кислоты
ЖХ-МС (ХИАД): M++H+=258,3, М+-56 (-изобутилен) 202,3, М+-ВОС=158,3 (основной пик). 1Н-ЯМР (CDCl3, млн-1): 1.29 d (3Н), 1.54 s (9,1 Н), 1.50 s (2,95 Н), 4.25 m (1,1 Н), 5.5 bs (1,81-1), 7,9 ds (0,6 Н). трет-Бутиловый эфир R-1-{2.5-диоксо-4-фенилимидазолидин-4-S-ил)этилкарбаминовой кислоты
ЖХ-МС (ХИАД): M++H+=320,3, M+-56 (-изобутилен) 264,3, M+-BOC=230,3 (основной пик). 1Н-ЯМР (CDCl3, млн-1): 1.31 d (3 Н), 1.35 s (9,2 Н), 4.65 m (0,9 Н), 6.10 d (0,94 Н), 7,25 m (3,2 Н), 7.60 d (2,05 Н). трет-Бутил-(2S)-2-[(4R)-2,5-диоксоимидазолидин-4-ил]пирролидин-1-карбоксилат ЖХ-МС: M++H+=170,0 (M+-BOC). 1Н-ЯМР (CDCl3, млн-1): 1.26 s (9 H), 1.7-1.9 m (3,37 Н), 2.1-2.2 m (0,84 Н), 3.35-3.44 m (1,82 H), 4.1 bs(1,1 H). трет-Бутил-(2S)-2-[(4S)-2,5-диоксоимидазолидин-4-ил]пирролидин-1-карбоксилат ЖХ-МС: M++H+=170,0 (М+-ВОС). 1Н-ЯМР (CDCl3, млн-1): 1.27 s (9 H), 1.65-2.0 m (широкий) (4,47 Н), 3.55 m (1,15 Н), 3.62 m (0,55 Н), 4.4 m (0,87 Н). трет-Бутил-(2R)-2-[(4S)-2,5-диоксоимидазолидин-4-ил]пирролидин-1-карбоксилат ЖХ-МС: M++H+=170,0 (М+-ВОС). 1Н-ЯМР (CDCl3, млн-1): 1.47 s (9 H), 1.7-2.2 m (широкий) (4,30 Н), 3.6 m (1,12 H), 3.8 m (0,78 Н), 3.6 m (1,1 Н). трет-Бутил-(2R)-2-[(4R)-2,5-диоксоимидазолидин-4-ил]пирролидин-1-карбоксилат ЖХ-МС: M++H+=170,0 (М+-BOC). 1Н-ЯМР (CDCl3, млн-1): 1.47 s (9 H), 1.7-2.2 m (широкий) (4,30 Н), 3.6 m (1,12 Н), 3.8 m (0,78 Н), 3.6 m (1,1 Н). трет-Бутил-(2R)-2-[(4S)-4-метил-2,5-диоксоимидазолидин-4-ил]пирролидин-1-карбоксилат ЖХ-МС: M++Н+=183,1 (М+-ВОС). 1Н-ЯМР (CDCl3, млн-1): 1.4 s (9 H), 1.50 s (3,2 Н), 1.65-2.1 m (широкий) (4,20 Н), 3.4 m (1,1 Н), 3.5 bs (0,78 Н), 4.4 m (0,94 Н). Удаление защиты с ВОС-защищенных гидантоинов осуществляли с помощью 40% трифторуксусной кислоты в дихлорметане (ДХМ), и конечное соединение трифторацетат 5-(1-аминоэтил)-5-алкилимидазолин-2,4-диона осаждали диэтиловым эфиром после упаривания до сухости. Трифторацетат R-5-(S-1-аминоэтил)имидазолин-2,4-диона ЖХ-МС (ХИАД): M++H+=144,2 (m/z). Трифторацетат R-5-(1-аминоэтил)-5-S-метилимидазолидин-2,4-диона ЖХ-МС (ХИАД): M++H+=158,2 (m/z). Трифторацетат R-5-(1-аминоэтил)-5-R-метилимидазолидин-2,4-диона ЖХ-МС (ХИАД): M++H+=158,2 (m/z). Трифторацетат R-5-(1-аминоэтил)-5-S-фенилимидазолидин-2,4-диона ЖХ-МС (ХИАД): M++H+=220,3 (m/z). Трифторацетат (5R)-5-[(2S)-пирролидин-2-ил]имидазолидин-2,4-диона ЖХ-МС (ХИАД): M++H+=169,1 (m/z). (5R)-5-[(2R)-пирролидин-2-ил]имидазолидин-2,4-дион ЖХ-МС (ХИАД): M++H+=169,1 (m/z). (5R)-5-[(2S)-пирролидин-2-ил]имидазолидин-2,4-дион ЖХ-МС (ХИАД): M++H+=169,1 (m/z). (5S)-5-[(2S)-пирролидин-2-ил]имидазолидин-2,4-дион ЖХ-МС (ХИАД): M++H+=169,1 (m/z). (5S)-5-метил-5-[(2R)-пирролидин-2-ил]имидазолидин-2,4-дион ЖХ-МС (ХИАД): M++Н+=183,21 (m/z). (в) Получение гидантоинов формулы I Синтез проводили параллельно на 20-луночных планшетах, производя операции вручную. В каждую лунку вносили примерно по 7,5 мкмоль соответствующего сульфонилхлорида в 0,5 мл ДХМ, а затем примерно по 15-20 мкмоль трифторацетата 5-(1-аминоэтил)-5-алкилимидазолин-2,4-диона в 0,5 мл ДХМ (для полного растворения, если необходимо, добавляли небольшое количество ДМФ) и добавляли 10 мг диэтиламинометилполистирольной смолы. Эту смесь встряхивали в течение ночи, фильтровали через 200 мг силикагеля (промывали 3-5 мл этилацетата и мониторинг степени очистки осуществляли с помощью ЖХ-МС). Растворы упаривали до сухости с получением всех ожидаемых соединений с достаточной степенью чистоты. 4-R-(4-Хлорфенокси-N-(1-(2,5-диоксоимидазолин-4-S-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): M++H+=411,1 (m/z). 4-R-(5-Хлорпиридин-2-окси)-N-(1-(2,5-диоксоимидазолин-4-S-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): M++H+=412,1 (m/z). R-N-(1-(2,5-Диоксоимидазолидин-S-4-ил)этил)-4-(пиридин-2-илокси)бензолсульфонамид
ЖХ-МС (ХИАД): М++2 H+=378,9 (m/z). R-N-(1-(2,5-Диоксоимидазолидин-S-4-ил)этил)-4-(пиридин-4-илокси)бензолсульфонамид
ЖХ-МС (ХИАД): M++2 H+=378,9 (m/z). 4-R-(4-Цианофенокси-N-(1-(2,5-диоксоимидазолин-4-S-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): M++H+=401,5 (m/z). 4-R-(4-Фторфенокси-N-(1-(2,5-диоксоимидазолин-4-S-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): M++Н+=394,3 (m/z). 4-R-(4-Трифторметилфенокси-N-(1-(2,5-диоксоимидазолин-4-S-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): M++H+=444,4 (m/z). 4-R-(4-Метилфенокси-N-(1-(2,5-диоксоимидазолин-4-S-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): М++H+=389,43 (m/z). 4-R-(4-Метоксифенокси-N-(1-(2,5-диоксоимидазолин-4-S-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): М++H+=406,4 (m/z). 4-R-(4-Фенокси-N-(1-(2,5-диоксоимидазолин-4-S-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): М++2 H+=376,2 (m/z). R-N-(1-(4-Метил-2,5-диоксоимидазолидин-4-S-ил)этил-4-феноксибензолсульфонамид
ЖХ-МС (ХИАД): M++H+=390,4 (m/z). 4-(4-Хлорфенокси-N-(1-(4-S-метил-2,5-диоксоимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=423,4 (m/z). 4-(5-Хлорпиридил-2-окси)-N-(1-(4-S-метил-2,5-диоксоимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=424,4 (m/z). N-(1-(4-S-Метил-2,5-диоксоимидазолидин-4-R-ил)этил-4-(пиридин-2-илокси)бензолсульфонамид
ЖХ-МС (ХИАД): M++2 H+=392,4 (m/z). N-(1-(4-S-Метил-2,5-диоксоимидазолидин-4-R-ил)этил)-4-(пиридин-2-илокси)бензолсульфонамид
ЖХ-МС (ХИАД): M++2 H+=392,4 (m/z). 4-(4-Цианофенокси-N-(1-(4-S-метил-2,5-диоксоимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++2 Н+=415,4 (m/z). R-N-(1-(4-Метил-2,5-диоксоимидазолидин-4-R-ил)этил-4-феноксибензолсульфонамид
ЖХ-МС (ХИАД): M++H+=390,4 (m/z). 4-(4-Хлорфенокси-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=423,4 (m/z). 4-(5-Хлорпиридил-2-окси)-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-R-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): M++H+=424,4 (m/z). N-(1-(4-R-Метил-2,5-диоксоимидазолидин-4-R-ил)этил)-4-(пиридин-2-илокси)бензолсульфонамид
ЖХ-МС (ХИАД): M++2 H+=392,4 (m/z). N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-R-ил)этил)-4-(пиридин-2-илокси)бензолсульфонамид
ЖХ-МС (ХИАД): М++2 H+=392,4 (m/z). 4-(4-Цианофенокси-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=415,4 (m/z). 4-(4-Фторфенокси-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-S-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=407,4 (m/z). 4-(4-Трифторметилфенокси-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-S-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=458,4 (m/z). 4-(4-Метилфенокси-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-S-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=404,5 (m/z). 4-(4-Метоксифенокси-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-S-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++Н+=420,5 (m/z). 4-(4-Фенокси-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-S-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): М++H+=390,5 (m/z). 4-(4-Фторфенокси-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=407,4 (m/z). 4-(4-Трифторметилфенокси-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=458,4 (m/z). 4-(4-Метилфенокси-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=404,5 (m/z). 4-(4-Метоксифенокси-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=420,5 (m/z). 4-(4-Фенокси-N-(1-(4-R-метил-2,5-диоксоимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=390,5 (m/z). 4-(4-Хлорфенокси-N-(1-((2,5-диоксо-4-S-фенилимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): М++H+=486,8 (m/z). 4-(5-Хлорпиридин-2-илокси)-N-(1-((2,5-диоксо-4-S-фенилимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=487,8 (m/z). N-(1-S-(2,5-Диоксо-4-фенилимидазолидин-4-R-ил)этил-4-(пиридин-2-илокси)бензолсульфонамид
ЖХ-МС (ХИАД): М++2 H+=454,6 (m/z). N-(1-S-(2,5-Диоксо-4-фенилимидазолидин-4-R-ил)этил-4-(пиридин-4-илокси)бензолсульфонамид
ЖХ-МС (ХИАД): M++2 H+=454,6 (m/z). 4-(4-Цианофенокси-N-(1-((2,5-диоксо-4-S-фенилимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=477,6 (m/z). 4-(4-Фторфенокси-N-(1-((2,5-диоксо-4-S-фенилимидазолидин-4-R-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): M++Н+=470,5 (m/z). 4-(4-Трифторметилфенокси-N-(1-((2,5-диоксо-4-S-фенилимидазолидин-4-R-ил)этилбензолсульфонамид
ЖХ-МС (ХИАД): M++H+=519,1 (m/z). 4-(4-Метилфенокси)-N-(1-((2,5-диоксо-4-S-фенилимидазолидин-4-R-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): M++H+=466,4 (m/z). 4-(4-Метоксифенокси-N-(1-((2,5-диоксо-4-S-фенилимидазолидин-4-R-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): M++H+=482,4 (m/z). 4-(4-Фенокси)-N-(1-((2,5-диоксо-4-S-фенилимидазолидин-4-R-ил)этил)бензолсульфонамид
ЖХ-МС (ХИАД): M++H+=452,5 (m/z). 5-(1-{[4-(4-Хлорфенокси)фенил]сульфонил}пирролидин-2-ил)-5-метилимидазолидин-2,4-дион
ЖХ-МС (ХИАД): M++H+=450,5 (m/z). 5-(1-{[4-(4-Метоксифенокси)фенил]сульфонил}пирролидин-2-ил)-5-метилимидазолидин-2,4-дион
ЖХ-МС (ХИАД): M++H+=446,2 (m/z). 5-(1-{[4-(4-Метилфенокси)фенил]сульфонил}пирролидин-2-ил)-5-метилимидазолидин-2,4-дион
ЖХ-МС (ХИАД): M++H+=430,1 (m/z). 5-(1-{[4-(4-Фторфенокси)фенил]сульфонил}пирролидин-2-ил)-5-метилимидазолидин-2,4-дион
ЖХ-МС (ХИАД): M++H+=434,1 (m/z). (1-{[4-(4-Цианофенокси)фенил]сульфонил}пирролидин-2-ил)-5-метилимидазолидин-2,4-дион
ЖХ-МС (ХИАД): М++H+=441,1 (m/z). 5-(1-{[4-(4-Хлорфенокси)фенил]сульфонил}пирролидин-2-ил)имидазолидин-2,4-дион
ЖХ-МС (ХИАД): M++H+=436,1 (m/z). 5-(1-{[4-(4-Фторфенокси)фенил]сульфонил}пирролидин-2-ил)имидазолидин-2,4-дион
ЖХ-МС (ХИАД): M++H+=420,1 (m/z). 5-(1-{[4-(4-Метилфенокси)фенил]сульфонил}пирролидин-2-ил)имидазолидин-2,4-дион
ЖХ-МС (ХИАД): M++H+=416,1 (m/z). 5-(1-{[4-(4-Метоксифенокси)фенил]сульфонил}пирролидин-2-ил)имидазолидин-2,4-дион
ЖХ-МС (ХИАД): M++H+=432,1 (m/z). 5-(1-{[4-(4-Цианофенокси)фенил]сульфонил}пирролидин-2-ил)имидазолидин-2,4-дион
ЖХ-МС (ХИАД): M++H+=427,1 (m/z). ПРИМЕР 4 [(4R)-2,5-Диоксоимидазолидинил]метансульфонилхлорид, [(4S)-2,5-диоксоимидазолидинил]метансульфонилхлорид или [(R)-2,5-диоксоимидазолидинил]метансульфонилхлорид подвергали взаимодействию с соответствующим первичным или вторичным амином с получением соединений, перечисленных ниже. Все используемые амины имеются в продаже. Сульфонилхлорид (0,060 ммоль), амин (0,060 ммоль), триэтиламин (0,0084 мл, 0,060 ммоль) в безводном тетрагидрофуране (0,70 мл) перемешивали при комнатной температуре в течение ночи. Добавляли полистиролметилизоцианат (0,025 г, 0,030 ммоль) и эту смесь встряхивали в течение ночи. Белую суспензию фильтровали и твердые вещества промывали тетрагидрофураном (2×1 мл). Фильтраты упаривали, белое твердое вещество суспендировали в воде (5 мл), собирали на фильтре, промывали водой (2×1 мл), отсасывали воду и высушивали в вакууме при 45°С в течение ночи с получением соединений, указанных в заголовке. Исходные вещества получали следующим образом. 5-Метил-5-{[(фенилметил)тио]метил}имидазолидин-2,4-дион В стальной сосуд загружали этанол и воду (315 мл/135 мл). Добавляли 31,7 г (0,175 моль) бензилтиоацетона, 22,9 г (0,351 моль) цианида калия и 84,5 г (0,879 моль) карбоната аммония. Закрытый реакционный сосуд выдерживали в масляной бане (температура бани 90°С) при энергичном перемешивании в течение 3 ч. Реакционный сосуд охлаждали ледяной водой (0,5 ч), желтоватую суспензию упаривали до сухости, твердый остаток распределяли между 400 мл воды и 700 мл этилацетата и разделяли. Водную фазу экстрагировали этилацетатом (300 мл). Объединенные органические фазы промывали насыщенным рассолом (150 мл), высушивали (Na2SO4), фильтровали и упаривали до сухости. Если продукт не кристаллизовался, к маслу добавляли 300 мл дихлорметана. Выпаривание привело к получению продукта в виде слегка желтоватого порошка, 43,8 г (90%). ЖХ-МС (ХИАД): m/z 251,1 (МН+). 1H ЯМР (ДМСО-d6) 13С ЯМР (ДМСО-d6) (5S)-5-Метил-5-{[(фенилметил)тио]метил}имидазолидин-2,4-дион Соединение, указанное в заголовке, получали хиральным разделением рацемического вещества, используя колонку 250 мм ×50 мм в системе препаративной ВЭЖХ с динамической осевой компрессией (Dynamic Axial Compression Preparative HPLC). Использовали стационарную фазу CHIRALPAK AD, в качестве элюента – метанол, скорость потока равнялась 89 мл/мин, температура равна температуре окружающей среды, ультрафиолетовое излучение (УФ) 220 нм, концентрация образца 150 мг/мл, впрыскиваемый объем 20 мл. Время удерживания для соединения, указанного в заголовке, составило 6 мин. Анализ хиральной чистоты проводили, используя колонку CHIRALPAK-AD 250 мм ×4,6 мм от Daicel, скорость потока 0,5 мл/мин, элюент – этанол, УФ 220 нм, температура окружающей среды. Время удерживания для соединения, указанного в заголовке, составило 9,27 мин. Установлено, что чистота составила более 99% ее (enantiomeric excess, энантиомерный избыток). ЖХ-МС (ХИАД): m/z 251,1 (MH+). [ 1H ЯМР (ДМСО-d6) 13C ЯМР (ДМСО-d6) (5R)-5-Метил-5-{[(фенилметил)тио]метил}имидазолидин-2,4-дион Соединение, указанное в заголовке, было получено хиральным разделением рацемического вещества с использованием колонки 250 мм ×50 мм системы препаративной ВЭЖХ с динамической осевой компрессией. Использовали стационарную фазу CHIRALPAK AD, элюент – метанол, скорость потока 89 мл/мин, температуру окружающей среды, УФ=220 нм, концентрацию образца 50 мг/мл, впрыскиваемый объем 20 мл. Время удерживания для соединения, указанного в заголовке, составило 10 мин. Анализ хиральной чистоты проводили, используя колонку CHIRALPAK-AD 250 мм × 4,6 мм от Daicel, скорость потока 0,5 мл/мин, элюент – этанол, УФ 220 нм, температура окружающей среды. Время удерживания для соединения, указанного в заголовке, составило 17,81 мин. Установленная хиральная чистота составила более 99% ее. ЖХ-МС (ХИАД): m/z 251,0 (MH+). [ 1H ЯМР (ДМСО-d6) 13С ЯМР (ДМСО-d6) [(4S)-4-Метил-2,5-диоксоимидазолидин-4-ил]метансульфонилхлорид (5S)-5-Метил-5-{[(фенилметил)тио]метил}имидазолидин-2,4-дион (42,6 г; 0,17 моль) растворяли в смеси АсОН (450 мл) и Н2O (50 мл). Эту смесь погружали в баню лед/вода. Cl2 (газ) барботировали через этот раствор, поток газа регулировали таким образом, чтобы поддерживать температуру ниже +15°С. Через 25 мин этот раствор становился желто-зеленым по цвету, в этот момент отбирали образец для ЖХ-МС и ВЭЖХ анализа. Анализ показал, что исходное вещество израсходовано. Желтый прозрачный раствор перемешивали в течение 30 мин, при этом образовывался непрозрачный раствор/суспензия. Растворитель удаляли на роторном испарителе, используя водяную баню с температурой, поддерживаемой при +37°С. Желтоватое твердое вещество суспендировали в толуоле (400 мл) и на том же роторном испарителе удаляли растворитель. Операцию повторяли еще раз. Затем неочищенный продукт суспендировали в изогексане (400 мл) и нагревали до +40°С при перемешивании, суспензию оставляли охлаждаться до комнатной температуры, после чего нерастворимый продукт удаляли фильтрованием, промывали изогексаном (6×100 мл) и высушивали при пониженном давлении при +50°С в течение ночи. Это дало продукт в виде слегка желтого порошка. Получили 36,9 г (95%) соединения, указанного в заголовке. Чистота по ВЭЖХ 99%, ЯМР подтвердил эту чистоту. [ 1H ЯМР (ТГФ-d8) 13С ЯМР (ТГФ-d8) [(4R)-4-Метил-2,5-диоксоимидазолидин-4-ил]метансульфонилхлорид Следуя методике, описанной для [(4S)-4-метил-2,5-диоксоимидазолидин-4-ил]метансульфонилхлорида, начиная с (5R)-5-метил-5-{[(фенилметил)тио]метил}имидазолидин-2,4-диона (10,0 г, 40 ммоль), получили 8,78 г (выход 96%) соединения, указанного в заголовке. Чистота по ЯМР более 98%. [ 1H ЯМР (ТГФ-d8) 13С ЯМР (ТГФ-d8)
Ниже в таблице 1 приведена группа «Амин» для каждого соединения указанной выше структуры. Таблица 1
Ниже в таблице 2 приведена группа «Амин» для каждого соединения указанной выше структуры. Таблица 2
Ниже в таблице 3 приведена группа «Амин» для каждого соединения указанной выше структуры. Таблица 3
N-[4-(4-Хлорфенокси)фенил]-C-((4S)-4-метил-2,5-диоксиимидазолидин-4-ил)метансульфонамид ЖХ-МС (ХИАД): m/z 410 (MH+). 1H ЯМР (ДМСО-d6) N-(4-Бензилфенил)-С-((4S)-метил-2,5-диоксоимидазолидин-4-ил)метансульфонамид ЖХ-МС (ХИАД): m/z 374 (MH+). 1H ЯМР (ДМСО-d6) N-(4-Бензоилфенил)-С-((4S)-4-метил-2,5-диоксоимидазолидин-4-ил)метансульфонамид ЖХ-МС (ХИАД): m/z 388 (МН+). 1H ЯМР (ДМСО-d6) ПРИМЕР 5 Соединения этого примера получали из коммерчески доступного М-Вос-4-пиперидона способами, описанными в примере 3.
ПРИМЕР 6 Изготовление фармацевтических композиций и лекарственных средств, содержащих ингибитор металлопротеиназ Приведенные ниже примеры иллюстрируют типичные фармацевтические лекарственные формы, содержащие соединение формулы (I) или (II) и предназначенные для лечения опосредованных металлопротеиназами заболеваний. (а)
(б)
Вышеуказанные препараты могут быть получены традиционными способами, хорошо известными в фармацевтической области техники. Таблетки могут быть покрыты оболочкой обычными способами. Способ изготовления Соединение формулы (I)/(II) помещают в сосуд, добавляют указанные эксципиенты, тщательно перемешивают до гомогенности (контролируя визуально). После этого (а) полученную смесь прессуют в таблетки или (б) этой смесью наполняют капсулы, пригодные для перорального введения.
Формула изобретения
1. Соединение формулы I или его фармацевтически приемлемая соль где X представляет собой NR1; Y1 и Y2 представляют собой О; Z выбран из SO2N(R6), N(R7)SO2; m равно 1 или 2; А выбран из прямой связи, (С1-6)алкила; R1 представляет собой Н; R2 и R3, каждый независимо, выбран из Н, алкила, арила, алкиларила, арилалкила; каждый R4 независимо выбран из Н, (С1-3)алкила; R6 выбран из Н, алкила, арила, гетероарила, алкиларила, алкилгетероарила, арилалкила, гетероарилалкила; R2 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R3 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R4 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов; R5 представляет собой моноциклическую, бициклическую, содержащую одну или две кольцевые структуры, каждая из которых содержит вплоть до 7 кольцевых атомов, независимо выбранные из циклоалкила, арила, гетероциклоалкила или гетероарила, причем каждая кольцевая структура независимо возможно замещена одним или более чем одним заместителем, независимо выбранным из галогена, гидрокси, алкила, алкокси, галогеноалкокси, циано, где любой алкильный радикал в пределах любого заместителя сам возможно может быть замещен одной или более чем одной группой, выбранной из галогена; когда R5 представляет собой бициклическую группу, каждая кольцевая структура соединена со следующей кольцевой структурой через прямую связь, через -O-, через (С1-6)алкил или конденсирована с этой следующей кольцевой структурой; R7 выбран из (С1-6)алкила; при условии, что когда Х представляет собой NR1, R1 представляет собой Н, Y1 представляет собой О, Y2 представляет собой О, Z представляет собой SO2N(R6), R6 представляет собой Н, R2 представляет собой Н, m равно 1, R3 представляет собой Н, R4 представляет собой Н и А представляет собой прямую связь, тогда R5 не представляет собой фенил, пара-нитрофенил, пара-этоксифенил или мата-метилфенил; когда Х представляет собой NR1, R1 представляет собой Н, Y1 представляет собой О, Y2 представляет собой О, Z представляет собой SO2N(R6), R6 представляет собой алкил, R2 представляет собой Н, m равно 1, один из R3 и R4 представляет собой Н, а другой представляет собой алкил, R3 и R6 или R4 и R6 соединяются с образованием 5-членного кольца и А представляет собой прямую связь, тогда R5 не представляет собой фенил. 2. Соединение формулы I по п.1 или его фармацевтически приемлемая соль, где Х представляет собой NR1, R1 представляет собой Н, по меньшей мере один из Y1 и Y2 представляет собой О, Z представляет собой SO2N(R6), m равно 1. 3. Соединение по п.1 или 2 или его фармацевтически приемлемая соль, где R2 представляет собой Н, алкил, арилалкил, алкиларил. 4. Соединение по любому из пп.1-3 или его фармацевтически приемлемая соль, где каждый из R3 и R4 независимо выбран из Н, метила. 5. Соединение формулы I по любому из пп.1-4 или его фармацевтически приемлемая соль, где R3 и R6 образуют 5- или 6-членное кольцо, или R4 и R6 образуют 5- или 6-членное кольцо, или R2 и R3 образуют 5-членное кольцо, или R2 и R6 образуют 5-членное кольцо. 6. Соединение формулы I по любому из пп.1-5 или его фармацевтически приемлемая соль, где R5 содержит возможно замещенные арильные или гетероарильные 5- или 6-членные кольца в количестве одного или двух. 7. Соединение формулы I по любому из пп.1-6 или его фармацевтически приемлемая соль, где R5 представляет собой бициклическую группу, содержащую две возможно замещенные кольцевые структуры. 8. Соединение формулы I по п.1 или его фармацевтически приемлемая соль, где Y1 представляет собой О, Y2 представляет собой О, Х представляет собой NR1, R1 представляет собой Н, R2 представляет собой Н, m равно 1, R3 представляет собой Н, R4 представляет собой Н, Z представляет собой SO2N(R6), R6 представляет собой Н, (С1-4)алкил, метилбензил или метилпиридил, А представляет собой прямую связь и R5 представляет собой бициклическую группу, содержащую две возможно замещенные кольцевые структуры. 9. Соединение формулы I по п.1 или его фармацевтически приемлемая соль, где Y1 представляет собой О, Y2 представляет собой О, Х представляет собой NR1, R1 представляет собой Н, R2 представляет собой H, метил или бензил, m равно 1, R3 представляет собой Н или метил, R4 представляет собой Н, Z представляет собой SO2N(R6), R6 представляет собой Н, А представляет собой прямую связь и R5 представляет собой бициклическую группу, содержащую две возможно замещенные кольцевые структуры. 10. Соединение формулы II или его фармацевтически приемлемая соль где каждый из G1 и G2 представляет собой моноциклическую кольцевую структуру, каждая из которых содержит вплоть до 7 кольцевых атомов, независимо выбранную из циклоалкила, арила, гетероциклоалкила или гетероарила, причем каждая кольцевая структура независимо возможно замещена одним или двумя заместителями, независимо выбранными из галогена, гидрокси, галогеноалкокси, циано, алкила, алкокси, где любой алкильный радикал в пределах любого заместителя может быть сам возможно замещен одной или более чем одной группой, выбранной из галогена, гидрокси, амино, N-алкиламино, N,N-диалкиламино, циано, нитро, алкокси, галогеноалкокси; Z представляет собой SO2N(R6); В выбран из прямой связи, О, (С1-6)алкила; R2 выбран из Н, (С1-6)алкила или R2 представляет собой группу формулы III
С и D независимо выбраны из прямой связи, Н, (С1-6)алкила; G3 представляет собой моноциклическую кольцевую структуру, содержащую вплоть до 7 кольцевых атомов, независимо выбранную из циклоалкила, арила, гетероциклоалкила или гетероарила; R3 и R4 независимо выбраны из Н или (С1-3)алкила; R6 выбран из Н или R6 представляет собой (С1-3)алкил, возможно замещенный арилом, гетероарилом; R2 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R3 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов, либо R4 и R6 могут соединяться с образованием кольца, содержащего вплоть до 7 кольцевых атомов. 11. Соединение формулы II по п.10 или его фармацевтически приемлемая соль, где Z представляет собой SO2N(R6), и атом S группы Z присоединен к кольцу G2. 12. Соединение формулы II по п.10 или 11 или его фармацевтически приемлемая соль, где В представляет собой прямую связь или О. 13. Соединение формулы II по любому из пп.10-12 или его фармацевтически приемлемая соль, где R2 не является возможно замещенным, или R2 выбран из Н, (С1-6)алкила, арил-(С1-6)алкила или гетероарил-(С1-6)алкила. 14. Соединение формулы II по любому из пп.10-13 или его фармацевтически приемлемая соль, где каждый из R3 и R4 представляет собой Н. 15. Соединение формулы II по любому из пп.10-14 или его фармацевтически приемлемая соль, где R6 представляет собой Н, бензил или метиленпиридин. 16. Соединение формулы II по любому из пп.10-15 или его фармацевтически приемлемая соль, где G1 и G2, каждый, выбраны из арила или гетероарила. 17. Соединение формулы II по любому из пп.10-16 или его фармацевтически приемлемая соль, где R3 и R6 образуют 5- или 6-членное кольцо, или R4 и R6 образуют 5- или 6-членное кольцо, или R2 и R6 образуют 5-членное кольцо. 18. Фармацевтическая композиция, полезная в ингибировании металлопротеиназ, содержащая соединение формулы I по п.1 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель. 19. Фармацевтическая композиция, полезная в ингибировании металлопротеиназ, содержащая соединение формулы II по п.10 или его фармацевтически приемлемую соль и фармацевтически приемлемый носитель. 20. Применение соединения формулы I или формулы II либо их фармацевтически приемлемой соли в изготовлении лекарства для применения в лечении заболевания или состояния, опосредованного одним или более чем одним ферментом, представляющим собой металлопротеиназу.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||

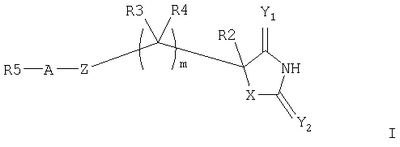
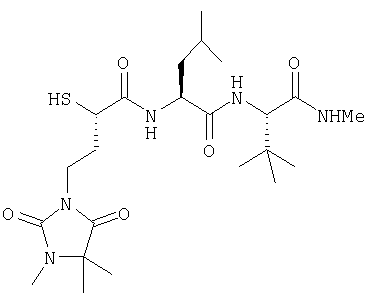
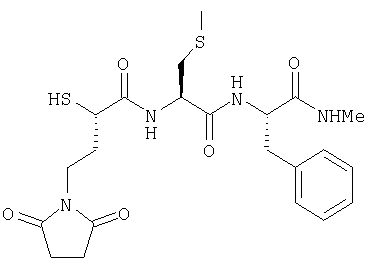
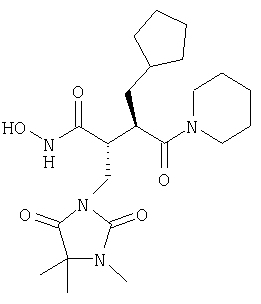
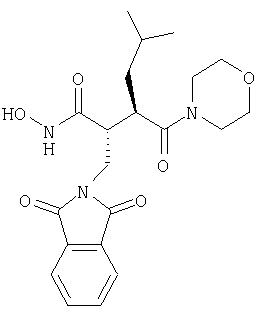
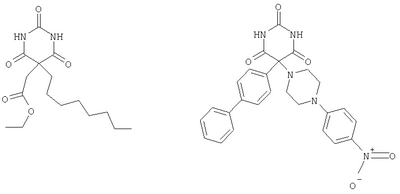
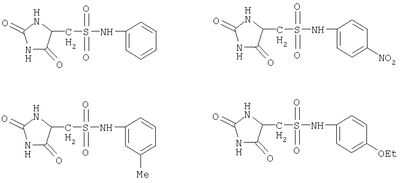
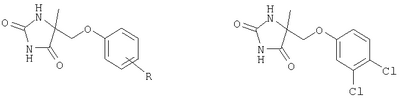
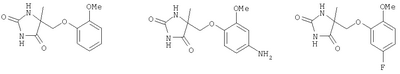
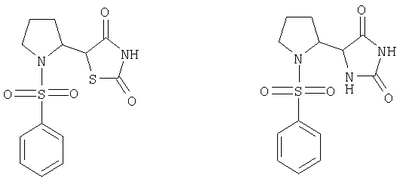
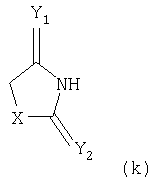
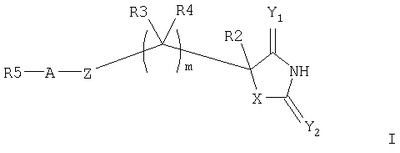
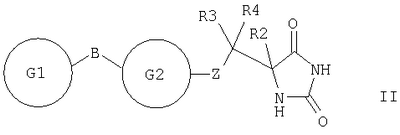
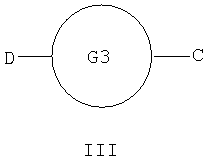
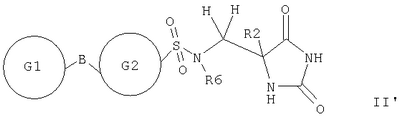
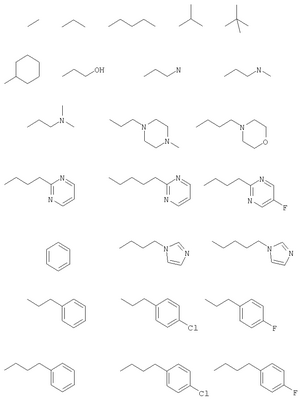
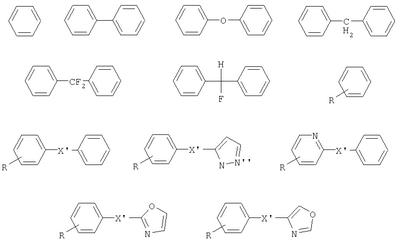
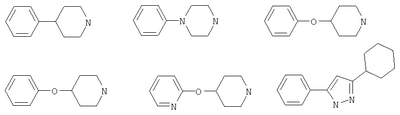
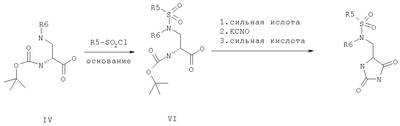
 -аминоальдегидов формулы VII, полученных согласно Fehrentz J.A., Castro В.: Synthesis, 676, (1983).
-аминоальдегидов формулы VII, полученных согласно Fehrentz J.A., Castro В.: Synthesis, 676, (1983).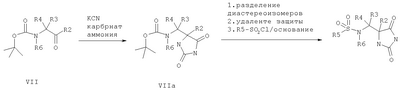
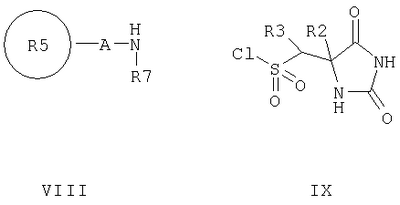
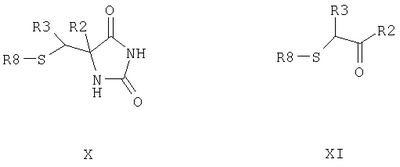
 ех 328 нм и
ех 328 нм и 
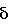 H 7,27 млн-1), диметилсульфоксид-d6 (
H 7,27 млн-1), диметилсульфоксид-d6 (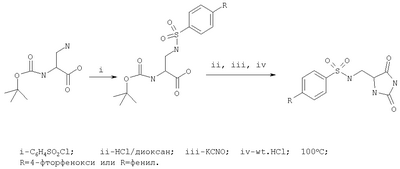
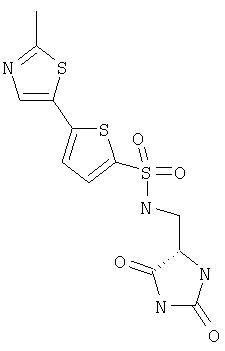
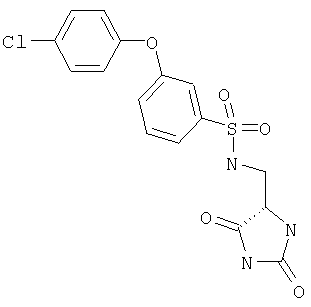
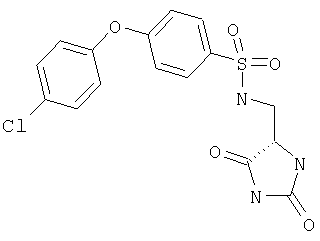
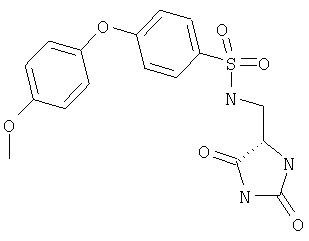
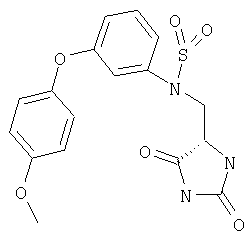
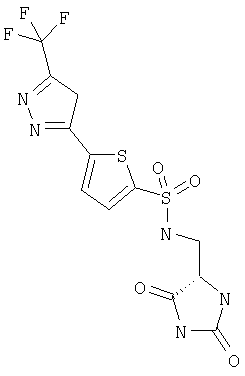
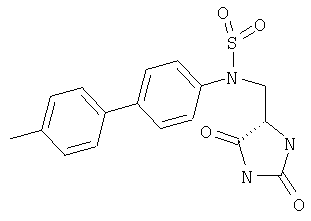
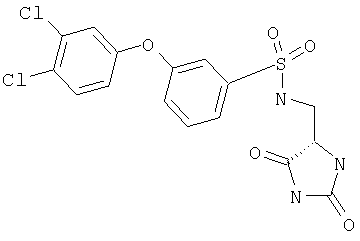
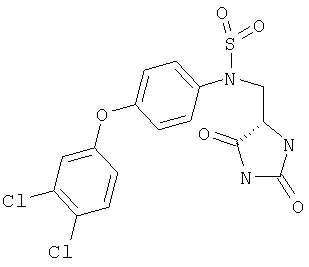
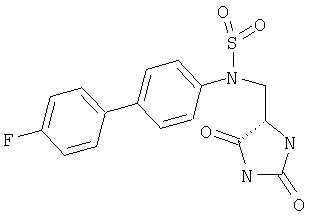
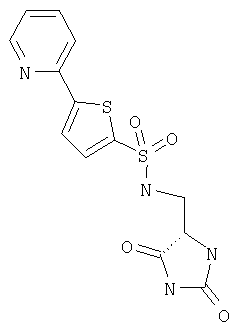
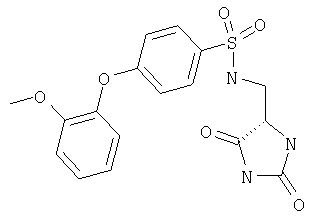
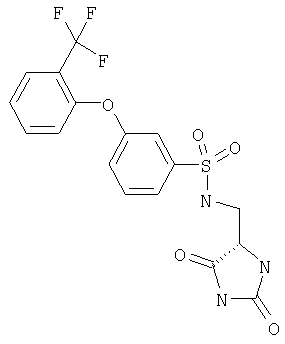
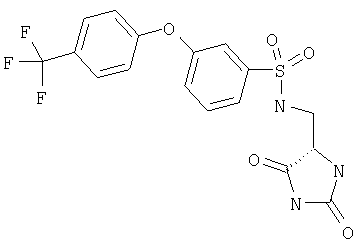
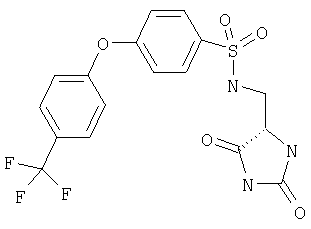
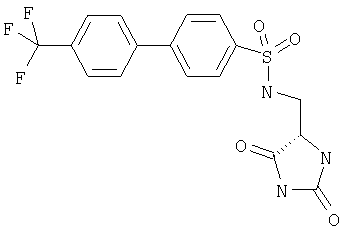
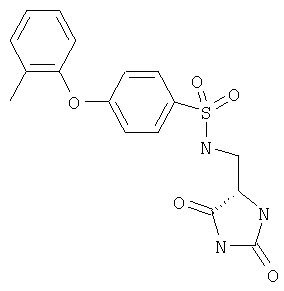
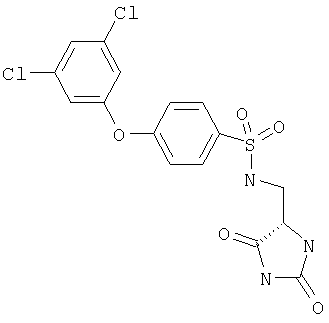
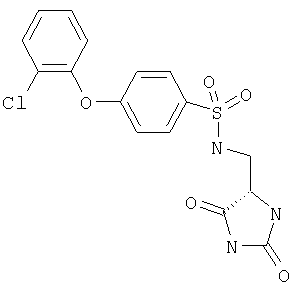
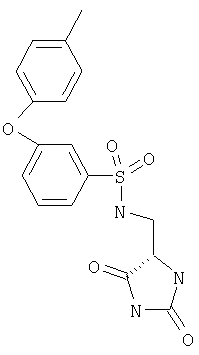
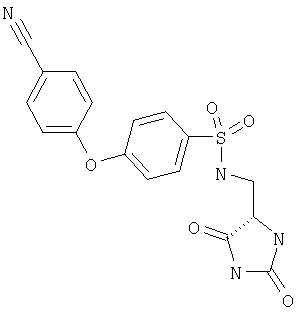
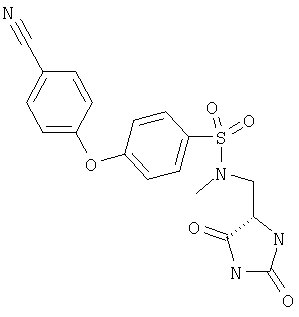
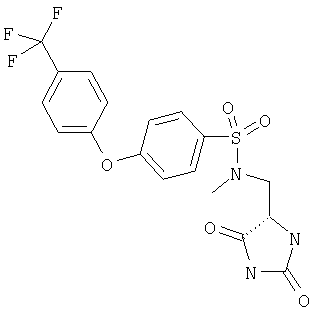
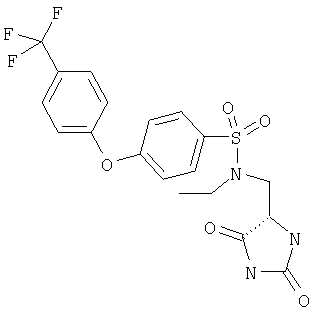
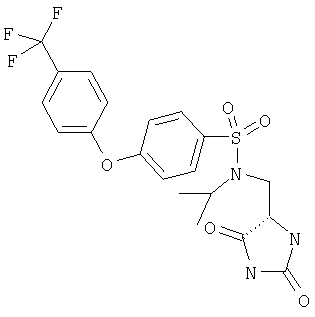
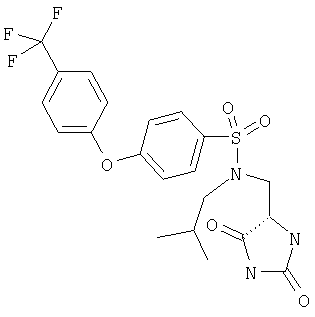
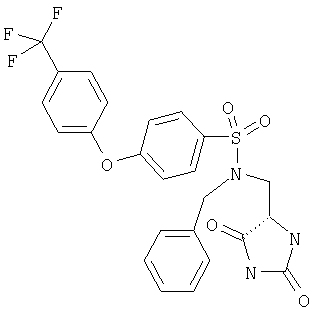
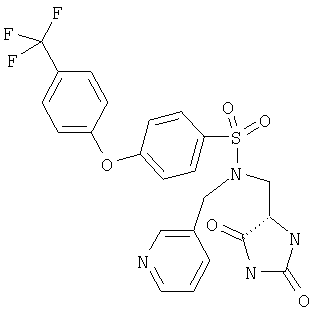
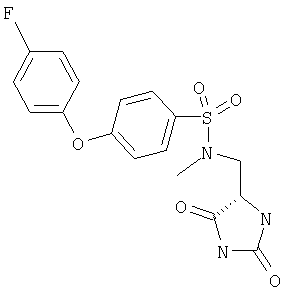
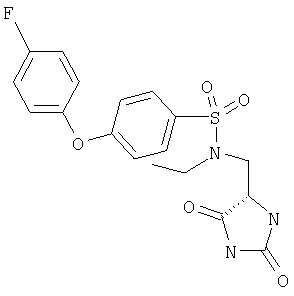
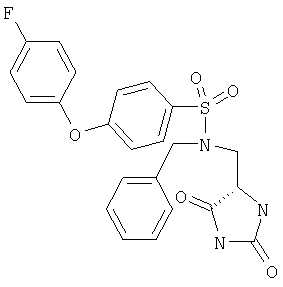
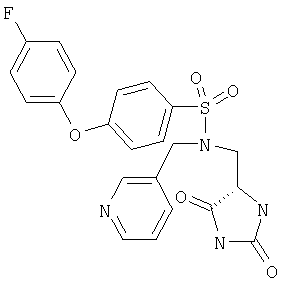
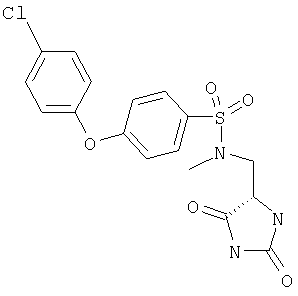
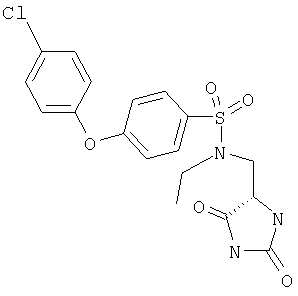
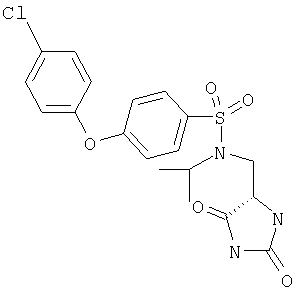
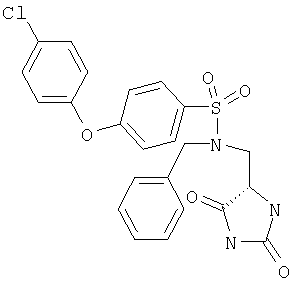
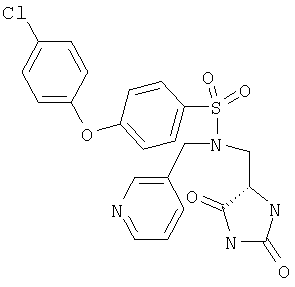
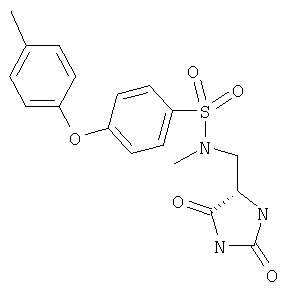
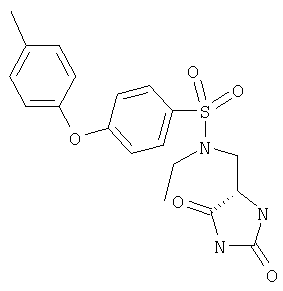
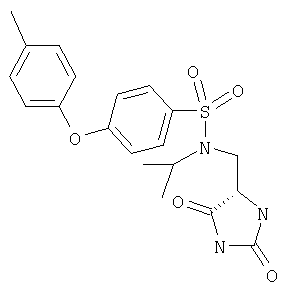
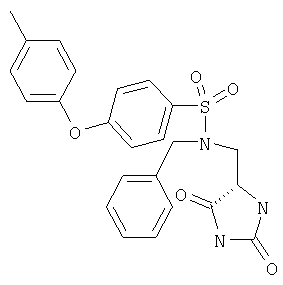
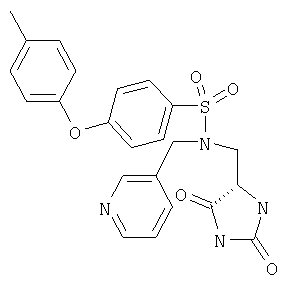
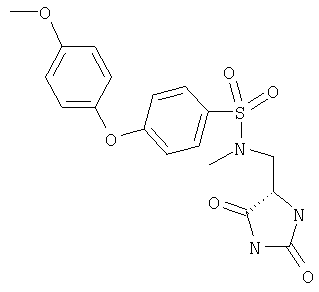
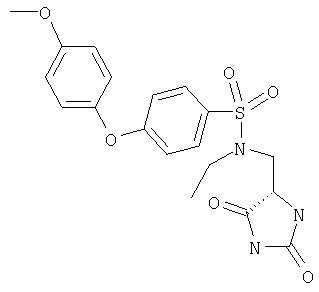
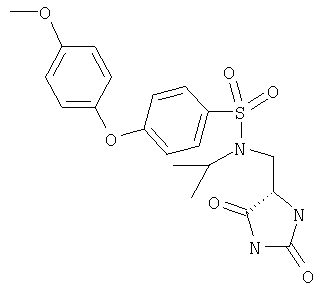
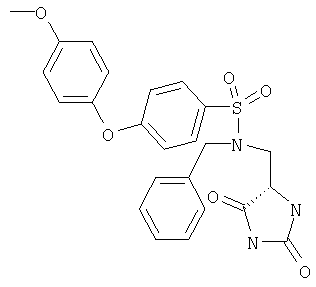
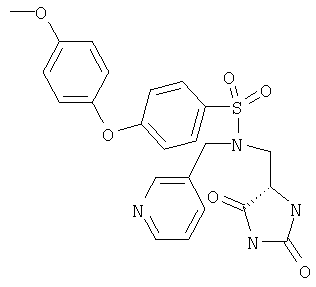
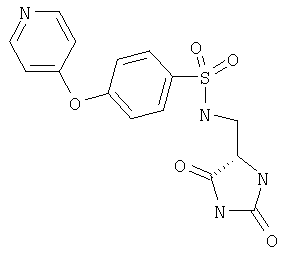
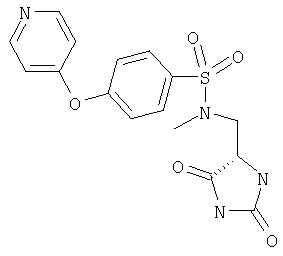
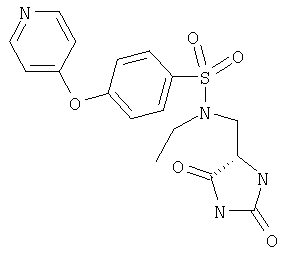
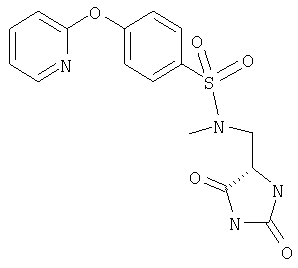
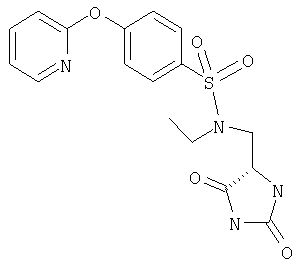
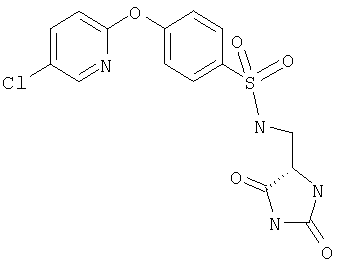
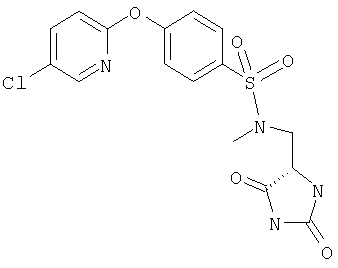
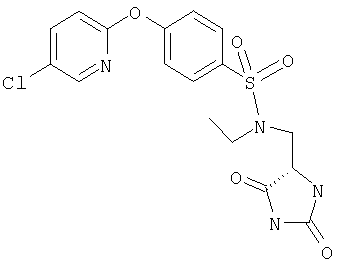
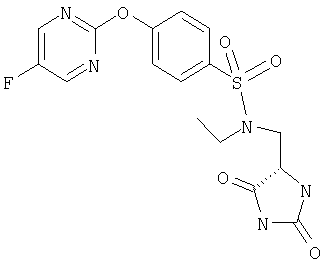
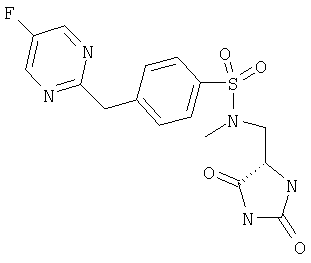
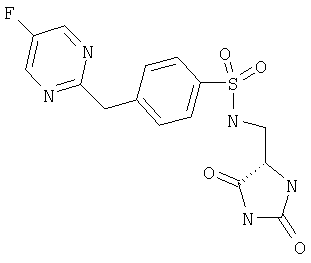
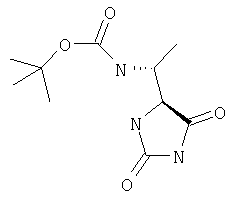
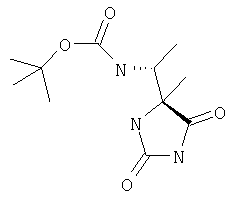
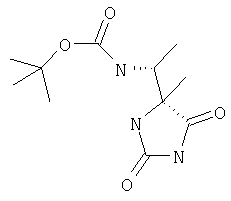
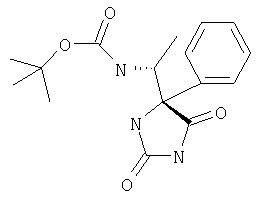
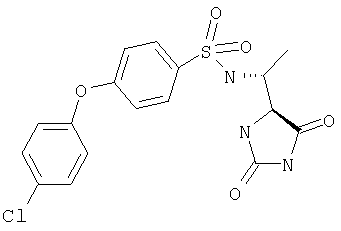
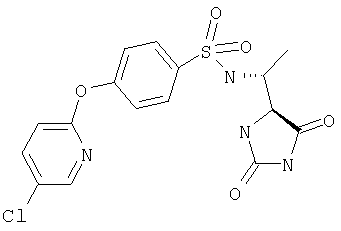
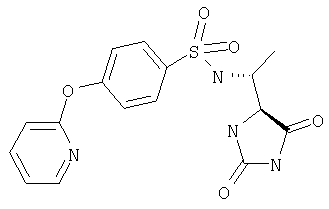
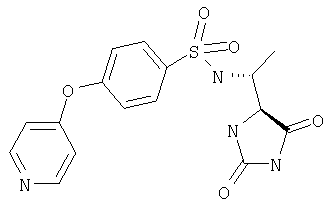
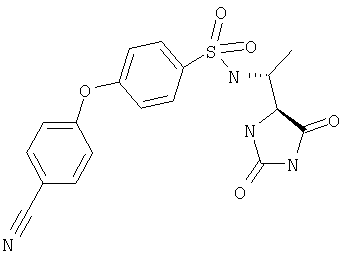
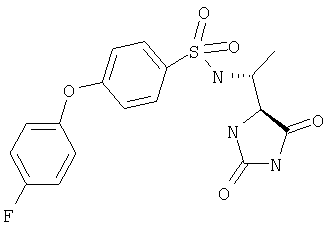
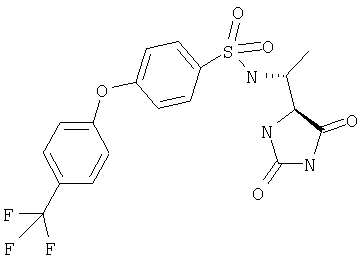
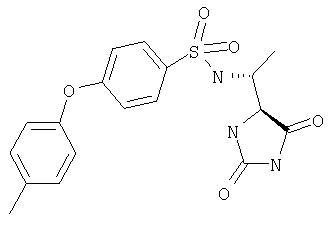
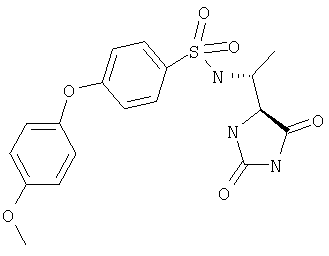
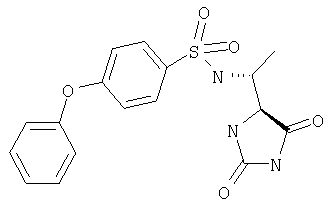
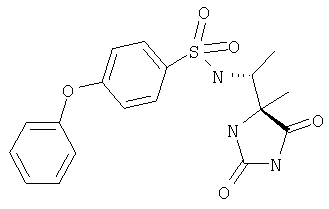
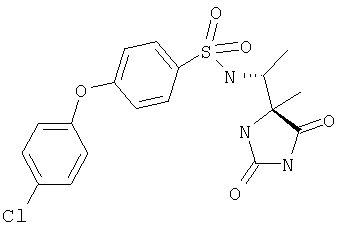
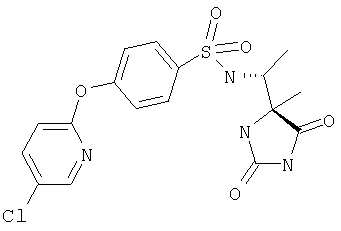
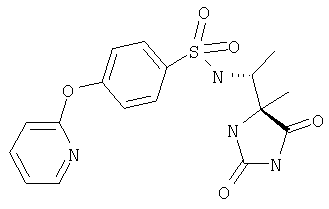
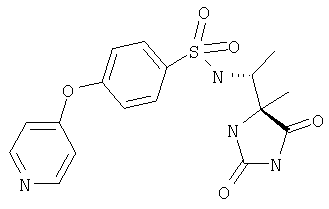
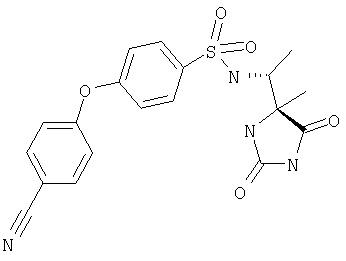
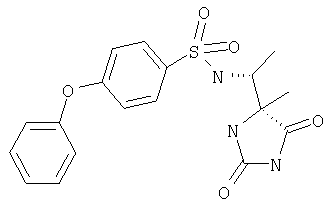
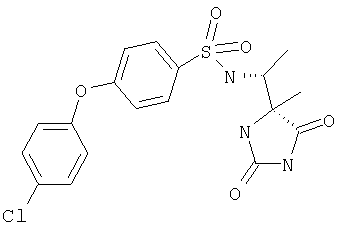
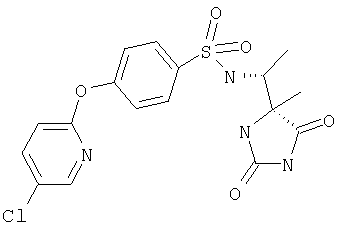
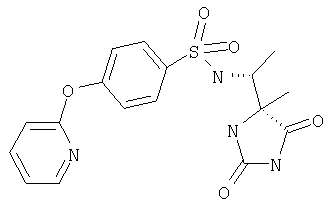
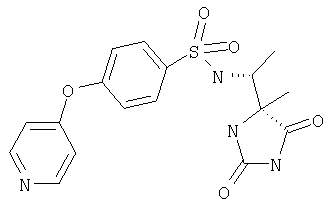
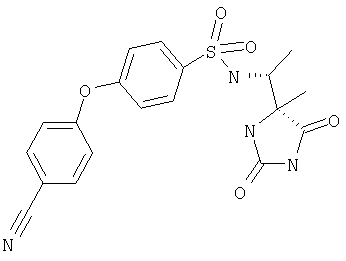
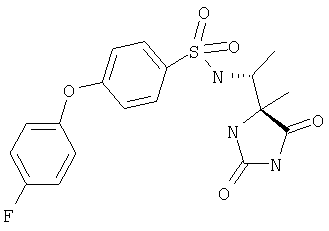
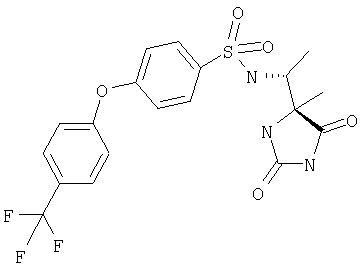
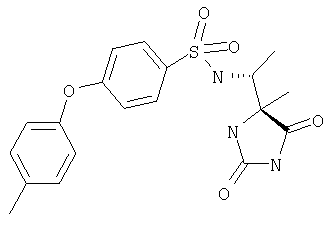
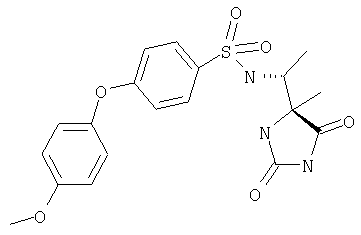
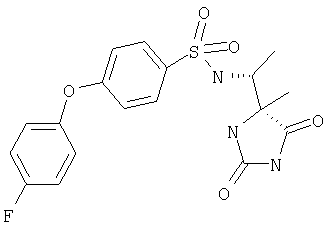
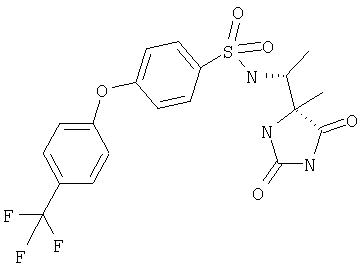
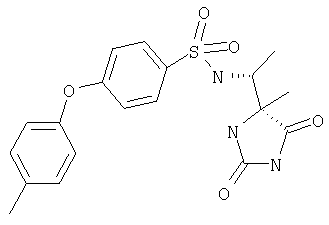
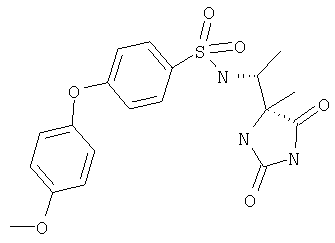
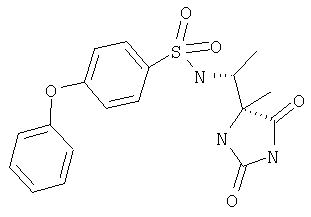
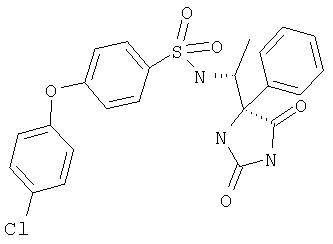
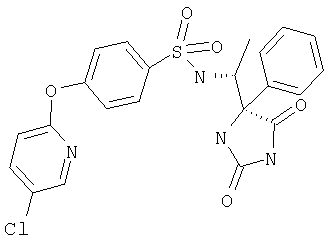
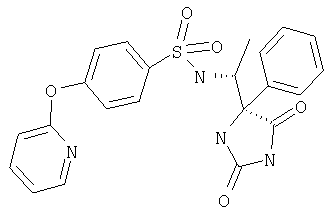
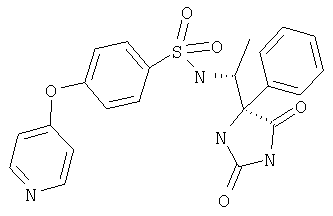
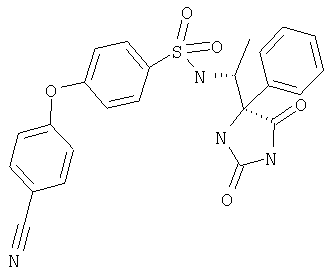
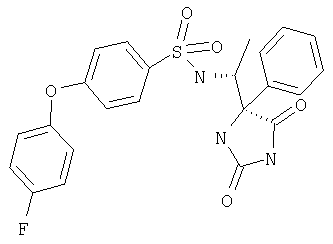
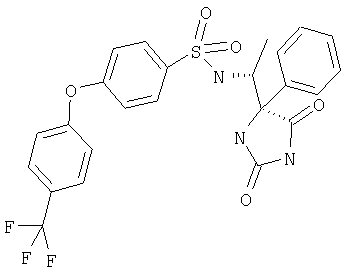
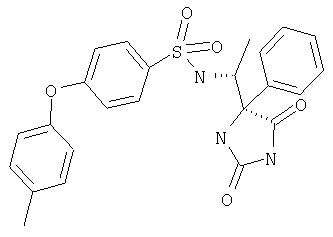
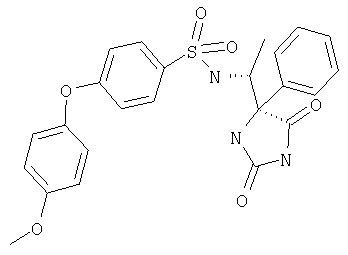
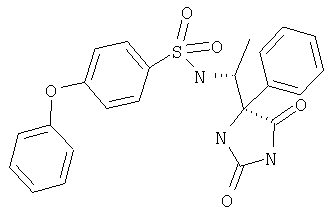
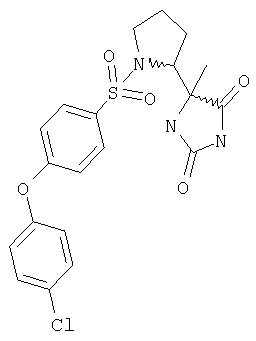
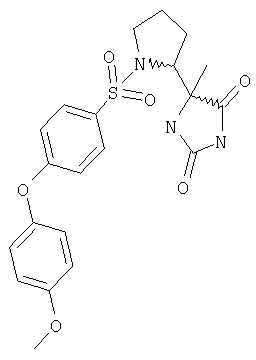
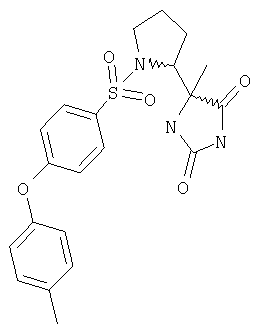
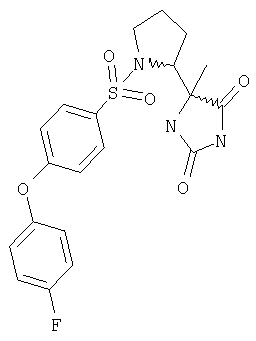
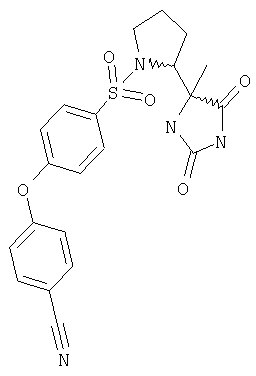
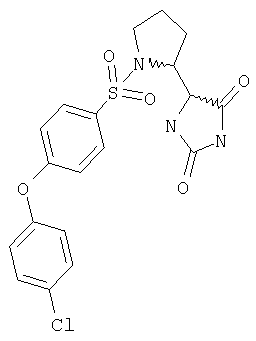
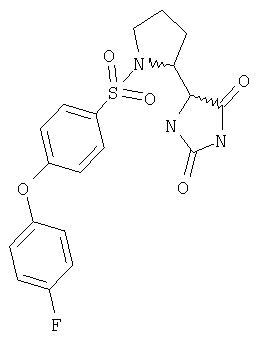
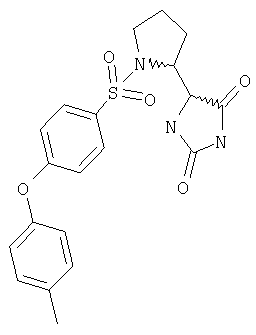
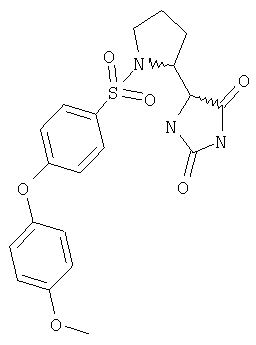
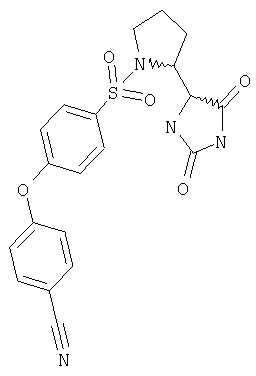
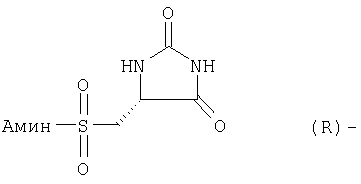
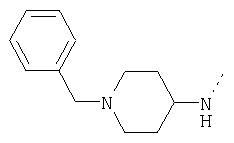
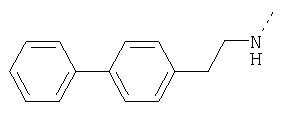
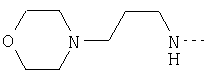
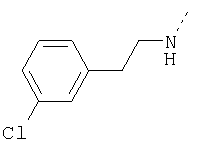
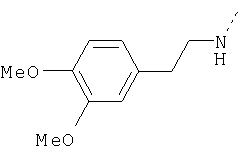
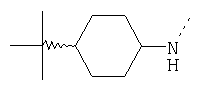
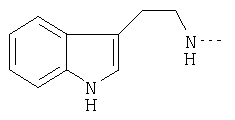
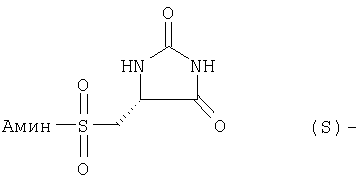
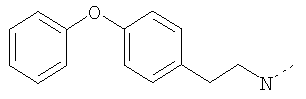
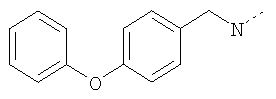
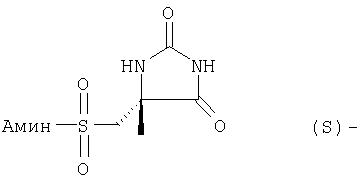
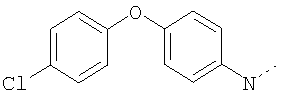
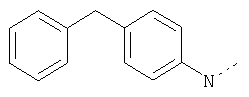
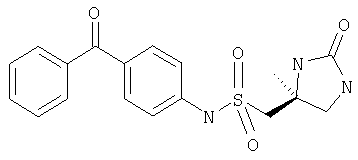
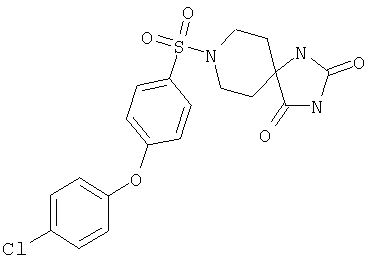 m/z 437 (MH+), М.м. 435,89
m/z 437 (MH+), М.м. 435,89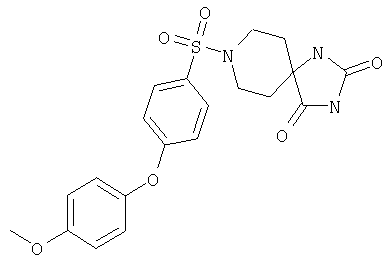 m/z 432 (MH+), М.м. 431,47
m/z 432 (MH+), М.м. 431,47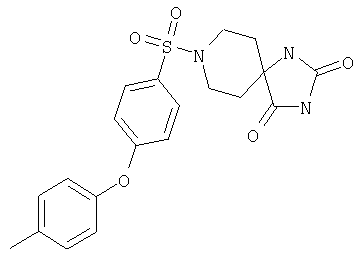 m/z 416 (MH+), М.м. 415.47
m/z 416 (MH+), М.м. 415.47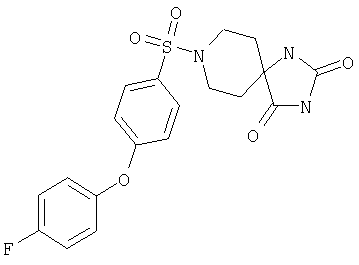 m/z 420 (MH+), М.м. 419.43
m/z 420 (MH+), М.м. 419.43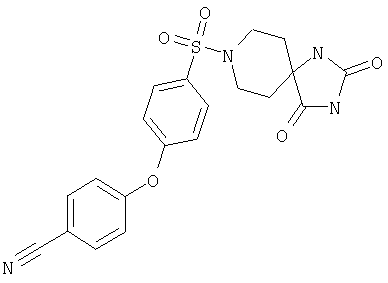 m/z 427 (MH+), М.м. 426,45
m/z 427 (MH+), М.м. 426,45