|
|
(21), (22) Заявка: 2005118124/15, 10.06.2005
(24) Дата начала отсчета срока действия патента:
10.06.2005
(46) Опубликовано: 27.01.2007
(56) Список документов, цитированных в отчете о
поиске:
Лабораторные методы исследования в клинике, под ред. В.В.Меньшикова, Москва, «Медицина», 1987, с.310-311. ВЛАДИМИРОВ Ю.А. “Активированная хемилюминесценция и биолюминесценция как инструмент в медико-биологических исследованиях”, Соросовский образовательный журнал, 2001, т.7, №1, с.16-23. HAMERS M.N. et al. “Kinetics and mechanism of the
Адрес для переписки:
614081, г.Пермь, ул. Голева, 13, ИЭГМ УрО РАН, директору В.А. Демакову
|
(72) Автор(ы):
Ширшев Сергей Викторович (RU),
Куклина Елена Михайловна (RU),
Заморина Светлана Анатольевна (RU),
Никитина Наталья Михайловна (RU),
Некрасова Ирина Валерьевна (RU)
(73) Патентообладатель(и):
Институт экологии и генетики микроорганизмов Уральского отделения Российской академии наук (ИЭГМ УрО РАН) (RU),
Ширшев Сергей Викторович (RU)
|
(54) СПОСОБ ОПРЕДЕЛЕНИЯ ФАГОЦИТАРНОЙ АКТИВНОСТИ НЕЙТРОФИЛОВ ПЕРИФЕРИЧЕСКОЙ КРОВИ ЧЕЛОВЕКА ПО СТЕПЕНИ ГАШЕНИЯ БИОЛЮМИНЕСЦЕНЦИИ
(57) Реферат:
Изобретение относится к области лабораторной диагностики и может быть использовано для определения фагоцитарной активности нейтрофилов периферической крови человека. Сущность способа состоит в том, что определение фагоцитарной активности нейтрофилов периферической крови человека основано на поглощении объектов фагоцитоза, в качестве которых используется культура люминесцентных бактерий генно-инженерного штамма E.coli lux+. Данные бактерии обладают способностью к биолюминесценции, которая фиксируется при помощи биолюминометра и в процессе их поглощения нейтрофилами периферической крови человека значительно снижается. Техническим результатом является разработка более точного способа определения фагоцитарной активности нейтрофилов. 2 табл., 1 ил.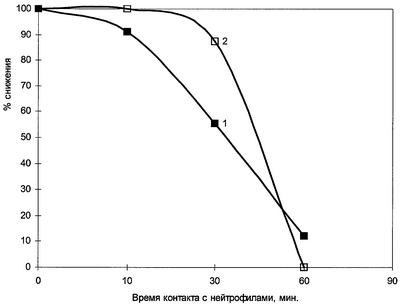
(56) (продолжение):
CLASS=”b560m”bactericidal action of human neutrophils against Escherichia coli”, Blood. 1984 Sep; 64(3):635-641. SU 1837231 A1, 30.08.1993. RU 2131609 C1, 10.06.1999.
Изобретение относится к биологии и медицине, а именно к способам определения фагоцитарной активности нейтрофилов периферической крови человека.
В качестве прототипа нами выбран метод определения фагоцитарной активности нейтрофилов периферической крови, основанный на поглощении объектов фагоцитоза, в качестве которых выступают стафилококки штамма 209 (Лабораторные методы исследования в клинике: Справочник / Меньшиков В.В., Делекторская Л.Н., Золотницкая Р.П. и др.; Под ред. В.В.Меньшикова. – М.: Медицина, 1987. – С.310-311.). Методика способа-аналога не предусматривает оценку завершенности фагоцитоза бактерий, кроме того отсутствует возможность оценки динамики процесса. Показатели фагоцитарной активности лейкоцитарной взвеси не в полной мере отражают функционирования нейтрофилов как фагоцитирующих клеток, т.к. фракционирование нейтрофилов методикой способа-аналога не предусмотрено.
Цель изобретения – совершенствование способа определения фагоцитарной активности нейтрофилов.
Указанная цель достигается путем использования в качестве объектов фагоцитоза бактерий генно-инженерного штамма E.coli lux, обладающих способностью к биолюминесценции и являющихся одновременно комменсалами и потенциальными патогенами.
Способ осуществляется следующим образом.
Оборудование: биолюминометр, например «Биотокс-6» (область спектральной чувствительности 300-800 нм; область максимальной чувствительности 440-490 нм; динамический диапазон измерения светового потока 106-109 квант/сек; диапазон времени измерения реакции 4 сек). Термостат, центрифуга.
Реактивы: фиколл-верографин (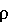 1,077 и 1,077 и 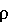 1,112) («Sigma», США; «Спофа», Чехия, соответственно), физиологический раствор (стерильный), дистиллированная вода (стерильная), лиофилизированный штамм E.coli lux+. 1,112) («Sigma», США; «Спофа», Чехия, соответственно), физиологический раствор (стерильный), дистиллированная вода (стерильная), лиофилизированный штамм E.coli lux+.
Цельную кровь в количестве 2-4 мл забирали из локтевой вены в стерильную пробирку, содержащую гепарин (50 Ед/мл), и тщательно ресуспендировали. В пластиковую пробирку было внесено по 3 мл раствора низкой плотности фиколл-верографина (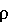 1,077 г/мл), затем подслаивалось 3 мл раствора высокой плотности ( 1,077 г/мл), затем подслаивалось 3 мл раствора высокой плотности (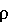 1,112 г/мл). Кровь, разбавленная в 2-3 раза физиологическим раствором, наслаивалась на фиколл-верографин и помещалась в центрифугу на 40 мин при 1700 об/мин. Нейтрофилы собирали с нижней интерфазы. Выделенные клетки помещали в пластиковую центрифужную пробирку и дважды отмывали физиологическим раствором. Концентрацию нейтрофилов доводили до 5×106/мл. 1,112 г/мл). Кровь, разбавленная в 2-3 раза физиологическим раствором, наслаивалась на фиколл-верографин и помещалась в центрифугу на 40 мин при 1700 об/мин. Нейтрофилы собирали с нижней интерфазы. Выделенные клетки помещали в пластиковую центрифужную пробирку и дважды отмывали физиологическим раствором. Концентрацию нейтрофилов доводили до 5×106/мл.
Для оценки фагоцитарной активности в качестве объектов фагоцитоза использовали лиофилизированную культуру люминесцентных бактерий генно-инженерного штамма E.coli lux+. Одну ампулу препарата разводили в 1 мл холодной дистиллированной воды, выдерживали 1 час при 4°С, после чего доводили физиологическим раствором до 50 мл, получая рабочую концентрацию бактерий 5×106/мл.
Суспензию нейтрофилов в количестве 100 мкл смешивали с 1000 мкл разведенной культуры (5×106/мл) E.coli lux+, тщательно ресуспендировали, затем измеряли биолюминесценцию на 0, 10, 30 и 60 минутах инкубации при 37°С. Измерения биолюминесценции проводили на приборе “Биотокс-6”. Исследование проб проводили в соответствии с методическими рекомендациями “Методика экспрессного определения токсичности воды с помощью люминесцентного бактериального теста “Эколюм””, утвержденными руководителем Департамента Госсанэпиднадзора Минздрава России А.А.Монисовым 08.06.2000 МР №11 1/133-09, сертифицированными Государственным комитетом Российской Федерации по стандартизации и метрологии, Свидетельство №01.19.231/2001.
Пример
Предлагаемым способом была измерена фагоцитарная активность нейтрофилов человека по уровню гашения биолюминесценции. Готовый раствор сенсора (рабочая концентрация бактерий E.coli lux+ 5×106/мл) смешивали с суспензией фракционированных нейтрофилов (5×106/мл), содержащей 25% аутоплазмы, в соотношении 10:1, тщательно ресуспендировали, после чего измеряли биолюминесценцию на 0, 10, 30 и 60 минутах инкубации при 37°С. Параллельно проводились высевы культуры E.coli lux+ на среду Эндо (селективная среда для энтеробактерий) в те же временные периоды контакта бактерий с лейкоцитами цельной крови, после чего спустя сутки под кварцевой лампой оценивали количество жизнеспособных клеток по числу колониеобразующих единиц (КОЭ).
Как видно из фиг.1, нейтрофилы периферической крови на протяжении всего срока наблюдения почти полностью (от 100% до 20%) подавляли биолюминесценцию E.coli lux+, и это проявлялась уже на 10 мин инкубации. Показано, что гашение биолюминесценции опережает снижение числа жизнеспособных клеток (КОЭ) в динамике эксперимента. Возможно, это связано с особенностями адгезии и поглощения бактерий нейтрофилами. Гашение биолюминесценции и снижение числа КОЕ в посевах обусловлено процессом фагоцитирования E.coli lux+ нейтрофилами крови.
Важно отметить, что биолюминесценция E.coli lux+ в отсутствие клеток крови снижалась весьма незначительно в сравнении с экспериментальными пробами, в то время как число КОЭ оставалось неизменным (табл.1).
Таблица 1
Изменение активности биолюминесценции и числа живых клеток E.coli lux+ (КОЭ) при разных сроках контакта с моноцитами крови |
| Время инкубации |
Биолюминесценция, Имп/сек |
|
КОЭ, кл/мл |
| E.coli lux+ 5×106/мл + физиологический раствор (контроль) |
E.coli lux+ 5×106/мл + суспензия нейтрофилов |
ИАА |
E.coli lux+ 5×106/мл + физиологический раствор (контроль) |
E.coli lux+ 5×106/мл + Суспензия нейтрофилов |
| 0 мин |
361824 (100%) |
278511 (100%) |
23 |
160×105 (100%) |
160×105 (100%) |
| 10 мин |
373981 (103%) |
253449 (91%) |
32,2 |
160×105 (100%) |
160×105 (100%) |
| 30 мин |
397823 (108%) |
154079 (55,3%) |
61,3 |
160×105 (100%) |
140×105 (87,5%) |
| 60 мин |
402800 (110,8%) |
33889 (12,2%) |
91,6 |
160×105 (100%) |
0,02×105 (0,012%) |
Для оптимального выражения результатов исследования можно применять расчет индекса антагонистической активности (ИАА), отражающий процент гашения биолюминесценции в сравнении с исходным уровнем. Таким образом, ИАА=100×(X1-X1)/X1, где X1 – интенсивность биолюминесценции контрольной пробы, Х2 – опытной пробы. Установлено, что ИАА значительно увеличивается в динамике эксперимента, достигая после часовой инкубации значения 91,6 (табл.1). Для оценки фагоцитарной активности нейтрофилов можно применять как ИАА, так и рассчитывать процент гашения биолюминесценции в пробах в динамике в сравнении с началом измерения (0 мин). Для клинических исследований преимущественное значение имеет ИАА, в то время как для научных исследований помимо ИАА представляется важным отследить динамику гашения люминесценции.
Параллельно для сравнения полученных результатов оценивали фагоцитарную активность нейтрофилов по поглощению объектов фагоцитоза (частицы латекса; 1,5 мкм «ДиаМ», Россия). Для этого в капроновых пробирках смешивали 100 мкл трижды отмытых в физиологическом растворе объектов фагоцитоза (концентрация 107/мл), и 100 мкл суспензии фракционированных нейтрофилов (106/мл). Пробы инкубировали 20 мин при 37°С. Затем содержимое пробирок ресуспендировали и готовили мазки, которые фиксировали метанолом и окрашивали по Романовскому-Гимзе. Рассчитывали следующие показатели:
1) Процент фагоцитоза – т.е. количество клеток, захвативших 1 и более объектов фагоцитоза из 100 подсчитанных фагоцитов. Такие клетки в дальнейшем именуются «истинными фагоцитами».
2) Фагоцитарное число – количество объектов фагоцитоза, которое в среднем приходится на 1 из 100 подсчитанных фагоцитов.
3) Фагоцитарный индекс – количество объектов фагоцитоза, которое приходится на один «истинный» фагоцит.
Фагоцитарная активность нейтрофилов существенно повышалась в динамике наблюдения, причем повышалось как число «истинных» фагоцитов, так и их поглотительная активность (табл.2).
Таблица 2
Изменение фагоцитарной активности лейкоцитов крови в отношении Е.coli lux+ при разных сроках контакта с нейтрофилами крови |
| Время Инкубации |
% фагоцитоза |
Фагоцитарное число |
Фагоцитарный индекс |
| 10 мин |
35
(100%) |
1,29
(100%) |
0,37
(100%) |
| 30 мин |
50
(142,8%) |
1,99
(154,3%) |
0,40
(108,1%) |
| 60 мин |
58,21
(166,3%) |
2,59
(200,8%) |
0,44
(118,9%) |
Таким образом, чем выше степень фагоцитарной активности нейтрофилов, тем выше степень снижения биолюминесценции и ниже количество КОЭ. Степень гашения биолюминесценции E.coli lux+ в присутствии клеток крови является маркером фагоцитарной активности нейтрофилов и позволяет дифференцировать как снижение, так и повышение фагоцитарной активности клеток. Метод можно использовать в научных и клинических исследованиях, так как изучение фагоцитарной активности моноцитов имеет большое значение в комплексном анализе диагностики различных иммунодефицитных состояний. Приведенные примеры исследований убедительно подтверждают существенные преимущества заявляемого способа в сравнении с прототипом. Заявляемый способ отличается более высокой объективностью, лишен субъективности и трудоемкости микроскопического метода и позволяет оценивать степень завершенности фагоцитоза.
Формула изобретения
Способ определения фагоцитарной активности нейтрофилов крови, отличающийся тем, что в качестве фагоцитируемого объекта используют лиофилизированную культуру люминесцентных бактерий генно-инженерного штамма Е.coli lux+, разводят холодной дистиллированной водой, выдерживают 1 ч при 4°С, затем разводят физиологическим раствором до концентрации бактерий 5×10 /мл, смешивают с суспензией нейтрофилов в концентрации 5×106/мл, фракционированных на двойном градиенте фиколл-верографина с 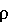 1,077 и 1,113, содержащей 25% аутоплазмы, в соотношении 10:1, тщательно ресуспендируют, инкубируют при 37°С, измеряют биолюминисценцию на 0, 10, 30 и 60 мин инкубации и фагоцитарную активность нейтрофилов (ФА) определяют по проценту гашения биолюминесценции по сравнению с исходным уровнем по формуле 1,077 и 1,113, содержащей 25% аутоплазмы, в соотношении 10:1, тщательно ресуспендируют, инкубируют при 37°С, измеряют биолюминисценцию на 0, 10, 30 и 60 мин инкубации и фагоцитарную активность нейтрофилов (ФА) определяют по проценту гашения биолюминесценции по сравнению с исходным уровнем по формуле
ФА=100×(X1-X2)/X1,
где X1 – интенсивность биолюминесценции контрольной пробы;
Х2 – интенсивность биолюминесценции опытной пробы.
РИСУНКИ
|
|