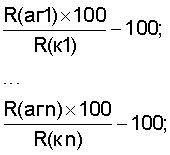Патент на изобретение №2291437
|
||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ МОНИТОРИНГА ЗА СОСТОЯНИЕМ БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ И РАЗВИТИЕМ НЕВРОЛОГИЧЕСКИХ И СОСУДИСТЫХ ЕГО ОСЛОЖНЕНИЙ
(57) Реферат:
Изобретение относится к области лабораторной диагностики и может быть использовано для оценки состояния больных сахарным диабетом и развитием у них неврологических и сосудистых осложнений. Сущность изобретения состоит в том, что определяют иммунореактивность сыворотки крови по отношению к инсулину, к антиинсулиновым антителам или их антигенсвязывающим фрагментам, к антиантиинсулиновым антителам, связывающим антитела к инсулину и антитела к фактору роста или их антигенсвязывающим фрагментам и антигену ANCA и по увеличению иммунореактивности сыворотки по отношению к определяемым параметрам относительно нормы определяют степень прогрессии сахарного диабета и неворологических и сосудистых осложнений. Техническим результатом является повышение точности мониторинга за состоянием больных сахарным диабетом.
(56) (продолжение): CLASS=”b560m”Lab Anal. 1993; 7(5):293-300. WINOCOUR PH et al. The relevance of persistent C-peptide secretion in type 1 (insulin-dependent) diabetes mellitus to glycaemic control and diabetic complications Diabetes Res Clin Pract. 1990 Apr; 9(1):23-35. EP 0569800, 18.11.1993.
Изобретение относится к медицине, в частности к терапии и эндокринологии, и может найти применение в оценке эффективности терапии сахарного диабета 1 и 2 типа. Известно, что иммунная система здорового человека постоянно продуцирует естественные регуляторные аутоантитела (ауто-АТ) к любым антигенным компонентам собственного организма, в том числе ауто-АТ к компонентам клеток поджелудочной железы и инсулиновым рецепторам (Полетаев А.Б. и др. Регуляторная метасистема, М.: Медицина, 2002). Синтез ауто-АТ в здоровом организме поддерживается в определенных границах, необходимых для выполнения последними определенных регуляторных функций, а их избыточная, равно как и недостаточная продукция могут вести к развитию патологических состояний, в том числе инсулинзависимого сахарного диабета (СД типа 1) и инсулиннезависимого сахарного диабета (СД типа 2), а также сосудистых и неврологических осложнений основного заболевания, нередко ведущих к стойкой инвалидности. Вышесказанное явилось основанием для разработки предлагаемого способа, пригодного для диагностической и прогностической оценки уровней ряда ауто-АТ, содержание которых отражает уровень аутоиммуноагрессии к инсулинсекретирующим клеткам поджелудочной железы при СД-1, к периферическим инсулиновым рецепторам при СД-2, а также осуществлять контроль за развитием основных осложнений сахарного диабета (сосудистых и неврологических). Общепринятым способом диагностики сахарного диабета и мониторинга за их состоянием является определение уровня сахара в крови (В.В.Медведев, Ю.З.Волчек. “Клиническая лабораторная диагностика” “Гиппократ” СПб, 1997, стр.154). Недостатком этого известного способа является его сравнительно невысокая надежность и невозможность мониторинга за развитием основных сосудистых и неврологических осложнений, сопровождающих сахарный диабет. Задача изобретения – способ мониторинга за состоянием больных сахарным диабетом и развитием неврологических и сосудистых его осложнений, позволяющий более объективно судить о прогрессии сахарного диабета и о развитии неврологических и сосудистых осложнений. Поставленная задача решается способом, заключающимся в том, что определяют иммунореактивность сыворотки крови по отношению к инсулину, к антиинсулиновым антителам (связывающим антитела к рецепторам инсулина) или их антигенсвязывающим фрагментам, антиантиинсулиновым антителам, связывающим антитела к инсулину и антитела к фактору роста нервов (антиидиотипам антиинсулиновых антител) или их антигенсвязывающим фрагментам и антигену ANCA и при увеличении иммунореактивности на 6-15% по отношению к инсулину и/или к антиинсулиновым антителам или их антигенсвязывающим фрагментам делают вывод об умеренной прогрессии сахарного диабета, а при одновременном в такой же степени повышении иммунореактивности по отношению к антиантиинсулиновым антителам, связывающим антитела к инсулину и антитела к фактору роста нервов или антигенсвязывающим фрагментам делают вывод об умеренной прогрессии диабетической нейропатии, а при одновременном повышении в такой же степени иммунореактивности по отношению к ANCA делают вывод о диабетической ангиопатии, а при более высокой иммунореактивности по отношению к перечисленным реагентам делают вывод о высокой степени прогрессии сахарного диабета и его неврологических и сосудистых осложнений. Практическое осуществление способа включает следующие стадии: I. Сорбцию на стандартные 96-луночные полистироловые планшеты для ИФА а) инсулина, б) молекул идиотипических антиинсулиновых антител (или их фрагментов) – иммунохимических аналогов инсулиновых рецепторов; б) антиидиотипических антител (антиантител), специфически взаимодействующих с антителами к инсулину; в) анионных белков цитоплазмы нейтрофилов (ANCA); II. Нанесение на них тестируемых проб сывороток пациентов и эталонной референс-сыворотки, полученной от здоровых лиц; III. Выявление образующихся антигенантительных комплексов с помощью конъюгатов вторичных (антивидовых) иммуноглобулинов, меченных пероксидазой хрена или иным ферментом; IV. Проявление реакции в лунках планшета с помощью субстрата-хромогена; V. Сравнение интенсивности реакции в лунках, содержащих тестируемые сыворотки с лунками, содержащими референс-сыворотку. Для проведения анализа ЭЛИ-ДИА-Тест требуется около 0,03 мл сыворотки крови обследуемого (например, полученной из подушечки пальца). ПОЛУЧЕНИЕ ОСНОВНЫХ КОМПОНЕНТОВ, ИСПОЛЬЗУЕМЫХ ПО ПРЕДЛАГАЕМОМУ СПОСОБУ (ТЕСТ-СИСТЕМЕ ЭЛИ-ДИА-ТЕСТ). 1. В работе используется коммерческий препарат инсулина. 2. Получение антиинсулиновых антител или их антигенсвязывающих фрагментов проводили с помощью стандартных процедур иммуноаффинной хроматографии, как описано ранее (Полетаев А.Б. и др. Ж. Нейроиммунология, 2003, 1, 1, 11-17). 3. Получение антиантиинсулиновых антител или их антигенсвязывающих фрагментов проводили с помощью стандартных процедур иммуноаффинной хроматографии, как описано ранее (Полетаев А.Б. и др. Ж. Нейроиммунология, 2003, 1, 1, 11-17). 4. Получение антигена ANCA проводили следующим образом: из цельной крови человека выделяли фракцию нейтрофилов, экстрагировали ее с помощью нейтрального буферного раствора (например, трис-хлоридного), экстракт пропускали через анионообменную колонку (например, ДЕАЕ-целлюлоза), связавшийся материал элюировали солевым раствором (например, 1 М хлоридом натрия) и использовали в работе. МЕТОДИКА ПРОВЕДЕНИЯ НЕПРЯМОГО ИФА. 1. Для сорбции на стандартные 96-луночные плоскодонные планшеты для иммуноферментного анализа готовили растворы каждого из компонентов тест-системы на карбонатном буфере рН 9-10. Приготовленные растворы вносили в отдельные лунки планшета и инкубировали в течение 1-24 ч. 2. После инкубации отмывали планшеты отмывочным буфером (например, 0.15 М NaCl с 0.05% твин-20) и проводили тестирование сывороток; для этого: а) в отдельных флаконах или ванночках для ИФА готовили разведения сывороток (например, 1:200) на отмывочном буфере, б) вносили разведенные сыворотки в лунки планшета, в) планшеты инкубировали ночь при +4°С или 1-3 ч при +37…+39°С, г) отмывали планшеты и проявляли реакцию с помощью стандартных приемов, используя конъюгат пероксидазы хрена (или иного фермента) с антителами к иммуноглобулинам IgG человека и раствор субстрата-хромогена (например, 0.01-0.05% о-фенилендиамин с 0.001-0.01% перекиси водорода на 0.01-0.05 М цитрат-фосфатном буфере в случае применения пероксидазных конъюгатов). 3. Инкубировали планшеты в темноте 10-30 мин при комнатной температуре. 4. По достижении оптимального уровня окрашивания (обычно через 10-20 мин инкубации в темноте) реакцию останавливают добавлением 0.2-0.4 М кислоты. 5. Регистрация результатов реакции: интенсивность окрашивания оценивают с помощью иммуноферментного анализатора (ИФА-ридера) любой модели. 6. Обработка полученных данных: по полученным значениям оптической плотности лунок рассчитывают относительную интенсивность реакции тестировавшихся сывороток с каждым из компонентов тест-системы ЭЛИ-ДИА-Тест по отношению к реакции контрольной сыворотки с тем же антигеном за минусом 100 единиц и выражают в условных единицах. Для расчета используют формулу: где R(aг1) – величина оптической плотности анализируемой сыворотки крови в лунках с антигеном-1; R(агn) – величина оптической плотности анализируемой сыворотки крови в лунках с антигеном-n; R(к1…кn) – величина оптической плотности контрольной сыворотки крови в лунках с антигенами 1…n. 7. Интерпретация полученных данных: а) в случае если интенсивность реакции исследуемой сыворотки с любым из компонентов тест-системы не выходила за пределы +5% по отношению к реакции сыворотки-эталона, данную сыворотку относят к 1-й классификационной группе (лица без прогрессии основного заболевания и без признаков развития осложнений), б) в случае если интенсивность реакции исследуемой сыворотки с любым из компонентов выходит за пределы группы-1, но не превышает +15% по отношению к реакции сыворотки-эталона, данную сыворотку относят ко 2-й классификационной группе или группе умеренных отклонений (лица с прогрессией СД и/или его осложнениями умеренной выраженности), в) в случае, если интенсивность реакции исследуемой сыворотки с любым из компонентов выходит за пределы 1-й и 2-й групп, данную сыворотку относят к 3-й классификационной группе или группе выраженных отклонений (лица с высоким риском быстрой прогрессии основного заболевания и/или его осложнений), г) вероятность прогрессии СД-1 пропорциональна степени отклонений от нормы в содержании ауто-АТ к инсулину, д) вероятность прогрессии СД-2 пропорциональна степени отклонений от нормы в содержании ауто-АТ к инсулиновым рецепторам, выявляемым по реакции в лунках с адсорбированными антиинсулиновыми антителами (идиотипическими) или их фрагментами, е) вероятность прогрессии диабетической нейропатии пропорциональна степени отклонений от нормы в содержании антител, перекрестно реагирующих как с инсулином, так и с фактором роста нервов, выявляемым по реакции в лунках с адсорбированными анти-антиинсулиновыми антителами (антиидиотипическими) или их фрагментами, ж) вероятность прогрессии диабетической ангиопатии пропорциональна степени отклонений от нормы в содержании антител, реагирующих с антигеном ANCA, з) по динамике изменений в содержании соответствующих ауто-АТ можно судить о позитивных или нарастании негативных тенденций в состоянии обследуемых, например, на фоне проводимого лечения. Необходимо отметить, что выполнение анализов производится в условиях in vitro без какого-либо вреда для обследуемого. ПРИМЕРЫ ПРИМЕР 1 Обследуемый 1 Результаты анализов ЭЛИ-ДИА-Тест (иммунореактивность в % от реакции контрольной сыворотки):
Диагноз: Впервые выявленный сахарный диабет типа-2; давность заболевания около 6 мес. Клинических признаков осложнений не выявлено. ПРИМЕР 2 Обследуемый 2 Результаты анализов ЭЛИ-ДИА-Тест (иммунореактивность в % от реакции контрольной сыворотки):
Диагноз: Сахарный диабет типа-1 с признаками инсулинорезистентности; давность заболевания около 5 лет. Клинические признаки диабетической нейропатии. ПРИМЕР 3 Обследуемый 3 Результаты анализов ЭЛИ-ДИА-Тест (иммунореактивность в % от реакции контрольной сыворотки):
Диагноз: Сахарный диабет типа-2 с признаками инсулинорезистентности (смешанный тип 1+2); давность заболевания около 8 лет. Клинические признаки диабетической ангиопатии с изменениями на глазном дне, признаки нейропатии. ПРИМЕР 4 Обследуемый 4 Результаты анализов ЭЛИ-ДИА-Тест (иммунореактивность в % от реакции контрольной сыворотки):
Диагноз: Сахарный диабет типа-1, состояние декомпенсации; признаки инсулинорезистентности; давность заболевания около 3 лет. Клинические признаки диабетической нейропатии. Обострение хронического инфекционного процесса. ПРИМЕР 5 Обследуемый 5 Результаты анализов ЭЛИ-ДИА-Тест (иммунореактивность в % от реакции контрольной сыворотки):
Диагноз: Сахарный диабет типа-2, компенсированный, без признаков аутоиммунного патогенетического компонента; давность заболевания около 10 лет. Клинические признаки диабетической ангиопатии. В отличие от рассмотренного выше способа-прототипа новый способ позволяет: 1) регистрировать патологические изменения в сывороточном содержании ауто-АТ, взаимодействующих с инсулином (их изменения – характерный признак СД-1), 2) регистрировать патологические изменения в сывороточном содержании ауто-АТ, взаимодействующих с мембранными инсулиновыми рецепторами (их изменения – характерный признак СД-2), 3) регистрировать патологические изменения в сывороточном содержании ауто-АТ, изменения которых предшествуют и сопровождают развитие основных сосудистых и неврологических осложнений диабета как типа 1, так и типа 2 (диабетическая ангиопатия, диабетическая нейропатия), 4) регистрировать патологические изменения, опасные для страдающих сахарным диабетом, но давать прогноз динамики развития основного заболевания у всех лиц, страдающих сахарным диабетом.
Формула изобретения
Способ мониторинга за состоянием больных сахарным диабетом, заключающийся в том, что определяют иммунореактивность сыворотки крови по отношению к инсулину, к антиинсулиновым антителам или их антигенсвязывающим фрагментам, к антиантиинсулиновым антителам, связывающим антитела к инсулину и антитела к фактору роста, или их антигенсвязывающим фрагментам и антигену ANCA и при увеличении иммунореактивности на 6-15% к норме по отношению к инсулину и/или антиинсулиновым антителам или их антигенсвязывающим фрагментам делают вывод об умеренной прогрессии сахарного диабета, а при одновременном в такой же степени повышении иммунореактивности по отношению к антиантиинсулиновым антителам или антигенсвязывающим фрагментам делают вывод об умеренной прогрессии диабетической нейропатии, а при одновременном повышении в такой же степени иммунореактивности по отношению к ANCA делают вывод о диабетической ангиопатии, а при более высокой иммунореактивности по отношению к перечисленным реагентам делают вывод о высокой степени прогрессии сахарного диабета и его неврологических и сосудистых осложнений.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 27.10.2006
Извещение опубликовано: 20.06.2008 БИ: 17/2008
|
||||||||||||||||||||||||||||||||||||||||||||