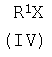Патент на изобретение №2290398
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 5-АМИНО-3-N-R1-АМИНО-1-R-1,2,4-ТРИАЗОЛОВ
(57) Реферат:
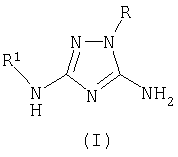
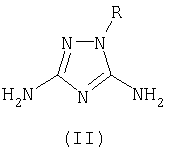
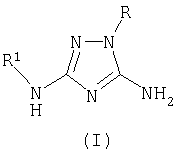
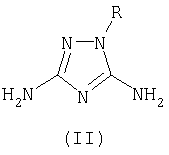
Описывается новый способ получения производных 1,2,4-триазола общей формулы I где R означает фенил, бензил, 4-фенилтиазол-2-ил или 4-метил-5-карбэтокситиазол-2-ил радикал; R1 означает ацетил, трифторацетил, сукциноил, бензоил, метилбензоил или толуолсульфонил радикал, заключающийся в том, что к смеси 3,5-диамино-1-R-1,2,4-триазола общей формулы II где R имеет указанные выше значения, апротонного растворителя, такого как ацетонитрил или диметилформамид, и органического основания (III), которое представляет собой триэтиламин или пиридин, прибавляют ацилирующий агент общей формулы IV, где R1 имеет указанные выше значения, а Х означает Cl или группу OR1, где R1 имеет указанные выше значения, и взаимодействие осуществляют при температуре -10÷+120°С и перемешивании, при мольном соотношении II:III:IV=1,00:1,15-1,40:1,05-1,35. Описываемый способ позволяет получить целевой продукт с высокой степенью чистоты и без перерасхода реагентов.
Изобретение относится к области получения органических веществ и может быть использовано в производстве лекарственных или биологически активных соединений. Задачей изобретения является разработка способа получения 5-амино-3-N-ациламино-1-R-1,2,4-триазолов и 5-амино-3-N-сульфониламино-1-R-1,2,4-триазолов общей формулы (I), с высокой чистотой целевых продуктов, без образования побочных соединений и перерасхода реагентов. Поставленная задача достигается за счет того, что в предлагаемом способе получения 5-амино-3-N-ациламино-1-R-1,2,4-триазолов и 5-амино-3-N-сульфониламино-1-R-1,2,4-триазолов общей формулы (I), включающем ацилирование 3,5-диамино-1-R-1,2,4-триазолов (II), к смеси 3,5-диамино-1-R-1,2,4-триазола формулы (II), апротонного растворителя и органического основания (III), которое представляет собой триэтиламин или другой третичный алифатический амин или пиридин или замещенный пиридин, прибавляют ацилирующий агент общей формулы (IV), при мольном соотношении (II):(III):(IV)=1.00:1.15-1.40:1.05-1.35, реакционную смесь перемешивают при температуре -10÷+120°С. Проведенные исследования показали, что в предлагаемом способе можно использовать различные апротонные растворители, однако наилучшие результаты были получены при использовании ацетонитрила, диметилформамида, диметилсульфоксида, тетрагидрофурана и ацетона. В качестве органических оснований можно использовать третичные алифатические амины или соединения пиридинового ряда, однако наиболее целесообразно использовать триэтиламин или пиридин, поскольку эти соединения являются наиболее дешевыми. Мольное соотношение (II):(III):(IV)=1.00:1.15-1.40:1.05-1.35 является оптимальным. Изменение мольного соотношения приводит либо к образованию побочных соединений и низкой чистоте целевых продуктов (I), либо перерасходу реагентов, что экономически нецелесообразно. Ацилирование должно проводиться в указанном температурном интервале. При температуре ниже -10°С значительно уменьшается скорость реакции и увеличивается продолжительность процесса, что технологически нецелесообразно. При температуре выше 120°С происходит уменьшение выхода целевых соединений (I) вследствие протекания побочных реакций. Способ осуществляется следующим образом. К смеси 3,5-диамино-1-R-1,2,4-триазола (II), апротонного растворителя и органического основания (III) прибавляют ацилирующий агент общей формулы (IV) при мольном соотношении (II):(III):(IV)=1.00:1.15-1.40:1.05-1.35, реакционную смесь перемешивают при температуре -10÷+120°С в течение 10-30 минут, выпавший осадок целевого продукта (I) отфильтровывают и перекристаллизовывают. Пример 1 К смеси 1 г (5.7 ммоль) 3,5-диамино-1-фенил-1,2,4-триазола, 0.64 г (8.0 ммоль) пиридина и 5 мл ацетонитрила приливают при перемешивании 0.69 г (6.8 ммоль) уксусного ангидрида. Реакционную смесь перемешивают 10 мин при температуре 81-83°С, охлаждают до 20°С, выпавший осадок отфильтровывают. Получают 1.1 г (90%) 5-амино-3-ацетиламино-1-фенил-1,2,4-триазола. tпл=239-241°С (из воды). Спектр ЯМР 1Н, Найдено (%): С 55.30; Н 5.12; N 32.21. C10H11N5O Вычислено (%): С 55.29; Н 5.10; N 32.24. Пример 2 К смеси 1 г (5.7 ммоль) 3,5-диамино-1-фенил-1,2,4-триазола, 0.64 г (8.0 ммоль) пиридина и 5 мл ацетонитрила приливают по каплям при перемешивании и температуре минус 10-0°С раствор 0.82 г (7.2 ммоль) трифторуксусного ангидрида в 3 мл ацетонитрила. Реакционную смесь перемешивают при температуре минус 10-0°С 20 минут, выпавший осадок отфильтровывают. Получают 0.94 г (61%) 5-амино-3-трифторацетиламино-1-фенил-1,2,4-триазола. tпл=213-214°C (этанол). Спектр ЯМР 1Н, Найдено (%): С 44.30; Н 2.95; N 25.86. C10H8F3N5О Вычислено (%): С 44.29; Н 2.97; N 25.82. Пример 3 К смеси 1 г (5.7 ммоль) 3,5-диамино-1-фенил-1,2,4-триазола, 0.64 г (8.0 ммоль) пиридина и 5 мл ацетонитрила приливают раствор 0.73 г (7.3 моль) янтарного ангидрида в 3 мл ацетонитрила. Реакционную смесь перемешивают 15 мин при температуре 81-83°С, охлаждают до 20°С, подкисляют 1 н. HCl до рН 4-5, выпавший осадок отфильтровывают. Получают 1.1 г (63%) 5-амино-3-сукциноиламино-1-фенил-1,2,4-триазола. tпл=206°C с разл. (этанол). Спектр ЯМР 1Н, Найдено (%): С 52.38; Н 4.75; N 25.46. C12H13N5O3 Вычислено (%): С 52.36; Н 4.76; N 25.44. Пример 4 К смеси 1 г (5.7 ммоль) 3,5-диамино-1-фенил-1,2,4-триазола, 0.8 г (8.0 ммоль) триэтиламина и 5 мл ацетонитрила приливают по каплям 1.1 г (7 ммоль) пара-метилбензоилхлорида. Реакционную смесь перемешивают 10 мин при температуре 81-83°С, выпавший осадок отфильтровывают. Получают 1.31 г (71%) 5-амино-3-пара-метилбензоиламино-1-фенил-1,2,4-триазола. tпл=231-232°C (этанол). Спектр ЯМР 1Н, Найдено (%): С 66.50, Н 5.17, N 23.85. C16H15N5O Вычислено (%): С 66.52, Н 5.15, N 23.88. Пример 5 К смеси 1 г (5.7 ммоль) 3,5-диамино-1-фенил-1,2,4-триазола, 0.64 г (8.0 ммоль) пиридина и 5 мл ацетонитрила приливают по каплям раствор 1.37 г (7.2 ммоль) пара-толуолсульфохлорида в 3 мл ацетонитрила. Реакционную смесь перемешивают 25 мин при температуре 81-83°С, охлаждают до 20°С, выпавший осадок отфильтровывают. Получают 1.51 г (73%) 5-амино-3-пара-толуолсульфониламино-1-фенил-1,2,4-триазола. tпл=256-257°C (диметилформамид). Спектр ЯМР 1Н, Найдено (%): С 54.72; Н 4.57; N 21.25. C15H15N5O2S Вычислено (%): С 54.70; Н 4.59; N 21.26. Пример 6 К смеси 1 г (5 ммоль) 3,5-диамино-1-бензил-1,2,4-триазола, 0.64 г (8.0 ммоль) пиридина и 5 мл ацетонитрила приливают по каплям раствор 0.6 г (6.8 ммоль) уксусного ангидрида в 3 мл ацетонитрила. Реакционную смесь перемешивают 10 мин при температуре 81-83°С, выпавший осадок отфильтровывают. Получают 1 г (75%) 5-амино-3-ацетиламино-1-бензил-1,2,4-триазола. tпл=224-225°C (этанол). Спектр ЯМР 1Н, Найдено (%): С 57.15; Н 5.68; N 30.25. С11Н13N5O Вычислено (%): С 57.13; Н 5.67; N 30.28. Пример 7 К смеси 1 г (5 ммоль) 3,5-диамино-1-бензил-1,2,4-триазола, 0.62 г (7.8 ммоль) пиридина и 5 мл ацетонитрила приливают по каплям раствор 0.84 г (6.5 ммоль) бензоилхлорида в 3 мл ацетонитрила. Реакционную смесь перемешивают 10 мин при температуре 81-83°С, охлаждают до 20°С, выпавший осадок отфильтровывают. Получают 1.07 г (63%) 5-амино-3-бензоиламино-1-бензил-1,2,4-триазола. tпл=168-170°C (этанол). Спектр ЯМР 1Н, Найдено (%): С 65.53; Н 5.16; N 23.89. C16H15N5O Вычислено (%): С 65.52; Н 5.15; N 23.88. Пример 8 К смеси 1 г (5 ммоль) 3,5-диамино-1-бензил-1,2,4-триазола, 0.65 г (8.2 ммоль) пиридина и 5 мл ацетонитрила приливают по каплям раствор 1.1 г (6.6 ммоль) пара-толуолсульфонилхлорида в 3 мл ацетонитрила. Реакционную смесь перемешивают 25 мин при температуре 81-83°С, охлаждают до 20°С, выпавший осадок отфильтровывают. Получают 1.29 г (65%) 5-амино-3-пара-толуолсульфониламино-1-бензил-1,2,4-триазола. tпл=271-273°С(этанол). Спектр ЯМР 1Н, Найдено (%): С 55.94; Н 4.97; N 20.38. C16H17N5O2S Вычислено (%): 55.96; Н 4.99; N 20.39. Пример 9 К смеси 1 г (3.8 ммоль) 3,5-диамино-1-[-4-метил-5-карбэтокситиазолил-2]-1,2,4-триазола, 0.7 г (7.0 ммоль) триэтиламина и 3 мл диметилформамида приливают по каплям раствор 0.97 г (5.1 ммоль) пара-толуолсульфонилхлорида в 2 мл диметилформамида. Реакционную смесь перемешивают 15 мин при температуре 115-120°С, охлаждают до 20°С, выпавший осадок отфильтровывают. Получают 0.83 г (53%) 5-амино-3-пара-толуолсульфониламино-1-[-4-метил-5-карбэтокситиазолил-2]-1,2,4-триазола. tпл=288-290°C (этанол). Спектр ЯМР 1Н, Найдено (%): С 45.48; Н 4.27; N 19.90. C16H18N6O4S2 Вычислено (%): 45.49; Н 4.29; N 19.89. Пример 10 К смеси 1 г (3.8 ммоль) 3,5-диамино-1-[-4-метил-5-карбэтокситиазолил-2]-1,2,4-триазола, 0.54 г (6.8 ммоль) пиридина и 5 мл ацетонитрила приливают по каплям раствор 0.63 г (5.1 ммоль) бензоилхлорида в 3 мл ацетонитрила. Реакционную смесь перемешивают 10 мин при температуре 115-120°С, охлаждают до 20°С, выпавший осадок отфильтровывают. Получают 0.42 г (30%) 5-амино-3-бензоиламино-1-[-4-метил-5-карбэтокситиазолил-2]-1,2,4-триазола. tпл=258-260°С (этанол). Спектр ЯМР 1Н, Найдено (%): С 51.61; Н 4.32; N 22.56. C16H16N6OS Вычислено (%): С 51.60; Н 4.33; N 22.57. Пример 11 К смеси 1 г (3.9 ммоль) 3,5-диамино-1-[-4-фенилтиазолил-2]-1,2,4-триазола, 0.47 г (6.0 ммоль) пиридина и 3 мл диметилформамида приливают по каплям раствор 0.53 г (5.2 ммоль) уксусного ангидрида. Реакционную смесь перемешивают 10 мин при температуре 115-120°С, охлаждают до 20°С, выпавший осадок отфильтровывают. Получают 0.92 г (65%) 5-амино-3-ацетиламино-1-[-4-фенилтиазолил-2]-1,2,4-триазола. tпл=294°С (этанол). Спектр ЯМР 1Н, Найдено (%): С 51.98; Н 4.02; N 27.99. C13H12N6OS Вычислено (%): С 51.99; Н 4.03; N 27.98.
Формула изобретения
Способ получения 5-амино-3-N-R1-амино-1-R-1,2,4-триазолов общей формулы I где R означает фенил, бензил, 4-фенилтиазол-2-ил или 4-метил-5-карбэтокситиазол-2-ил радикал; R1 означает ацетил, трифторацетил, сукциноил, бензоил, метилбензоил или толуолсульфонил радикал, заключающийся в том, что к смеси 3,5-диамино-1-R-1,2,4-триазола общей формулы II где R имеет указанные выше значения, апротонного растворителя, такого, как ацетонитрил или диметилформамид, и органического основания (III), которое представляет собой триэтиламин или пиридин, прибавляют ацилирующий агент общей формулы IV где R1 имеет указанные выше значения, а Х означает Cl или группу OR1, где R1 имеет указанные выше значения, и взаимодействие осуществляют при температуре -10 – +120°С и перемешивании при мольном соотношении II:III:IV=1,00:1,15-1,40:1,05-1,35.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 16.02.2007
Извещение опубликовано: 27.07.2008 БИ: 21/2008
|
||||||||||||||||||||||||||

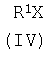
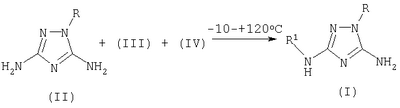
 , м.д. (DMSO d6) 2.05 с (3Н, СН3), 6.38 с (2Н, NH2), 7.30-7.55 м (5Н, аром.), 9.92 с (1Н, NH).
, м.д. (DMSO d6) 2.05 с (3Н, СН3), 6.38 с (2Н, NH2), 7.30-7.55 м (5Н, аром.), 9.92 с (1Н, NH).