Патент на изобретение №2288733
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВА, ОБЛАДАЮЩЕГО НООТРОПНОЙ АКТИВНОСТЬЮ
(57) Реферат:
Изобретение относится к фармацевтической промышленности, в частности к способу получения розавина, обладающего ноотропной активностью. Способ получения розавина, включающий трехкратную экстракцию 70-90% этиловым спиртом измельченных корневищ родиолы розовой (Rhodiola rosea L.) при определенном соотношении сырье:экстрагент, упаривание объединенных экстрактов под вакуумом до густого остатка, хроматографическое разделение на силикагеле, упаривание элюатов и кристаллизацию, причем первую экстракцию проводят при комнатной температуре, а остальные две экстракции при определенной температуре с обратным холодильником. Вышеописанный способ позволяет увеличить выход целевого продукта из корневищ родиолы розовой, сократить продолжительность технологического процесса. 3 табл.
Изобретение относится к химико-фармацевтической промышленности, в частности к производству лекарственных средств в виде субстанций и индивидуальных биологически активных соединений (БАС), и касается способа получения розавина из корневищ родиолы розовой (Rhodiola rosea L.). Корневища родиолы розовой содержат в качестве доминирующих биологически активных соединений фенилпропаноиды, включая розавин (1) [1, 4-8, 15, 16], и являются ценным сырьем для производства тонизирующих, адаптогенных и иммуномодулирующих лекарственных средств [2-5, 7-12, 14, 18]. Известны способы получения розавина, обладающего нейротропной активностью [4, 6, 19], однако недостатком известных способов является сложность технологического процесса и низкий выход целевого продукта. За прототип изобретения нами взят способ получения розавина из корневищ родиолы розовой [6], однако выделение этого вещества осуществляется с использованием громоздкой технологии, заключающейся в экстракции сырья метанолом, упаривании метанольного экстракта до сиропообразного остатка, хроматографической очистке на полиамиде с использованием в качестве элюента смеси растворителей (метанол и хлороформ), последующей рехроматографии фракций, содержащих целевой продукт (розавин), на силикагеле (элюент:хлорофом-метанол в различных соотношениях), упаривании фракций, содержащих целевой продукт до сиропообразной пленки, растворении остатка в кипящем этиловом спирте, фильтрации, кристаллизации, отделении технического розавина путем фильтрации и окончательной очистки целевого продукта путем перекристаллизации из этилового спирта с выходом целевого вещества 3,2 г или 0,64% от воздушно-сухого сырья [6]. Данный способ является не только громоздким и продолжительным (143 ч), но и дает низкий выход целевого вещества – розавина (0,64%). Кроме того, на стадии экстракции сырья используется такой опасный растворитель, как метиловый спирт. Учитывая колоссальную значимость розавина как государственного стандартного образца [13], предложенного нами для целей стандартизации сырья и препаратов родиолы розовой [2, 7, 8, 11], весьма актуальными являются исследования по совершенствованию способа получения розавина. Целью изобретения является увеличение выхода розавина из корневищ родиолы розовой. Поставленная цель достигается тем, что в качестве экстрагента используют 70…90% этиловый спирт, позволяющий исчерпывающе извлекать целевой продукт – розавин (1) из корневищ родиолы розовой с последующим хроматографическим разделением экстрактивных веществ на силикагеле и перекристаллизацией технического целевого продукта. Проведенный заявителем поиск по научно-техническим и патентным источникам информации и выбранный из перечня аналогов прототип [6] позволили выявить отличительные признаки в заявленном техническом решении. Следовательно, заявляемый способ получения удовлетворяет критерию изобретения “новизна”. Проведенный заявителем дополнительный поиск известных технических решений [2, 4, 5, 7, 12, 14, 18, 19] с целью обнаружения в них признаков, сходных с признаками заявляемого способа получения, показал, что эти признаки отсутствуют, следовательно, заявляемое техническое решение удовлетворяет критерию “изобретательский уровень”. Заявляемый способ иллюстрируется следующими примерами. Пример 1. Измельченные воздушно-сухие корневища родиолы розовой (500,0 г) экстрагируют 80% этиловым спиртом в соотношении 1:6 при комнатной температуре в течение 24 ч и затем проводят две экстракции (2×30 мин) при температуре 80-85°С с обратным холодильником. Объединенные водно-спиртовые экстракты упаривают под вакуумом до густого остатка (500 мл), который смешивают с 100 г силикагеля L 40/100, высушивают в течение 24 ч и вносят в колонку (8×10 см), заполненную силикагелем в виде взвеси в хлороформе. Хроматографическую колонку промывают хороформом (0,5 л) и смесью хлороформ-этиловый спирт в соотношении 90:10 (2 л). Целевое вещество элюируют с хлороформ-этиловый спирт в соотношении 85:15 (2 л) и 80:20 (1 л). Контроль за разделением веществ осуществляли хроматографированием на пластинках “Силуфол УФ-254” в системе растворителей: хлороформ-метиловый спирт-вода (26:14:3). Элюаты, содержащие розавин, упаривают под вакуумом до сиропообразной пленки, остаток растворяют в этиловом спирте при нагревании, фильтруют и оставляют на 10 ч. По истечении этого времени образовавшийся кристаллический осадок розавина отделяют, полученный технический целевой продукт растворяют при нагревании в этиловом спирте и оставляют на 10 ч. По истечении этого времени образовавшийся кристаллический осадок розавина отделяют, промывают этиловым спиртом и высушивают на воздухе. Получают 5,3 г целевого вещества выходом 1,06% от воздушно-сухого сырья (табл.1). Спектральные и физико-химические свойства розавина (циннамил-O-(6′-O- Пример 2. Измельченные воздушно-сухие корневища родиолы розовой (500,0 г) экстрагируют 90% этиловым спиртом в соотношении 1:6 при комнатной температуре в течение 24 ч и затем проводят две экстракции (2×30 мин) при температуре 80-85°С с обратным холодильником. Объединенные водно-спиртовые экстракты упаривают под вакуумом до густого остатка (500 мл), который смешивают с 100 г силикагеля L 40/100, высушивают в течение 24 ч и вносят в колонку (8×10 см), заполненную силикагелем в виде взвеси в хлороформе. Далее технологический процесс осуществляют в соответствии с примером 1. Выход целевого продукта – индивидуального розавина составляет 4,35 г или 0,87% от массы воздушно-сухого сырья. Физико-химические и спектральные характеристики розавина соответствуют требованиям ФС 42-0071-01 [13]. Пример 3. Измельченные воздушно-сухие корневища родиолы розовой (500,0 г) экстрагируют 70% этиловым спиртом в соотношении 1:6 при комнатной температуре в течение 24 ч и затем проводят две экстракции (2×30 мин) при температуре 80-85°С с обратным холодильником. Объединенные водно-спиртовые экстракты упаривают под вакуумом до густого остатка (500 мл), который смешивают с 100 г силикагеля L 40/100, высушивают в течение 24 ч и вносят в колонку (8×10 см), заполненную силикагелем в виде взвеси в хлороформе. Далее технологический процесс осуществляют в соответствии с примером 1. Выход целевого продукта – индивидуального розавина составляет 4,75 г или 0,95% от массы воздушно-сухого сырья. Физико-химические и спектральные характеристики розавина соответствуют требованиям ФС 42-0071-01 [13]. Изучение запредельных параметров (примеры 4-6), а именно: осуществление экстракции 60% и 96% этиловым спиртом, использование хроматографии на полиамиде и рехроматографии на силикагеле – приводит к заметному снижению выхода целевого продукта – соответственно до 0,61%, 0,50% и 0,70% (табл.1). Следовательно, оптимальными параметрами способа получения розавина являются: экстракция 70…90% этиловым спиртом в соотношении сырье-экстрагент 1:6 с последующим хроматографическим разделением экстрактивных веществ на силикагеле и кристаллизацией целевого продукта из этилового спирта.
Использование в заявляемом способе 70…90% этилового спирта позволяет исчерпывающе извлекать целевой продукт из корневищ родиолы розовой. При этом заявляемый способ позволяет в 1,77 раза увеличить выход целевого продукта из корневищ родиолы розовой по сравнению с прототипом (табл.2). Кроме того, заявляемый способ позволяет в 1,8 раза сократить продолжительность технологического процесса, в 1,8 раза уменьшить расход дорогостоящего растворителя (хлороформ) и исключить из технологической схемы использование на стадии экстракции опасного растворителя – метилового спирта, а также дорогостоящего сорбента – полиамида.
Ноотропную активность розавина исследовали в условиях методики “открытое поле”, позволяющей оценивать ориентировочно-исследовательскую реакцию крыс [17]. В качестве препарата сравнения изучали эталонный препарат “Пирацетам” [3, 12]. Исследования выполнены на белых беспородных крысах обоего пола с исходной массой 170-210 г., содержавшихся в стандартных условиях вивария на обычном рационе. При этом использовали квадратную камеру размером 100×100×40 см. Ее пол был разделен на 25 квадратов с отверстием в центре. Регистрацию проводили в течение 5 минут. Подсчитывали перемещение с квадрата на квадрат (горизонтальная активность), причем как в 16 внешних, так и в 9 внутренних, количество вставаний на задние лапки (вертикальная активность), количество обследованных отверстий (исследовательская активность), количество умываний (груминг) и количество актов дефекации по количеству фекальных шариков (болюсов). Исследуемые препараты вводили животным внутрижелудочно через зонд, предварительно растворив в дистиллированной воде в различных дозировках: 10 мг/кг (розавин) и 200 мг/кг (пирацетам) один раз в сутки от одного до 5 дней, последний раз за 30 минут до исследования. Основное назначение ориентировочной реакции состоит в повышении возбудимости анализаторов для наилучшего восприятия действия на нервную систему раздражителей с целью установления их биологического значения. Любой вид анализа происходит при активном участии ориентировочного рефлекса. Реакция привыкания или негативного научения оберегает нервную систему, избавляя животное от ненужного числа раздражителей окружающей среды. В то же время она способствует вычленению биологически значимого сигнала. Привыкание является одним из адаптивных навыков у грызунов. В наших экспериментах помещение животного в новое окружение приводит к возникновению исследовательского поведения, которому одновременно препятствует страх. Две антагонистические тенденции характеризуются разным временным ходом, причем лучшим выражением уменьшения страха у животных считается исследование ими внутренних квадратов экспериментальной установки. Результаты исследования, представленные в таблице 3, свидетельствуют о том, что наибольшей степени общая двигательная активность (сумма горизонтальной активности во внешних, внутренних квадратах и вертикальной активности) увеличивалась под воздействием розавина – на 26,0%, тогда как в случае пирацетама этот показатель составил всего 10% (табл.3). Введение розавина существенно увеличивало выход животных во внутренние квадраты: с 0,16±0,1 в контроле до 4,0±0,4* в опыте, то есть в 25 раз, тогда как в случае пирацетама этот показатель увеличился лишь в 6,7 раза (табл.3). Это свидетельствует об уменьшении эмоциональности и страха животных под влиянием данных препаратов. При введении розавина возрастала также вертикальная активность (с 15,1±4,7 подъемов на задние лапки до 25,5±3,1* в опыте), а также горизонтальная активность в наружных квадратах: с 12,5±2,0 в контроле до 15,0±3,7* пересечений квадратов в опыте (табл.3).
Таким образом, использование заявляемого способа получения розавина дает следующие преимущества: 1. Использование в заявляемом способе 70-90% этилового спирта позволяет исчерпывающе извлекать целевой продукт из корневищ родиолы розовой. 2. Заявляемый способ позволяет в 1,77 раза увеличить выход целевого продукта из корневищ родиолы розовой по сравнению с прототипом. 3. Заявляемый способ позволяет в 1,8 раза сократить продолжительность технологического процесса. 4. Заявляемый способ позволяет в 1,8 раза уменьшить расход дорогостоящего растворителя и исключить из технологической схемы на стадии экстракции использование опасного растворителя – метилового спирта, а также дорогостоящего сорбента – полиамида. 5. Заявляемый способ позволяет получить вещество, значительно превосходящее в дозе 10 мг/кг по фармакологическому действию эталонный ноотропный препарат “Пирацетам” (исследуемая доза – 200 мг/кг). Источники информации: 3. Государственный реестр лекарственных средств. – Т.1. Официальное издание. – М., 2002. – 1300 с. 4. Запесочная Г.Г., Куркин В.А. Гликозиды коричного спирта из корневищ Rhodiola rosea II Химия природ. соедин. – 1982. – № 6. – С.723-727. 8. Куркин В.А. Фенилпропаноиды – перспективные природные биологически активные соединения. – Самара: СамГМУ, 1996. – 80 с. 11. Куркин В.А. Фармакогнозия: учебник для студентов фармацевтических вузов. – Самара: ООО “Офорт”, ГОУВПО “СамГМУ”, 2004. – 1180 с. 12. Машковский М.Д. Лекарственные средства. – Т.1 и 2. – М.: Новая Волна, 2000. 13. Розавин – стандартный образец. – ФС 42-0071-01. – М., 2001. – 4 с. 14. Саратиков А.С., Краснов Е.А. Родиола розовая (золотой корень). – Томск: Изд-во Томского ун-та, 2004. – 292 с. 19. Tolonen A., Pakonen M., Hohtola A. et al. Phenylpropanoid glycosides from Rhodiola rosea II Chem. Pharm. Bull. – 2003. – Vol.51, No.4. – P.467-470.
Формула изобретения
Способ получения розавина, включающий трехкратную экстракцию органическим растворителем измельченных корневищ родиолы розовой (Rhodiola rosea L.) при соотношении сырье: экстрагент 1:6, упаривание объединенных экстрактов под вакуумом до густого остатка, хроматографическое разделение на силикагеле, упаривание элюатов и кристаллизацию, отличающийся тем, что экстракцию осуществляют 70-90%-ным этиловым спиртом, при этом первую экстракцию проводят при комнатной температуре, а остальные две экстракции при температуре 80-85°С с обратным холодильником.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 09.08.2008
Извещение опубликовано: 10.07.2010 БИ: 19/2010
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

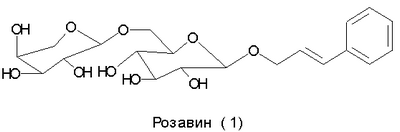
 -L-арабинопиранозил)-
-L-арабинопиранозил)- -D-глюкопиранозид) (1). Бесцветные кристаллы состава С20Н28О10 с т. пл. 171-173°С; УФ-спектр:
-D-глюкопиранозид) (1). Бесцветные кристаллы состава С20Н28О10 с т. пл. 171-173°С; УФ-спектр:  max EtOH – 252 нм. Спектр 1H-ЯМР (200 МГц, C5D5N)
max EtOH – 252 нм. Спектр 1H-ЯМР (200 МГц, C5D5N)  , м.д.: 7.4-7.2 (м, 5Аr-Н). 6.82 (д, 16 Гц, Н-7), 6.5 (дт, 6 и 16 Гц, Н-8), 4.94 (д, 7 Гц, Н-1′), 4.87 (д, 6 Гц, Н-1”), 4.90 (м, 1Н-9), 4.65 (дд, 6 и 12 Гц, 1Н-9), 4.55-3.95 (м, 10Н глюкозы), 3.7 (кв, 2 и 13 Гц, Н-5”е). Качество розавина отвечает требованиям ФС 42-0071-01 [13].
, м.д.: 7.4-7.2 (м, 5Аr-Н). 6.82 (д, 16 Гц, Н-7), 6.5 (дт, 6 и 16 Гц, Н-8), 4.94 (д, 7 Гц, Н-1′), 4.87 (д, 6 Гц, Н-1”), 4.90 (м, 1Н-9), 4.65 (дд, 6 и 12 Гц, 1Н-9), 4.55-3.95 (м, 10Н глюкозы), 3.7 (кв, 2 и 13 Гц, Н-5”е). Качество розавина отвечает требованиям ФС 42-0071-01 [13].