|
|
(21), (22) Заявка: 2005120084/28, 28.06.2005
(24) Дата начала отсчета срока действия патента:
28.06.2005
(46) Опубликовано: 20.11.2006
(56) Список документов, цитированных в отчете о
поиске:
ШОРМАНОВ В.К, ИВАНОВ В.П., КОРОЛЕВ В.А., ПИСТУНОВИЧ Е.В. Определение фюзилада в семенах подсолнечника. Масложировая промышленность. 2004, №4, с.16-17. RU 2234534 C1, 20.08.2004. RU 2034295 C1, 30.04.1995. SU 1273785 A1, 30.11.1986.
Адрес для переписки:
305041, г.Курск, ул. К. Маркса, 3, КГМУ, патентный отдел, З.Н. Куприяновой
|
(72) Автор(ы):
Шорманов Владимир Камбулатович (RU),
Иванов Владимир Петрович (RU),
Елизарова Мадина Камбулатовна (RU),
Королёв Владимир Анатольевич (RU),
Коробанова Татьяна Юрьевна (RU),
Пистунович Елена Владимировна (RU),
Прокошев Александр Алексеевич (RU)
(73) Патентообладатель(и):
Шорманов Владимир Камбулатович (RU),
Иванов Владимир Петрович (RU),
Елизарова Мадина Камбулатовна (RU),
Королёв Владимир Анатольевич (RU)
|
(54) СПОСОБ ОПРЕДЕЛЕНИЯ Н-БУТИЛОВОГО ЭФИРА 2-[4-(5-ТРИФТОРМЕТИЛПИРИДИЛ-2-ОКСИ)ФЕНОКСИ]ПРОПИОНОВОЙ КИСЛОТЫ В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ
(57) Реферат:
Использование: в практике санэпидемстанций, химико-токсикологических, ветеринарных и экологических лабораторий. Сущность: анализируемую пробу измельчают, настаивают с ацетоном, ацетоновое извлечение фильтруют, концентрируют, подвергают хроматографической очистке. Очищают на колонке с использованием нормальнофазного сорбента силикагеля L 40/100  с применением подвижной фазы гексан – ацетон (8:2). Последующее хроматографическое определение осуществляют методом ВЭЖХ в колонке, заполненной сорбентом “Nova-Pak С-18”, с применением подвижной фазы ацетонитрил – вода (7:3) и детектора на основе фотодиодной матрицы. Технический результат изобретения заключается в повышении чувствительности. 3 табл. с применением подвижной фазы гексан – ацетон (8:2). Последующее хроматографическое определение осуществляют методом ВЭЖХ в колонке, заполненной сорбентом “Nova-Pak С-18”, с применением подвижной фазы ацетонитрил – вода (7:3) и детектора на основе фотодиодной матрицы. Технический результат изобретения заключается в повышении чувствительности. 3 табл.
Изобретение относится к биологии, экологии, токсикологической и санитарной химии, а именно к способам определения н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты в биологическом материале, и может быть использовано в практике санэпидемстанций, химико-токсикологических, ветеринарных и экологических лабораторий. Способ относится к числу массовых.
Известен способ определения органических веществ в биологическом материале путем измельчения биологического объекта, неоднократного настаивания с этанолом (каждый раз в течение суток), объединения вытяжек, сгущения объединенного извлечения, осаждения в нем белков абсолютным этанолом, фильтрования, упаривания фильтрата до густоты сиропа и разбавления его водой с последующей экстракцией анализируемых соединений сначала из кислого, а затем из щелочного раствора (Швайкова М.Д. Токсикологическая химия. – М.: Медицина, 1975. – С.119-123).
Способ трудоемок, требует значительных затрат времени на его осуществление, характеризуется низкой степенью извлечения н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты.
Известен способ определения н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты в биологическом материале, заключающийся в том, что биологическую пробу измельчают, настаивают 3-4 часа с 36% раствором хлороводородной кислоты, а затем 24 часа с 36% раствором хлороводородной кислоты и гексаном, фильтруют смесь через бумажный фильтр, фильтрат концентрируют при температуре не выше 40°С до полного испарения гексана, водный остаток обрабатывают 36% раствором хлороводородной кислоты в условиях нагревания при 60°С в течение часа, реакционный раствор охлаждают, доводят до рН 1, экстрагируют диэтиловым эфиром, экстракт отделяют, экстрагент испаряют, остаток растворяют в ацетоне, к полученному раствору прибавляют растворы хлорида аммония и ортофосфорной кислоты, а также силикагель АСК, смесь встряхивают, выдерживают 10 минут, фильтруют, рН фильтрата доводят до 1, после чего фильтрат экстрагируют тетрахлорметаном, органический слой отделяют, экстрагируют 1% раствором гидрокарбоната натрия, водный экстракт отделяют, подкисляют концентрированным раствором хлороводородной кислоты до рН 1, экстрагируют тетрахлорметаном, полученный экстракт отделяют, экстрагент испаряют, сухой остаток растворяют в гексане, хроматографируют на пластинах «Силуфол» UV-254 с использованием подвижной фазы диэтиловый эфир н-гексан муравьиная кислота (60:40:2), хроматограммы проявляют в УФ-свете и определяют анализируемое соединение в виде 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты визуально по интенсивности окраски и площади пятна на хроматограмме (Методы определения микроколичеств пестицидов в продуктах питания, кормах и внешней среде / Т.1 – М.: Колос, 1992. – С.360-361).
Способ характеризуется недостаточно высокими точностью и чувствительностью, длителен и относительно сложен по выполнению. Он не позволяет определять н-бутиловый эфир 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты непосредственно, а предусматривает косвенное определение этого вещества по одному из продуктов его гидролиза.
Задачей настоящего изобретения является повышение чувствительности определения.
Поставленная задача достигается с помощью предлагаемого способа, который заключается в том, что анализируемую пробу измельчают, двукратно настаивают с ацетоном, полученное извлечение фильтруют, испаряют растворитель из фильтрата, остаток растворяют в смеси растворителей гексан – ацетон (8:2), очищают на колонке с силикагелем L 40/100  с применением подвижной фазы гексан – ацетон (8:2), фракции элюата, содержащие анализируемое вещество, объединяют, элюент испаряют, остаток растворяют в смеси растворителей ацетонитрил – вода (7:3) с последующим хроматографическим определением методом ВЭЖХ в колонке размером 150×3,9 мм, заполненной сорбентом «Nova-Pak C-18» с применением подвижной фазы ацетонитрил – вода (7:3) и детектора на основе фотодиодной матрицы. с применением подвижной фазы гексан – ацетон (8:2), фракции элюата, содержащие анализируемое вещество, объединяют, элюент испаряют, остаток растворяют в смеси растворителей ацетонитрил – вода (7:3) с последующим хроматографическим определением методом ВЭЖХ в колонке размером 150×3,9 мм, заполненной сорбентом «Nova-Pak C-18» с применением подвижной фазы ацетонитрил – вода (7:3) и детектора на основе фотодиодной матрицы.
Способ осуществляется следующим образом: биологическую ткань, содержащую н-бутиловый эфир 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты, измельчают, настаивают с ацетоном дважды по 45 минут, извлечения отделяют от твердых частиц биоматериала, объединяют, объединенное извлечение фильтруют, испаряют растворитель из фильтрата, остаток растворяют в смеси растворителей гексан – ацетон (8:2), вносят в колонку с силикагелем L 40/100  , хроматографируют с применением подвижной фазы гексан – ацетон (8:2), фракции элюата, содержащие анализируемое вещество, объединяют, элюент испаряют, остаток растворяют в смеси растворителей ацетонитрил – вода (7:3) с последующим хроматографическим определением методом ВЭЖХ в колонке с сорбентом «Nova-Pak С-18» с применением подвижной фазы ацетонитрил – вода (7:3) и детектора на основе фотодиодной матрицы. , хроматографируют с применением подвижной фазы гексан – ацетон (8:2), фракции элюата, содержащие анализируемое вещество, объединяют, элюент испаряют, остаток растворяют в смеси растворителей ацетонитрил – вода (7:3) с последующим хроматографическим определением методом ВЭЖХ в колонке с сорбентом «Nova-Pak С-18» с применением подвижной фазы ацетонитрил – вода (7:3) и детектора на основе фотодиодной матрицы.
Пример 1
Определение: н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты в ткани печени
К 10 г мелкоизмельченной ткани печени прибавляют 5 мг н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты, тщательно перемешивают биологическую ткань с веществом и оставляют на сутки при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, заливают 20 мл ацетона и выдерживают 45 минут при периодическом перемешивании. Извлечение отделяют, операцию настаивания повторяют в указанных условиях. Отдельные вытяжки объединяют, фильтруют через бумажный фильтр, экстрагент и извлеченную из биологической ткани воду испаряют из фильтрата в токе воздуха. Остаток растворяют в 10 мл смеси растворителей гексан – ацетон (8:2). 2 мл полученного раствора вносят в колонку размером 490×11 мм, заполненную 10 г силикагеля типа L 40/100  . После вхождения раствора в сорбент в колонку вносят подвижную фазу гексан – ацетон (8:2) и осуществляют процесс хроматографирования, поддерживая высоту столба жидкости (элюента) над поверхностью сорбента на уровне 22-24 см. Элюат собирают отдельными фракциями по 2 мл каждая. Фракции 5 и 6 объединяют, элюент испаряют, остаток растворяют в 17,5 мл ацетонитрила, количественно переносят в мерную колбу вместимостью 25 мл и доводят водой до метки. Содержимое колбы перемешивают. 8 мкл полученного раствора вводят в хроматограф «Alliance» фирмы «Waters». . После вхождения раствора в сорбент в колонку вносят подвижную фазу гексан – ацетон (8:2) и осуществляют процесс хроматографирования, поддерживая высоту столба жидкости (элюента) над поверхностью сорбента на уровне 22-24 см. Элюат собирают отдельными фракциями по 2 мл каждая. Фракции 5 и 6 объединяют, элюент испаряют, остаток растворяют в 17,5 мл ацетонитрила, количественно переносят в мерную колбу вместимостью 25 мл и доводят водой до метки. Содержимое колбы перемешивают. 8 мкл полученного раствора вводят в хроматограф «Alliance» фирмы «Waters».
Процесс хроматографирования осуществляют на колонке размерами 150×3,9 мм, заполненной обращеннофазным сорбентом «Nova-Pak С-18», используя подвижную фазу ацетонитрил – вода (7:3) и детектор на основе фотодиодной матрицы. Скорость подачи элюента составляет 1 мл/мин при температуре колонки 20°С. Оптическую плотность регистрируют при длине волны 269 нм.
Пик на хроматограмме с временем удерживания 5,17 мин (объем удерживания 5170 мкл) соответствует н-бутиловому эфиру 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты.
Количественное содержание н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты определяют, исходя из площади хроматографического пика, по уравнению калибровочного графика и пересчитывают на навеску анализируемого вещества, внесенную в ткань печени.
Построение калибровочного графика
В ряд мерных колб вместимостью 50 мл вносят 1,25; 2,5; 5,0; 10,0; 20,0 мл 0,0025% раствора и 1,25; 2,5; 5,0; 10,0; 20,0 мл 0,08% раствора н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты в ацетонитриле, прибавляют 33,75; 32,5; 30,0; 25,0; 15,0 и 33,75; 32,5; 30,0; 25,0; 15,0 мл ацетонитрила соответственно и доводят объем содержимого в каждой колбе до метки водой. 8 мкл каждого из полученных растворов вводят в хроматограф. Хроматографирование осуществляют в колонке размером 150×3,9 мм с сорбентом «Nova-Pak С-18», используя подвижную фазу ацетонитрил – вода (7:3) и детектор на основе фотодиодной матрицы. Скорость подачи элюента составляет 1 мл/мин при температуре колонки 20°С. Оптическую плотность регистрируют при длине волны 269 нм. По результатам измерений на хроматографе строят график зависимости площади пика от концентрации определяемого вещества. График линеен в интервале концентраций 0,005-2,56 мкг. Методом наименьших квадратов рассчитывают уравнение калибровочного графика, которое в данном случае имеет вид:
S=933771·С-358,
где S – площадь хроматографического пика;
С – концентрация определяемого вещества в хроматографируемой пробе, мкг.
Результаты количественного определения н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты представлены в таблице 1.
Пример 2
Определение н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты в ткани семян подсолнечника
К 10 г мелкоизмельченной ткани семян подсолнечника прибавляют 5 мг н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты, тщательно перемешивают биологическую ткань с веществом и оставляют на сутки при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, заливают 20 мл ацетона и выдерживают 45 минут при периодическом перемешивании. Извлечение отделяют, операцию настаивания повторяют в указанных условиях. Отдельные вытяжки объединяют, фильтруют через бумажный фильтр, экстрагент и извлеченную из биологической ткани воду испаряют из фильтрата в токе воздуха. Остаток растворяют в 10 мл смеси растворителей гексан – ацетон (8:2). 2 мл полученного раствора вносят в колонку размером 490×11 мм, заполненную 10 г силикагеля типа L 40/100  . После вхождения раствора в сорбент в колонку вносят подвижную фазу гексан – ацетон (8:2) и осуществляют процесс хроматографирования, поддерживая высоту столба жидкости (элюента) над поверхностью сорбента на уровне 22-24 см. Элюат собирают отдельными фракциями по 2 мл каждая. Фракции 5 и 6 объединяют, элюент испаряют, остаток растворяют в 17,5 мл ацетонитрила, количественно переносят в мерную колбу вместимостью 25 мл и доводят водой до метки. Содержимое колбы перемешивают. 8 мкл полученного раствора вводят в хроматограф «Alliance» фирмы «Waters». . После вхождения раствора в сорбент в колонку вносят подвижную фазу гексан – ацетон (8:2) и осуществляют процесс хроматографирования, поддерживая высоту столба жидкости (элюента) над поверхностью сорбента на уровне 22-24 см. Элюат собирают отдельными фракциями по 2 мл каждая. Фракции 5 и 6 объединяют, элюент испаряют, остаток растворяют в 17,5 мл ацетонитрила, количественно переносят в мерную колбу вместимостью 25 мл и доводят водой до метки. Содержимое колбы перемешивают. 8 мкл полученного раствора вводят в хроматограф «Alliance» фирмы «Waters».
Процесс хроматографирования осуществляют на колонке размерами 150×3,9 мм, заполненной обращеннофазным сорбентом «Nova-Pak С-18», используя подвижную фазу ацетонитрил – вода (7:3) и детектор на основе фотодиодной матрицы. Скорость подачи элюента составляет 1 мл/мин при температуре колонки 20°С. Оптическую плотность регистрируют при длине волны 269 нм.
Пик на хроматограмме с временем удерживания 5,17 мин (объем удерживания 5170 мкл) соответствует н-бутиловому эфиру 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты.
Количественное содержание н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты определяют, исходя из площади хроматографического пика, по уравнению калибровочного графика и пересчитывают на навеску анализируемого вещества, внесенную в ткань семян подсолнечника.
Построение калибровочного графика и его уравнение приводятся в примере 1.
Результаты количественного определения н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты в семенах подсолнечника представлены в таблице 2.
Предлагаемыми способ по сравнению с прототипом в 200 раз повышает чувствительность определения в хроматографируемой пробе и более чем в 100 раз – в биологическом материале.
Сравнительные характеристики предлагаемого и известного способов представлены в таблице 3.
| Таблица 1 |
| Результаты определения н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты в ткани печени (n=5; р=0,95) |
| N |
Внесено н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты, мг в 10 г печени |
Найдено |
Метрологические характеристики |
| мг |
% |
| 1. |
5,00 |
4,759 |
95,18 |
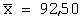 |
| 2. |
5,00 |
4,606 |
92,12 |
S=2,10 |
| 3. |
5,00 |
4,494 |
89,87 |
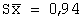 |
| 4. |
5,00 |
4,698 |
93,96 |
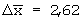 |
| 5. |
5,00 |
4,568 |
91,35 |
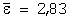 |
Таблица 2
Результаты определения н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты в ткани семян подсолнечника (n=5; p=0,95) |
| N |
Внесено н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты, мг в 10 г ткани семян подсолнечника |
Найдено |
Метрологические характеристики |
| мг |
% |
| 1. |
5,00 |
4,618 |
92,36 |
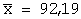 |
| 2. |
5,00 |
4,691 |
93,81 |
S=1,22 |
| 3. |
5,00 |
4,531 |
90,62 |
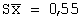 |
| 4. |
5,00 |
4,572 |
91,43 |
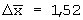 |
| 5. |
5,00 |
4,637 |
92,74 |
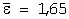 |
| Таблица 3 |
| Сравнительная характеристика предлагаемого и известного способов (на примере исследования тканей семян подсолнечника) |
| Показатели |
Предлагаемый способ |
Известный способ |
| Чувствительность (открываемый минимум) |
|
|
| а) в 100 г биоматериала; |
0,5 мкг |
50-80 мкг |
| б) в хроматографируемой пробе |
0,005 мкг |
1 мкг |
Формула изобретения
Способ определения н-бутилового эфира 2-[4-(5-трифторметилпиридил-2-окси)фенокси]пропионовой кислоты в биологическом материале, заключающийся в том, что анализируемую пробу измельчают, настаивают с ацетоном, ацетоновое извлечение фильтруют, концентрируют, подвергают хроматографической очистке при использовании нормальнофазного сорбента и подвижной фазы гексан – ацетон (8:2) с последующим определением анализируемого вещества, отличающийся тем, что хроматографическую очистку проводят в колонке с силикагелем L 40/100  , а определение осуществляют методом ВЭЖХ в колонке, заполненной обращеннофазным сорбентом “Nova-Pak С-18” с применением подвижной фазы ацетонитрил – вода (7:3) и детектора на основе фотодиодной матрицы. , а определение осуществляют методом ВЭЖХ в колонке, заполненной обращеннофазным сорбентом “Nova-Pak С-18” с применением подвижной фазы ацетонитрил – вода (7:3) и детектора на основе фотодиодной матрицы.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 29.06.2007
Извещение опубликовано: 20.02.2009 БИ: 05/2009
|
|