Патент на изобретение №2287515
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ АЛЬФА,ОМЕГА-ХЛОРАЛКАНОЛОВ (ХЛОРГИДРИНОВ)
(57) Реферат:
Изобретение относится к способу получения
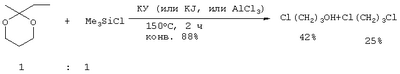
Предлагаемое изобретение относится к области органической химии, в частности к способу получения хлоралканолов (хлоргидринов). Хлоргидрины применяют для получения моноэфиров диолов, используемых в качестве растворителей в лакокрасочной промышленности, а также в производстве полиоксиамидов (лак Ниплон-2), предназначенных для пропитки стеклоуглетканей с целью придания им теплозащитных свойств. Хлоргидрины используют в качестве промежуточных веществ при производстве красителей, галогензамещенных полимеров, фармацевтических препаратов, катализаторов полимеризации, пластификаторов. Одним из методов получения Восстановление ClCH2CH2COOEt действием LiBH4 в присутствии (МеО3)B (эфир, кипячение, 1 ч) с последующим гидролизом раствором NaOH приводит к 3-хлорпропанолу с выходом 84% (Brown H.C., Narasimhan S., J. Org. Chem., Vol.49, №21, 3891-3898 (1984) [2]). Метод имеет ряд недостатков: 1. Труднодоступность и дороговизна восстановителей (LiAlH4, LiBH4). 2. Многостадийный синтез исходных эфиров. 3. Сложности в процессе выделения хлоргидринов из-за образования побочных продуктов и значительного количества отходов. Смесь Недостатки метода: 1. Труднодоступность 2. Образование смеси продуктов, неселективность процесса. 3. Сложности при выделении целевого продукта. Взаимодействие диоксациклоалканов с эквимолярным количеством Me3SiCl в присутствии апротонных катализаторов протекает с разрывом С-O-связи цикла и образованием неустойчивых Недостатками метода является неселективность процесса и низкий выход целевого продукта. 4-Хлорбутанол получают взаимодействием тетрагидрофурана с HCl (газ) в присутствии катализатора. В качестве катализаторов используют смолу, содержащую заместители – галогенид тетраалкиламмония формулы S]-NR3Х (R=алкил C1-С10, Х=Cl, Br, J) или аминогруппу формулы NR2 (например, сополимер стирола с дивинилбензолом, содержащий S]-NMe3Cl-и NMe2-группы). Реакцию ведут при температуре 20-87°, используя катализатор (например, “Amberlyst-26”, “Amberlyst-21”) в количестве 9-30 ч на 100 ч ТГФ. В качестве катализатора используют смолу (обычно в форме гранул), которая не разлагается в процессе реакции и не растворяется в конечном продукте реакции (Hammond K.G. Synthesis of 4-haloalkyl alcohols. Пат.4334109, США (1982) [5]). Недостатки метода: 1. Использование газообразного HCl в большом количестве. 2. Большой расход катализатора (10%). 3. Умеренный выход целевого продукта. Нагреванием смеси 1 моля тетрагидрофурана, 1 моля SiCl4 и 1 г ZnCl2 до кипения в течение 5 часов получены Cl(СН2)4Cl, выход 15%, и [СН2Cl(СН2)3О]2-SiCl2, при гидролизе которого в эфирном растворе водным раствором Na2СО3 образуется кремневая кислота и 1-хлорбутанол-4 СН2Cl(СН2)3ОН. В отсутствие катализатора реакция не проходит (Шуйкин Н.И., Бельский И.Ф. Докл. АН СССР, т.113, №2, 366-667 (1957) [6]). Недостатки метода: 1. Использование дорогостоящего хлорирующего агента (SiCl4) в эквимольном количестве. 2. Образование побочных продуктов (Н2SiO3). 3. Образуется значительное количество неорганических отходов и сточных вод, которые необходимо утилизировать, что требует больших затрат (трудо- и энергозатраты).
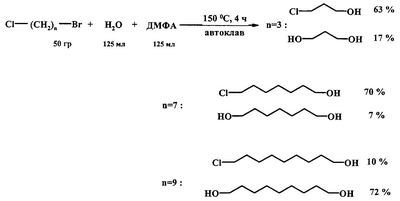
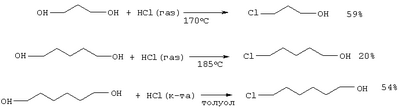
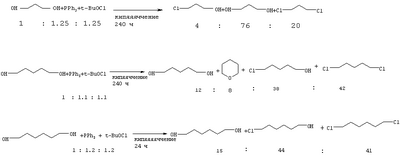
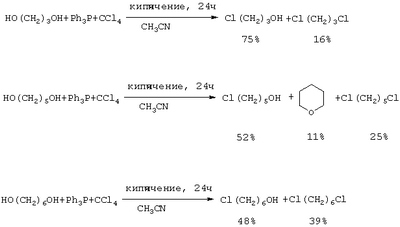
Аналогичная реакция 1,5-пентандиола с HCl (185°С) приводит 1-хлорпентанолу-5 с выходом 20%, а при взаимодействии HCl (кислоты) с 1,6-гександиолом в присутствии толуола образуется 1-хлоргексанол-6 с выходом 54% (Vejdeiek Z.J., Trcka V., Vysatova V. Chem. listy, Vol.48, №5, 685-691 (1954) [7]). Для получения 1-хлор-12-оксидодекана 1,12-додекандиол нагревают с раствором концентрированной HCl до 95-100°С в растворе бензола и получают целевой продукт с выходом 63% (Захаркин Л.И., Гусева В.В. Способ получения Нагревание 1,10-декандиола с концентрированной HCl в присутствии воды сокращает время реакции до 12 часов, а выход соответствующего хлоралканола составляет 72% (Anand N., Wadia P.S., Dhar M.L., J. Scient and Jndustr. Res., Vol.13, №4, Sec. В., 260-269 (1954) [9]). Недостатки указанных методов: 1. Агрессивная кислая среда. 2. После нейтрализации реакционной массы образуется большое количество неорганических отходов и сточных вод, которые необходимо утилизировать. 3. Значительная продолжительность процессов и связанные с этим энерго- и трудозатраты. 4. Невысокий выход целевых продуктов. Различные диолы взаимодействуют с реагентом Ph3Р-трет-BuOCl с образованием, в зависимости от строения, циклических эфиров, региоизомерных хлоргидринов и дихлоридов. К смеси 5 ммолей 1,3-пропиленгликоля, 6.25 ммоля Ph3Р в 10 мл хлороформа, охлажденному до -70°С, по каплям прибавляют 6.25 ммоля трет-BuOCl, дают нагреться до 20°С, кипятят 24 ч и получают смесь, состоящую из трех продуктов: исходного диола, хлоргидрина и 1,3-дихлорпропана (Barry С.N., Evans Jr S. A. J. Org. Chem, Vol.48, №17, 2825-2828 (1983) [10]) Недостатки метода: 1. Большой расход дорогостоящего и токсичного катализатора (стехиометрические количества PPh3). 2. Образование сложной смеси продуктов реакции. 3. Низкая селективность процесса. 4. Труднодоступность хлорирующего агента (трет-BuOCl). 5. Сложность обеспечения низкотемпературных (-70°С) условий проведения реакции. Реагент трифенилфосфин – этиловый эфир трихлоруксусной кислоты эффективен для последовательного замещения гидроксильных групп галогеном в Недостатки метода: 1. Большой расход катализатора (PPh3). 2. Низкий выход целевого продукта (7-17%). 3. Образование большого количества побочных продуктов. В работе (Barry С.N., Evans Jr S.A. J. Org. Chem., Vol.46, №16, 3361-3364 (1981) [12]) для замещения НО-группы в диолах предложен реагент PPh3 – CCl4. Реакция проходит при длительном кипячении в ацетонитриле (24 ч), а продуктами ее являются хлоргидрины и дихлориды. На основании сходства по четырем признакам (исходный реагент – диол, присутствие галоидметана (CCl4), использование катализатора (PPh3), образование в результате реакции хлоргидрина) за прототип взят метод хлорирования диолов с помощью системы PPh3 – CCl4 [12]. Прототип имеет следующие недостатки: 1. Длительность процесса (24 ч). 2. Использование стехиометрического количества дорогостоящего и токсичного катализатора (PPh3). 3. Низкая селективность (образование дихлоридов). 4. Умеренный выход целевого продукта. 5. Невозможность повторного использования катализатора из-за его окисления в трифенилфофиноксид (Ph3Р=О). Авторами предлагается способ получения хлоргидринов, не имеющий указанных недостатков. Сущность способа заключается в хлорировании диолов с помощью CCl4 под действием молибденсодержащего катализатора Мо(СО)6 при 120-140°С в течение 3-8 часов, при мольном соотношении [Мо]: [диол]:[CCl4]=1:200:1000. В оптимальных условиях при конверсии диола 96-99% единственным продуктом реакции является хлоргидрин. Существенные отличия предлагаемого способа от прототипа. 1. Для получения хлоргидринов в хлорировании диолов используется система Мо(СО)6 – CCl4. Преимущества предлагаемого метода 1. Низкий расход катализатора. 2. Уменьшении продолжительности реакции (3-8 часов). 3. Отсутствие агрессивных хлорирующих агентов. 4. Удешевление себестоимости и упрощение технологии в целом за счет уменьшения энерго- и трудозатрат и из-за отсутствия стадии ректификационной очистки продукта и утилизации отходов. 5. Селективность процесса. Предлагаемый способ поясняется примерами. Пример I. В микроавтоклав (ампулу) под аргоном помещали 0.1 ммоль Мо(СО)6, 20 ммоль 1.3-пропандиола и 100 ммоль CCl4 (который играет роль реагента и растворителя одновременно), автоклав герметично закрывали (ампулу запаивали) и нагревали при 120°С в течении 8 часов. После окончания реакции микроавтоклав (ампулу) охлаждали до 20°С, вскрывали, реакционную массу фильтровали через слой силикагеля (2 г), CCl4 отгоняли, остаток перегоняли при атмосферном давлении или в вакууме. Пример II. В микроавтоклав (ампулу) под аргоном помещали 0.1 ммоль Мо(СО)6, 20 ммоль 1.10-декандиола и 100 ммоль CCl4, автоклав герметично закрывали (ампулу запаивали) и нагревали при 140°С в течении 3 часов. После соответствующей обработки (как в примере I) был выделен 10-хлордекан с выходом 62%. Другие примеры, подтверждающие способ, приведены в таблице 1. Выделенные хлоргидрины имели следующие константы. 3-Хлорпропанол. Выход 96%, т.кип.82°С (80 мм рт.ст.). Спектр ЯМР 13С, 4-Хлорбутанол. Выход 98%, т.кип.73-74°С (7 мм рт.ст.). Спектр ЯМР 13С, 5-Хлорпентанол. Выход 95%, т.кип.57-58°С (1 мм рт.ст.). Спектр ЯМР 13С, 6-Хлоргексанол. Выход 98%, т.кип.97 13С (10 мм рт.ст.). Спектр ЯМР 1Н, 7-Хлоргептанол. Выход 87%, т.кип.80°С (15 мм рт.ст.). Спектр ЯМР 1Н, 5, м.д.: 1.15-2.0 м (10Н, 5СН2), 3.25-3.75 м (4Н, СН2Cl, СН2OH). Спектр ЯМР 13С, 9-Хлорнонанол. Выход 74%, т.кип.142-143°С (20 мм рт.ст.). Спектр ЯМР 1Н, 10-Хлордеканол. Выход 62%, т.кип.144-145°C (2 мм рт.ст.). Спектр ЯМР 13С, 12-Хлордодеканол. Выделен колоночной хроматографией (элюент-эфиртексан=1:2). Выход 48%. Спектр ЯМР 1Н,
Формула изобретения
Способ получения
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 16.08.2007
Извещение опубликовано: 10.03.2009 БИ: 07/2009
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 ,
, -хлоралканолов (хлоргидринов), которые применяют для получения моноэфиров диолов, используемых в качестве растворителей в лакокрасочной промышленности, в производстве полиоксиамидов (лак Ниплон-2), предназначенных для пропитки стеклоуглетканей с целью придания им теплозащитных свойств, а также в качестве промежуточных веществ при производстве красителей, галогензамещенных полимеров, фармацевтических препаратов, катализаторов полимеризации, пластификаторов. Способ включает каталитическое хлорирование диолов с помощью четыреххлористого углерода при повышенной температуре. При этом процесс ведут в присутствии 0,1 ммоля молибденсодержащего катализатора Мо(СО)6 при температуре 120-140°С, в течение 3-8 часов, при мольном соотношении [Мо(СО)6]:[диол]:[CCl4]=1:200:1000. Способ позволяет снизить расход катализатора, уменьшить продолжительность реакции, проводить процесс селективно, а также снизить себестоимость и упростить технологию. 1 табл.
-хлоралканолов (хлоргидринов), которые применяют для получения моноэфиров диолов, используемых в качестве растворителей в лакокрасочной промышленности, в производстве полиоксиамидов (лак Ниплон-2), предназначенных для пропитки стеклоуглетканей с целью придания им теплозащитных свойств, а также в качестве промежуточных веществ при производстве красителей, галогензамещенных полимеров, фармацевтических препаратов, катализаторов полимеризации, пластификаторов. Способ включает каталитическое хлорирование диолов с помощью четыреххлористого углерода при повышенной температуре. При этом процесс ведут в присутствии 0,1 ммоля молибденсодержащего катализатора Мо(СО)6 при температуре 120-140°С, в течение 3-8 часов, при мольном соотношении [Мо(СО)6]:[диол]:[CCl4]=1:200:1000. Способ позволяет снизить расход катализатора, уменьшить продолжительность реакции, проводить процесс селективно, а также снизить себестоимость и упростить технологию. 1 табл.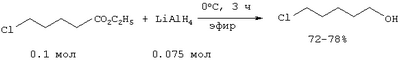
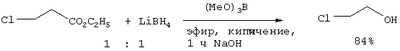

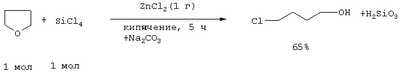
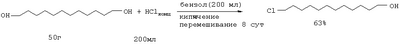
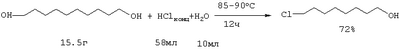
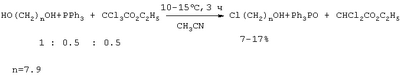
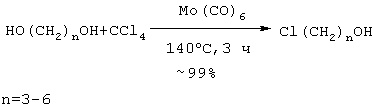
 , м. д., ТМС: 59.49 (С1), 34.89 (С2), 43.30 (С3). Масс-спектр, m/z (Iотн (%)): [М]+отсут., 76(11), 58(72), 57(48), 41(16), 39(8), 31(100), 30(36), 29(55) (лит.: т.кип.67°С (19 мм рт.ст.) Edward J. D., GerrardW., Lappert M. F. J. Chem. Soc., №1, 348-356 (1957) [13]).
, м. д., ТМС: 59.49 (С1), 34.89 (С2), 43.30 (С3). Масс-спектр, m/z (Iотн (%)): [М]+отсут., 76(11), 58(72), 57(48), 41(16), 39(8), 31(100), 30(36), 29(55) (лит.: т.кип.67°С (19 мм рт.ст.) Edward J. D., GerrardW., Lappert M. F. J. Chem. Soc., №1, 348-356 (1957) [13]).