|
|
(21), (22) Заявка: 2005130191/15, 27.09.2005
(24) Дата начала отсчета срока действия патента:
27.09.2005
(46) Опубликовано: 20.11.2006
(56) Список документов, цитированных в отчете о
поиске:
SU 1599302 A1, 15.10.1990. SU 1214584 A, 28.02.1986. SU 1237629 A1, 15.06.1986. SU 1627508 A1, 15.02.1991. EP 0535514 A, 07.04.1993. GB 1179120 A, 28.01.1970.
Адрес для переписки:
445652, Самарская обл., г. Тольятти, ул. Новозаводская, 6, ОАО “КуйбышевАзот”, патентный отдел
|
(72) Автор(ы):
Герасименко Виктор Иванович (RU),
Огарков Анатолий Аркадьевич (RU),
Ардамаков Сергей Витальевич (RU),
Лукьянов Игорь Валентинович (RU),
Артемов Арсений Валерьевич (RU)
(73) Патентообладатель(и):
Открытое акционерное общество “КуйбышевАзот” (ОАО “КуйбышевАзот”) (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ ГИДРОКСИЛАМИНСУЛЬФАТА
(57) Реферат:
Изобретение относится к способу получения гидроксиламинсульфата, применяемого в синтезе капролактама. Способ заключается в получении гидроксиламинсульфата (ГАС) при избыточном давлении путем смешения в реакционном объеме синтез-газа, состоящего из оксида азота (II) и водорода, смеси серной кислоты и воды и катализатора “платина на электрографите”, т.е. платина, нанесенная на электродный графит. Процесс проводят в присутствии 2-30%-ного водного раствора комплексообразователя состава: Гидроксиэтилиден-1,1-дифосфоновая кислота (I) формулы СН3-С(ОН)=[Р(O)(ОН)2]2,
Циклический Р-комплекс (II) общей формулы
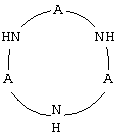
где А есть = Р(O)СН3ОН, при мольном отношении I:II, равном 1:1, при массовом отношении водного раствора комплексообразователя и железа, содержащегося в реакционной системе, равном 100-500 ppm на 1 ppm Fe. Способ позволяет более чем в 3 раза снизить содержание NO в отходящих газах и увеличить выход основного продукта реакции – ГАС, а также возрастает межрегенерационный период работы катализатора. 2 табл.
Настоящее изобретение относится к химической промышленности, а именно – к способу получения гидроксиламинсульфата (ГАС), используемого в качестве основного реагента в производстве капролактама.
Известен способ получения ГАС, включающий приготовление реакционной смеси аммиака, кислорода и водяного пара, каталитическое парофазное окисление аммиака, смешение полученного нитрозного газа с водородом, стабилизацию нитрозного газа гидрированием избыточного кислорода в присутствии Ag-Mn катализатора, его двухстадийное концентрирование конденсацией водяных паров, смешение концентрированного монооксида азота с водородом и синтез ГАС в среде разбавленной серной кислоты. Конденсат второй стадии концентрирования нитрозного газа гидрируют водородом в присутствии платинового катализатора в жидкой фазе. Образующийся при этом чистый оксид азота (II) используют для синтеза ГАС, а продукт гидрирования с массовой долей азотной кислоты до 0,45 мас.% вместе с конденсатом первой ступени используют для разбавления концентрированной серной кислоты, обеспечивая тем самым безотходность технологии [заявка ВВП №0945401, МПК6 С 07 В 21/14, 1999 г.]. Преимуществом данного способа является получение концентрированного оксида азота (II) и утилизация отходов производства в виде разбавленных растворов азотной кислоты. Однако недостатком данного способа является то, что при стабилизации состава нитрозного газа гидрированием избыточного кислорода на Ag-Mn катализаторе безвозвратно теряется оксид азота (II), и образуются азот и оксид азота (I), которые снижают эффективность работы стадии синтеза ГАС.
Известен также способ получения ГАС, включающий приготовление реакционной смеси аммиака, кислорода и водяного пара, каталитическое парокислородное окисление аммиака, смешение полученного нитрозного газа с водородом, стабилизацию нитрозного газа путем гидрирования на Ag-Mn катализаторе избыточного кислорода на 70-75%, его двухстадийное концентрирование конденсацией паров воды, смешение концентрированного оксида азота (II) с водородом и синтез ГАС в среде разбавленной серной кислоты. В данном способе получения ГАС на стадии стабилизации нитрозного газа избыточный кислород гидрируют на 70-75% вместо обычных 90%. В результате этого на второй стадии концентрирования нитрозного газа образуется конденсат, содержащий в 1,5-2,5 раза больше азотной кислоты по сравнению с предыдущим способом. При его жидкофазном гидрировании образуется больше чистого оксида азота (II). Кроме того, при гидрировании избыточного кислорода на 70-75% в процессе стабилизации нитрозного газа оксид азота (II) практически не теряется и не образуются дополнительно инертные примеси, а объемная доля оксида азота (II) в концентрированном нитрозном газе на 2,3-2,5% больше, чем в предыдущем способе [Патент Украины №50681 А, МПК7 С 01 В 21/14, 2002 г.].
Общим недостатком обоих вышеописанных способов является сложность схемы в целом, предусматривающей как стадию стабилизации состава нитрозного газа гидрированием части избыточного кислорода, так и стадии жидкофазного гидрирования конденсата второй ступени концентрирования нитрозного газа. Кроме того, схема отличается жесткой взаимосвязью между стадиями окисления аммиака и синтеза ГАС, обусловленной необходимостью сжатия оксида азота (II), что усложняет управление процессом.
Наиболее близким решением поставленной технической задачи является способ получения ГАС по патенту Украины №14329, МПК7 C 01 В 21/14, в соответствии с которым процесс проводят при избыточном давлении путем смешения в реакционной зоне нитрозного газа, водорода, смеси серной кислоты и воды и катализатора “платина на электрографите”. Водный раствор серной кислоты вводят одним потоком в среднюю часть реакционной зоны. Перемешивание в реакционной зоне осуществляют расположенной в центральной зоне мешалкой без дополнительной турбулизации смеси в центральной части реакционной зоны. Процесс проводят в нескольких реакционных зонах (каскаде из 5-6 реакторов смешения). Контроль за ходом процесса обычно осуществляют по остаточному содержанию NO в хвостовых газах. Увеличение остаточного содержания NO в хвостовых газах свидетельствует о частичной дезактивации катализатора за счет отравления его активных центров примесями, присутствующими в реакционной системе, прежде всего соединениями железа. Частично дезактивированный катализатор выводят из системы и регенерируют с использованием известных приемов. В среднем рабочий “пробег” катализатора до стадии его регенерации составляет 14-21 суток (2-3 недели).
Недостатком прототипа является малый межрегенерационный период работы катализатора.
Известно, что важную роль в процессе получения ГАС играет содержание катализатора в реакторах, его активность и селективность. Поддержание массовой концентрации катализатора в пределах 30-50 г/дм3, а также необходимой его активности и селективности, обеспечивает высокую скорость реакции и стабильность ведения процесса. Для поддержания на необходимом уровне активности и селективности катализатора необходимо точное соблюдение оптимального соотношения водород оксид азота (II) в синтез-газе, регулирование степени отравления катализатора при регенерации в сочетании с периодичностью его частичной замены в реакторах. При регенерации катализатора платину частично отравляют для снижения скоростей протекания побочных реакций, прежде всего образования аммиака и сульфата аммония. Регенерированный катализатор обеспечивает селективность по целевому процессу на уровне 90-95%. Селективность процесса постепенно снижается за счет накопления в реакционной зоне соединений железа и соединений других элементов семейства железа. Эти соединения, с одной стороны, необратимо отравляют активные центры катализатора, а с другой стороны, катализируют распад целевого продукта реакции – гидроксиламина. Поэтому поиск путей вывода каталитических ядов – соединений железа и элементов его семейства представляет актуальную техническую задачу, решение которой позволит интенсифицировать процесс и увеличить межрегенерационный период работы катализатора.
Целью настоящего изобретения является интенсификация процесса и увеличение межрегенерационного периода работы катализатора.
Согласно изобретению поставленная цель достигается способом получения ГАС при избыточном давлении путем смешения в реакционном объеме синтез-газа, состоящего из оксида азота (II) и водорода, смеси серной кислоты и воды и катализатора, представляющего собой платину на электродном графите («платина на электрографите»), с последующей регенерацией катализатора. Процесс проводят в присутствии 2-30%-ного водного раствора комплексообразователя состава:
Гидроксиэтилиден-1,1-дифосфоновая кислота (I) формулы
СН3-С(ОН)=[Р(O)(ОН)2]2,
Циклический Р-комплекс (II) общей формулы
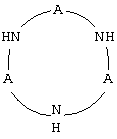
где А есть = Р(O)СН3ОН, при мольном отношении I:II, равном 1:1, при массовом отношении водного раствора комплексообразователя и железа, содержащегося в реакционной системе, равном 100-500 ppm на 1 ppm Fe.
Проведение реакции привело к существенной интенсификации процесса и значительному увеличению межрегенерационного периода работы катализатора.
Существенными отличительными признаками данного способа является проведение процесса в присутствии комплексообразователя состава:
Гидроксиэтилиден-1,1-дифосфоновая кислота (I) формулы CH3-С(ОН)=[P(O)(ОН)2]2,
Циклический Р-комплекс (II) общей формулы

где А есть = P(O)CH3ОН, при мольном отношении I:II, равном 1:1. Используют 2-30%-ный водный раствор смеси I и II. Количество водного раствора комплексообразователя составляет 100-500 ppm на 1 ppm Fe, содержащегося в реакционной системе.
Использование этого комплексообразователя приводит к значительному снижению содержания железа и других элементов его семейства в образцах катализатора. Этот факт был подтвержден специальным анализом катализатора с применением метода масс-спектрометрии с ионизацией в индуктивно связанной плазме. Анализировали 4 образца катализатора “платина на электрографите”:
Образец 1: до регенерации, каскад А.
Образец 2: после регенерации по стандартной методике, каскад А.
Образец 3: образец 1, отмытый в течение 24 часов заявляемым комплексообразователем.
Образец 4: образец 2, отмытый в течение 24 часов заявляемым комплексообразователем.
Анализ содержания элементов в образцах катализатора проводили с использованием метода масс-спектрометрии для элементного и изотопного анализа с ионизацией в индуктивно связанной плазме (ИСПМС) на приборе “VG PLASMA QUAD PQ 2-TURBO”. Метод ИСПМС является эффективным аналитическим методом и позволяет определять концентрации элементов и изотопов, содержащихся в растворе, на уровне 10-9 г/мл. ИСПМС соединяет в себе достоинства высокочастотной индуктивно связанной плазмы, как источника ионов, и квадрупольного масс-анализатора, производящего разделение по массам и детектирование ионов. Образцы в виде мелкодисперсного аэрозоля вводятся в центральный канал плазменного факела. В плазме происходит их эффективное испарение, атомизация и ионизация. Степень ионизации элементов, имеющих потенциал ионизации ниже 10 эВ (а они составляют большинство в периодической таблице), приближается к 100%. Образующиеся ионы экстрагируются из плазмы через отверстие пробоотборника и, увлекаемые газодинамическим потоком, попадают в вакуумную камеру, где, после фокусировки ионно-оптической системой и разделения по массам квадрупольным масс-анализатором, детектируются вторично-электронным умножителем (ВЭУ). Импульсы ВЭУ после усиления поступают на вход многоканального анализатора (МКА) и накапливаются в течение анализа. Полученный массив данных обрабатывается микрокомпьютером.
Пробоподготовка: образцы катализатора обрабатывали избытком смеси азотной и соляной кислот (обе – категории ОСЧ) в мольном соотношении 2:1. Растворение проводили с помощью системы микроволнового разложения MSD-2000.
Элементный анализ полученных растворов проводили на вышеуказанном приборе при следующих условиях: мощность разряда 1,3 кВт, расход транспортирующего газа (аргона) – 0,89 л/мин, расход плазмообразующего газа 12 л/мин. В качестве внутреннего стандарта в растворы вводили индий в концентрации 25 мкг/л. Калибровку прибора проводили по стандартным растворам с известным содержанием определяемых элементов.
Результаты анализа приведены в таблице 1.
Таблица 1.
Результаты анализа образцов катализатора “платина на электрографите” методом ИСПМС. Содержание элементов – в ppm. Среднее из трех параллельных испытаний. |
| Элемент |
|
Образец 1 |
Образец 2 |
Образец 3 |
Образец 4 |
| |
|
|
|
|
|
| Литий |
Li |
0,014 |
0,009 |
0,012 |
0,006 |
| Бериллий |
Be |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Бор |
В |
5,683 |
5,127 |
4,218 |
3,926 |
| Натрий |
Na |
1456,328 |
20894,153 |
284,256 |
883,354 |
| Магний |
Mg |
63,329 |
126,352 |
8,237 |
12,345 |
| Алюминий |
Al |
742,647 |
624,357 |
71,256 |
120,344 |
| Кремний |
Si |
3892,341 |
2748,356 |
3578,827 |
2675,988 |
| Фосфор |
P |
189,576 |
76,2567 |
175,345 |
64,873 |
| Сера |
S |
2351,348 |
1876,228 |
2281,547 |
1027,113 |
| Калий |
К |
926,453 |
1197,834 |
87,546 |
64,278 |
| Кальций |
Ca |
482,396 |
512,783 |
36,925 |
44,367 |
| Скандий |
Sc |
1,524 |
0,984 |
0,882 |
0,723 |
| Титан |
Ti |
510,638 |
678,254 |
487,356 |
512,662 |
| Ванадий |
V |
5,682 |
4,273 |
4,883 |
3,994 |
| Хром |
Cr |
988,574 |
158,274 |
116,356 |
25,288 |
| Железо |
Fe |
1356,278 |
472,825 |
28,573 |
126,627 |
| Марганец |
Mn |
88,924 |
76,372 |
76,952 |
62,338 |
| Кобальт |
Co |
4,894 |
3,925 |
1,338 |
1,003 |
| Никель |
Ni |
54,286 |
36,884 |
17,892 |
9,338 |
| Медь |
Cu |
44,826 |
26,338 |
4,982 |
6,984 |
| Цинк |
Zn |
157,826 |
67,337 |
123,963 |
45,828 |
| Галлий |
Ga |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Германий |
Ge |
26,834 |
17,928 |
23,874 |
10,836 |
| Мышьяк |
As |
12,964 |
8,346 |
11,528 |
6,995 |
| Селен |
Se |
10,852 |
14,356 |
9,286 |
10,452 |
| Рубидий |
Rb |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Стронций |
Sr |
8,551 |
6,925 |
1,117 |
0,873 |
| Иттрий |
Y |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Цирконий |
Zr |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Ниобий |
Nb |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Молибден |
Mo |
5,016 |
3,827 |
1,012 |
2,336 |
| Рутений |
Ru |
8,972 |
11,073 |
2,956 |
5,075 |
| Родий |
Rh |
1,892 |
0,752 |
0,057 |
0,078 |
| Палладий |
Pd |
3,962 |
2,875 |
1,746 |
2,057 |
| Серебро |
Ag |
0,783 |
0,936 |
0,035 |
0,064 |
| Кадмий |
Cd |
5,893 |
8,372 |
2,842 |
3,833 |
| Индий |
In |
0,083 |
0,095 |
0,056 |
0,073 |
| Олово |
Sn |
11,056 |
9,542 |
7,378 |
8,956 |
| Сурьма |
Sb |
0,893 |
0,245 |
0,753 |
0,185 |
| Теллур |
Те |
0,087 |
0,056 |
0,036 |
0,025 |
| Йод |
I |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Цезий |
Cs |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Барий |
Ba |
0,084 |
0,106 |
0,048 |
0,068 |
| Лантан |
La |
0,056 |
0,073 |
0,048 |
0,064 |
| Церий |
Се |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Празеодим |
Pr |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Неодим |
Nd |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Самарий |
Sm |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Европий |
Eu |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Гадолиний |
Gd |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Тербий |
Tb |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Диспрозий |
Dy |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Гольмий |
Ho |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Эрбий |
Er |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Тулий |
Tm |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Иттербий |
Yb |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Лютеций |
Lu |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Гафний |
Hf |
0,064 |
0,085 |
0,052 |
0,034 |
| Тантал |
Та |
0,026 |
0,067 |
0,052 |
0,047 |
| Вольфрам |
W |
0,126 |
0,097 |
0,107 |
0,047 |
| Рений |
Re |
2,894 |
3,092 |
1,653 |
2,596 |
| Ирридий |
Ir |
6,173 |
4,927 |
3,075 |
2,093 |
| Осмий |
Os |
12,752 |
16,357 |
9,927 |
8,356 |
| Платина |
Pt |
4567,826 |
4792,357 |
4628,337 |
4692,883 |
| Золото |
Au |
0,378 |
0,267 |
0,263 |
0,217 |
| Ртуть |
Hg |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Таллий |
Tl |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Свинец |
Pb |
23,479 |
14,963 |
18,903 |
8,628 |
| Висмут |
Bi |
0,937 |
0,862 |
0,052 |
0,027 |
| Торий |
Th |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
| Уран |
U |
<0,001 |
<0,001 |
<0,001 |
<0,001 |
Результаты анализа свидетельствуют об эффективном связывании заявляемым комплексообразователем соединений железа и элементов его семейства. Ниже приведены примеры осуществления процесса по прототипу и по заявляемому способу.
Пример 1. Процесс проводят в условиях прототипа. Смесь оксида азота (II) и водорода (т.н. синтез-газ) через распределительное устройство подают в каждый из реакторов каскада. Синтез ГАС проводят при интенсивном перемешивании жалюзийной мешалкой в среде разбавленной серной кислоты, которую вводят в среднюю часть реакционной зоны. Процесс синтеза ГАС ведут при избыточном давлении 0,3-0,35 МПа. Верхняя зона реактора снабжена жалюзийным пеногасителем для ликвидации образования ПГС. Отходящие (хвостовые) газы стадии синтеза ГАС направляют на сжигание. Продукты синтеза направляют в продуктовую секцию. Результаты ведения процесса приведены в табл.1.
Примеры 2-6. Процесс проводят в условиях заявляемого способа. Смесь оксида азота (II) и водорода (т.н. синтез-газ) через распределительное устройство подают в каждый из реакторов каскада. Синтез ГАС проводят при интенсивном перемешивании жалюзийной мешалкой в среде разбавленной серной кислоты, которую вводят в среднюю часть реакционной зоны. Процесс синтеза ГАС ведут при избыточном давлении 0,3-0,35 МПа. Верхняя зона реактора снабжена жалюзийным пеногасителем для ликвидации образования ПГС. Отходящие (хвостовые) газы стадии синтеза ГАС направляют на сжигание. Продукты синтеза направляют в продуктовую секцию.
Процесс синтеза ГАС проводят в присутствии комплексообразователя состава:
Гидроксиэтилиден-1,1-дифосфоновая кислота (I) формулы CH3-С(ОН)=[P(O)(ОН)2]2,
Циклический Р-комплекс (II) общей формулы

где А есть = P(O)СН3ОН, при мольном отношении I:II, равном 1:1.
Используют 2-30%-ный водный раствор смеси I и II. Количество водного раствора комплексообразователя составляет 100-500 ppm на 1 ppm Fe, содержащегося в реакционной системе.
Результаты ведения процесса приведены в табл.2.
Как видно из приведенных в табл.2 данных, организация процесса по заявленному способу позволяет более чем в 3 раза снизить содержание NO в отходящих газах, что свидетельствует о более глубоком протекании процесса синтеза ГАС по сравнению с прототипом. По сравнению с прототипом также увеличивается выход основного продукта реакции – ГАС. Значительно возрастает межрегенерационный период работы катализатора. Эти положительные результаты связаны с эффективным связыванием комплексообразователя каталитических ядов, прежде всего соединений железа и соединений других элементов его семейства. Кроме того, поскольку эти же соединения являются катализаторами распада целевого продукта – гидроксиламина, использование комплексообразователя приводит к увеличению выхода целевого продукта.
Таблица 2.
Результаты проведения синтеза ГАС |
| № п/п |
Способ |
Использование добавок комплекса |
Конц. водного раствора комплекса мас.% |
Массовое отношение раствор комплекса: Fe |
Давление МПа |
NO в синтез-газе, кг/час |
Отходящие газы стадии синтеза ГАС, нм3/ч |
Продукты синтеза, кг/ч |
| NO |
Н2 |
N2 |
N2O |
Сумма |
ГАС |
Сульфат аммония |
N2O |
| 1 |
Прототип |
– |
– |
– |
0,3-0,35 |
1249,7 |
14,6 |
121,6 |
27,5 |
10,8 |
174,5 |
3184,2 |
114,9 |
9,4 |
| 2 |
Заявлен.*) |
+ |
2,0 |
500 |
0,38 |
1279,6 |
8,4 |
112,8 |
21,8 |
8,4 |
151,4 |
3282,7 |
108,5 |
6,9 |
| 3 |
Заявлен.*) |
+ |
12,0 |
450 |
0,4 |
1284,9 |
7,3 |
114,2 |
22,4 |
9,2 |
153,1 |
3245,8 |
104,7 |
8,4 |
| 4 |
Заявлен.*) |
+ |
20,0 |
300 |
0,35-0,38 |
1296,5 |
6,1 |
112,6 |
23,0 |
9,7 |
151,4 |
3267,7 |
106,3 |
9,0 |
| 5 |
Заявлен.*) |
+ |
25,0 |
250 |
0,56 |
1284,2 |
5,2 |
108,5 |
24,2 |
10,0 |
147,9 |
3234,6 |
105,4 |
8,2 |
| 6 |
Заявлен.*) |
+ |
30,0 |
100 |
0,6 |
1278,5 |
6,8 |
112,6 |
24,6 |
9,1 |
153,1 |
3258,2 |
106,9 |
8,1 |
*) процесс проводят в присутствии 2-30%-ного водного раствора комплексообразователя состава:
Гидроксиэтилиден-1,1-дифосфоновая кислота (I) формулы CH3 -С(ОН)=[P(O)(ОН)2]2,
Циклический Р-комплекс (II) общей формулы

где А есть = P(O)CH3ОН, при мольном отношении I:II, равном 1:1, при массовом отношении водного раствора комплексообразователя и железа, содержащегося в реакционной системе, равном 100-500 ppm на 1 ppm Fe. |
Формула изобретения
Способ получения гидроксиламинсульфата (ГАС) при избыточном давлении путем смешения в реакционном объеме синтез-газа, состоящего из оксида азота (II) и водорода, смеси серной кислоты и воды и катализатора “платина на электрографите”, отличающийся тем, что процесс проводят в присутствии 2-30%-ного водного раствора комплексообразователя состава:
Гидроксиэтилиден-1,1-дифосфоновая кислота (I) формулы
СН3-С(ОН)=[Р(O)(ОН)2]2,
Циклический Р-комплекс (II) общей формулы
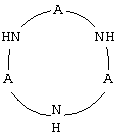
где А есть = Р(O)СН3ОН, при мольном соотношении I:II, равном 1:1, при массовом отношении водного раствора комплексообразователя и железа, содержащегося в реакционной системе, равном 100-500 ppm комплексообразователя на 1 ppm железа.
|
|