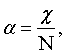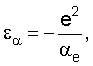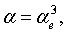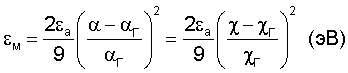Патент на изобретение №2287153
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ИЗМЕРЕНИЯ ЭНЕРГИИ МЕЖАТОМНЫХ И МЕЖМОЛЕКУЛЯРНЫХ ВЗАИМОДЕЙСТВИЙ И КООРДИНАЦИОННОГО ЧИСЛА АТОМНЫХ И МОЛЕКУЛЯРНЫХ ВЕЩЕСТВ
(57) Реферат:
Использование: при построении теории электронного строения вещества, а также при создании искусственных веществ и проектировании наноматериалов и наноустройств. Сущность: измеряют диэлектрическую восприимчивость исследуемого вещества, соответствующую идеальному состоянию и заданной плотности. Рассчитывают соответствующие им поляризуемости. С учетом поляризуемости вычисляют радиус атома или молекулы, а энергию взаимодействия и координационное число вычисляют в соответствии с предлагаемыми расчетными формулами. Технический результат изобретения заключается в установлении зависимости между энергией взаимодействия и координационным числом от поляризуемости и диэлектрической восприимчивости. 1 табл.
Настоящее изобретение относится к области исследования физико-химических свойств веществ в конденсированном состоянии и атомно-молекулярных систем, а именно к области исследования структуры и межатомных и межмолекулярных взаимодействий ван-дер-ваальсовых систем, в том числе нано- и мезоструктур. Известны методы измерения межатомных и межмолекулярных взаимодействий, основанные на установлении поведения физико-химических свойств вещества в зависимости от его плотности в виде вириального разложения (1). Бэкингем Э. В кн. «Межмолекулярные взаимодействия: от двухатомных молекул до биополимеров» – М.: Мир, 1981, С.85; 2). Мейсон Э., Сперлинг Т. Вириальное уравнение состояния. – М.: Мир, 1972. – 280 с.). Данный подход основан на наблюдении отклонения некоторого равновесного свойства реального вещества от соответствующего свойства идеального газа в предположении, что оно пропорционально разности между средним вкладом в это свойство пары реальных молекул и пары невзаимодействующих молекул. В общем случае макроскопическое равновесное свойство Q в виде разложения в ряд по степеням плотности
где
где q12 – вклад пары молекул 1 и 2, имеющих энергию взаимодействия u12; q12 и u12 являются функциями относительного положения молекул 1 и 2; интегрирование ведется по всем положениям и ориентациям молекулы 2 относительно молекулы 1; Подход, основанный на разложении типа (1), широко применяется в термодинамике для описания различных свойств вещества. Общим недостатком метода вириального разложения является его нечувствительность к структурным особенностям вещества. Известны также методы измерения энергии межчастичных взаимодействий, основанные на определении теплоты испарения (Рид Р. и др. Свойства газов и жидкостей. – Л.: Химия, 1982, С.183-196), калориметрические методы, основанные на измерении термодинамических параметров (Рудаков Е.С.Термодинамика межмолекулярного взаимодействия. – Новосибирск, Наука, 1968, С.8-12), другие методы, основанные на измерении макроскопических свойств веществ (Каплан И.Г. Введение в теорию межмолекулярных взаимодействий. – М.: Наука, 1982. С.245-258). Наиболее близким к предлагаемому методу измерения энергии межатомных и межмолекулярных взаимодействий является метод, основанный на вириальном разложении диэлектрической функции Клаузиуса-Моссотти (Э.Бэкингем. В кн.: «Межмолекулярные взаимодействия: от двухатомных молекул до биополимеров». – М.: Мир, 1981, С.86):
где Здесь первый вириальный коэффициент АК.-М. представляет собой уравнение Клаузиуса-Моссотти, соответствующее идеальному газу. Второй диэлектрический вириальный коэффициент ВК.-М. учитывает отклонение от уравнения Клаузиуса-Моссотти, обусловленное парным взаимодействием молекул. Третий коэффициент СК.-М. дает поправку на взаимодействие между тремя молекулами. Выбор функции Клаузиуса-Моссотти в качестве исходной функции разложения основан на предположении о независимости (или весьма слабой зависимости) поляризуемости атомов или молекул от плотности вещества. Такой вывод в свое время был сделан на основании экспериментального факта, свидетельствующего о независимости поляризации (или рефракции) Недостатком данного метода измерения межчастичных взаимодействий является относительно низкая чувствительность его к межатомным (межмолекулярным) взаимодействием. Объясняется это тем, что основной вклад в энергию межчастичных взаимодействий скрыт в величине Задачей настоящего изобретения является устранение данного недостатка за счет выбора в качестве диэлектрической функции разложения собственно диэлектрической восприимчивости
где А Смысл коэффициентов А
где Входящие в это уравнение величины NA и М не зависят от плотности Второй диэлектрический вириальный коэффициент В, как уже было сказано, описывает отклонения от аддитивности уравнения (4) в линейном по плотности приближении. Анализ экспериментальных данных показывает, что в широком диапазоне плотностей от нуля и до плотностей, соответствующих конденсированному состоянию, диэлектрическая восприимчивость большинства недипольных веществ оказывается линейной по плотности. Отсюда следует, что зависимость диэлектрических величин (
Разложение (3) в линейном по плотности приближении эквивалентно уравнению
где Настоящее уравнение имеет простой физический смысл, заключающийся в том, что измеряемая величина ( Идеальное состояние вещества должно предполагать то, что составляющие его микрочастицы в том или ином приближении сохраняют свою электронную структуру. В диэлектрическом и/или оптическом эксперименте критерием сохранения электронной структуры является его поляризуемость У атомных систем характер межатомных взаимодействий наиболее простой. Он представлен единственным дисперсионным механизмом притяжения между атомами. К этому же классу могут быть отнесены вещества, образованные недипольными молекулами. В общем случае можно представить молекулу в виде совокупности жестко связанных между собой атомов с эффективным и характерным для нее размером а. Каждая молекула выступает как источник флуктуирующего электрического поля Еа, которым оно оказывает поляризующее действие на свое ближайшее окружение. В результате каждая молекула испытывает со стороны своих соседей всестороннее растяжение, и размеры молекулы во всех направлениях увеличиваются на С другой стороны, стабильность и устойчивость атомов, входящих в состав молекулы, обеспечивают силы кулоновского притяжения, которым соответствует энергия Определим относительное возмущение электронной оболочки поляризующим полем Еа как отношение энергии возмущения
где pi – индуцированный дипольный момент, равный pi=2 Примем соотношение
Подстановка (8) в (7) дает выражение для энергии связи Из этого уравнения следует, что в качестве меры межатомного (межмолекулярного) взаимодействия выступает величина относительных изменений поляризуемости Энергию Это соотношение показывает, что энергия межатомного (межмолекулярного) взаимодействия сводится к измерению относительной разности диэлектрической восприимчивости (проницаемости) вещества по отношению к его гипотетическому состоянию, которому соответствует предположение об отсутствии межчастичных взаимодействий. Энергия межатомного (межмолекулярного) взаимодействия где u – энергия взаимодействия 1 моля вещества, NA – число Авогадро, Предлагаемый метод может быть распространен на бинарные и многокомпонентные системы. Т.о., в предлагаемом способе по сравнению с наиболее близким аналогом реализуется внутренне присущая связь диэлектрической восприимчивости вещества (и соответственно поляризуемости составляющих его атомов или молекул) с энергией межатомных или межмолекулярных взаимодействий, и как следствие этого реализуются высокие метрологические характеристики применяемой для измерения диэлектрической восприимчивости аппаратуры. Погрешность измерения энергии взаимодействия определяется погрешностью измерения входящих в (11) величин, которые в конечном итоге сводятся к погрешности измерения диэлектрической восприимчивости У предлагаемого метода измерения Формула (11) была принята для расчета энергии межатомного (межмолекулярного) взаимодействия, выраженную в единицах Важным обстоятельством при сравнении полученных данных u с литературными данными является необходимость в учете структурной анизотропии молекул. Предлагаемый метод дает усредненные значения энергий межатомных (межмолекулярных) взаимодействий. Методы, основанные на измерении энергии испарения с поверхности вещества, дают составляющую часть энергии в направлении, выделенным осевой симметрией молекулы. Эффект становится заметным уже у гомоядерных молекул и многократно увеличивается у цепочных молекул (на примере алканов СnН2n+2). Энергия u по (11) измеряется от 3,3 ккал/моль у метана СН4 до 5,2 ккал/моль у додекана С10H22. Тогда как метод, основанный на измерении теплоты испарения, дает энергию, изменяющуюся у этих же веществ от 3,9 ккал/моль до 25 ккал/моль. Конечно же, эти данные требуют дополнительных пояснений. Их нельзя отождествлять с собственно энергией межмолекулярных взаимодействий. Необходимо иметь дополнительные данные измерений энергий взаимодействия по другим координатным осям, в совокупности обеспечивающие возможность получения среднего значения энергии взаимодействия. Примером молекул с жесткими связями могут служить гомоядерные молекулы Н2 и N2. Различие рассчитанных и литературных данных u у них связано, по-видимому, с тем, что определяемая по данным измерения теплот испарения энергия u скорее представляет собой работу выхода молекулы с поверхности вдоль цилиндрической оси молекулы. У молекул хлора Cl2, кроме этого, начинает проявляться нежесткость ковалентной связи (при относительно высокой поляризуемости). Особенно сильно структурная анизотропия проявляется в энергии u высших алканов (С5Н12÷С10Н22); у алканов также проявляется дополнительная неопределенность данных u из-за наличия заторможенного вращения отдельных фрагментов молекул относительно С-С связей. Энергия межатомных (межмолекулярных) взаимодействий самым непосредственным образом связана с надатомной (надмолекулярной) структурой, описание которой достигается, в первую очередь, с помощью параметров кристаллической решетки и координационных чисел. Координационное число определяется, как число атомов (молекул) ближайшего к выделенному атому (молекуле) окружения. Известны различные методы измерения координационных чисел, таких как термохимические методы и методы, основанные на измерении вязкости, диффузии, сжимаемости и др. Наиболее широко распространены дифракционные методы (Киттель Ч. Введение в физику твердого тела. – М.: Наука, 1978, глава II). Они основаны на рассеянии излучения или потока частиц. Условием наблюдения дифракции является соизмеримость длины волны излучения с характерными размерами атомов (молекул). В структурных исследованиях измеряют интенсивность рассеяния в зависимости от угла рассеяния. Среди дифракционных методов различают рентгенографические, электроно-графические и нейтронографические методы. Количественно рассеивающую способность атомов (молекул) выражают через посредство амплитуды рассеяния К недостаткам метода относятся весьма сложная процедура измерения и последующая идентификация пространственного положения микрочастиц. Предлагаемый способ измерения направлен на устранение данного недостатка. Сущность изобретения (в части определения координационного числа). Предлагаемый метод определения координационных чисел
где R – расстояние между микрочастицами, Решая совместно уравнения (9) и (12), получаем
где Рассчитанные по данному уравнению координационные числа приведены в таблице 1. Они согласуются с имеющимися литературными данными и отражают правомерность предлагаемого настоящим изобретением подхода. По сравнению с наиболее близким аналогом предлагаемый способ измерения координационного числа позволяет упростить процедуру измерений и повысить точность измерений за счет сведения их к измерению величин диэлектрической восприимчивости и поляризуемости. К существенным признакам изобретения следует отнести: 1) функциональную связь между радиусом атома (молекулы) с его поляризуемостью с учетом взаимной поляризации атомов (молекул) в результате уплотнения вещества; 2) связь изменений поляризуемости атомов (молекул), обусловленных переходом из газовой фазы (соответствующей идеальному состоянию вещества) в конденсированное состояние исследуемого вещества, с энергией межатомных (межмолекулярных) взаимодействий и координационным числом; 3) причинная обусловленность энергии межатомного (межмолекулярного) взаимодействия энергией связи 4) взаимосвязь и взаимообусловленность энергии межатомных (межмолекулярных) взаимодействий 5) существенным представляется то, что в формуле для расчета энергии взаимодействия отсутствует трудно определяемая молекулярная величина – расстояние между атомами (молекулами). Т.о., предложен способ измерения энергии межатомных и межмолекулярных взаимодействий и координационного числа атомных и молекулярных веществ, основанный на их связи с поляризуемостью атомов или молекул данного вещества и зависимости поляризуемости атомов или молекул данного вещества от его плотности при переходе из газообразного состояния в конденсированное и заключающийся в том, что измеряют диэлектрическую восприимчивость или по формуле где NА – число Авогадро, и координационное число по формуле
Решаемые задачи. 1. Прямой метод измерения энергии межатомных и межмолекулярных взаимодействий как параметра, обеспечивающего описание устойчивости и стабильности вещества. Энергия межатомных и межмолекулярных взаимодействий предопределяет электронное строение и соответственно физические и химические свойства веществ; данное обстоятельство предполагает возможность расчета функциональных и эксплуатационных свойств большого класса молекулярных веществ. Метод определения параметров сольватации. 2. Метод измерения так называемой потенциальной функции, которая представляет собой зависимость энергии взаимодействия от расстояния между микрочастицами (или от плотности вещества). Знание вида потенциальной функции лежит в основе построения различных теорий электронного строения вещества. 3. Определение энергии парного взаимодействия между микрочастицами на основании данных измерения энергии межатомного или межмолекулярного взаимодействия и координационного числа (как результат их отношения). Эти данные необходимы для исследований в области синтеза искусственных веществ, а также для целей конструирования наноматериалов и наноустройств. 4. Физический смысл и механизм формирования межатомных и межмолекулярных взаимодействий атомно-молекулярных систем, заключающиеся в частичном переносе электронного заряда за счет взаимной поляризации атомов и молекул в процессе уплотнения вещества и соответствующего увеличения электронной плотности в пространстве между атомами и молекулами. Данное обстоятельство важно учитывать при проектировании искусственных веществ и наносистем, поскольку начальные размеры атомов и молекул (до сборки) при их соединении (объединении) увеличиваются до 30-40%. Примером может служить рассмотрение одного из наиболее распространенных в атомной и молекулярной физике потенциала Ленарда-Джонса [3, с.121]
где Для того, чтобы можно было сравнивать энергию взаимодействия с параметрами потенциала Ленарда-Джонса, приведем уравнение (9) к виду
где Величина ( В свою очередь, атомная (молекулярная) плотность равна Если следовать правилу размерности, то величина Осуществление изобретения. Для осуществления изобретения необходима аппаратура для измерения диэлектрических величин ( Для измерения диэлектрических величин (е или
ЛИТЕРАТУРА 1. Потапов А.А. Деформационная поляризация: поиск оптимальных моделей. – Новосибирск: Наука, 2004. – 511 с. 2. Бараш Ю.С. Силы Ван-дер-Ваальса. – М.: Наука, 1988. – 344 с. 3. Киттель Ч. Введение в физику твердого тела. – М.: Наука, 1978. – 792 с. 4. Потапов А.А. Молекулярная диэлькометрия. – Новосибирск, Наука, 1994. – 285 с. 5. Свойства неорганических соединений. Справочник. – Л.: Химия, 1983. – 392 с. 6. Химическая энциклопедия. – М.: Большая Российская энциклопедия, 1995.
Формула изобретения
Способ измерения энергии межатомных и межмолекулярных взаимодействий и координационного числа атомных и молекулярных веществ, основанный на их связи с поляризуемостью атомов или молекул данного вещества и зависимости поляризуемости атомов или молекул данного вещества от его плотности при переходе из газообразного состояния в конденсированное и заключающийся в том, что измеряют диэлектрическую восприимчивость
рассчитывают величину энергии связи по формуле
где e – элементарный заряд,
а затем рассчитывают энергию межатомного или межмолекулярного взаимодействия по формуле
или по формуле где NA – число Авогадро, и координационное число по формуле
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 газа имеет вид [1]
газа имеет вид [1]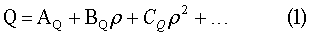
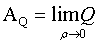 – величина свойства Q, соответствующая идеальному газу (что соответствует условию малости межмолекулярного взаимодействия),
– величина свойства Q, соответствующая идеальному газу (что соответствует условию малости межмолекулярного взаимодействия), 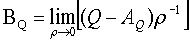 – второй вириальный коэффициент свойства Q, которым описывается отклонение от свойств идеального газа в первом приближении. Для одного моля газа АQ=Naq1, где NA – число Авогадро, q1 – средний вклад молекулы в макроскопическое свойство. Для второго вириального коэффициента статистическая механика дает следующий результат:
– второй вириальный коэффициент свойства Q, которым описывается отклонение от свойств идеального газа в первом приближении. Для одного моля газа АQ=Naq1, где NA – число Авогадро, q1 – средний вклад молекулы в макроскопическое свойство. Для второго вириального коэффициента статистическая механика дает следующий результат: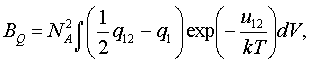
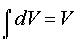 – объем, занимаемый одним молем газа.
– объем, занимаемый одним молем газа.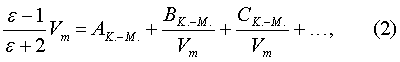
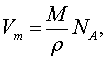 Vm – молекулярный объем, М – относительная молекулярная масса, А
Vm – молекулярный объем, М – относительная молекулярная масса, А , В
, В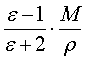 многих веществ в широком диапазоне плотности
многих веществ в широком диапазоне плотности 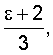 и энергетическое поведение вещества в этом случае представлено в виде изменений энергии взаимодействия атомов и молекул относительно данного уровня
и энергетическое поведение вещества в этом случае представлено в виде изменений энергии взаимодействия атомов и молекул относительно данного уровня 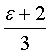 [1].
[1]. . Выбор диэлектрической восприимчивости однозначно отвечает общему уравнению (1) как по форме, так и по сути. Действительно, диэлектрическая восприимчивость
. Выбор диэлектрической восприимчивости однозначно отвечает общему уравнению (1) как по форме, так и по сути. Действительно, диэлектрическая восприимчивость  N, или диэлектрической поляризации
N, или диэлектрической поляризации 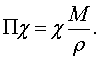 Это единственно теоретически обоснованное соотношение, удовлетворяющее требованиям, которые предъявляются к уравнению идеального состояния газа. Отклонения от этого уравнения причинно обусловлены действием сил межатомного (межмолекулярного) взаимодействия, количественной мерой которых служат соответствующие вириальные коэффициенты, так что
Это единственно теоретически обоснованное соотношение, удовлетворяющее требованиям, которые предъявляются к уравнению идеального состояния газа. Отклонения от этого уравнения причинно обусловлены действием сил межатомного (межмолекулярного) взаимодействия, количественной мерой которых служат соответствующие вириальные коэффициенты, так что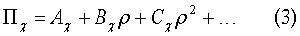
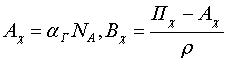 – (в линейном по
– (в линейном по 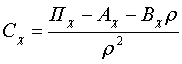 (в квадратичном по
(в квадратичном по 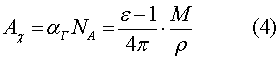
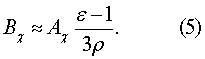
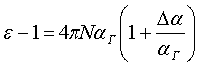 или
или 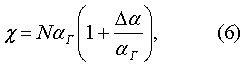

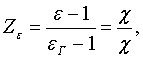 где
где 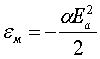 к энергии связи атома (молекулы)
к энергии связи атома (молекулы) 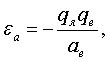 так что
так что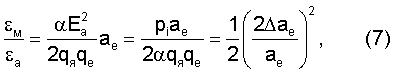
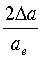 – относительные изменения поляризационного радиуса в результате взаимной поляризации атомов (молекул) [1]. При выводе уравнения (7) эффективное поле Еa выражено через причинно обусловленную этим полем величину pi, так что Еa=рi/
– относительные изменения поляризационного радиуса в результате взаимной поляризации атомов (молекул) [1]. При выводе уравнения (7) эффективное поле Еa выражено через причинно обусловленную этим полем величину pi, так что Еa=рi/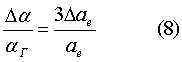
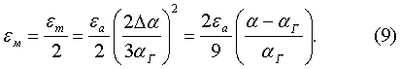
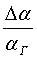 атомов (молекул) как результат их взаимной поляризации, усиливающейся по мере уплотнения вещества. Достоверность уравнения (9) подтверждается результатами апробации вириальной теории деформационной поляризации [1].
атомов (молекул) как результат их взаимной поляризации, усиливающейся по мере уплотнения вещества. Достоверность уравнения (9) подтверждается результатами апробации вириальной теории деформационной поляризации [1].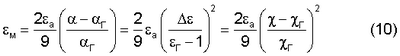
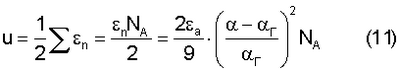
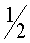 учитывает парный характер взаимодействия (в элементарном взаимодействии участвует пара микрочастиц).
учитывает парный характер взаимодействия (в элементарном взаимодействии участвует пара микрочастиц).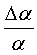 и
и 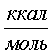 (см. таблицу). В таблице приведены рассчитанные энергии u для атомов благородных газов и некоторых простых молекул. Здесь же приведены для сравнения наиболее достоверные литературные данные по энергиям межчастичного взаимодействия. Согласие между ними носит качественный характер и скорее отражает тот факт, что в настоящее время отсутствуют заведомо безапелляционные методы измерения энергии межатомных (межмолекулярных) взаимодействий. Различие между рассчитываемыми по (11) и литературными данными минимально у атомов благородных газов и увеличивается по мере усложнения структурны молекул и увеличения у них числа атомов.
(см. таблицу). В таблице приведены рассчитанные энергии u для атомов благородных газов и некоторых простых молекул. Здесь же приведены для сравнения наиболее достоверные литературные данные по энергиям межчастичного взаимодействия. Согласие между ними носит качественный характер и скорее отражает тот факт, что в настоящее время отсутствуют заведомо безапелляционные методы измерения энергии межатомных (межмолекулярных) взаимодействий. Различие между рассчитываемыми по (11) и литературными данными минимально у атомов благородных газов и увеличивается по мере усложнения структурны молекул и увеличения у них числа атомов. (
( ), где
), где 
 основан на непосредственной связи энергии межатомных (межмолекулярных) взаимодействий
основан на непосредственной связи энергии межатомных (межмолекулярных) взаимодействий 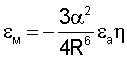 или
или 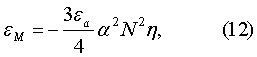
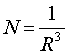 , N – плотность микрочастиц.
, N – плотность микрочастиц.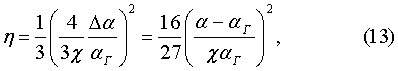
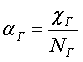 и
и 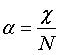 рассчитывают величину энергии связи по формуле
рассчитывают величину энергии связи по формуле 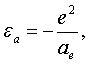 где е – элементарный заряд, ае – радиус атома или молекулы, который находят в соответствии с соотношением
где е – элементарный заряд, ае – радиус атома или молекулы, который находят в соответствии с соотношением 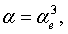 а затем рассчитывают энергию межатомного или межмолекулярного взаимодействия по формуле
а затем рассчитывают энергию межатомного или межмолекулярного взаимодействия по формуле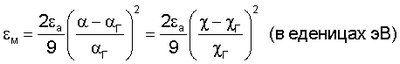
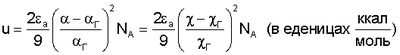
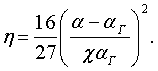
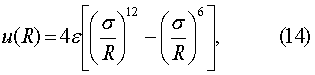
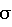 – эмпирические константы.
– эмпирические константы.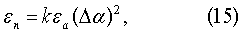
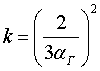 – постоянный для данного веществ коэффициент,
– постоянный для данного веществ коэффициент, 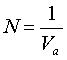 , где Va – атомный (молекулярный) объем, равный Va=а3 a, где aa – среднее расстояние между микрочастицами. Отсюда следует что
, где Va – атомный (молекулярный) объем, равный Va=а3 a, где aa – среднее расстояние между микрочастицами. Отсюда следует что 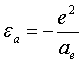 (где е – элементарный заряд, а3 е=
(где е – элементарный заряд, а3 е=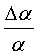
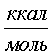 расчет по [11]
расчет по [11]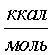 лит. данные [1, 5, 6]
лит. данные [1, 5, 6]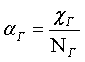 и
и