Патент на изобретение №2285694
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ N-ЗАМЕЩЕННЫХ ИМИДОВ ДИФЕНОВОЙ КИСЛОТЫ
(57) Реферат:
Изобретение относится к получению N-замещенных имидов дифеновой кислоты. Способ осуществляют реакцией дифеновой кислоты с имидирующими агентами в органическом растворителе. Процесс проводят в индифферентном органическом растворителе, образующем азеотропную смесь с водой при температуре кипения реакционной массы с отгонкой образующейся воды. В качестве имидирующего реагента используют N,N’-дизамещенные мочевины формулы (NHR2)СО, где R-метил, фенил. Добавляют уксусный ангидрид в реакционную массу после прекращения выделения воды при следующих мольных соотношениях реагентов: дифеновая кислота: мочевина: уксусный ангидрид 1,0:(1,0÷4,0):(1,0÷20,0) соответственно. Технический результат – повышение выхода целевого продукта, снижение токсичности и агрессивности используемых реагентов. 2 табл.
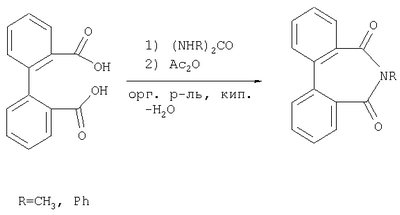
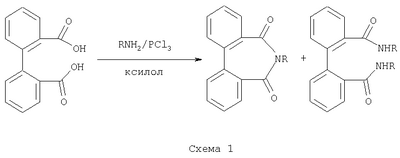
Изобретение направлено на разработку селективного метода получения N-замещенных имидов дифеновой кислоты (ДК) непосредственно из самой ДК, обеспечивающего высокий выход целевых продуктов и снижение токсичности и агрессивности используемых реагентов и образующихся отходов. Известен трехстадийный способ получения имидов ДК [Сэкигути Т.J. Chem. Soc. Jap. Ind. Chem. Sec. 1970. Vol.73. №8. P.1853-1858.; Chapman J.M, Jr, Wyrick S.D., Voorstad D.J., Maguire J.H., Cocolas G.H., Hall I.H. J.Pharm. Sci. 1984. Vol.73. №10. P.1482-1484.], согласно которому на первой стадии кипячением ДК в уксусном ангидриде получают ангидрид ДК, затем полученным ангидридом ацилируют соответствующий первичный амин, получают N-замещенный моноамид ДК, на заключительной стадии полученный моноамид вновь кипятят в уксусном ангидриде и получают конечный имид. Основной недостаток данного способа заключается в невозможности получения N-замещенных имидов ДК, так как имидирование ДК N,N’-дизамещенными мочевинами приводит к образованию N-замещенных моноамидов ДК, а не имидов. Наиболее близким по технической сущности к заявляемому изобретению является одностадийный метод синтеза N-замещенных имидов ДК [Кулев Л.П., Гирева Р.Н., Степнова Г.М. Ж. общ. хим. 1962. Т.32. №9. С.2812-2816.], суть которого заключается в прямом амидировании ДК первичным амином в среде ксилола в присутствии PCl3 (Схема 1). К 0,05 молям ДК, 0,05 молям амина в 100 мл безводного ксилола постепенно прибавляют 0,05 моль треххлористого фосфора и нагревают смесь при 120°С с перемешиванием 3 часа. Из еще горячего раствора сначала выпадают длинные иглы замещенного имида ДК, затем при стоянии постепенно выкристаллизовывается диамид. Очистку имида и диамида осуществляют путем перекристаллизации их из ксилола или хлорбензола. Препаративные выходы не указаны. К недостаткам описанного способа необходимо отнести применение агрессивного и высокотоксичного реагента – треххлористого фосфора, выделение в процессе реакции агрессивного газа – хлористого водорода, а главное, невысокую селективность процесса, обусловленную одновременным образованием диамидов ДК. Задачей настоящего изобретения является разработка селективного метода получения N-замещенных имидов ДК, исключающего из процесса агрессивные и высокотоксичные реагенты и отходы и обеспечивающего высокие выходы целевых продуктов. Поставленная задача достигается тем, что сначала ведут процесс амидирования ДК N,N’-дизамещенной мочевиной в индифферентном органическом растворителе несмешивающимся с водой и образующим с ней азеотропную смесь, в отсутствии каких-либо катализаторов, конденсирующих или влагопоглащающих реагентов. Образующуюся в ходе реакции воду отгоняют с растворителем, в котором проводится реакция, с возвратом растворителя в реакционную массу после отделения воды. На этой стадии процесса основным продуктом реакции является N-замещенный моноамид ДК. После завершения процесса амидирования ДК в реакционную смесь добавляют уксусный ангидрид и кипятят смесь еще 1 ч. При этом происходит дегидратация N-замещенного моноамида ДК, сопровождающаяся его циклизацией в соответствующий имид. При выборе растворителя для осуществления процесса важно соблюдение следующих условий. 1) Растворитель не должен смешиваться с водой, т.к. в этом случае после азеотропной отгонки и разделения растворитель можно вернуть в реакционную массу. 2) С целью сокращения времени процесса желательно выбирать растворитель с более высокой температурой кипения (табл.1). Примеры получения N-замещенных имидов из ДК и N,N’-дизамещенных мочевин с использованием различных индифферентных растворителей, образующих азеотропные смеси с водой, приведены в табл.1. Важным условием протекания процесса является соблюдение мольных соотношений реагентов. Использование N,N’-дизамещенных мочевин в количествах порядка 0,5 моль мочевины на 1 моль ДК и ниже приводит к неполной конверсии последней и соответственно к значительному снижению выхода конечного продукта и увеличению затрат на его очистку от непрореагировавшей ДК. (табл.2, п.9). При увеличении количества мочевины выше 0,5 моль на 1 моль ДК выход имида постепенно возрастает. Однако увеличение количества мочевины выше 4 моль на 1 моль ДК приводит к непроизводительному расходу амидирующего реагента, увеличению расхода уксусного ангидрида и росту затрат на очистку целевого продукта от избыточного количества амидирующего реагента и продуктов его дальнейших превращений (табл.2, п.1-4, 10-11). При выборе количества уксусного ангидрида, прибавляемого на второй стадии процесса, следует учитывать, что этот реагент расходуется не только на дегидратацию моноамида, но и на ацилирование оставшейся мочевины и продуктов ее распада – аминов. При использовании уксусного ангидрида в количествах менее 1 моль на 1 моль мочевины в реакционной массе остается значительное количество промежуточного продукта – моноамида ДК, который в данном случае не может количественно превратиться в имид (табл.2, п.6, 12). Поэтому для увеличения выхода конечного продукта, необходимо брать избыточное количество уксусного ангидрида: 1-5 моль Ас2О на 1 моль мочевины (см. табл.2, п.2, 5-6, 10, 12). Больший избыток уксусного ангидрида приводит к непроизводительному расходу этого реагента, так как не происходит существенного увеличения выхода продукта (табл.2, п.13). Об окончании первой стадии процесса можно судить по прекращению выделения воды из конденсата паров реакционной массы, а также по исчезновению исходной ДК в реакционной массе. Найденные условия синтеза N-замещенных имидов ДК и установленные соотношения реагентов справедливы и при масштабировании загрузок реагентов. Так, например, при загрузке 1,000 г (4,13 ммоль) ДК, 0,728 г (8,26 ммоль) N,N-диметилмочевины и 4,250 г (41,30 ммоль) уксусного ангидрида выход N-метилимида составляет 65%, а при пропорциональном увеличении количества реагентов в 5 раз – 67% (см. табл.2, п.2, 8). Таким образом, совокупность нововведенных признаков позволяет селективно получать N-замещенные имиды ДК с выходами до 70%, со значительным снижением токсичности и агрессивности используемых реагентов и образующихся отходов. Пример: В одногорлую колбу, снабженную насадкой Дина-Старка с обратным холодильником, загружают 5,00 г (20,65 ммоль) ДК, 3,64 г (41,30 ммоль) N,N’-диметилмочевины и 150 мл о-ксилола. Реакционную смесь кипятят 4 ч до прекращения выделения воды из конденсата паров азеотропной смеси. После этого в реакционную смесь добавляют 20 мл уксусного ангидрида и кипятят с обратным холодильником 1 ч. Затем полностью отгоняют основной растворитель. Кубовому остатку дают охладиться до комнатной температуры и добавляют к нему 2-3-х кратный избыток воды. Выпавший осадок отфильтровывают, промывают на фильтре водой и перекристаллизовывают из изопропилового спирта. Выход продукта 67%. Способ получения N-замещенных имидов дифеновой кислоты
Формула изобретения
Способ получения N-замещенных имидов дифеновой кислоты реакцией дифеновой кислоты с имидирующими агентами в органическом растворителе отличающийся тем, что процесс проводят в индифферентном органическом растворителе, образующем азеотропную смесь с водой при температуре кипения реакционной массы с отгонкой образующейся воды, в качестве имидирующего реагента используют N,N’-дизамещенные мочевины формулы (NHR2)CO, где R-метил, фенил, с добавлением уксусного ангидрида в реакционную массу после прекращения выделения воды при следующих соотношениях реагентов:
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 29.03.2007
Извещение опубликовано: 20.11.2008 БИ: 32/2008
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||